Giriş ve Genel Bilgi
Aromataz inhibitörleri, postmenopozal kadınlarda meme kanserinin tedavisinde kullanılan, anti-östrojenik, anti-proliferatif ve anti-tümör özelliklere sahip ilaçlardır. Bu ilaçlar genellikle film kaplı tablet veya draje formunda oral yoldan alınır. Günümüzde kullanımdaki aromataz inhibitörlerinin tamamı üçüncü nesil ajanlardır. İlk üçüncü nesil aromataz inhibitörü olan anastrozol, 1995 yılında ABD’de (Arimidex®) ve 1996 yılında İsviçre’de onaylanmıştır. Daha eski birinci nesil (ör. aminoglutetimid) ve ikinci nesil (ör. formestan, fadrozol) aromataz inhibitörleri ise etkinlik ve tolerabilite sorunları nedeniyle artık klinikte kullanılmamaktadır.
Etki Mekanizması
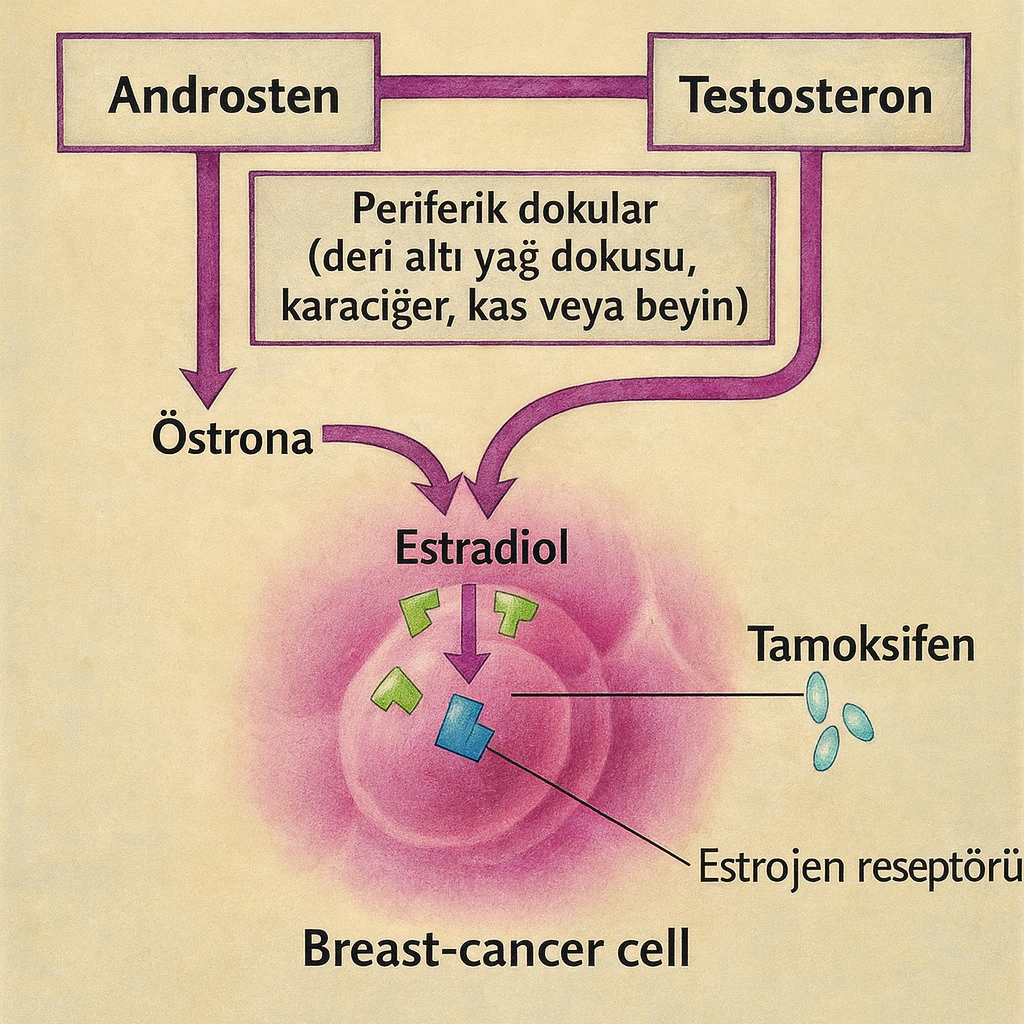
Aromataz inhibitörlerinin etkisi, androjenlerden östrojen sentezini katalize eden aromataz enziminin (CYP19A1) baskılanmasına dayanır. Aromataz enzimi, androstenedion ve testosteron gibi androjenleri estron ve estradiol gibi östrojenlere dönüştüren, östrojen biyosentezinin son adımını gerçekleştiren bir sitokrom P450 bileşenidir. Aromataz inhibitörleri bu enzimi engelleyerek vücuttaki östrojen üretimini büyük oranda azaltırlar. Sonuçta dolaşımdaki östrojen seviyeleri düşer, bu da hormon bağımlı tümör hücrelerinin büyüme uyarısını azaltır. Bu mekanizma sayesinde aromataz inhibitörleri anti-östrojenik etki yaratır ve meme kanserinde tümör hücrelerinin çoğalmasını engelleyerek anti-tümör etki gösterir.
Kimyasal Yapı ve Sınıflandırma
Üçüncü nesil aromataz inhibitörleri kimyasal yapılarına göre steroidal ve steroidal olmayan olarak sınıflandırılır.
- Steroidal olmayan (non-steroidal) inhibitörler, yapısal olarak steroid değildir ve enzime geri dönüşümlü biçimde bağlanırlar. Bu gruba giren ilaçlar genellikle triazol türevi bileşiklerdir; örneğin anastrozol ve letrozol steroidal olmayan inhibitörlerdir.
- Steroidal inhibitörler, androjen substratlara yapısal olarak benzer ve enzime geri dönüşümsüz biçimde bağlanarak onu etkisiz hale getirirler. Bu nedenle “intihar inhibitörleri” olarak da adlandırılır. Eksemestan, androstenedion türevi steroid yapılı bir aromataz inhibitörüdür.
Mevcut Etken Maddeler
- Non-steroidal (geri dönüşümlü) inhibitörler: Anastrozol (Arimidex®), Letrozol (Femara®).
- Steroidal (geri dönüşümsüz) inhibitörler: Eksemestan (Aromasin®).
Birinci nesil (aminoglutetimid) ve ikinci nesil (formestan, fadrozol) inhibitörler güncel klinik kullanımda değildir.
Endikasyonlar
Aromataz inhibitörlerinin temel endikasyonu, postmenopozal kadınlarda hormon reseptörü pozitif meme kanseri tedavisidir. Özellikle östrojen reseptörü (ER) ve/veya progesteron reseptörü (PR) pozitif, menopoz sonrası ileri evre veya metastatik meme kanserlerinde ilk veya ikinci basamak hormonal tedavi olarak tercih edilmektedir. Ayrıca erken evre hormon pozitif meme kanserinde cerrahi sonrası adjuvan tedavide 5 yıla kadar kullanımı standart bir yaklaşımdır. Premenopozal kadınlarda ise yumurtalıklar aktif östrojen üretmeye devam ettiğinden tek başına etkili değildir.
Kullanım ve Dozaj
Aromataz inhibitörleri genellikle günde bir kez kullanılır. Bu ilaçlar uzun yarı ömürleri sayesinde tek dozla sürekli bir aromataz baskılanması sağlar. Anastrozol ve letrozol sırasıyla 1 mg ve 2,5 mg dozlarında günlük olarak alınır. Tedavi süresi, erken evre kanserde adjuvan olarak genellikle 5 yıl olup, gerektiğinde 7–10 yıla kadar uzatılabilir. Metastatik olgularda ise tedavi, hastalığın seyrine göre daha uzun sürebilir.
Kötüye Kullanım (Doping)
Aromataz inhibitörleri, anabolik steroid kullanan sporcular tarafından jinekomasti riskini azaltmak amacıyla doping aracı olarak kötüye kullanılabilmektedir. Bu ilaçlar testosteronun östrojene dönüşümünü engelleyerek erkeklerde meme dokusu büyümesini önler. Ancak bu tür kullanımlar tıbbi olarak önerilmez, ciddi yan etkilere yol açabilir ve WADA tarafından yasaklı kabul edilmektedir.
Kontrendikasyonlar
- İlacın etkin veya yardımcı maddelerine karşı aşırı duyarlılık
- Premenopozal hormonal durum
- Hamilelik
- Emzirme
Ayrıca ciddi karaciğer veya böbrek yetmezliği olanlarda dikkatli kullanılmalıdır.
İlaç Etkileşimleri
Letrozol ve eksemestan, CYP450 izoenzimleri tarafından metabolize edilir. Bu nedenle CYP450 indükleyici ilaçlar (ör. rifampisin, fenitoin, karbamazepin) etkinliklerini azaltabilir. CYP3A4 inhibitörleri eksemestan düzeylerini yükseltebilir. Östrojen tedavileri, aromataz inhibitörlerinin etkisini ortadan kaldırabileceği için birlikte kullanılmamalıdır.
Yan Etkiler
Yan etkiler, östrojen eksikliğine bağlı olarak menopoz semptomlarına benzer:
- Sıcak basmaları ve aşırı terleme
- Deri döküntüleri
- Baş ağrısı
- Kas ve eklem ağrıları
- Yorgunluk
- Uyku bozuklukları
- Ruh hali değişiklikleri
- Bulantı
Uzun vadede östrojenin sürekli baskılanması, osteoporoz ve buna bağlı kırık riskinde artışa yol açabilir. Bu nedenle düzenli kemik yoğunluğu ölçümü ve gerekirse destek tedaviler (kalsiyum, D vitamini, bifosfonatlar) önerilir. Ayrıca uzun süreli kullanımda kolesterol düzeylerinde artış ve kardiyovasküler risklerde yükselme bildirilmektedir.
Keşif
1. Aromataz Enziminin Keşfi
- yüzyılın ortalarında steroid biyosentez yolları aydınlatılmaya başlandığında, androjenlerden östrojenlerin oluşumunu katalize eden özel bir enzim olduğu fark edildi. Bu enzim, daha sonra “aromataz” olarak adlandırıldı. Araştırmalar, androjen çekirdeğinde C-19 karbonunun oksidatif olarak kaybolmasıyla birlikte A halkasında aromatik bir yapı oluştuğunu, bunun da östrojen sentezinin anahtarı olduğunu ortaya koydu. 1960’larda, östrojen biyosentezinde bu enzimin rolü açık biçimde tanımlandı ve aromatazın kadın üreme organlarında, plasentada ve menopoz sonrası yağ dokusunda yoğun olarak bulunduğu gösterildi. Bu keşif, özellikle menopoz sonrası meme kanserinin östrojen bağımlılığını anlamak için bir dönüm noktası oldu.
2. Birinci Nesil İnhibitörlerin Ortaya Çıkışı
Aromataz inhibitörlerinin ilk temsilcisi, aslında aromataz için değil epilepsi tedavisi için geliştirilmiş bir ilaçtı: aminoglutetimid. 1960’larda antikonvülzan olarak pazara sunulan bu molekülün steroid sentezini baskıladığı fark edildi. Meme kanserli kadınlarda kullanıldığında, adrenal hormon sentezini de engellediği için glukokortikoid desteğiyle birlikte verilmesi gerekiyordu. Buna rağmen, östrojen seviyelerini düşürmedeki gücü sayesinde meme kanseri tedavisinde ilk klinik başarıları sağladı. Ancak seçici olmaması ve ciddi yan etkileri nedeniyle uzun vadede kullanımı sınırlı kaldı. Birinci nesil ilaçlar arasında ayrıca testolakton gibi steroid yapılı moleküller de vardı; fakat bunlar da zayıf etkilere sahipti.
3. İkinci Nesil İnhibitörler
1980’lere gelindiğinde, araştırmacılar daha seçici moleküller geliştirmeye yöneldi. Bu dönemde formestan (4-hidroksiandrostenedion) ön plana çıktı. Steroid yapıda olan bu molekül, androjen substratlara benzediği için aromatazın aktif bölgesine daha güçlü bağlanıyor ve östrojen sentezini etkili biçimde baskılıyordu. Klinik denemelerde etkinliği kanıtlandı ve bir süre klinikte kullanıldı. Aynı dönemde fadrozol ve vorozol gibi imidazol türevi non-steroidal ajanlar da geliştirildi. Bu ikinci nesil inhibitörler birinci nesle göre daha az yan etkiye sahipti, ancak halen tam anlamıyla seçici değillerdi.
4. Üçüncü Nesil İnhibitörlerin Rönesansı
1990’lara gelindiğinde ilaç kimyası ve biyoteknoloji alanındaki ilerlemeler sayesinde üçüncü nesil aromataz inhibitörleri geliştirildi. Bu nesil, önceki ilaçlardan farklı olarak hem çok daha güçlü hem de son derece seçiciydi.
- Anastrozol (Arimidex®): Bir triazol türevi olan bu molekül, 1995 yılında ABD’de onay aldı. Klinik çalışmalar, tamoksifene kıyasla daha iyi sonuçlar verdiğini gösterdi.
- Letrozol (Femara®): Yine bir triazol türevi olan letrozol, aromatazı güçlü ve geri dönüşümlü biçimde inhibe ediyordu. 1998’de FDA tarafından onaylandı.
- Eksemestan (Aromasin®): Bu ilaç ise steroid yapıda olup “intihar inhibitörü” olarak tanımlanıyordu. Aromataz enzimiyle geri dönüşsüz bir bağ kurarak kalıcı inhibisyon sağlıyordu. 1999 yılında onaylandı.
Bu üç ilaç, klinik etkinlikleri ve yan etki profilleriyle kısa sürede meme kanseri tedavisinin standart ajanları haline geldi.
5. Modern Dönem
Bugün üçüncü nesil aromataz inhibitörleri, hormon reseptör pozitif meme kanserinde uluslararası kılavuzların önerdiği ilk seçeneklerden biridir. Erken evre kanserde adjuvan tedavi olarak tamoksifenin yerini büyük ölçüde almış, ileri evrede ise yaşam süresini uzatan ve nüks riskini azaltan ajanlar haline gelmiştir. Ayrıca, yeni nesil hedefe yönelik ilaçlarla kombinasyonları da yaygınlaşmıştır. Örneğin letrozol, CDK4/6 inhibitörleriyle birlikte metastatik hastalıkta standart tedavi haline gelmiştir. Eksemestan ise everolimus gibi mTOR inhibitörleriyle birlikte kullanılabilmektedir.
Aromataz inhibitörlerinin keşif yolculuğu, tesadüfi gözlemlerden başlayıp moleküler düzeyde tasarlanmış yüksek seçicilikte ilaçlara uzanan yarım yüzyıllık bir bilimsel serüvendir. Bugün hâlâ meme kanseri tedavisinde en güçlü endokrin silahlardan biri olmaya devam etmektedir.
İleri Okuma
- Brodie, A. M., & Longcope, C. (1977). Inhibition of peripheral aromatization of androgens by aminoglutethimide in vivo. The Journal of Clinical Endocrinology & Metabolism, 45(5), 1003–1010.
- Brodie, A. M., Schwarzel, W. C., Shaikh, A. A., & Brodie, H. J. (1977). The effect of an aromatase inhibitor, 4-hydroxy-androstenedione, on estrogen-dependent processes in reproduction and breast cancer. Endocrinology, 100(6), 1684–1695.
- Coombes, R. C., Goss, P. E., Dowsett, M., Gazet, J. C., Brodie, A. M., & Smith, I. E. (1984). Aminoglutethimide as therapy for postmenopausal women with advanced breast cancer. Cancer Research, 44(11), 4798s–4801s.
- Santen, R. J., Santner, S. J., & Lipton, A. (1986). Pharmacology and clinical use of aminoglutethimide. Endocrine Reviews, 7(1), 1–28.
- Dowsett, M., Stein, R. C., Mehta, A., Coombes, R. C. (1990). A comparative study of the pharmacodynamics of fadrozole, a new aromatase inhibitor, with aminoglutethimide in postmenopausal women with breast cancer. Clinical Cancer Research, 46(6), 4237–4241.
- Buzdar, A. U., Robertson, J. F. R., Eiermann, W., Nabholtz, J. M., & Bonneterre, J. (1999). Anastrozole versus megestrol acetate in the treatment of postmenopausal women with advanced breast carcinoma: Results of two randomized trials. Cancer, 86(5), 836–842.
- Mouridsen, H., Gershanovich, M., Sun, Y., Pérez-Carrión, R., Boni, C., Monnier, A., … & Bapsy, P. P. (2001). Superior efficacy of letrozole versus tamoxifen as first-line therapy for postmenopausal women with advanced breast cancer: Results of a phase III study of the International Letrozole Breast Cancer Group. Journal of Clinical Oncology, 19(10), 2596–2606.
- Paridaens, R., Dirix, L., Lohrisch, C., Beex, L., Nooij, M., Cameron, D., … & Piccart, M. (2003). Exemestane compared with tamoxifen as initial adjuvant therapy for postmenopausal women with early breast cancer: The TEAM (Tamoxifen Exemestane Adjuvant Multicenter) trial. Journal of Clinical Oncology, 21(6), 852–860.