Locus Kiesselbachi
Etimolojik köken ve adlandırma mantığı
“Locus Kiesselbachi” terimi, Latince “locus” (yer, bölge) sözcüğü ile bir eponimi birleştirir: Kiesselbach. Anatomi ve klinik tıp geleneğinde, belirli bir yapıyı ilk kez ayrıntılı biçimde tanımlayan, klinik önemini vurgulayan ya da cerrahi/klinik pratikte yerleştiren kişilerin adlarıyla anılan oluşumlar yaygındır. Bu bağlamda Locus Kiesselbachi, burun septumunun ön bölümünde, özellikle epistaksis (burun kanaması) açısından kritik bir damar ağına verilen isimdir. Türkçe kullanımda “Kiesselbach alanı” ya da “Kiesselbach pleksusu” ifadeleriyle de karşılanır.
Terimin iki yönlü bir semantik işlevi vardır:
- Topografik bir bölgeyi işaret eder (nazal septumun ön-ventral/anterior-inferior kısmı).
- Bu bölgede bulunan damarların bir “pleksus” biçiminde örgütlendiğini, yani çok sayıda küçük arteriyol ve venülün yoğun bir anastomoz ağı oluşturduğunu anlatır.
Bu adlandırma, klinisyen için doğrudan pratik bir çağrışım taşır: Burun kanamalarının en sık kaynağı olan, yüzeyel ve travmaya açık bir mukozal damar alanı.
Anatomik ve histotopografik tanım
Locus Kiesselbachi, nazal septumun anteroinferior bölümünde yer alan, çoğu bireyde septumun ön-alt üçte birlik kesiminde belirginleşen yüzeyel bir damarlaşma alanıdır. Bu bölge, septal mukozanın nispeten ince olduğu, epitel altında damarların yüzeye yakın seyrettiği, ayrıca hava akımının kurutucu etkisinin en yoğun hissedildiği bir “yüksek risk” mikro-çevre oluşturur.
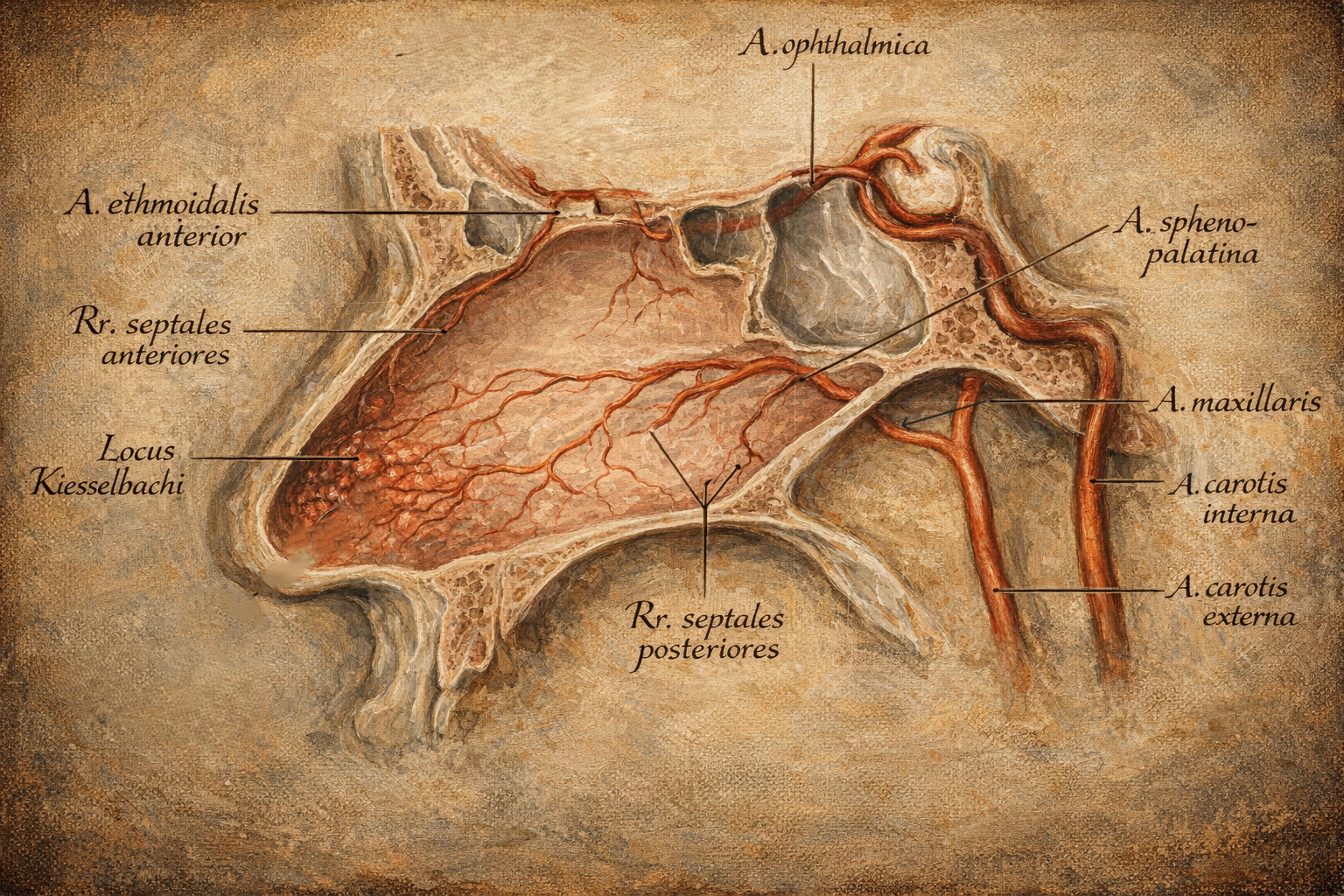
Damarsal bileşenler klasik anatomik tarifte çoğunlukla şu sistemlerin septal dallarını içerir:
- A. sphenopalatina’nın septal dalları (posterior nazal dolaşımdan katkı)
- A. ethmoidalis anterior’un septal dalları (orbito-kranial kaynaktan katkı)
- A. labialis superior’un septal dalları (eksternal karotid sistemin fasiyal kolundan katkı)
- A. palatina major’un anterior septal katkıları (oral-kaviter kaynaklı katkı)
Bu damarlar, septumun ön kısmında birbirleriyle zengin anastomozlar yaparak yüzeyel bir pleksus görüntüsü verir. Klinik pratikte “kapiller pleksus” ifadesi sıklıkla kullanılsa da, gerçek yapı yalnızca kapillerlerden ibaret değildir; arterioller, venüller ve aradaki mikrovasküler ağın bir “anastomotik kavşak” gibi çalışması söz konusudur. Bu nedenle, kanamanın paterni (sızıntı tarzı yüzeyel kanama ile daha basınçlı arteriyel kanama arasında) olgudan olguya değişebilir.
Histolojik düzlemde burun septumunun ön kısmındaki mukoza:
- Görece ince bir mukoperikondrium tabakası
- Yüzeye yakın subepitelyal damarlar
- Lokal inflamasyon, kuruluk ve mikrotravmalarla kolay bozulan epitel bariyeri
özelliklerini taşır. Bu mikroanatomik kırılganlık, Kiesselbach bölgesini kanama açısından “kolay tetiklenen” bir hedef haline getirir.
Tarihsel gelişim: eponimden klinik paradigma’ya
Nazal kanama, antik dönemlerden beri bilinen bir klinik belirti olmasına rağmen, belirli bir anatomik “kanama odağı” fikrinin yerleşmesi, modern anatomik disseksiyon teknikleri ile klinik gözlemin birleştiği 19. yüzyıl tıbbında belirginleşir. Bu dönemde burun boşluğu ve septumun damar anatomisi daha ayrıntılı biçimde sınıflandırılmaya başlanmış; epistaksisin, rastlantısal bir olay değil, belirli vasküler “zayıf halkaların” klinik sonucu olabileceği anlaşılmıştır.
Wilhelm Kiesselbach’ın katkısı, epistaksisin en sık kaynağını oluşturan anterior septal damar ağının klinik önemini görünür kılmasıyla ilişkilendirilir. Böylece epistaksise yaklaşım, “genel kanama” yönetiminden “odaklı anatomik hemostaz” yönetimine doğru evrilir. Bu evrim, birkaç klinik ilkeyi tıp pratiğine yerleştirir:
- Kanama kaynağı çoğu kez anterior septumdadır.
- Görülebilir bir odak, basit mekanik yöntemlerle kontrol edilebilir.
- Lokal tedavi, sistemik nedenleri dışlamanın yerine geçmez; fakat ilk basamakta çoğunlukla etkilidir.
- yüzyıl boyunca nazal endoskopinin gelişmesi, optik büyütme ve aydınlatmanın iyileşmesiyle, anterior ve posterior epistaksis ayrımı daha netleşmiş; Kiesselbach alanının “gözle görülebilir kanama odağı” olarak önemi pratikte daha da pekişmiştir. Bu dönemde kimyasal ve elektriksel koterizasyon yöntemleri, uygun seçilmiş olgularda hedefe yönelik hemostazı standartlaştırmıştır. Günümüzde ise lokal hemostatik ajanlar, emilebilir tamponlar, bipolar koter ve gerektiğinde endoskopik damar ligasyonu ya da anjiyografik embolizasyon gibi basamaklı yaklaşımlar, Kiesselbach alanı kaynaklı kanamayı daha güvenli ve öngörülebilir biçimde yönetilebilir kılar.
Evrimsel biyolojik bağlam: burun, iklim ve mikrovasküler uyum
Locus Kiesselbachi’nin varlığını ve klinik kırılganlığını yalnızca “rastlantısal bir damar yığını” olarak değil, burun boşluğunun evrimsel işlevleriyle bağlantılı bir mikrosistem olarak düşünmek açıklayıcı olabilir. İnsan burnu, yalnızca koku organı ya da hava iletim kanalı değildir; solunan havayı ısıtma, nemlendirme ve filtreleme gibi kritik görevler üstlenir. Bu görevler, geniş bir yüzey alanı, yoğun bir mukozal damar ağı ve dinamik vazomotor kontrol gerektirir.
Isı ve nem düzenlemesi: Soğuk ve kuru hava, üst solunum yoluna girdiğinde mukozanın hızlı ısınma ve nemlendirme sağlaması gerekir. Burun mukozasındaki zengin damar ağı, “ısı değiştirici” gibi çalışır. Anterior septum bölgesi, hava akımının ilk temas ettiği yerlerden biri olduğundan, burada yüzeyel damarlaşmanın bulunması fizyolojik açıdan avantaj sağlar.
Bedeli: Bu fizyolojik avantajın bir “trade-off”u vardır. Yüzeye yakın damarlar, travma ve kuruluğa daha açık hale gelir. İnsanlarda iki ayaklılık, yüzün ön kısmının çevresel etkilerle daha doğrudan karşılaşması, ayrıca kültürel davranışlar (kapalı mekânda kuru hava, irritanlara maruziyet, burun temizleme alışkanlıkları) bu kırılganlığı daha görünür kılar.
Mikrovasküler plastisite: Burun mukozası, vazodilatasyon ve vazokonstriksiyonla hızlı biçimde kan akımını ayarlayabilir. Bu, termoregülasyon ve nemlendirme için faydalıdır; ancak inflamasyon, alerjik rinit veya enfeksiyon gibi durumlarda damarların genişlemeye eğilimli hale gelmesi, Kiesselbach alanında kanama olasılığını artırır. Evrimsel biyolojinin diliyle söylersek: burun mukozası, çevresel değişkenliğe uyum için yüksek reaktivite kazanmış; bu reaktivite belirli koşullarda “epistaksise yatkınlık” olarak ortaya çıkar.
Güncel bilimsel anlayış: patofizyoloji, risk katmanları ve klinik korelasyon
Günümüzde Kiesselbach bölgesi, epistaksisin patofizyolojisini anlamada “mikro-çevre” kavramını temsil eder: damar, epitel bariyeri, mukus tabakası, lokal inflamasyon ve mekanik stresin kesişim noktası.
1) Bariyer bozulması ve kuruluk ekseni
Anterior septum, hava akımına en açık bölgelerden olduğundan, düşük nemli ortamlarda epitelin su kaybı artar. Kuruyan mukoza çatlamaya eğilim kazanır; subepitelyal damarlar yüzeye yakın seyrettiği için küçük fissürler bile kanamaya yol açabilir. Bu mekanizma, özellikle kış aylarında, kaloriferli ortamlarda, uzun süre maske kullanımıyla değişen hava akımı dinamiğinde ya da nazal dekonjestanların aşırı kullanımında daha belirgin hale gelebilir.
2) İnflamasyon ve damar reaktivitesi
Alerjik rinit, viral rinit ve kronik irritan maruziyeti; mukozal ödem, hiperemi ve kırılganlık oluşturur. İnflamatuvar süreçler, mikrovasküler geçirgenliği artırır ve damar duvarını mekanik strese daha duyarlı kılar. Bu nedenle, Kiesselbach alanı kaynaklı kanama, çoğu zaman “tek bir damar yırtılması”ndan ziyade, inflamasyonla duyarlılaşmış yüzeyel ağın minimal bir tetikle kanamaya geçmesi şeklinde ortaya çıkar.
3) Mekanik mikrotravma
Burun karıştırma, sert sümkürme, nazal travmalar, septumda kabuklanma ve bunun koparılması, çocukluk çağında sık görülen epistaksisin en temel tetikleyicilerindendir. Burada “küçük travma, büyük kanama” paradoksu, bölgenin yüzeyel vaskülaritesiyle açıklanır.
4) Sistemik faktörlerin lokal yansıması
Kiesselbach bölgesi çoğu olguda primer kaynak olsa da, altta yatan sistemik durumlar kanamanın şiddetini ve süresini belirleyebilir:
- Antikoagülan ve antiagregan kullanımı
- Trombosit fonksiyon bozuklukları
- Koagülopati durumları
- Hipertansiyonun kanama kontrolünü zorlaştırması
Bu faktörler, bölgeyi “başlatıcı odak” olmaktan çıkarmaz; fakat kanamanın “sönümlenmesini” geciktirerek klinik tabloyu ağırlaştırabilir.
Klinik önem: epistaksisin anatomik odak noktası
Epistaksis, pratikte iki büyük grupta düşünülür: anterior ve posterior. Anterior epistaksisin büyük kısmı Kiesselbach alanından kaynaklanır ve çoğu olguda muayene ile kanama noktası görülebilir. Bu durum, yönetimde basamaklı bir yaklaşımı mümkün kılar:
- Kompresyon ve lokal vazokonstriksiyonla ilk kontrol
- Kanama odağının doğrudan hemostazı
- Nüks eğilimi olan olgularda altta yatan predispozanların giderilmesi
Kiesselbach alanının klinik “değeri”, yalnızca kanamanın sık kaynağı olması değildir; aynı zamanda görünür, erişilebilir ve hedefe yönelik tedaviye elverişli bir anatomik pencere sunmasıdır. Bu yüzden KBB pratiğinde, epistaksis değerlendirmesinin erken adımlarından biri, anterior septumun iyi aydınlatma altında inspeksiyonu ve kanama odağının aranmasıdır.
Diferansiyel çerçeve: benzer bölgeler ve kavramsal ayrımlar
Locus Kiesselbachi ile sıkça birlikte anılan bir diğer damarlaşma alanı, posterior septal bölgede tanımlanan Woodruff pleksusudur. Bu iki kavramın ayrımı, epistaksisin klinik davranışını anlamada önem taşır: anterior kanamalar daha sık, daha yüzeyel ve daha kolay kontrol edilebilirken; posterior kanamalar daha az görülür ama daha şiddetli olabilir ve daha ileri girişim gerektirebilir. Bu klinik ayrım, Kiesselbach alanını “ilk akla gelen kaynak” haline getirir.
Modern yaklaşımda önleme ve bakım ilkeleri
Kiesselbach alanı kaynaklı nüks epistaksislerde, güncel klinik yaklaşım yalnızca kanamayı durdurmaya değil, mukozal bariyeri güçlendirmeye ve tetikleyicileri azaltmaya da odaklanır. Bu çerçevede:
- Ortam neminin artırılması ve nazal nemlendirme stratejileri
- Kabuklanmayı azaltan lokal bakım
- İrritanlardan kaçınma
- Alerjik inflamasyonun kontrolü
- Uygunsuz dekonjestan kullanımının önlenmesi
gibi önlemler, anatomik kırılganlığın klinik yansımasını azaltabilir. Bu önleme ekseni, Kiesselbach alanını yalnızca “kanayan yer” değil, “bariyer ekolojisi bozulduğunda kanayan yer” olarak yeniden konumlandırır.
Keşif
Burun kanaması, tıbbın en eski “görünür acilleri”nden biridir: hasta kanar, hekim bakar ve kanamanın hem kaynağını hem de anlamını çözmeye çalışır. Locus Kiesselbachi’nin keşif hikâyesi de tam burada başlar. Bugün “anterior septumun en sık kanayan yeri” diye bir cümleyle özetlediğimiz bu alanın arkasında, aydınlatmanın icadından damar anatomisinin inceliğine, klinik gözlemden endoskopiye ve girişimsel radyolojiye uzanan iki yüzyıllık bir entelektüel ilerleme çizgisi vardır.
1) İlk sezgiler: kanamanın “yer”i olmalı
Antik hekimler epistaksisi tanıyordu; fakat modern anlamda “bu kanama genellikle şurada başlar” düşüncesi için iki şey gerekliydi:
- Burun içinin güvenle ve yeterli ışıkla görülebilmesi
- Kanamanın rastgele değil, belirli anatomik zayıflık noktalarından çıktığını düşündürecek tekrarlayan klinik örüntüler
Bu iki koşul, ancak 19. yüzyılın klinik muayene devrimleriyle yerli yerine oturdu. O döneme kadar burun boşluğu, hekimin “girdiği” ama “tam gördüğü” bir alan değildi; kanama genellikle bir “olay” olarak ele alınıyor, odak fikri belirsiz kalıyordu.
2) 19. yüzyıl: burun içine ışık girince anatomi konuşmaya başladı
- yüzyılın ortalarından itibaren muayene aletleri, aydınlatma teknikleri ve “doğrudan bakış” kültürü, KBB’yi ayrı bir disiplin olarak şekillendirdi. Burun spekulumu, daha iyi ışık, daha sistematik muayene… Bunlar yalnızca konfor artırmadı; bilgi üretti. Çünkü artık hekimler, burun kanaması geldiğinde yalnızca kanı değil, kanın çıktığı noktayı arayabilir hale gelmişti.
Bu dönemde klinisyenlerin zihninde kritik bir soru belirginleşti:
“Eğer çoğu burun kanaması aynı yerden geliyorsa, o yer anatomik olarak özel olmalı.”
İşte Locus Kiesselbachi’ni “keşfe açık” kılan bilimsel merak, tam olarak bu soruydu.
3) James Lawrence Little (1879): kanamayı bir “lezyon” gibi tarif etmek
Amerikalı cerrah James Lawrence Little, 1879’da burun kanamasının sık tekrarlayan bir odağına dair dikkat çekici bir adım attı: anterior septumda, belirli bir bölgede epistaksisi açıklayan, o güne kadar ayrıntılı biçimde tarif edilmemiş bir “lezyon/odak” fikrini klinik vakalar üzerinden somutlaştırdı.
Little’ın katkısı yalnızca “şurada kanar” demek değildi. Daha rafine bir şey yaptı:
- Kanamanın rastgele olmadığını, belirli bir topoğrafyaya yerleştiğini ileri sürdü
- Bu topoğrafyanın muayene edilebilir ve hedeflenebilir olduğunu gösterdi
- Böylece epistaksisi, “genel bir kanama eğilimi”nden çok “yerel bir anatomik zayıflık” üzerinden düşünmeyi teşvik etti
Little’ın anlatısı, o dönemin tıbbında sık görülen bir dönüşümün parçasıydı: semptomu bir “fenomen” olmaktan çıkarıp “lokalize edilebilir bir patoloji” haline getirmek.
4) Wilhelm Kiesselbach (1880’ler, özellikle 1884): pleksusun anatomik mantığını kurmak
Little’ın klinik sezgisi ve betimi, Almanya’da hızla gelişen KBB ekolünün anatomik titizliğiyle birleşince bir sonraki basamağa sıçradı. Alman KBB hekimi Wilhelm Kiesselbach, 1880’lerde epistaksisi ve burun septumunun damar organizasyonunu daha sistematik bir çerçevede ele aldı; 1884’te yayımladığı çalışması, anterior septumun bu kritik bölgesinin bir damar anastomoz alanı olarak kavranmasına güçlü bir zemin sağladı.
Kiesselbach’ın asıl “kalıcı” etkisi, bir odağı sadece tarif etmekten öteye taşımasıdır:
- Odağın damar kaynaklı bir anastomoz kavşağı olduğunu vurgulayarak, neden bu kadar sık kanadığını açıklamaya çalıştı
- Kanama yönetimini, “basınç uygulayalım” refleksinden “damar ağını hedefleyelim” aklına yaklaştırdı
- Böylece odak, bir eponimle (Kiesselbach) tıbbi hafızaya yerleşti ve klinik dilin parçası oldu
Bu aşamada bilimsel merak, artık “neresi?” sorusundan “neden orası?” sorusuna geçiyordu. Bu da entelektüel ilerlemenin tipik bir işaretidir: tariften mekanizmaya.
5) 20. yüzyılın başı–ortası: anterior–posterior ayrımı ve kanama topografyasının genişlemesi
Kiesselbach alanı, pratikte “en sık” kaynak olduğu için klinik odak noktası haline geldi; ancak zamanla hekimler başka bir gerçeği daha net görmeye başladı: bazı kanamalar, özellikle yaşlılarda ve ağır olgularda, burun arkasından geliyor; kontrolü daha zor; klinik davranışı farklı.
Bu farkın anatomik izini sürmek, epistaksis bilgisini ikinci bir eksen boyunca geliştirdi: anterior ve posterior epistaksis ayrımı.
George H. Woodruff (1949): posterior kanamada “başka bir pleksus” fikri
1949’da George H. Woodruff, burun arka bölümünde, inferior meatus çevresinde yer alan ve posterior epistaksisle ilişkilendirilen bir damar ağı tarifledi. Bu yapı zamanla Woodruff pleksusu diye anılmaya başladı. Woodruff’un katkısı, Kiesselbach alanının önemini azaltmadı; aksine epistaksisin topografik haritasını tamamladı:
- Anterior kanama çoğu kez Kiesselbach alanından
- Posterior kanama ise farklı bir damar mimarisi ve farklı klinik risklerle
Burada da bilimsel merak aynı kalıpta ilerledi: “bu kanama neden bu kadar inatçı?” sorusu, “burun arkasında nasıl bir damar düzeni var?” sorusuna dönüştü.
6) 20. yüzyılın ikinci yarısı: hemostaz teknikleri, cerrahi ligasyon ve girişimsel radyoloji çağının doğuşu
Epistaksis yönetimi, bilgi arttıkça teknikleşti. Kiesselbach alanı kaynaklı anterior kanamalarda koterizasyon ve hedefe yönelik müdahaleler gelişirken, posterior kanamalarda daha agresif stratejiler doğdu.
Cerrahi ligasyonun çizgisi
Posterior epistaksiste daha proksimal damarların kontrolü fikri, 20. yüzyıl boyunca cerrahi literatürde giderek olgunlaştı. İç maksiller arter ligasyonu gibi yöntemler tarif edildi, unutuldu, tekrar gündeme geldi. Bu dönem, tıbbın tipik “deneme–seçme–standartlaştırma” evresidir: teknikler ortaya çıkar, komplikasyonlar öğrenilir, daha güvenli ve hedefe yakın yöntemler aranır.
Embolizasyon (1974): kateterle hemostaz fikrinin sahneye çıkışı
1974’te Sokoloff ve çalışma arkadaşlarının epistaksiste embolizasyon uygulamalarına dair erken raporları, epistaksis tedavisinde yeni bir çağ açtı: kanamayı burun içinden değil, damar içinden “kapatmak”. Bu, yalnızca bir teknik yenilik değildi; disiplinler arası bir düşünce biçimiydi:
- KBB’nin anatomik hedefi
- Radyolojinin damar içi erişimi
- Acil tıbbın hız ve stabilizasyon ihtiyacı
aynı klinik problemde birleşti.
Girişimsel radyoloji, epistaksisi özellikle refrakter posterior olgularda “son çare” olmaktan çıkarıp birçok merkezde planlı bir kurtarıcı basamağa dönüştürdü.
7) Endoskopi dönemi: kanayan yeri büyütmek, hedefi küçültmek
Fiberoptik ve rijit endoskopinin KBB pratiğine yerleşmesi, epistaksiste adeta bir epistemolojik sıçrama yarattı: artık “nereden” sorusu, çok daha yüksek doğrulukla yanıtlanabiliyordu. Bu, özellikle posterior epistaksiste sfenopalatin arter ve dallarının endoskopik olarak hedeflenmesini mümkün kıldı.
Endoskopik yaklaşımlar, klinik düşünceyi şöyle dönüştürdü:
- Kör tamponlama yerine görerek hemostaz
- Geniş alan baskısı yerine seçici damar kontrolü
- Daha az morbidite hedefiyle daha “akıllı” girişimler
Bu çizgi, Kiesselbach alanının yönetimini de dolaylı biçimde etkiledi: anterior kanamalarda bile daha net odak saptama, daha sınırlı koter, daha iyi nüks kontrolü.
8) 2000’ler–2020’ler: kanama ekolojisi, standart rehberler ve ilaç temelli hemostazın yükselişi
Günümüz, yalnızca “damarı yak” dönemi değildir. Epistaksis, özellikle Kiesselbach alanı bağlamında, bir mikro-çevre bozukluğu olarak daha incelikli yorumlanır:
- Kuruluk ve bariyer kırılganlığı
- İnflamasyon ve vazomotor reaktivite
- Travma ve tekrarlayan mikrohasar
- Antikoagülan/antiagregan kullanımıyla eşiklerin değişmesi
Bu daha bütüncül bakış, standart rehberlerin de diline girdi.
2020 klinik uygulama rehberi: basamaklı, kanıta dayalı yol haritası
2020’de yayımlanan “Nosebleed (Epistaxis)” klinik uygulama rehberi, epistaksis yönetimini geniş bir klinisyen kitlesi için basamaklı bir algoritma mantığında birleştirdi: kompresyon ve vazokonstriktörden koterizasyona, uygun tamponlamadan endoskopik ligasyona ve girişimsel radyolojiye kadar uzanan bir çerçeve sundu. Bu rehber, Kiesselbach alanı gibi klasik anatomik kavramların modern sistematik içinde “nerede durduğunu” da yeniden tanımlar: çoğu olguda ilk basamak, çünkü çoğu olguda kaynak orasıdır; ama her olguda yalnızca orası değildir.
Traneksamik asit ve topikal hemostaz: “tampon mu, ilaç mı?” tartışmasının bilimleşmesi
Son yıllarda, özellikle acil servis pratiğinde, topikal traneksamik asit uygulamaları epistaksis yönetiminde önemli bir araştırma alanı haline geldi. Çift-kör randomize çalışmalar, farklı doz karşılaştırmaları ve klinik derlemeler, özellikle atraumatik anterior epistaksiste topikal TXA’nın tampon ihtiyacını azaltabileceği, kanamayı daha hızlı kontrol edebileceği ve hasta konforunu artırabileceği fikrini güçlendirdi. Bu literatür aynı zamanda tıbbın tipik bir olgunlaşma sürecini gösterir: ilk heyecan, çelişkili sonuçlar, daha iyi tasarlanmış çalışmalar, doz ve uygulama standardizasyonu arayışı.
Bu noktada Locus Kiesselbachi’nin hikâyesi, ilk keşif dönemine tuhaf bir biçimde geri döner: yine aynı yer, yine aynı soru… Sadece araçlar değişmiştir. 1879’da spekulumla görülen bir odak, 2020’lerde hemostatik ajanlar, emilebilir materyaller, endoskopi ve gerektiğinde damar içi girişimlerle yönetilen bir “mikrohemodinamik düğüm”e dönüşmüştür.
9) Bugün: Kiesselbach alanı artık bir “nokta” değil, bir kavşak
Güncel yaklaşımda Locus Kiesselbachi, yalnızca dört-beş arterin buluştuğu bir anastomoz olarak değil;
- hava akımının kurutucu etkisinin yoğun olduğu
- epitel bariyerinin kolay bozulduğu
- inflamasyonun damar kırılganlığını artırdığı
- sistemik antitrombotiklerin yerel kanamayı uzatabildiği
bir kavşak olarak değerlendirilir.
İleri Okuma
- Kiesselbach, W. (1884). Über spontanes Nasenbluten.
- Kiesselbach, W. (1902). Über spontane Nasenblutungen.
- Woodruff, G. H. (1949). Cardiovascular epistaxis and the naso-nasopharyngeal plexus. The Laryngoscope, 59(11), 1238–1247. DOI: 10.1288/00005537-194911000-00003.
- Little, J. W. (1977). Epistaxis. Journal of the American Medical Association, 238(17), 1889–1891.
- Sokoloff, J., Wickbom, I., McDonald, D. (1974). Transcatheter embolization in epistaxis.
- Kucik, C. J., Clenney, T. (2005). Management of Epistaxis. American Family Physician, 71(2), 305–311.
- Chiu, T. W., Shaw-Dunn, J., McGarry, G. W. (2008). Woodruff’s plexus. The Journal of Laryngology & Otology.
- Schlosser, R. J. (2009). Epistaxis. New England Journal of Medicine, 360(8), 784–789. DOI: 10.1056/NEJMcp0806262.
- Dubel, G. J., et al. (2013). Transcatheter Embolization in the Management of Epistaxis. Seminars in Interventional Radiology.
- Wormald, P. J. (2013). Endoscopic Sinus Surgery: Anatomy, Three-Dimensional Reconstruction, and Surgical Technique. Thieme. ISBN: 978-1604067471.
- Tunkel, D. E., Anne, S., Payne, S. C., et al. (2020). Clinical Practice Guideline: Nosebleed (Epistaxis). Otolaryngology–Head and Neck Surgery, 162(1_suppl), S1–S38.
- Mudry, A. (2021). History of otorhinolaryngology in Germany before 1921. HNO.
- Solomon, M., et al. (2021). Epistaxis. The New England Journal of Medicine.
- Hosseinialhashemi, M., Jahangiri, R., Faramarzi, A., et al. (2022). Intranasal topical application of tranexamic acid in atraumatic anterior epistaxis: a double-blind randomized clinical trial. Annals of Emergency Medicine.
- Arikan, C., et al. (2024). Appropriate dose of tranexamic acid: 500 mg vs 1000 mg in epistaxis. The Laryngoscope.
- Braschi, É. (2025). Tranexamic acid solution for nosebleeds. Canadian Family Physician, 71(9), 571.