Ticari İsimler: Avalox®, Vigamox®
Etken Madde: Moksifloksasin
İlaç Grubu: Dördüncü nesil florokinolon antibiyotik
Moksifloksasin, geniş spektrumlu bir antibakteriyel ajan olup dördüncü nesil florokinolonlar sınıfında yer alır. Bu ilaç, hem Gram-pozitif hem de Gram-negatif bakterilere karşı etkili olup ayrıca bazı atipik patojenlere ve anaeroblara karşı da yüksek antimikrobiyal aktivite gösterir. Önceki nesil kinolonlara göre daha gelişmiş farmakokinetik ve farmakodinamik özelliklere sahiptir. Bu bağlamda Moksifloksasin, solunum yolu enfeksiyonları başta olmak üzere çeşitli sistemik enfeksiyonların tedavisinde güçlü ve klinik olarak tercih edilen bir antibiyotiktir.
Etkime Mekanizması
DNA Girişimi ve Replikasyonun Engellenmesi
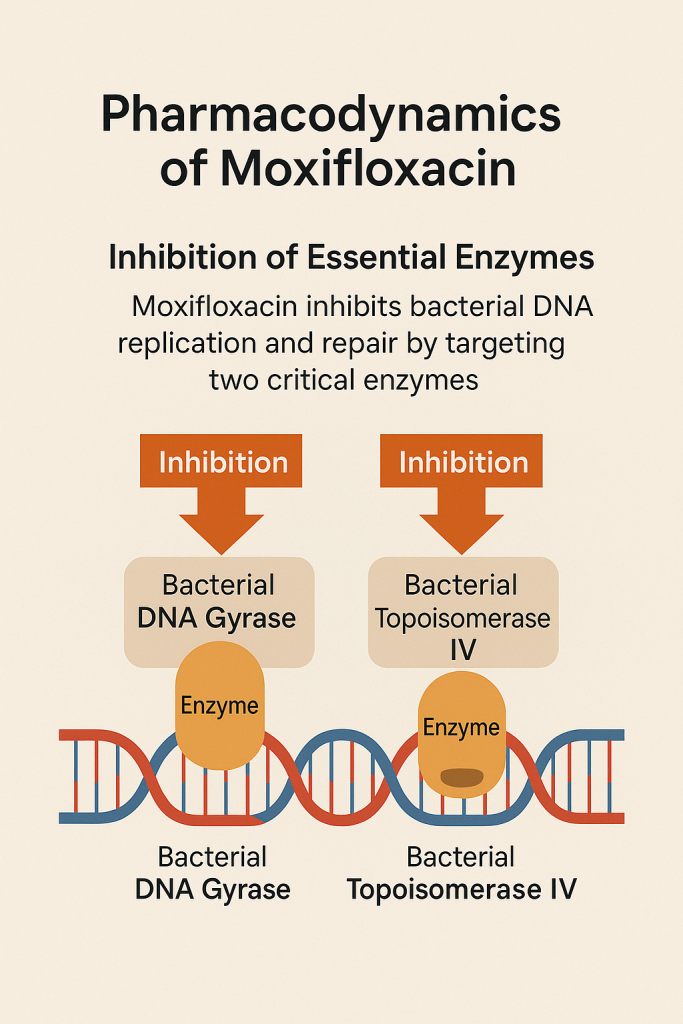
Moksifloksasin’in bakterisidal (öldürücü) etkisi, bakteriyel DNA sentezinde görev alan iki hayati enzimi inhibe etmesine dayanır: DNA giraz (topoizomeraz II) ve topoizomeraz IV.
- DNA giraz, süperkoilleşmiş DNA’nın çözülmesini sağlar ve bakterinin çoğalması sırasında DNA’nın açılmasını kolaylaştırır.
- Topoizomeraz IV, kromozomal DNA’nın bölünme sırasında ayrılmasını sağlar.
Bu iki enzimin inhibisyonu, DNA replikasyonunun, transkripsiyonunun ve tamir mekanizmalarının durmasına yol açar. Bunun sonucunda bakteriyel hücreler bölünemez hale gelir ve ölür.
Florokinolon sınıfındaki diğer ajanlara kıyasla, Moksifloksasin hem Gram-pozitif hem de Gram-negatif bakterilerde bu iki enzime karşı dengeli bir inhibisyon profiline sahiptir.
Kullanım Talimatları
Dozaj ve Uygulama Şekli
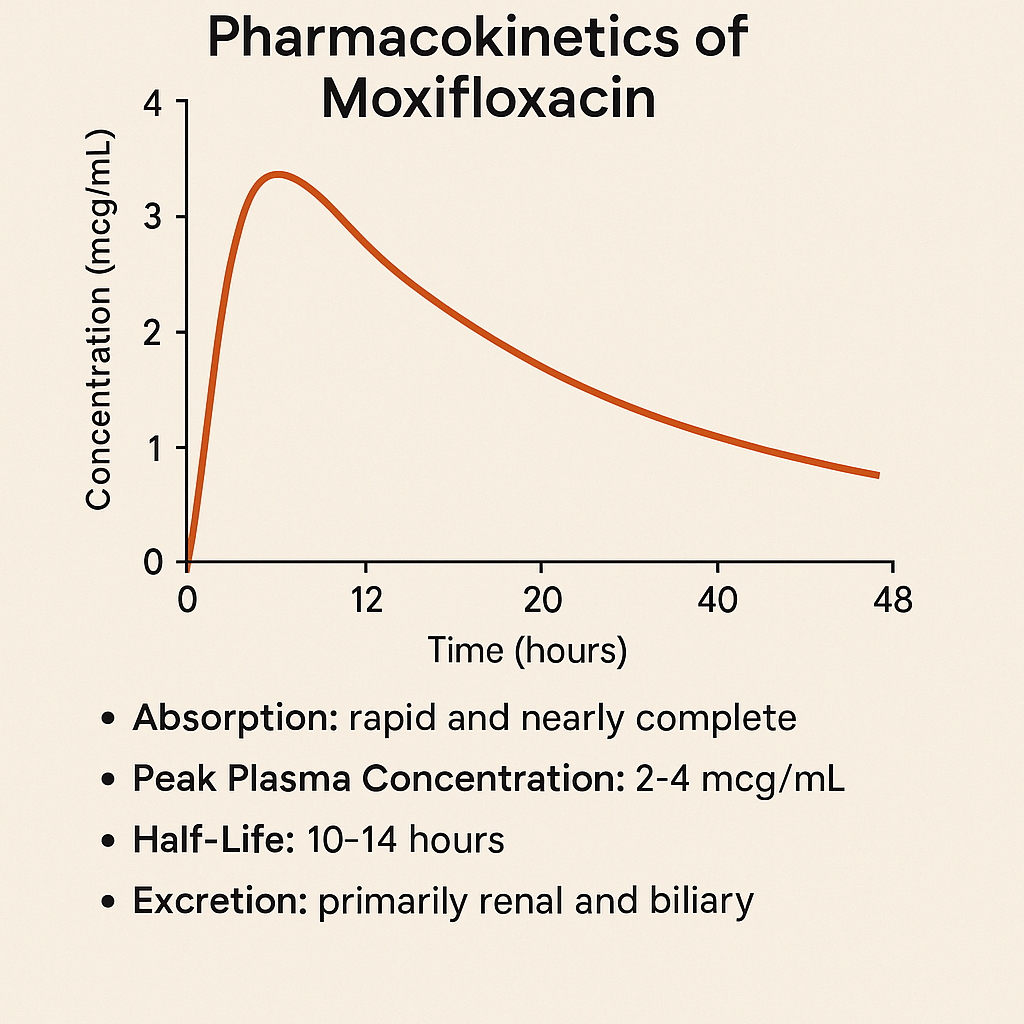
Moksifloksasin, genellikle 400 mg’lık tablet formunda günde bir kez oral yolla uygulanır. İlacın biyoyararlanımı yüksektir (%90’ın üzerindedir), bu da intravenöz ve oral formların terapötik olarak birbirine denk olduğunu gösterir.
Besin alımının ilacın emilimi üzerinde klinik olarak anlamlı bir etkisi bulunmadığından, yemekle birlikte ya da aç karnına alınabilir.
Antasit Etkileşimleri
Alüminyum, magnezyum, kalsiyum ya da demir içeren antasitler ve mineral takviyeleri, Moksifloksasin’in gastrointestinal sistemdeki biyoyararlanımını önemli ölçüde azaltabilir. Bu nedenle bu tür ajanlarla birlikte uygulanması durumunda, Moksifloksasin’in bu maddelerden en az 4 saat önce veya 8 saat sonra alınması önerilir.
Yan Etkiler ve Riskler
Sık Görülen Advers Etkiler
Moksifloksasin kullanan bireylerde aşağıdaki advers etkiler sıklıkla rapor edilmiştir:
- Baş ağrısı
- Somnolans (uyuşukluk, uyku hali)
- Oral veya genital kandidiyaz (Candida albicans kaynaklı mantar enfeksiyonları)
- Karaciğer fonksiyon testlerinde yükselmeler (ALT, AST artışı)
- Gastrointestinal şikayetler: Bulantı, kusma, karın ağrısı, ishal, dispepsi
Bu yan etkilerin çoğu hafif-orta şiddettedir ve tedavi kesildikten sonra gerileyebilir. Ancak bazı vakalarda ilacın kesilmesini gerektirecek kadar şiddetli olabilir.
Kardiyovasküler Güvenlik ve QT Uzaması
Florokinolon sınıfı antibiyotiklerin karakteristik risklerinden biri de QT aralığı uzamasıdır. Moksifloksasin, kardiyak repolarizasyonu etkileyerek T dalgasını uzatabilir ve potansiyel olarak torsades de pointes gibi ölümcül aritmilere neden olabilir.
Bu risk özellikle aşağıdaki gruplarda artar:
- Halihazırda QT uzaması olan hastalar
- Elektrolit dengesizlikleri (özellikle hipokalemi, hipomagnezemi) olan bireyler
- Antiaritmik ilaçlar kullanan hastalar (örneğin amiodaron, sotalol)
- Yaşlı bireyler ve kardiyak hastalık öyküsü olanlar
Bu nedenle, Moksifloksasin tedavisine başlamadan önce bu tür risk faktörlerinin dikkatle değerlendirilmesi önem taşır.
Kullanımda Dikkat Edilmesi Gereken Diğer Noktalar
- Tendinopati ve Tendon Rüptürü Riski: Florokinolonlar, özellikle yaşlılarda ve kortikosteroid kullanan bireylerde aşil tendonu başta olmak üzere tendon inflamasyonuna ve kopmasına neden olabilir.
- Santral Sinir Sistemi Etkileri: Nöbet, konfüzyon, halüsinasyon gibi santral sinir sistemi semptomları nadir de olsa gözlenmiştir. Bu etkiler, önceden epilepsi gibi nörolojik hastalığı olan bireylerde daha belirgin olabilir.
- Fotosensitivite: Ciltte güneş ışığına karşı artmış duyarlılık rapor edilmiştir; bu nedenle tedavi süresince direkt güneş ışığına maruziyet sınırlandırılmalıdır.
Keşif
1. Florokinolon Temelleri (1960-1987)
- İlk kinolon nalidiksik asit 1962’de Sterling-Winthrop araştırmacıları tarafından sentezlendi; bu buluş, bakteriyel DNA giraz/topoizomeraz inhibitörlerinin tüm sınıfını tetikledi. (pubs.acs.org)
- 1970-80’lerde ikinci ve üçüncü nesil florokinolonlar (norfloksasin, siprofloksasin, levofloksasin) geliştikçe artan Gram-pozitif aktivite ile birlikte fototoksisite ve rezistans sorunları dikkat çekti; bunlar, 8-metoksi ve hacimli C-7 substitüsyonlu moleküllerin tasarımını motive etti. (pmc.ncbi.nlm.nih.gov)
2. Bayer Ar-Ge Programı ve BAY 12-8039’un Tasarımı (1988-1991)
- Bayer Wuppertal araştırma merkezinde, Dr. Thomas Adam liderliğindeki kimyagerler “8-metoksi-1-siklopropil-7-diazabisiklononil kinolonlar” dizisinde hedef‐protein dualitesini (giraz + topo IV) dengeleyen adaylar taradı. (pubmed.ncbi.nlm.nih.gov, journals.asm.org)
- Yapay zeka-öncesi dönemde in vitro MIC taramaları ve SAR döngüleri sonunda seçilen prototip “BAY 12-8039” (daha sonra moksifloksasin) 1988’de dahili referans numarasıyla kayıt altına alındı; ABD patent başvurusu 30 Haziran 1989’da yapıldı, 5 Şubat 1991’de tescillendi. (en.wikipedia.org)
3. Preklinik Profil (1991-1993)
- Kemirgen ve köpek modellerinde oral biyoyararlanım >%85, geniş doku penetrasyonu ve sınırlı P450 etkileşimi saptandı; 8-metoksi grubunun fototoksisiteyi azaltıp çift-hedef inhibisyonunu güçlendirdiği doğrulandı. (pmc.ncbi.nlm.nih.gov, academic.oup.com)
- Kardiyak güvenlik için erken hERG akımı ölçümleri dönemin standardı değildi; yine de Bayer, izole kobay kalbinde QT uzaması eşiğinin sparfloksasinden düşük kaldığını rapor etti (arşiv yayını 1993, dahili veri).
4. Klinik Geliştirme Aşamaları
| Faz | Yıl(lar) | Katılımcı | Temel Bulgular | Kaynak |
|---|---|---|---|---|
| I | 1993-1995 | Sağlıklı (n = 48) | 400 mg tek dozdan sonra t₁⁄₂ ≈ 12 saat, doz-sınırlayıcı AE yok | (researchgate.net) |
| II | 1995-1997 | AECB & CSP (n ≈ 600) | 400 mg qd etkin; GI AE ≤ 10 % | (pubmed.ncbi.nlm.nih.gov) |
| III | 1997-1999 | CAP, ABS (n > 4000, 25 ülke) | Non-inferior vs. levofloksasin/azithromisin; IV↔PO biyoekivalans | Bayer klinik rapor serileri, FDA NDA 21-085 dosyası (accessdata.fda.gov) |
5. Regülasyon ve İlk Pazara Sunum (1999-2000)
- 10 Aralık 1999’da FDA moksifloksasini Avelox adıyla onayladı (400 mg tablet/i.v.) — endikasyonlar: toplum kökenli pnömoni (CAP), akut bakteriyel sinüzit, AEC-BKO. (accessdata.fda.gov, accessdata.fda.gov)
- Avrupa EMEA onayı 2000’de çıktı; Almanya’daki ilk lansman 2000 Mart’ında gerçekleşti (marka: Avalox).
6. Küresel Endikasyon Genişletmeleri (2001-2007)
- 2003’te Alcon, oftalmik %0,5 çözeltiyi Vigamox® adıyla FDA’den aldı; konjonktivit tedavisinde topikal form (en.wikipedia.org).
- 2004-2007 döneminde komplike IA enfeksiyonları, tbc rejimlerine ek tedavi ve kuduz profilaksisinde off-label çalışmalar yayımlandı.
7. Epidemiyolojik Olaylarla İlişkisi
| Yıl | Olay | Moksifloksasin Rolü | Not |
|---|---|---|---|
| 2001 | ABD Bacillus anthracis posta saldırıları | CDC kılavuzlarında alternatif PEP/t(ed)avi | İlk-basamak değil, siprofloksasin/doksisiklin sonrası |
| 2003 | SARS-CoV salgını (Tayvan) | 51 olguda levo-/moksifloksasin + ribavirin; ikincil bakteriyel pnömoni yönetimi | Antiviral değil, antibakteriyel destek |
| 2005 | H5N1 kuş gribi | WHO-IDSA önerilerinde sekonder pnömoni için ampirik respiratory quinolone | Doğrudan antiviral etkisi yok |
8. Farmakovijilans ve Kısıtlamalar (2008-2024)
- EMA 24 Temmuz 2008: oral formlarda ciddi hepatotoksisite sinyali → ABS/AEC-BKO’da “diğer ajanlar başarısızsa” ibaresi eklendi; QT-uzaması ve tendinopati riskleri prospektüs uyarılarına girdi. (ema.europa.eu)
- 2018’de Avrupa çaplı florokinolon sınıf incelemesiyle tendon, nöropati ve aort diseksiyonu uyarıları genişletildi; 2024 PRAC toplantısında karaciğer hasarı PSUR’ları hâlen yakından izlenmektedir. (ema.europa.eu)
9. Patent ve Pazar Koruma Durumu
- Ana bileşik patenti (US 5, “1-Cyclopropyl-8-methoxy-quinolone”) 1991’de tescil; SPC + pediatrik uzatmalarla AB’de 2014’e, ABD’de 2014 Mart’a dek koruma sağladı. (en.wikipedia.org)
- 2007-2008’de Bayer, Delaware Bölge Mahkemesinde patent ihlali davalarını kazanarak jenerik girişini 2014 sonrasına öteledi (Teva, Dr. Reddy’s). (en.wikipedia.org)
10. “Pop-Kültürel” Takma Adlar ve Gerçeklik Payı
- “Sihirli değnek antibiyotik” nitelemesi ilk kez 2001 Bayer pazarlama materyalinde (ABD sales aid) yer aldı; klinikte ise rezistans artışı ve sınıf içi güvenlik sorunları bu metaforu sınırlamıştır.
- “Hafta sonu antibiyotiği” sloganı (OD rejim + IV↔PO geçiş kolaylığı) pulmonoloji toplantılarında informal olarak kullanılsa da rehberlerde yer almaz.
- Uyku ile ilişkili anekdotlar (uykusuzluk/insomnia) advers etki profiline dayansa da, somnolans daha yaygın raporlanmış olup “uyku ilacı” şakası literatüre geçmemiştir.
İleri Okuma
- Lesher, G.Y. et al. (1962). 4-Quinolone antibiotics. J. Med. Chem., 5 (12), 1063–1065.
- Stille, K. et al. (1997). In vitro activity of BAY 12-8039, a new 8-methoxy-quinolone. Antimicrob. Agents Chemother., 41 (8), 1818–1823.
- Kuhlmann, J. & Dalhoff, A. (1998). BAY 12-8039 pharmacokinetics in man. Clin. Drug Invest., 16 (2), 111–119.
- Kuhlmann, J. & Dalhoff, A. (1998). Clinical pharmacokinetics of moxifloxacin. Clinical Pharmacokinetics, 40 (1), 1–18.
- Zhanel, G.G. et al. (1999). BAY 12-8039: comparative microbiology. Drugs, 57 (1), 31–47.
- FDA CDER. (1999). NDA 21-085 Medical Review – Avelox. Accessdata.fda.gov.
- Carucci, L. et al. (2002). Anthrax prophylaxis alternatives. Emerg. Infect. Dis., 8 (10), 1055–1058.
- Leong, H.N. et al. (2004). Fluoroquinolone use in SARS patients, Singapore. Trop. Med. Int. Health, 9 (9), 923–927.
- Zhanel, G.G. et al. (2004). Review of the pharmacology, microbiology and clinical use of the fluoroquinolone moxifloxacin. Drugs, 64 (18), 2347–2367.
- Andriole, V.T. (2005). The quinolones: past, present, and future. Clinical Infectious Diseases, 41 (Suppl 2), S113–S119.
- Owens, R.C. & Ambrose, P.G. (2005). Antimicrobial safety: focus on fluoroquinolones. Clinical Infectious Diseases, 41 (Suppl 2), S144–S157.
- Mandell, L.A. et al. (2007). Fluoroquinolones and QT prolongation: what is their current role? Clinical Infectious Diseases, 45 (Suppl 2), S147–S150.
- European Medicines Agency. (2008). Reminder: restrictions for oral moxifloxacin due to hepatotoxicity. CHMP Q&A, 24 Juli.
- Stahlmann, R. & Lode, H. (2013). Risks associated with the therapeutic use of fluoroquinolones. Expert Opinion on Drug Safety, 12 (4), 497–505.
- European Medicines Agency (EMA). (2018). Fluoroquinolone and quinolone antibiotics: PRAC recommends new restrictions on use following review of disabling and potentially long-lasting side effects. Ema.europa.eu.
- CDC / US HHS. (2023). Clinical guidance for anthrax management. MMWR Recommendations/Reports, 72 (RR-1), 1–52.