─────────────────────────────────────────
İçindekiler
I. ETİMOLOJİ VE TARİHSEL ARKA PLAN
Rifampisin adı, iki kökenin sentezinden türemektedir: İtalyanca’da “Rififi” olarak bilinen 1955 yapımı Fransız kriminal filmine yapılan kültürel bir atıf ve antibiyotiğin elde edildiği toprak bakterisi Amycolatopsis rifamycinica’ya verilen bilimsel isim. Birleşik Krallık ve Avrupa’da yaygın kullanımda “rifampicin” olarak yazılırken, Amerika Birleşik Devletleri ve diğer bazı ülkelerde “rifampin” adıyla anılmaktadır. Bu terminolojik ikililik, ilacın hem uluslararası klinik uygulamadaki yerini hem de farklı bilimsel geleneklerin kesiştiği kökenini simgelemektedir.
İlacın keşif öyküsü, 1950’lerin ortasına ve Milano’daki Dow-Lepetit araştırma laboratuvarlarına uzanmaktadır. Pietro Sensi ve arkadaşları, 1957 yılında Fransız Rivierası yakınlarında alınan toprak örneklerinden izole edilen Streptomyces mediterranei (sonradan Amycolatopsis rifamycinica olarak yeniden sınıflandırılan) adlı bir aktinobakteri türünden rifamisin ailesi bileşiklerini başarıyla elde ettiler. Bu keşfin ardından gerçekleştirilen yarı sentetik kimyasal modifikasyonlar, 1966 yılında rifampisinin sentezlenmesiyle sonuçlandı; ilaç, 1968 yılında klinik kullanım için onay aldı ve o tarihten bu yana tüberküloz başta olmak üzere pek çok ciddi bakteriyel enfeksiyonun tedavisinde vazgeçilmez bir yer edinmiştir.
II. KİMYASAL YAPI VE FİZİKOKİMYASAL ÖZELLİKLER
Rifampisin, C₄₃H₅₈N₄O₁₂ molekül formülüne sahip olup molekül ağırlığı yaklaşık 823 g/mol’dür. Yapısal açıdan değerlendirildiğinde, makrosiklik halka üzerinde konumlanmış bir naftiridimid kromofor çekirdeği içermektedir; bu temel iskelet üzerine çeşitli fonksiyonel gruplar eklenmiştir. Madde, oda sıcaklığında kırmızımsı kahverengiden kahverengimsi kırmızıya uzanan bir renk skalasında kristal toz formunda bulunmaktadır. Suda düşük çözünürlük gösterse de organik çözücülerde görece iyi çözünmektedir; bu özelliği, farmasötik formülasyon süreçlerini doğrudan etkileyen önemli bir parametredir.
Molekülün temel iskeletini oluşturan ansamisin (ansa) yapısı, bir aromatik kromofor çekirdeği ile bunu çevreleyen alifatik bir köprüden meydana gelmektedir. Bu ansamakrolid mimarisi, rifampisinin RNA polimeraz enzimini seçici biçimde tanımasına ve inhibisyon kompleksi oluşturmasına zemin hazırlayan özgün üç boyutlu konfigürasyonun kaynağıdır. Rifampisin, yarı sentetik bir bileşik olup rifamisin SV’nin kimyasal dönüşümü yoluyla elde edilmektedir; bu işlem sırasında 3 numaralı konumdaki hidroksi grubuna 4-metil-1-piperazinoaminoimin yan zinciri bağlanmaktadır. Söz konusu modifikasyon, ana bileşiğe kıyasla antibakteriyel aktivitenin ve farmakokinetik profil ile biyoyararlanımın belirgin biçimde iyileşmesini sağlamaktadır.
III. ETKİ MEKANİZMASI: RNA POLİMERAZ İNHİBİSYONU
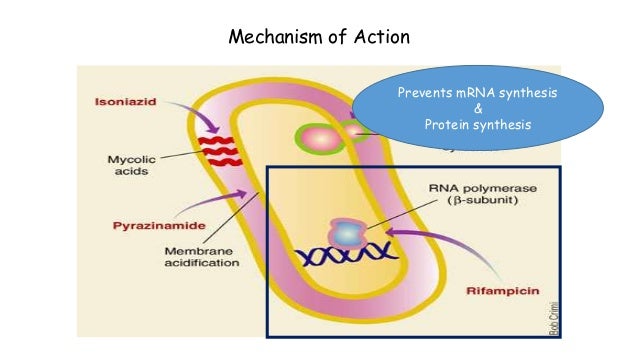
Rifampisinin antimikrobiyal etkinliğinin temelinde, bakteriyel DNA’ya bağımlı RNA polimerazın son derece seçici ve güçlü inhibisyonu yatmaktadır. Bu enzim, prokariyotik hücrelerde DNA şablonundan RNA zincirinin sentezlenmesini, yani transkripsiyon sürecini katalize etmektedir; dolayısıyla tüm gen ekspresyonunun ve nihayetinde protein sentezinin odak noktasını oluşturmaktadır. Rifampisin, RNA polimerazın beta (β) alt birimine bağlanarak enzimin aktif merkezine yakın konumdaki RNA çıkış kanalını sterik olarak tıkamaktadır. Başlangıç aşamasını geçmiş bir transkripsiyonu engelleyememekle birlikte, RNA zincirinin büyümesinin henüz 2-3 nükleotit düzeyinde olduğu erken uzama aşamasını baskılamaktadır.
Rifampisinin hedeflediği β alt birimini kodlayan rpoB geni, antibiyotiğe karşı gelişen direnç mutasyonlarının neredeyse tamamının lokalize olduğu bölgedir. Bu mutasyonlar, ilacın bağlanma afinitesini dramatik biçimde azaltmakta ve ilaçla muamele edilmiş kültürlerde çok hızlı biçimde seçilmektedir. Klinik açıdan kritik bir öneme sahip bu durum, rifampisinin neden asla monoterapi şeklinde kullanılmaması gerektiğini de açıklamaktadır. Tek başına uygulandığında, spontan direnç mutasyonları taşıyan bakteri klonları hızla baskın popülasyona dönüşebilmekte ve tedavinin kısa sürede başarısızlıkla sonuçlanmasına yol açmaktadır. Memeli RNA polimerazının yapısal farklılıkları sayesinde bu bağlanma çok daha düşük afiniteyle gerçekleştiğinden, rifampisin memeli hücrelerine yönelik son derece düşük toksik potansiyele sahiptir.
IV. ANTİMİKROBİYAL SPEKTRUM VE KLİNİK ENDİKASYONLAR
4.1. Mikobakteriyal Enfeksiyonlar
Rifampisinin klinik uygulamadaki en kritik endikasyonu, dünya genelinde önde gelen bulaşıcı hastalık ölüm nedenlerinden biri olan tüberkülozun tedavisidir. Mycobacterium tuberculosis’e karşı güçlü bakterisidal aktivite gösteren rifampisin, Dünya Sağlık Örgütü’nün standart kısa kurs tüberküloz tedavi rejimlerinin temel taşını oluşturmaktadır. İzoniazid, pirazinamid ve etambutol ile birlikte dört ilaçlı ilk iki aylık yoğun faz tedavisinin ardından, konsolidasyon aşamasında izoniazid ile birlikte uygulanmaya devam etmektedir. Mycobacterium leprae’ye karşı da etkili olması nedeniyle cüzzam tedavisinde, özellikle multibasiller hastalık formlarında kombine rejimlerin ayrılmaz bir bileşeni olarak yer almaktadır.
4.2. Diğer Bakteriyel Enfeksiyonlar
Rifampisinin antimikrobiyal spektrumu mikobakterilerle sınırlı değildir. Gram pozitif ve bazı gram negatif patojenler üzerinde de kayda değer aktivite göstermektedir. Metisiline dirençli Staphylococcus aureus (MRSA) enfeksiyonlarında rifampisin, tek başına kullanımda hızlı direnç gelişimi nedeniyle her zaman fusidik asit, trimethoprim-sülfametoksazol veya vankomisin gibi eşlik eden ilaçlarla kombinasyon halinde kullanılmaktadır. Meningokokal hastalık profilaksisinde bağımsız bir endikasyon alanı bulan rifampisin, özellikle Neisseria meningitidis maruziyeti sonrası temas profilaksisinde tercih edilebilecek seçeneklerden biridir. Bruselloz tedavisinde de doksisiklin ile kombinasyon rejimlerinin bir parçasını oluşturmaktadır.
V. FARMAKOKİNETİK VE FARMAKODİNAMİK PROFİL
Rifampisinin oral biyoyararlanımı yüksektir ve genellikle %90’ın üzerinde seyretmektedir; ancak bu değer, besinlerle eş zamanlı alındığında azalmaktadır. Bu nedenle ilacın yemekten en az 30 dakika önce, tercihen aç karnına alınması önerilmektedir. Dağılım hacmi geniştir ve rifampisin çoğu doku ile vücut boşluğuna penetre olabilmektedir; bu özelliği, beyin-omurilik sıvısına geçişini ve hücre içi patojenlere karşı etkinliğini sağlamaktadır. Karaciğerde yoğun ilk geçiş metabolizmasına uğrayan rifampisin, ağırlıklı olarak safraya, kısmen de idrarla atılmaktadır. Yarılanma ömrü 1 ile 5 saat arasında değişmekte olup ilginç biçimde, ilacın kendi metabolizmasını zamanla hızlandırmasından dolayı tedavinin ilk haftalarında yarılanma ömründe belirgin bir kısalma gözlemlenmektedir.
Hücre içi penetrasyon kapasitesi rifampisini özellikle mikobakteri enfeksiyonlarında değerli kılmaktadır. Mycobacterium tuberculosis, makrofaj fagolizozomları içinde hayatta kalarak konağın bağışıklık yanıtından korunmaktadır. Rifampisin, bu hücre içi rezervuara ulaşarak saklanan bakterileri etkili biçimde hedef alabilmektedir; bu özelliği, uzun ve karmaşık tedavi süreçleri gerektiren tüberküloz gibi hastalıklarda ilacın başarısının temel açıklayıcısıdır.
VI. İLAÇ ETKİLEŞİMLERİ: CYP450 İNDÜKSİYONU
Rifampisin, klinisyenlerin özellikle dikkatini gerektiren güçlü bir sitokrom P450 (CYP450) enzim indükleyicisidir. CYP3A4, CYP2C9, CYP2C19, CYP2B6 ve diğer CYP izozimlerinin ekspresyonunu artıran rifampisin, bu enzimlerin yavaş metabolize ettiği pek çok ilacın plazma konsantrasyonlarını dramatik biçimde düşürmektedir. Bu etkileşim mekanizması, yalnızca enzimler üzerinden değil, P-glikoprotein ve diğer membran taşıyıcı proteinler üzerinden de işlemekte; ilacın absorpsiyonunu, dağılımını ve atılımını etkileyen kapsamlı bir farmakokinetik değişikliğe yol açmaktadır.
Klinik önemi yüksek etkileşimler arasında özellikle antiretroviral ilaçlarla (HIV tedavisinde kullanılan proteaz inhibitörleri ve non-nükleozid ters transkriptaz inhibitörleri), oral kontraseptiflerle, varfarinle, siklosporin gibi immünosüpresanlarla, metadon ve bazı antifungal ve antikonvülzan ilaçlarla yaşananlar sayılabilir. Vorikonazol, telaprevir ve sakinavir-ritonavir kombinasyonu rifampisin ile birlikte kullanımı kontrendike olan ilaçlar arasındadır. Rifampisin tedavisine başlama ya da sonlandırma aşamalarında, eşzamanlı olarak kullanılan tüm ilaçların dozlarının yeniden değerlendirilmesi zorunludur.
VII. YAN ETKİLER VE GÜVENLİLİK PROFİLİ
7.1. Karaciğer Toksisitesi
Rifampisinin en ciddi güvenlilik kaygısı, hepatotoksik potansiyelidir. İlaç, karaciğer enzim değerlerinde geçici yükselmeden fulminan hepatite kadar uzanan geniş bir klinik tablo yelpazesiyle ilişkilendirilebilmektedir. Alkol kullanımı, mevcut karaciğer hastalığı veya siroz varlığı ve izoniazid gibi diğer hepatotoksik ilaçlarla eş zamanlı kullanım, karaciğer hasarı riskini belirgin biçimde artırmaktadır. Bu nedenle önceden karaciğer hastalığı tanısı konmuş hastalar, porfiride ve periferik nörit varlığında rifampisin kullanımı kontrendikedir. Tedavi süresince karaciğer fonksiyon testlerinin düzenli aralıklarla izlenmesi, klinik yönetimin temel bir gerekliliklerinden biridir.
7.2. Karakteristik Renk Değişimi
Rifampisinin en bilinen ve hastalar tarafından en sık bildirilen yan etkisi, vücut sıvılarında gözlemlenen karakteristik turuncu-kırmızı renk değişimidir. İdrar, ter, tükürük, gözyaşı ve dışkı bu renksel dönüşümden etkilenmekte olup bu durum zararlı olmamakla birlikte hastalar için genellikle beklenmedik ve endişe verici bir bulgu niteliği taşımaktadır. Gözyaşlarının bu pigmentle boyanması, kontakt lens kullanıcılarında kalıcı lens lekesine yol açabilmektedir; bu nedenle rifampisin tedavisi süresince yumuşak kontakt lens kullanımından kaçınılması gerekmektedir. Benzer biçimde, iç çamaşırlarında uzaklaştırılması güç izler bırakabilmektedir.
7.3. Diğer Yan Etkiler
Diğer görece yaygın yan etkiler arasında yorgunluk, uyuşukluk, baş ağrısı ve sersemlik hissi gibi nöropsikiyatrik semptomlar ile iştahsızlık, bulantı, karın ağrısı ve gaz şikayetlerinden oluşan gastrointestinal belirtiler sayılmaktadır. Gözlerde kızarıklık da sıklıkla bildirilen bulgular arasında yer almaktadır. Dermatolojik reaksiyonlar, kızarıklık, kaşıntı ve ürtiker ile tezahür edebilmektedir. Haftada iki kez veya daha seyrek aralıklarla uygulanan aralıklı doz rejimleri, günlük dozlamaya kıyasla daha yüksek immunolojik aracılıklı reaksiyon riskiyle ilişkilendirilmektedir.
VIII. DAYANIKLILIK (DİRENÇ) MESELESİ VE KLİNİK YÖNETİM
Rifampisine karşı direnç gelişimi, halk sağlığı açısından son derece kritik bir sorun oluşturmaktadır; zira rifampisin direnci, çok ilaca dirençli tüberkülozun (MDR-TB) tanımsal kriterleri arasında yer almaktadır. Küresel ölçekte MDR-TB olgu sayısı artmaya devam etmekte ve bu durum, ikinci basamak ilaçların kullanılmasını zorunlu kılmakta, tedavi süreçlerini zorlaştırmakta ve tedavi maliyetlerini katlamaktadır. Rifampisinoazol direncini tespit eden GenoType MTBDR ve Xpert MTB/RIF gibi hızlı moleküler testler, MDR-TB tanısının süratle konulmasını mümkün kılmakta ve uygun tedavi rejimlerinin gecikmeksizin başlatılmasına zemin hazırlamaktadır.
Direnç gelişiminin önlenmesi amacıyla rifampisin, tüberküloz ve cüzzam tedavisinde her koşulda ve tedavinin başından sonuna kesintisiz biçimde çok ilaçlı rejimler dahilinde kullanılmalıdır. Tedavi süresince ilaç uyumunun izlenmesi, direkt gözlem altında tedavi (DGAT) programlarının uygulanması ve hastanın tedaviyle ilgili endişe ve sorularına duyarlı bir yaklaşım sergilenmesi, direnç gelişimini önlemeye yönelik bütüncül bir klinik yönetim stratejisinin vazgeçilmez unsurlarını oluşturmaktadır.
IX. FARMASÖTİK FORMLAR VE PİYASADA YER ALAN ÜRÜNLER
Rifampisin, farklı klinik gereksinimlere yanıt verecek biçimde çeşitli farmasötik formülasyonlarda üretilmektedir: film kaplı tabletler, draje, kapsül ve enjeksiyon preparatı şeklinde piyasaya sunulmaktadır. Rimactan, Eremfat ve Rifa başlıca jenerik ve marka isimleri arasında yer almakla birlikte, Türkiye’de Rifadin (Sanofi Aventis) ve Rifcap (Koçak Farma) markaları altında da satılmaktadır. Bunların yanı sıra, tüberküloz tedavisinde tedavi uyumunu kolaylaştırmak ve yanlış monoterapi uygulaması riskini azaltmak amacıyla izoniazid, pirazinamid ve etambutol gibi diğer antitüberküloz ilaçlarla bir arada sunulan sabit doz kombinasyon preparatları da mevcuttur.
Peroral monoterapi amaçlı standart kullanımda, yetişkinler için önerilen günlük doz genellikle vücut ağırlığına göre belirlenmekte olup kılavuzlar tipik olarak 8-12 mg/kg dozaj aralığını tanımlamaktadır. Uzman hekimler tarafından belirlenen bireyselleştirilmiş dozaj şemaları, hem endikasyona hem de hastaya özgü farmakokinetik değişkenlere göre özenle uyarlanmalıdır.
─────────────────────────────────────────
Keşif
───────────────────────────────────────────────
I. TOPRAĞI DİNLEMEK: MİKROBİYOLOJİNİN YENİ ÇAĞI (1940’lar)
İkinci Dünya Savaşı’nın son yıllarında, Selman Waksman’ın New Jersey’deki Rutgers Üniversitesi laboratuvarlarında başlattığı devrimci program, tıp tarihinin en verimli dönemlerinden birinin fitilini yakıyordu. Waksman ve öğrencileri, toprak örneklerinde yaşayan aktinobakteri türlerinin —özellikle Streptomyces cinsine ait bakterilerin— olağanüstü kimyasal çeşitlilik ürettiklerini keşfetmişlerdi. 1943’te streptomisinin bulunması, tüberküloza karşı ilk kez gerçek anlamda etkili bir silahın elde edilmesi demekti ve bu buluş, yalnızca bir antibiyotik keşfi değil, toprak mikrobiyolojisini sistematik olarak taramaya dayanan tamamen yeni bir araştırma paradigmasının ilanıydı.
Waksman’ın metodolojisi zamanla bir ekole dönüştü. Dünyanın dört bir yanındaki araştırmacılar, farklı coğrafyaların topraklarından izole edilen aktinobakteri kültürlerini ekrana çekmeye başladılar. Her toprak örneği potansiyel olarak bilinmeyen bir bileşik hazinesi taşıyordu; yalnızca hangi mikroorganizmaların hangi molekülü ürettiğini ve bu moleküllerin hedef bakterilere nasıl etki ettiğini anlayabilmek için doğru yöntemi bulmak gerekiyordu. Bu heyecan verici biyolojik avın ortasında, İtalya’nın kuzeyindeki bir fabrika binasında, daha önce hiçbir dünya haritasında işaretlenmemiş küçük bir araştırma grubu sahneye çıkacaktı.
* * *
II. MİLANO’NUN GİZLİ LABORATUVARI: DOW-LEPETIT VE İLK KARŞILAŞMA (1957)
1950’lerin ortasında Milano’nun sanayi semtlerinden birinde, Grup Lepetit’in araştırma bölümü sessiz ama kararlı bir çalışmanın içindeydi. Kimyager Pietro Sensi, mikoloji ve mikrobiyoloji kökenli bir ekibi bünyesinde toplayan bu birimin yöneticisiydi. Sensi, Waksman’ın paradigmasından etkilenmekle birlikte araştırmasını yalnızca bilinen Streptomyces türlerine değil, o güne kadar neredeyse hiç incelenmemiş aktinobakteri gruplarına yöneltme kararı almıştı.
1957 yılında laboratuvara ulaşan bir toprak örnekleri koleksiyonunun içinde, Fransız Rivierası kıyılarından —büyük olasılıkla Nice yakınlarından— alınan bir numune vardı. Bu örnekte izole edilen ve başlangıçta Streptomyces mediterranei adıyla sınıflandırılan bir aktinobakteri türü, kültür ortamında beklenmedik pigmentler ve bileşikler üretiyordu. Sensi ve ekibinin dikkati, bu organizmanın salgıladığı kızıl-kahverengi sıvının güçlü antibakteriyal aktivite sergilemesi üzerine yoğunlaştı. Kimyasal analiz, yeni bileşiklerin hiçbir bilinen antibiyotik sınıfıyla örtüşmediğini ortaya koyuyordu; bu anlamlı bir işaretti: Elimde yeni bir şey var.
Sensi’nin yanında çalışan Maria Teresa Timbal ve diğer araştırmacılar, bu ilk bileşiği saflaştırma sürecinde kritik roller üstlendiler. Kaotik kültür karışımından saf fraksiyonlar elde edilmesi, o yıllarda son derece meşakkatli bir işti: Çözücü ekstraksiyon, kromatografi sütunları ve kristalizasyon adımları sabır ve teknik ustalık gerektiriyordu. Timbal, saflık kontrol süreçlerinin büyük bölümünü yürüterek yeni bileşiğin kimliğinin netleşmesine katkıda bulundu. Sensi ise bu bileşikler grubunu, keşfedildikleri bölgeye ve ürettikleri organizmanın adına bir atıfla “rifamisin” olarak adlandırmayı önerdi.
* * *
III. RİFAMİSİN AİLESİNİN ÇÖZÜMLENMESI: KİMYASAL HARİTA (1957–1963)
3.1. İlk Bileşikler ve Yapısal Bulmaca
İlk saflaştırma çalışmaları, tek bir bileşik değil, birbirine yakın ama farklı bileşiklerin bir ailesiyle karşı karşıya olduklarını ortaya koydu. Rifamisin A, B, C, D ve E olarak adlandırılan bu fraksiyonlar, farklı biyolojik aktivite ve kimyasal kararlılık profilleri sergiliyordu. Rifamisin B, yapısal olarak en istikrarlısıydı ve aerobik koşullarda en yüksek verimi sağlıyordu; ancak antibakteriyal aktivitesi yetersizdi. Buna karşın, sonraki tüm çalışmaların öncülü olan bu bileşik, kimyasal dönüşüm için mükemmel bir başlangıç noktası sunuyordu.
Rifamisin ailesinin yapısal çözümlenmesi, 1960’ların başında Ciba-Geigy araştırmacıları ve birkaç bağımsız kimya grubu tarafından gerçekleştirildi. Kritik katkı, Piero Piero’nun bağlantılı çalışmalarının yanı sıra İsviçreli kimyager Vladimir Prelog’un grubundan geldi. Prelog, ansamakrolid iskeleti olarak tanımlanan yapıyı —bir aromatik kromofor ile bunu çevreleyen alifatik bir köprüden oluşan makrosiklik halkayı— ilk kez net biçimde tarif etti. Bu yapısal çerçeve, aynı zamanda rifampisin molekülünün neden antibakteriyal aktivite gösterdiğini de öngörmek için bir kavramsal zemin sağlıyordu.
3.2. Rifamisin SV: Doğanın Sunduğu Aracı Molekül
Rifamisin B’nin asetik asitli ortamda bozunmasıyla elde edilen rifamisin SV, 1960’ların başında birden ilgi odağı haline geldi. Bu bileşik, rifamisin B’ye kıyasla dramatik biçimde daha yüksek antimikrobiyal aktivite sergiliyordu ve özellikle Mycobacterium tuberculosis’e karşı etkisi son derece dikkat çekiciydi. Parenteral formülasyonlarla yapılan erken klinik denemeler umut verici sonuçlar doğurdu; ancak rifamisin SV’nin oral biyoyararlanımı düşüktü ve karaciğer metabolizması karşısında çok hızlı bozunma eğilimi gösteriyordu. Bu sınırlamalar, ilacı geniş çaplı klinik kullanım için yetersiz kılıyordu.
Araştırmacılar açısından bu bir çıkmaz değil, bir davetiyeydi. Rifamisin SV’nin kimyasal iskeleti güçlüydü ve etki mekanizması —henüz tam olarak bilinmese de— özgündü. Yapının değiştirilmesi gerekiyordu; ama nereye ve nasıl müdahale edilmeli? Bu soruların yanıtı, Milano’daki laboratuvarda yürütülen yoğun yarı sentetik kimya çalışmalarında saklıydı.
* * *
IV. SENTEZ: RİFAMPİSİNİN DOĞUŞU (1963–1968)
Rifampisin, 1963 yılında Lepetit araştırmacıları —ağırlıklı olarak Piero Sensi, Pinhas Margalith ve Giuliana Gallo— tarafından sentezlendi. Rifamisin SV’nin 3 numaralı hidroksi grubuna 4-metil-1-piperazinoaminoimin yan zincirinin eklenmesi, hem oral biyoyararlanımı hem de antimikrobiyal güç bakımından çarpıcı bir sıçrama sağladı. Bu modifikasyon, o güne kadar yapılmış benzer kimyasal müdahalelerin içinde en verimli olanıydı; neredeyse tesadüfen bulunmuş gibi görünse de asıl gerçek, sistematik kimyasal tarama programının mantıksal bir meyvasıydı.
Yeni bileşiğin hayvan modellerinde gösterdiği etkinlik, araştırmacıları heyecanlandırdı. Tüberkülozlu deney hayvanlarında, rifampisinin küçük dozları, daha önceki tüm bileşiklerin çok üzerinde bir aktivite sergiliyordu. Üstelik oral yoldan verilebiliyordu; bu, streptomisinin baş edemediği lojistik bir üstünlüktü. Kısmen doku içi dağılımının genişliğinden, kısmen de lipid çözünürlüğünün sağladığı hücre içi penetrasyon kapasitesinden beslenen bu etkililik, bileşiği çağının en umut verici antitüberküloz adayına dönüştürdü.
1965’ten itibaren klinik denemeler başladı. İtalyan, Fransız ve İngiliz merkezlerinde yürütülen Faz I ve Faz II çalışmaları, ilacın güvenlilik ve etkinlik profilini ortaya koydu. Gastrointestinal yan etkiler ve karaciğer enzim yükselmesi en önemli güvenlilik sinyalleriydi; ancak bunlar kabul edilebilir sınırlar içindeydi. 1968 yılında rifampisin, İtalya ve ardından diğer Avrupa ülkelerinde klinik kullanım için onaylandı. Aynı yıl dünyaya açılan bu onay, tüberküloz tedavisinin tarihinde bir dönüm noktasını işaret ediyordu.
* * *
V. BÜYÜK BİR BULMACIN ÇÖZÜMÜ: NEDEN ETKİLİ? RNA POLİMERAZ HİKÂYESİ (1968–1980)
Rifamisin grubunun antibakteriyal aktivitesinin altında yatan mekanizma, 1960’ların sonunda hâlâ tartışmalıydı. İlk hipotezler, ilacın hücre duvarı sentezini bozduğunu ya da membran bütünlüğünü engellediğini öne sürüyordu; ancak bu açıklamaların hiçbiri deneysel verilerin tamamıyla örtüşmüyordu. Yanıt, moleküler biyolojinin henüz filizlenmekte olduğu bir dönemde geldi.
1968 yılında Wehrli ve Staehelin, Ciba-Geigy’deki araştırmaları aracılığıyla rifampisinin bakteriyel DNA’ya bağımlı RNA polimerazı inhibe ettiğini gösterdi. Bu, dönemin standartlarına göre son derece şaşırtıcı bir bulguydu; zira RNA polimeraz, tüm gen ekspresyonunun merkezinde yer alan ve o yıllarda büyük bir merakla incelenen bir enzimdi. Wehrli ve ekibi, rifampisinin enzimin β alt birimine bağlandığını ve RNA zincirinin uzama sürecinin erken aşamalarını bloke ettiğini in vitro deneylerle kanıtladı.
Bu keşfin önemi birkaç katmanda değerlendirilebilir. Birincisi, rifampisin memeli RNA polimerazını çok daha düşük bir afiniteyle bağlıyordu; bu nedenle terapötik konsantrasyonlarda konağa minimal toksisite gösteriyordu. İkincisi, etki mekanizmasının bakterisidal niteliği —yani sadece baktariyostatik değil, bakteri öldürücü olması— hem klinik etkinliği hem de tedavi sürelerinin kısaltılabilmesi açısından belirleyici bir önem taşıyordu. Üçüncüsü ve belki de en önemlisi, bu mekanizma rifampisini o güne kadar bilinen tüm antibiyotik sınıflarından yapısal ve işlevsel olarak ayırıyordu.
1970’ler boyunca Escherichia coli başta olmak üzere çeşitli bakteri türleri üzerinde yürütülen çalışmalar, rifampisin-RNA polimeraz etkileşiminin biyokimyasal ayrıntılarını giderek daha yüksek çözünürlükte ortaya koydu. Rifampisinin bağlandığı bölge olan “rifampisin direnci belirleyici bölgesi” (RRDR), β alt biriminde net biçimde tanımlandı ve bu bölgedeki mutasyonların ilaç direnciyle nasıl ilişkili olduğu sistematik olarak haritalandırıldı. Söz konusu erken genetik ve biyokimyasal çalışmalar, sonraki on yıllarda direnç izleme stratejilerinin temelini oluşturacaktı.
* * *
VI. KLİNİK DEVRİMİN İÇİNDE: TÜBERKÜLOZ TEDAVİSİNİN YENİDEN YAZILANMASI (1970’ler–1980’ler)
6.1. Kısa Kurs Kemoterapinin Doğuşu
Rifampisin öncesinde tüberküloz tedavisi, 18 ila 24 ay süren uzun, yorucu ve hasta açısından son derece yıkıcı bir süreçti. Streptomisin, izoniazid ve paraaminosalisilik asit üzerine kurulu rejimler kısmen etkili olsa da hastalarda tedaviye devamı sağlamak son derece güçtü; bu da direnç gelişimine zemin hazırlayan en önemli etkenlerden biriydi.
1970’lerin başında British Medical Research Council’ın öncülüğünde başlatılan kapsamlı klinik araştırmalar serisinin yöneticisi Wallace Fox ve ekibi, rifampisin ile izoniazid kombinasyonunun dikkat çekici bir potansiyel sergilediğini fark etti. Doğu Afrika, Hong Kong ve Singapur’da yürütülen uluslararası deneyler, rifampisin içeren rejimlerin tedavi sürelerini dramatik biçimde kısaltabileceğini gösterdi. Pirazinamidin eklenmesiyle birlikte olgunlaşan üçlü-dörtlü kombinasyon rejimleri, tüberküloz tedavisini 6 aya indirdi. Bu başarı, modern kısa kurs kemoterapinin doğumuydu.
Fox’un ekibi yalnızca klinik deney tasarımında değil, tedavinin evrensel erişilebilirliği konusunda da öncü bir tutum sergiledi. Gelişmekte olan ülkelerde yürütülen araştırmalar, rifampisin içeren rejimlerin farklı coğrafyalarda, farklı beslenme koşullarında ve farklı epidemiyolojik bağlamlarda tutarlı etkinlik sergilediğini doğruladı. Dünya Sağlık Örgütü, 1980’lerin başında bu kanıta dayalı sonuçları küresel tedavi kılavuzlarına yansıtmaya başladı.
6.2. Cüzzam ve Diğer Endikasyonlar
Rifampisinin antimikrobiyal yelpazesi yalnızca M. tuberculosis ile sınırlı değildi. 1970’lerin ortasında, özellikle Yawalkar ve Vischer’in İsviçre’deki araştırmalarının katkısıyla rifampisinin M. leprae’ye karşı da çarpıcı bakterisidal etkinlik gösterdiği anlaşıldı. O güne kadar cüzzam tedavisi yalnızca dapson üzerine kuruluydu; dapsona dirençli suşların giderek yaygınlaşması büyük bir tıkınmayı simgeliyordu. Rifampisinin tek bir dozda dahi M. leprae yükünü dramatik biçimde düşürebildiğini gösteren denemeler, cüzzamın çok ilaçlı tedavisinin kapısını araladı.
Aynı dönemde rifampisinin streptokok, meningokok ve stafilokoklar üzerindeki etkisi de sistematik olarak araştırıldı. Meningokokal menenjit profilaksisinde kemopreventif ajan olarak kullanımı, özellikle toplu yaşam alanlarında temas sonrası uygulamalarda etkili bir seçenek olarak kılavuzlara girdi. Metisiline dirençli Staphylococcus aureus ile mücadelede fusidik asit veya diğer ajanlarla kombine kullanımı ise 1980’lerin hastane enfeksiyon kontrolünde yavaş yavaş yerini bulmaya başladı.
* * *
VII. DİRENÇ: İLAÇ KULLANAN İNSANLIĞIN FATURASI (1990’lar–2000’ler)
1990’ların başı, tüberküloz tarihinin en karanlık dönemlerinden birinin eşiğiydi. Sovyetler Birliği’nin dağılmasının ardından Doğu Avrupa ve Orta Asya’da çöküşe uğrayan sağlık altyapısı, HIV pandemisinin Afrika’da ve dünya genelinde yol açtığı bağışıklık zayıflamasıyla birleşince tüberküloz vakaları patlama yaşadı. Daha da endişe verici olan, rifampisin direncinin —ve çok ilaca direncin— bu ortamda inanılmaz bir hızla yayılmasıydı.
Çok ilaca dirençli tüberküloz (MDR-TB), en az rifampisin ve izoniazide eş zamanlı direnç olarak tanımlanmaktadır; bu tanım, yalnızca tıbbi değil, siyasi ve sosyal boyutlarıyla da derin bir kriz anlamına geliyordu. New York’ta, Moskova’da ve Mumbai’de neredeyse eş zamanlı biçimde ortaya çıkan MDR-TB salgınları, rifampisinin nasıl kullanılması gerektiğine dair tüm öğretilerin ciddiye alınmadığında ne tür sonuçlar doğuracağını dramatik biçimde göstedi. Daha sonra kapsamlı genetik çalışmalarla net biçimde ortaya kondu: Direncin neredeyse tamamı, RNA polimeraz β alt birimini kodlayan rpoB genindeki tek nokta mutasyonlarından kaynaklanıyordu. Birkaç kritik kodon pozisyonu —531, 516 ve 526 numaralı kodonlar— vakaların büyük çoğunluğunu açıklıyordu.
Bu bulgular, moleküler epidemiyoloji açısından son derece değerliydi: Direnç mutasyonlarını taramaya yönelik PCR bazlı testler geliştirilebilir ve rifampisin duyarlılığı, haftalar süren kültür yöntemlerini beklemeksizin saatler içinde belirlenebilirdi. Nitekim 2000’lerin başında geliştirilen Line Probe Assay teknolojisi ve ardından gelen Xpert MTB/RIF testi, rifampisin direncini hem de Mycobacterium tuberculosis varlığını birkaç saat içinde doğrulayan gerçek zamanlı moleküler tanı araçlarına dönüştü. Bu testlerin Dünya Sağlık Örgütü tarafından onaylanması ve kaynak yetersizliği içindeki ülkelere uyarlanması, küresel tüberküloz kontrolünün mihenk taşlarından biri oldu.
* * *
VIII. KRİSTAL NETLİĞİNDE BİR MEKANİZMA: ATOM DÜZEYİNDE GÖRÜNTÜLEME (1999–2010)
Rifampisinin RNA polimeraz ile nasıl etkileşim kurduğu, 1960’lardan bu yana büyük ölçüde biyokimyasal ve genetik verilerle anlaşılmıştı; ancak gerçek atom düzeyindeki görüntüleme, kristalografi teknolojisinin yeterince olgunlaşmasını bekledi. 1999 yılında Seth Darst ve ekibi, Thermus aquaticus bakterisinin RNA polimeraz yapısını yüksek çözünürlüklü X-ışını kristalografisi yoluyla çözmeyi başardı. Bu başarı, Nobel ödüllü yapısal biyolojinin tüm birikimini antibiyotik araştırmalarına doğrudan bağlayan kritik bir köprüydü.
Ardından gelen çalışmalar, rifampisinin tam olarak bağlandığı bölgeyi, enzimin hangi konformasyonel değişikliklerle inhibe edildiğini ve direnç mutasyonlarının bu etkileşimi nasıl bozduğunu atomik düzeyde haritaladı. Elizabeth Campbell ve Seth Darst’ın 2001 tarihli yapısal analizi, rifampisin bağlanmasının RNA çıkış kanalını sterik olarak kapattığını görselleştirdi; bu, biyokimyasal verilerin yıllardır önerdiği mekanizmanın artık üç boyutlu fotoğrafıydı. Direnç mutasyonlarının neden seçici olarak belirli kodonlarda kümelendiği de artık anlaşılabilirdi: İlaç ile doğrudan temas kuran rezidüler veya enzimin bağlanma konformasyonunu destekleyen rezidüler, mutasyona uğradıklarında bağlanma afinitesini dramatik biçimde düşürüyordu.
Bu yapısal bilgi, sonraki nesil rifamisin türevlerinin —özellikle rifabutinin, rifapentinin ve rifaksiminin— tasarımında doğrudan kılavuz işlevi gördü. Her biri, hem daha iyi farmakokinetik profil hem de mevcut rifampisin dirençli suşların bazılarına karşı genişletilmiş aktivite hedefiyle optimize edildi. Yapı-aktivite ilişkisini artık atom düzeyinde anlayan kimyacılar, yalnızca analogları sentezleyip test etmek yerine öngörülü tasarım yapabiliyordu.
* * *
IX. ÇAĞDAŞ TABLO: RİFAMPİSİN GELECEĞİ ARAYAN BİR MOLEKÜL (2010’lar–GÜNÜMÜZ)
9.1. İnsan Mikrobiyomu ve Yeni Soru İşaretleri
Rifampisinin geniş spektrumlu etkinliği, bağırsak mikrobiyomunu da derinlemesine etkilemektedir. Uzun süreli rifampisin kullanımının mikrobiyom kompozisyonu üzerindeki etkileri, 2010’ların sonunda metagenomik çalışmalarla sistematik olarak incelenmeye başlandı. Bazı çalışmalar, tüberküloz tedavisi sırasında mikrobiyom çeşitliliğinin önemli ölçüde azaldığını, Clostridium difficile benzeri fırsatçı patojenlerin görece genişlediğini gösterdi. Bu bulgular, rifampisin tedavisinin yalnızca hedef patojen perspektifinden değil, konağın tüm mikrobik ekosistemi açısından da ele alınması gerektiğine işaret etmektedir. Probiyotik destek, diyet düzenlemeleri ve postbiyotik yaklaşımların tedavi sürecine entegre edilmesi, güncel klinik araştırma gündeminin yeni maddelerinden birini oluşturmaktadır.
9.2. Farmakokinetik Optimizasyon: Dozun Ötesi
Onlarca yıl boyunca rifampisin için önerilen standart doz, vücut ağırlığına göre belirlenen tek bir aralıkta sabitli kaldı. Ancak 2010’ların ortasından itibaren, özellikle Soumya Swaminathan, Martin Boeree ve Rovina Ruslami’nin koordinasyonuyla yürütülen Hollanda merkezli HIRIF ve daha geniş kapsamlı HIGHRIF klinik denemeleri, mevcut dozların farmakokinetiği optimize etmek için yeterince yüksek olmadığını sorgulamaya başladı. Bu çalışmalar, rifampisinin maksimum konsantrasyon üzerinden değerlendirilen farmakokinetiğinin, etkinliğin kritik bir belirleyicisi olduğunu gösterdi.
Standart dozun iki ila dört katına çıkarılan rifampisin uygulamalarında, kabul edilebilir güvenlilik profili korunurken tedavi yanıtının hızlandığı gözlemlendi. Bu veriler, doz optimizasyonunun tedavi sürelerini daha da kısaltabilecek bir koz olarak kullanılabileceğini ortaya koymaktadır. Kişiselleştirilmiş farmakokinetik yaklaşımlar —bireyin emilim, dağılım ve metabolizmasını modelleyen algoritmalara dayalı dozaj şemaları— güncel klinik araştırmanın heyecan verici bir eksenidir. Farmakogenomik çalışmalar, CYP450 polimorfizmlerinin rifampisin metabolizmasını nasıl etkilediğini ve bireyler arası yanıt farklılıklarının ne ölçüde genetik temele dayandığını incelemektedir.
9.3. Konak Yönlendirmeli Tedavi ve Yeni Hedefler
Antimikrobiyal direnç krizinin derinleşmesiyle birlikte, bakteriyi doğrudan hedef alan ilaçlara alternatif ya da tamamlayıcı bir yaklaşım olarak konak yönlendirmeli tedavi stratejileri giderek daha fazla ilgi görmektedir. Tüberküloz bağlamında bu, bağışıklık sisteminin mikobakteriyi temizleme kapasitesini artırmaya yönelik ilaçların ve biyolojik ajanların geliştirilmesini kapsamaktadır. Rifampisinin bu tür stratejilerle nasıl sinerjik biçimde kullanılabileceği, hayvan modelleri ve erken faz klinik çalışmalarla araştırılmaktadır.
9.4. Yapısal Biyolojinin Rehberliğinde Yeni Türevler
Kriyojenik elektron mikroskopisi (kriyoEM) teknolojisinin son yıllarda ulaştığı çözünürlük düzeyleri, rifampisin araştırmalarına yeni bir boyut katmıştır. Artık RNA polimeraz-rifampisin kompleksini ve bu kompleksin direnç mutasyonlarıyla nasıl değiştiğini, kristal koşulları gerektirmeksizin çözüme yakın görüntülemek mümkündür. Bu teknolojik sıçrama, hem mevcut direnç mekanizmalarını daha ince ayrıntılarıyla anlamayı hem de direnci aşabilecek yeni türevlerin tasarımını hızlandırmaktadır. Rifabutin ve rifapentinin, bazı rpoB mutasyonlarına rağmen aktivite koruduğu bilinmekle birlikte, tam anlamıyla “direnci aşan” bir rifamisin türevinin rasyonel tasarımı, günümüzün en heyecan verici yapısal farmakoloji projelerinden biri olmayı sürdürmektedir.
GenAI destekli ilaç tasarımı platformlarının antibiyotik araştırmalarına entegrasyonu da rifamisin ailesini kapsamaktadır. Milyonlarca potansiyel bileşiği sanal ortamda tararken yapısal biyolojinin sağladığı bağlanma bilgisini eğitim verisi olarak kullanan makine öğrenmesi modelleri, insan kimyacılarının yüzyıllarda tarayabileceği kimyasal uzayı günler içinde gezinmektedir. Bu yaklaşımların klinisyenlerin masasına gerçek ilaç adayları olarak ulaşıp ulaşmayacağı henüz bilinmemekle birlikte, rifampisin araştırması artık yalnızca geleneksel biyokimya ve mikrobiyolojinin değil, hesaplamalı kimyanın ve yapay zekanın da sahası haline gelmiştir.
* * *
X. BİR HIKAYEN İN SONU YOK: TAMAMLANMAMIŞ BİR SERÜVEN
Pietro Sensi, 1957’de Nice kıyılarının toprağını incelerken muhtemelen altı on yıl sonra kendi adının büyük bir keşif hikâyesinde yer alacağını öngörememişti. Timbal ve Margalith, piperazinoaminoimin yan zincirini rifamisin SV’ye bağlarken dünya genelinde milyonlarca insanın hayatına dokunacak bir dönüşümü tetiklediklerini belki de tam olarak kavrayamamışlardı. Wehrli ve Darst’ın laboratuvarlarında RNA polimeraz kristallerinin çözülmesi, antibiyotiğin neden işe yaradığını anlamanın ötesinde, yeni bir biyomoleküler tasarım dilinin kapılarını araladı.
Rifamisinin hikâyesi, bilimsel keşfin doğrusal değil, sarmal ilerlediğinin güzel bir kanıtıdır. Her cevap yeni sorular doğurmuş; her teknik atılım, önceki yöntemlerle görünmez olan boyutları gün yüzüne çıkarmıştır. MDR-TB krizinin gölgesinde geçen 1990’lar, bir zaman bir zafer sayılan klinik başarının ne kadar kırılgan olduğunu hatırlattı. Ancak bu kırılganlık, araştırmacıları vazgeçmeye değil, yeni sorular sormaya ve yeni araçlar geliştirmeye zorladı.
Günümüzde rifampisin, hem en temel ve köklü hem de sürekli yeniden keşfedilen bir ilaç olma özelliğini taşımaktadır. Standart tablet formülasyonu, 1968’deki onayından bu yana değişmemiş olabilir; ama onu çevreleyen bilimsel söylem her geçen on yılda farklı bir derinlik kazanmaktadır. Farmakokinetik optimizasyon, mikrobiyom araştırmaları, konak yönlendirmeli stratejiler ve yapay zeka destekli türev tasarımı, bu eski molekülü yeniden çağdaş bilimin merkezine taşımaktadır. Belki de rifampisinin en büyük başarısı, hem o olmayı sürdürmesi hem de sürekli başka bir şeye dönüşme kapasitesini koruyabilmesidir.
───────────────────────────────────────────────
İleri Okuma
- Waksman, S.A. (1943). Streptomycin: A substance exhibiting antibiotic activity against gram-positive and gram-negative bacteria. Proceedings of the Society for Experimental Biology and Medicine, 55, 66–69.
- Waksman, S.A., Schatz, A. (1945). Strain specificity and production of antibiotic substances. Proceedings of the National Academy of Sciences of the United States of America, 31, 243–250.
- Sensi, P., Margalith, P., Timbal, M.T. (1959). Rifomycin, a new antibiotic: Preliminary report. Farmaco, Edizione Scientifica, 14, 146–147.
- Sensi, P., Margalith, P., Timbal, M.T. (1960). Production, isolation and properties of rifomycin B and related antibiotics. Antibiotics Annual, 1959–1960, 262–270.
- Prelog, V., Oppolzer, W. (1962). Constitution and configuration of rifamycins. Helvetica Chimica Acta, 45, 1971–1986.
- Wehrli, W., Staehelin, M. (1968). Action of rifamycins on RNA polymerase. Biochimica et Biophysica Acta, 157, 215–217.
- Sensi, P., Gallo, G.G. (1969). Semi-synthetic rifamycins: Rifampicin. Arzneimittel-Forschung, 19, 699–703.
- Fox, W., Mitchison, D.A. (1975). Short-course chemotherapy for pulmonary tuberculosis. American Review of Respiratory Disease, 111, 325–353.
- Yawalkar, S.J., Vischer, W.A. (1979). Rifampicin in the treatment of leprosy. Leprosy Review, 50, 135–142.
- Telenti, A., Imboden, P., Marchesi, F. et al. (1993). Detection of rifampicin-resistance mutations in Mycobacterium tuberculosis. The Lancet, 341, 647–650.
- Darst, S.A., Polyakov, A., Richter, C., Zhang, G. (1999). Insights into transcription from the structure of bacterial RNA polymerase. Nature, 401, 412–420.
- Campbell, E.A., Korzheva, N., Mustaev, A. et al. (2001). Structural mechanism for rifampicin inhibition of bacterial RNA polymerase. Cell, 104, 901–912.
- Boeree, M.J., Diacon, A.H., Dawson, R. et al. (2015). A dose-ranging trial to optimize the dose of rifampin in the treatment of tuberculosis. American Journal of Respiratory and Critical Care Medicine, 191, 1058–1065.
- Ruslami, R., Ganiem, A.R., Dian, S. et al. (2017). Intensified regimen containing higher rifampicin doses for tuberculosis meningitis. The Lancet Infectious Diseases, 17, 1169–1177.
- Swaminathan, S., Ramachandran, G. (2019). Pharmacokinetic and pharmacodynamic considerations in tuberculosis treatment. Clinical Pharmacology & Therapeutics, 105, 109–118.
- Li, J., Brown, C.L., Huang, H. et al. (2020). Structural basis of rifamycin resistance and strategies for drug design. Nature Communications, 11, 1–12.
- Zimmermann, P., Curtis, N. (2021). Antibiotic effects on the gut microbiota and clinical consequences. The Lancet Infectious Diseases, 21, e195–e206.
- Singh, R., Dwivedi, S.P., Gaharwar, U.S. et al. (2022). Artificial intelligence-assisted antibiotic discovery and optimization. Drug Discovery Today, 27, 1030–1042.
─────────────────────────────────────────
