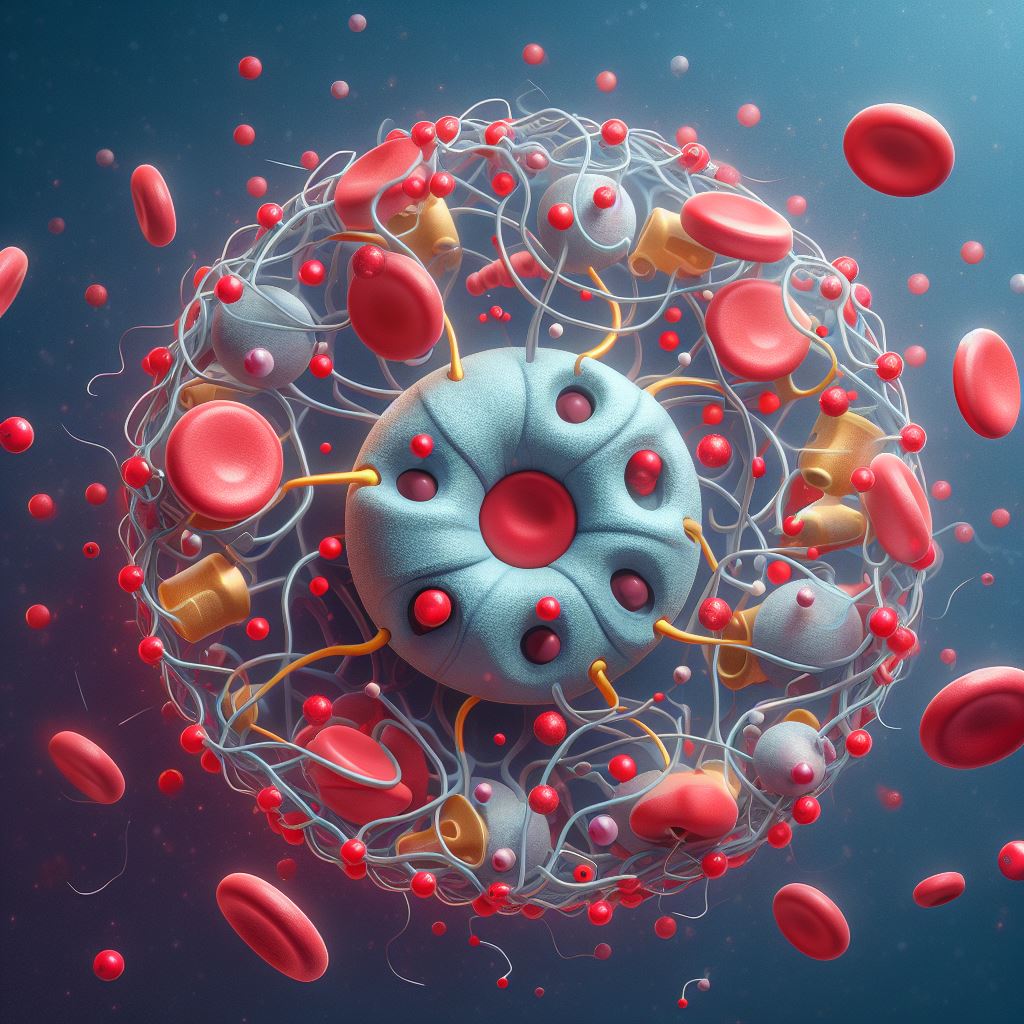
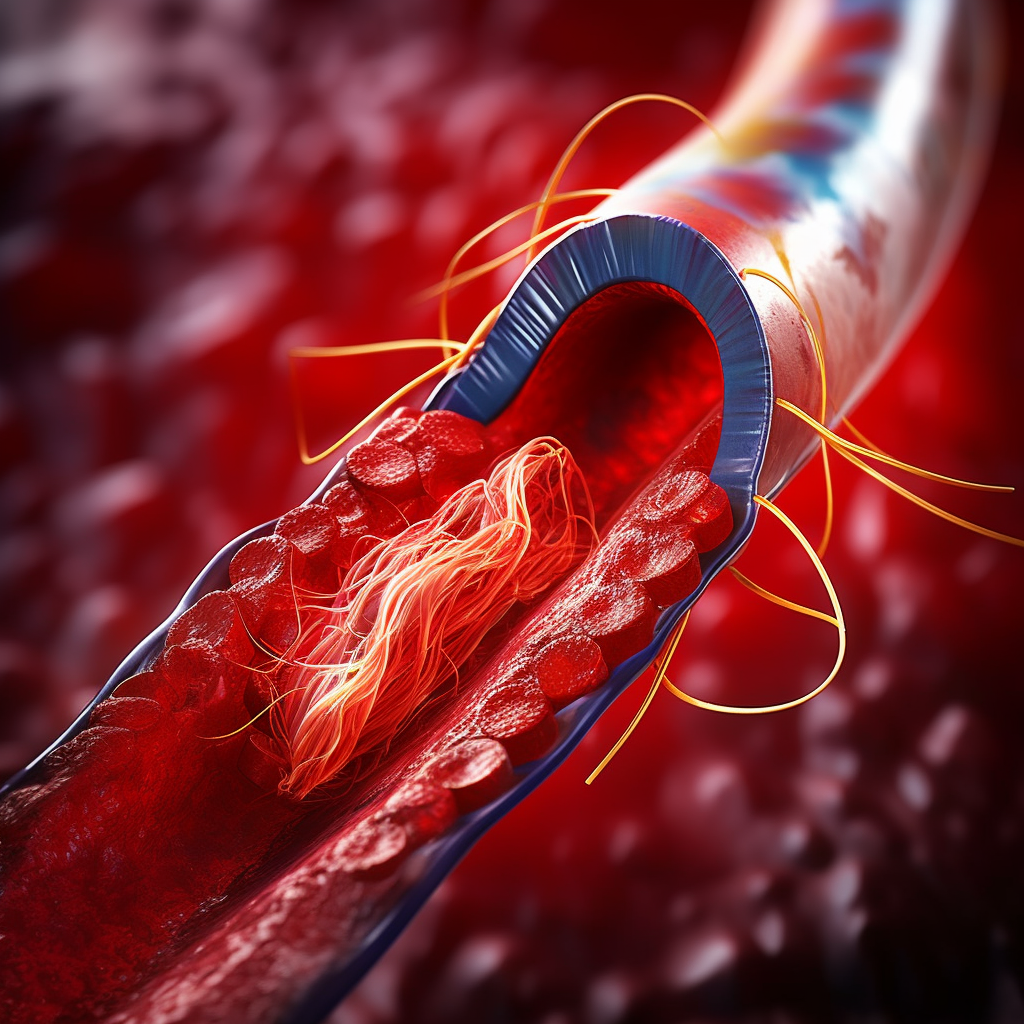
P2Y12 reseptörü
P2Y12 reseptörü, trombosit agregasyonu ve trombüs oluşumunda önemli bir rol oynayan bir G proteinine bağlı reseptördür (GPCR). Esas olarak trombositlerin ve bazı bağışıklık hücrelerinin yüzeyinde bulunur. Reseptör, kanın pıhtılaşması ve iltihaplanma gibi hem fizyolojik hem de patolojik süreçlere katkıda bulunan çeşitli sinyal yollarında yer alır. Etki Yapısı ve Mekanizması YapıP2Y12 reseptörü, GPCR’lerin karakteristik bir özelliği … Devamını oku