ventriculus dexter in çoğulu.
-veya aitlik bildiren hali.
Aurikula dekstra
Tanım ve Genel Bakış
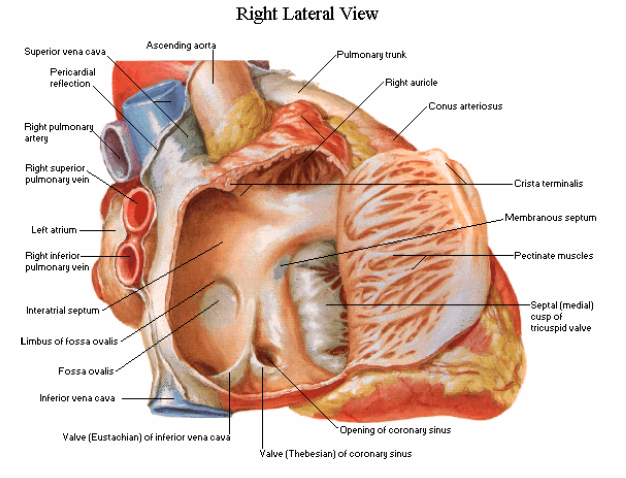
Auricula cordis dekstra (auricula atrii dextri, sağ atriyal apendiks; İngilizce: right atrial appendage, RAA), kalbin sağ kulakçığının (sağ atriyum) ön-üst kısmından dışa doğru uzanan, ince duvarlı, konik ya da piramidal yapıda, iç yüzü pektinat kaslarıyla (musculi pectinati) döşeli bir divertikül benzeri çıkıntıdır. Morfolojik olarak atriyumun geri kalan düz duvarlı bölgesinden belirgin biçimde ayrılır ve özellikle ekokardiyografi, kardiyak BT ve MR görüntülemede sağ atriyumun ayırt edici anatomik işaretlerinden biri olarak kullanılır.
Bu yapı, klasik anlamda “temel pompa” fonksiyonuna sahip olmaktan çok, atriyal hacim rezervuarı, duvar gerilimi düzenleyici ve atriyal natriüretik peptid (ANP) üretiminde rol alan bir “ek odacık” olarak kabul edilir. Klinik açıdan trombüs oluşumu özellikle sol atriyal apendikste (LAA) belirgin olmakla birlikte, sağ atriyal apendiksin de belirli durumlarda emboli kaynağı olabileceği bilinmektedir.
Etimoloji
Auricula cordis dekstra terminolojisi, büyük ölçüde klasik Latince’den türetilmiş üç ana öğeye dayanır:
- Auricula: Latince auris (“kulak”) sözcüğünün küçültme eki almış biçimidir ve “küçük kulak”, “kulakçık” anlamına gelir. Kalpteki aurikulanın kulak kepçesine benzeyen uzantılı, kıvrımlı görünümü nedeniyle bu isim verilmiştir.
- Atrium: Latince atrium, Roma evlerinin giriş holü, “ön salon” anlamına gelir. Kalbin atriyumları da “kalbe gelen kan için giriş odacıkları” olarak düşünüldüğünden bu terim anatomik terminolojiye uyarlanmıştır.
- Dexter / dekstra: Latince dexter “sağ tarafta bulunan, sağdaki” anlamındadır. Anatomi dilinde dexter sağ, sinister sol tarafı ifade eder. “Auricula cordis dekstra” ifadesi, kelime anlamıyla “kalbin sağdaki kulakçığı”dır.
Dolayısıyla “sağ atriyal apendiks”, hem şekil benzetmesi (kulak kepçesi gibi çıkıntı) hem de topografik yön (sağ taraf) içeren, tarihsel kökeni güçlü bir anatomi terimidir.
Makroskopik Anatomi
Konum ve Komşuluklar
Sağ atriyal apendiks, sağ atriyumun ön-üst yüzünde, kalbin sağ kenarına yakın bir noktada yer alır.
Başlıca komşulukları:
- Arkada ve hafif inferiorunda sağ atriyumun düz duvarlı bölümü (sinus venarum cavarum)
- Üstte v. cava superior’un atriyuma açıldığı bölge
- Altta v. cava inferior’a yakın atriyal duvar
- Anteriorunda truncus pulmonalis ve sağ ventrikülün konus arteriozus bölgesi
Bu konumlanma, cerrahi yaklaşımlarda ve TEE (transözofageal ekokardiyografi) altında yapılan anatomik tanımlamalarda önem taşır.
Şekil ve Boyut
Sağ aurikula genellikle:
- Konik ya da üçgenimsi bir kese şeklindedir
- Apex’i inferiorda ve öne doğru uzanır
- Bazı bireylerde uzun ve dar, bazılarında daha kısa ve geniş olabilir
- İç lümeni trabeküler görünüm veren belirgin pektinat kasları ile doludur
Sol aurikulaya kıyasla genellikle daha geniş tabanlı, daha az lobüle ve trombüs oluşumuna anatomik olarak daha az yatkın kabul edilir. Bu nedenle klinik literatürde tromboembolik olaylar açısından esas odak çoğu zaman sol atriyal apendiks (LAA) üzerindedir.
Mikroskopik Yapı ve Pektinati Kasları
Auricula cordis dekstra’nın duvarı temel olarak üç tabakadan oluşur: endokard, miyokard ve epikard (visseral perikard).
- Endokard:
- İnce bir endotelyal hücre tabakası
- Altında az miktarda bağ dokusu
- İç yüzeyi pektinat kaslarının kabartılarını izleyen dalgalı bir topografiye sahiptir.
- Miyokard:
- Aurikuladaki miyokard tabakası, atriyumun düz duvarlı bölümüne göre daha belirgin trabeküller (musculi pectinati) içerir.
- Pektinat kasları, krista terminalisten aurikula içine doğru uzanan tarak benzeri kas lifleridir. Bu kaslar, atriyumun kasılma gücünü belirli lokal alanlarda artırırken aynı zamanda lümen yüzeyini de düzensiz hâle getirir.
- ANP sentezleyen atriyal miyositler özellikle bu bölgede yoğunlaşmıştır.
- Epikard:
- İnce bir mezotel hücre tabakası
- Altında yağ dokusu ve yüzeyel koroner damarlar bulunabilir.
Mikroskopik düzeyde, sağ aurikuladaki kas lifleri ile ana atriyal miyokard arasında süreklilik vardır; iletim sistemi açısından bakıldığında, bu bölge sinoatriyal düğüme ve internodal ileti yolaklarına göre farklı düzeyde elektriksel davranış gösterebilir ve bu da atriyal aritmilerin substratını etkileyebilir.
Gelişimsel ve Evrimsel Perspektif
Embriyolojik Gelişim
İnsan embriyogenezinde:
- Erken dönemde tek bir ilkel atriyum bulunur.
- Zamanla venöz ve arterial kutupların ayrışması, septasyon süreçleri ve venlerin atriyuma farklı açılma paternleri ile atriyumun bir bölümü “düz duvarlı sinus venarum”a, bir bölümü ise “trabeküler, pektinat kaslı bölgeye” dönüşür.
- Aurikula, embriyolojik olarak ilkel atriyumun persistan trabeküler bölgesinin devamı olarak kabul edilebilir.
- Sağ atriyumun düz duvarlı kısmı büyük ölçüde sinus venosus’un inkorporasyonu ile oluşurken, aurikula kısmı ilkel atriyum dokusunun daha “orijinal” morfolojisini korur.
Bu nedenle, aurikula çoğu zaman “eski” atriyum dokusunun bir kalıntısı gibi düşünülebilir; trabeküler ve pektinat kaslı yapısı bu gelişimsel kökene karşılık gelir.
Evrimsel Perspektif
Omurgalı kalbinin evriminde:
- Daha basit dolaşım sistemine sahip balık ve amfibilerde atriyumun tümü, daha düzensiz, trabeküler bir yapı gösterir.
- Memeli ve kuşlarda dolaşım sistemi iki devreli hâle gelir (pulmoner ve sistemik). Atriyumlar ikiye bölünür ve daha sofistike bir valvüler-septal mimari gelişir.
- Bu süreçte atriyumun bir kısmı daha “düzlüklü”, venöz dönüşe adaptif, sinüs formunda bir yapı kazanırken, başka bir bölümü trabeküler, kaslı kalır ve fonksiyonel bir rezervuar/kompartment görevi görür.
Sağ ve sol atriyal apendiksler, işte bu trabeküler, kaslı “ilkel atriyum dokusunun” evrimsel olarak korunmuş uzantıları olarak yorumlanabilir.
Bu bağlamda:
- Aurikula, hacim dalgalanmalarını tolere eden,
- Duvar gerilimini dağıtan,
- Belli bir nöro-hormonal fonksiyon (ANP salınımı) üstlenen,
- Gelişimsel ve evrimsel bakımdan ilkel atriyal yapının süreğen bir mirasıdır.
İşlev (Fizyoloji)
Sağ atriyal apendiksin işlevi, klasik bir “pompa odacığı” işlevinden çok, hacim, gerilim ve hormonal düzenleme üzerinden açıklanır.
1. Hacim Rezervuarı ve Geometrik Tamponlama
- Kalbin tabanı ve büyük damarların (özellikle vena kava superior ve inferior) atriyuma giriş yaptığı bölgelerde geometrik boşluklar oluşur.
- Aurikula, bu boşlukları kısmen doldurarak atriyal lümenin daha akışkan bir geometri kazanmasına katkıda bulunur.
- Ani hacim yüklenmelerinde (örneğin hızlı sıvı yüklemesi, egzersiz sırasında venöz dönüş artışı) aurikula lümeni, atriyumun efektif hacminin bir kısmını tamponlayabilir ve duvar gerilimindeki ani artışları sınırlayabilir.
2. Atriyal Natriüretik Peptid (ANP) Üretimi
Auricula cordis dekstra, ANP (Atrial Natriüretik Peptid) sentezleyen atriyal miyositler açısından zengin bir bölgedir. ANP:
- Özellikle atriyal duvarın gerilmesine yanıt olarak salınır.
- Böbreklerde natriürezi ve diürezi artırır.
- Renin-anjiyotensin-aldosteron sistemini baskılayarak kan basıncını düşürücü, hacim azaltıcı etki gösterir.
- Damar düz kasında vazodilatasyon yapabilir.
Bu açıdan sağ aurikula, mekanik gerilim → hormonal yanıt ekseninde kardiyovasküler homeostaza katkı sunan bir “sensör-efektör” bölge olarak düşünülebilir.
3. Atriyal Hemodinamik ve İletim
- Aurikula kasılmaları, özellikle atriyal sistol sırasında sağ atriyumun toplam kasılma paternine katkıda bulunur.
- Pektinat kaslarının oryantasyonu, lokal kasılma vektörlerini değiştirerek atriyal iç akım dinamiklerini etkileyebilir.
- Elektriksel iletim açısından, aurikula ile krista terminalis ve sağ atriyum duvarı arasında süreklilik vardır; bu da, belirli aritmi odaklarının veya reentry devrelerinin bu bölgeden doğmasına zemin hazırlayabilir (özellikle atriyal taşikardiler ve atriyal flutter alt tipleri).
Auricular fonksiyonun “vazgeçilmez” olup olmadığı tartışmalıdır, zira özellikle sol atriyal apendiksin kapatılması veya rezeksiyonundan sonra hastaların önemli bir kısmı hemodinamik olarak iyi tolere edilebilmektedir. Ancak bu, uzun dönem hormonal ve incelikli hemodinamik etkilerin tamamen önemsiz olduğu anlamına gelmez.
Klinik Önemi
1. Tromboz ve Emboli
Tromboz açısından en yüksek klinik önem sol atriyal apendikste olsa da, sağ atriyal apendiks de belirli risk durumlarında trombüs oluşumuna yatkın olabilir:
- Atrial fibrilasyon (AF):
- AF’de atriyal kasılmanın mekanik bileşeni bozulur, kan akımı yavaşlar ve türbülans artar.
- En belirgin trombüs birikim yeri LAA olsa da, sağ atriyum ve sağ aurikula da staz alanları hâline gelebilir.
- Sağ atriyal ve sağ aurikular trombüsler daha çok santral venöz kateter varlığı, triküspit hastalıkları veya ciddi sağ kalp yetmezliği ile ilişkilidir.
- Merkezi venöz kateterler, pacemaker/ICD elektrodları:
- Sağ atriyum ve aurikula bölgesinde yabancı cisim varlığı, lokal endotel hasarı ve staza bağlı trombüs riskini artırabilir.
- Pulmoner emboli riski:
- Sağ atriyal veya aurikular trombüsler, koparak pulmoner arterlere embolize olabilir.
- Bu nedenle bazı olgularda sağ atriyal apendikste saptanan trombüs, pulmoner emboli açısından “kaynak lezyon” olarak kabul edilir.
Buna karşın, iskemik inme (apopleksi) ile en güçlü ilişki sol atriyal apendiks trombüslerindedir; sistemik emboli, çoğunlukla LAA kaynaklıdır. Bu nedenle kardiyoversiyon öncesi trombüs dışlama pratiği klinikte özellikle LAA’ya odaklanır.
2. Kardiyoversiyon Öncesi TEE
Elektriksel kardiyoversiyon planlanan hastalarda, özellikle uzun süreli veya ne zaman başladığı bilinmeyen atriyal fibrilasyon varlığında, transözofageal ekokardiyografi (TEE) yapılması önerilir.
- Amaç, özellikle sol atriyal apendikste trombüs olup olmadığını saptamaktır.
- Trombüs saptanması hâlinde kardiyoversiyon yapılması trombüsün yerinden kopup beyne veya periferik arterlere embolize olmasına ve inme (apopleksi) gibi ciddi komplikasyonlara neden olabilir.
- Sağ atriyal apendiks de TEE ile görüntülenebilir; pulmoner emboli riskini değerlendirmek veya sağ kalp trombüslerini saptamak için önem taşıyabilir.
Dolayısıyla TEE, hem sol hem de sağ atriyal apendikslerin değerlendirilmesine imkân tanıyan, tromboembolik risk yönetiminde kritik bir görüntüleme yöntemidir.
3. Sol Atriyal Apendiksin Kateter veya Cerrahi Yolla Kapatılması
Metinde de değinildiği gibi, klinik pratiğin önemli bir alanı sol atriyal apendiksin (LAA) girişimsel kapatılmasıdır. Bu prosedür:
- Özellikle non-valvüler atriyal fibrilasyon ve yüksek inme riski taşıyan,
- Ancak tam doz veya uzun süreli oral antikoagülasyon (OAK) kullanması kontrendike olan (örneğin yüksek kanama riski, ciddi gastrointestinal kanama öyküsü, intrakraniyal kanama öyküsü gibi)
hastalarda uygulanır.
Temel amaç, LAA’yı dolaşıma kapatarak burada trombüs oluşumunu ve dolayısıyla sistemik emboli riskini azaltmaktır.
Sağ atriyal apendiks için rutin bir “kapatma” pratiği yaygın değildir, çünkü:
- Tromboembolik risk açısından LAA kadar kritik kabul edilmez.
- Sağ taraftan emboliler çoğunlukla pulmoner yatağa yöneldiği için klinik spektrum farklıdır.
Ancak belirli cerrahi veya girişimsel kardiyoloji prosedürleri sırasında sağ aurikulanın da rezeksiyonu veya modifikasyonu söz konusu olabilir (örneğin belirli konjenital kalp hastalıklarının cerrahisi, trikuspid kapak rekonstrüksiyonu, atriyal flutter cerrahisi vb.).
4. Aritmiler ve Ablasyon Prosedürleri
- Sağ atriyal apendiks, özellikle tipik ve atipik atriyal flutter ya da fokal atriyal taşikardilerde reentry devresinin ya da odakların bir parçası olabilir.
- Kateter ablasyonunda krista terminalis, kavotriküspit istmus ve aurikula-atriyum geçiş bölgesi sıklıkla hedef alınan alanlardandır.
- Bu nedenle girişimsel elektrofizyologlar için, sağ aurikulanın topografisi ve komşuluk ilişkilerinin ayrıntılı bilinmesi önemlidir.
5. Cerrahi ve Yapısal Kardiyoloji Bağlamı
- Açık kalp cerrahisi sırasında sağ atriyal insizyonlar çoğunlukla aurikula bölgesine ya da ona yakın alanlara yapılır; böylece cerrahi erişim kolaylaşır ve iletim sistemi yapıları görece korunur.
- Bazı konjenital anomalilerde (örneğin atriyal septal defektler, triküspit kapak anomalileri) sağ atriyal anatomideki değişiklikler, aurikulanın şeklini ve hacmini de etkileyebilir.
- Bazı cerrahi antiaritmik prosedürlerde (Maze operasyonu vb.) aurikula da çizgisel kesiler ya da ablasyon hatlarıyla yeniden şekillendirilen veya izole edilen alanlardan biri olabilir.
Görüntüleme
Auricula cordis dekstra, farklı kardiyak görüntüleme modaliteleri ile ayrıntılı olarak değerlendirilebilir:
- Transtorasik Ekokardiyografi (TTE):
- Sağ atriyumun genel boyutları ve fonksiyonu değerlendirilirken aurikulanın kaba anatomik görünümü görülebilir, ancak LAA’ye kıyasla detaylı trombüs değerlendirmesi için sınırlıdır.
- Transözofageal Ekokardiyografi (TEE):
- Aurikula ve atriyum lümeni daha yüksek çözünürlükle görüntülenebilir.
- Trombüs, spontan eko kontrast (“duman” görüntüsü), akım paternleri incelenebilir.
- Kardiyak BT:
- Üç boyutlu anatomik rekonstrüksiyon imkânı verir.
- Özellikle sol atriyal apendiks kapatma prosedürleri planlanırken, atriyal apendikslerin şekli, hacmi ve komşulukları ayrıntılı biçimde değerlendirilebilir; sağ aurikula da bu inceleme içinde net olarak seçilir.
- Kardiyak MR:
- Atriyal hacim, fonksiyon ve doku karakterizasyonu (fibrozis, inflamasyon, trombüs vs.) hakkında bilgi sunabilir.
- Sağ aurikula içindeki akım dinamikleri ve duvar hareketi ayrıntılı biçimde incelenebilir.
Bu görüntüleme yöntemleri, hem tromboembolik riskin değerlendirilmesi, hem de girişimsel ve cerrahi işlemlerin planlanmasında anatominin netleştirilmesi açısından klinik pratikte büyük önem taşır.
Son Notlar
Auricula cordis dekstra, başlangıçta yalnızca “kulak kepçesine benzeyen” bir morfolojik uzantı gibi görünse de, embriyolojik ve evrimsel kökeni, pektinat kaslarıyla zenginleşmiş mikroyapısı, ANP üretimindeki rolü, hacim ve gerilim düzenleyici özellikleri ve aritmiler ile tromboz bağlamındaki klinik önemi nedeniyle kardiyak anatomi ve fizyolojinin son derece ilginç, işlevsel ve klinik açıdan anlamlı bir bileşenidir.
Keşif
1. Antik Dönemin Issız Laboratuvarları: İlk Fark Ediliş (MÖ 3. yy – MS 2. yy)
Kalbin sağ tarafında küçük bir çıkıntı olduğu gerçeği, ilk kez sistematik tıp çalışanlarının dikkatine, büyük olasılıkla İskenderiye Okulu döneminde girdi. Herophilos ve Erasistratos, dönemin en cesur anatomları olarak, insan cesedi üzerinde diseksiyon yapmaya izin verilen tek dönemin ayrıcalığıyla, kalbi bütüncül bir organ olarak incelemişlerdi. Atriyumları ayırt edebilmişler, ancak bugün “aurikula” dediğimiz yapının özgün kimliği henüz tam belirgin değildi. Onlar, bu yapıyı “girişteki etsi çıkıntılar” olarak tarif ettiler; fakat bir isim vermekten çekindiler.
Aradan birkaç yüzyıl geçti ve sahneye Galenos çıktı. Hayvan diseksiyonlarıyla sınırlı olsa da Galenos, kalbin üst bölgesinde kulak kepçesini andıran küçük çıkıntıları şimdi bildiğimiz isme çok benzeyen bir terimle anmaya başladı: “auriculae.” Sağ taraftaki çıkıntının sola göre daha hacimli olduğunu bile fark etmişti. Böylece, sağ atriyal apendiks ilk kez hem morfolojik hem terminolojik bir kimliğe kavuştu.
2. Orta Çağ: Bilginin Uykuya Yattığı Dönem (5.–14. yy)
Bu yüzyıllar boyunca kalbin aurikulaları tasvir edildi ama yeni bir keşif üretilmedi. Galenos’un metinleri neredeyse kutsal görülüyor, sorgulanmıyor, yalnızca aktarılıyordu. Sağ aurikula, tıbbi metinlerin satır aralarında, varlığı bilinen ama fonksiyonu açıklanamayan bir “minör çıkıntı” olarak bekledi.
3. Rönesans: Derinlik Kazanan Anatomik Aydınlanma (15.–16. yy)
Leonardo da Vinci (ca. 1507–1513)
Kalbin sağ aurikulayı gerçekçi biçimde betimleyen ilk kişi, anatominin en yetenekli ressamı Leonardo oldu. İnsan ve hayvan kalpleri üzerinde yaptığı detaylı incelemelerde sağ aurikulayı konik, trabeküler ve atriyumdan belirgin şekilde ayrılmış bir yapı olarak çizdi. İç yüzün pektinat kaslarıyla dolu olduğunu gösteren ilk çizimler de ona aitti. Leonardo, bu çıkıntının “bir tür odacık hissi veren küçük bir giriş” olduğunu yazmıştı.
Andreas Vesalius (1543)
Leonardo’nun çizimlerinin aksine, Vesalius’un çalışmaları matbaaya girmiş, Avrupa’nın her yerine yayılmış bilimsel bir devrimdi. De humani corporis fabrica, sağ aurikulayı tamamen bağımsız bir anatomik bütünlük olarak tanımladı. Vesalius’un terminolojisi çok netti: Atriyum ayrıydı, aurikula ayrıydı; sağ aurikula, sağ atriyumun ön çıkıntısıydı ve kendi iç mimarisi vardı.
Hieronymus Fabricius (16. yy sonları)
Fabricius, pektinat kaslarını tüm ayrıntısıyla tanımlayarak aurikulanın sadece bir kese olmadığını; kas lifleri düzeni bakımından özgün bir mikroanatomiye sahip olduğunu gösterdi. Bu, sağ aurikulaya morfolojik bir derinlik kazandıran kritik bir adımdı.
4. Erken Modern Dönem: İşlev Sorusu Sahneye Çıkıyor (17.–18. yy)
William Harvey (1628)
Harvey’in dolaşım kuramında aurikula, kalbin kasılma sıralamasında aktif bir basamak olarak tanımlandı. Sağ aurikulanın sistolün erken fazında kasıldığı, böylece sağ atriyuma dolan kanı ventriküle yönlendirmeye katkıda bulunduğu ortaya kondu. Henüz hormon üretimi veya elektrofizyoloji bilinmiyordu, fakat aurikula artık bir “çıkıntı” değil, fonksiyonel bir yapı olarak kabul edilmeye başlanmıştı.
Marcello Malpighi (1661)
Mikroskopi devrimini başlatan Malpighi, aurikulanın trabeküler anatomisini ilk kez mikroskobik düzeyde inceledi. Sağ aurikuladaki düzensiz kas örgüsünün, atriyumun düz duvarlı kısmından tamamen farklı olduğunu doğruladı.
Albrecht von Haller (18. yy)
Haller, sağ aurikulayı mekanik açıdan analiz eden ilk düşünürlerden biriydi. Trabeküler yapının kan akışında türbülans yaratabileceğini ve bunun doğrudan klinik sonuçlara yol açabileceğini öngörmüştü. Bu analiz, geleceğin “aurikula-trombüs” tartışmalarına bir ön işaretti.
5. 19. ve Erken 20. Yüzyıl: Anatomiden Fizyolojiye Geçiş
Bu dönem boyunca sağ aurikulaya ilgi, yavaş yavaş işlevsel sorulara kaydı. Kardiyovasküler fizyoloji gelişiyordu; atriyum basıncı, dolum dinamikleri, kasılma sıraları ölçülebilir hâle gelmişti. Aurikulanın atriyal gerilimi tamponlayan bir hacim rezervuarı olabileceği fikri belirdi.
Bu yüzyılın sonunda ise kalbin endokrin işlevini keşfetmeye yönelik çalışmalar başladı. Atriyal miyositlerin granüllü içeriği dikkat çekiyor, ancak bu granüllerin hangi maddenin taşıyıcısı olduğu henüz bilinmiyordu.
6. Yakın Tarih: Hormonal Fonksiyonun Keşfi (1950–1980)
- yüzyıl ortalarında atriyal miyositlerde bulunan elektron yoğun granüller mercek altına alındı. Bu granüllerin özellikle aurikula bölgesinde yoğunlaştığı fark edildi. Ardından yapılan deneysel çalışmalar, atriyal dokudan salınan maddelerin güçlü diüretik ve natriüretik etkileri olduğunu gösterdi.
1980’lere gelindiğinde bu maddenin adı kondu: ANP (Atrial Natriüretik Peptid).
Sağ aurikula, ANP üretiminin en yoğun olduğu bölge olarak tanımlandı. Böylece anatomik bir çıkıntı, ilk kez endokrin bir organ bölgesi olarak kabul edildi.
7. Modern Çağ: Trombüs, Aritmi ve Görüntüleme Devrimi (1990–günümüz)
Görüntüleme Modaliteleri
Transözofageal ekokardiyografi, kardiyak BT ve MR ile sağ aurikulayı detaylı ölçmek, hacmini belirlemek, trombüs olup olmadığını tespit etmek mümkün hâle geldi. Bu, aurikulayı klinik kardiyolojinin gündemine güçlü biçimde geri taşıdı.
Aritmofizyoloji
Sağ atriyal apendiksin pektinat kasları, atriyal flutter ve fokal atriyal taşikardiler açısından önemli bir elektriksel zemin oluşturduğu anlaşıldı. Elektrofizyoloji haritalama teknikleri gelişince, aurikulanın yalnızca mekanik değil, iletimsel özellikleri de öne çıktı.
Trombüs ve Emboli
Tromboembolik olaylar en çok sol aurikulayla ilgili olsa da, sağ aurikuladaki trombüslerin pulmoner emboli için önemli bir kaynak olabileceği kabul edildi. Özellikle uzun süreli atriyal fibrilasyon, sağ kalp yetmezliği veya santral venöz kateter varlığı gibi durumlarda sağ aurikulaya özel dikkat gerekmeye başladı.
Girişimsel Kardiyoloji
Sol atriyal apendiksin kapatılması (LAA closure) yaygın bir yöntem hâline gelirken, sağ aurikula için rutin kapatma yapılmıyor; ancak bazı aritmi ablasyonlarında ve konjenital cerrahi girişimlerde sağ aurikulanın anatomisi kritik bir referans noktası hâline geldi.
İleri Okuma
- Galenos (2. yüzyıl). De anatomicis administrationibus. Pergamon: Antik Yunanca tıbbi külliyat.
- Leonardo da Vinci (1507–1513). Anatomical Manuscripts of the Heart. Windsor Castle Royal Collection: Notebooks.
- Vesalius, A. (1543). De humani corporis fabrica. Basel: Oporinus Press.
- Fabricius, H. (1600). De venarum ostiolis. Padua: Typis Laurentii Pasquati.
- Harvey, W. (1628). Exercitatio anatomica de motu cordis et sanguinis in animalibus. Frankfurt: Guilielmi Fitzeri.
- Malpighi, M. (1661). De pulmonibus. Bologna: Typographia Ferroniana.
- Haller, A. von (1757). Elementa physiologiae corporis humani. Lausanne: Marci-Michaelis Bousquet et Socios.
- Thompson, J. (1893). The muscular architecture of the auricular appendages. Journal of Anatomy and Physiology, 27, 395–412.
- Keith, A. (1903). The anatomy of the right and left auricular appendages. Journal of Anatomy, 37, 289–312.
- James, T. N. (1961). The morphology of the atrial myocardium and the auricular appendages. Circulation, 24, 766–779.
- Lange, G. (1970). Atrial appendage trabeculation and flow patterns. Acta Anatomica, 75, 23–41.
- Kishida, H. (1974). Right atrial appendage morphology in congenital heart disease. Japanese Heart Journal, 15(4), 289–302.
- Henry, J. P., & Pearce, J. W. (1977). Atrial granules and endocrine function of the atrial appendages. American Journal of Physiology, 233, H110–H116.
- de Bold, A. J. (1981). Atrial natriuretic factor: Localization to cardiac atria. Proceedings of the National Academy of Sciences, 78(11), 7603–7607.
- Gerlis, L. M. (1985). Anatomy of the right atrial appendage and its clinical relevance. British Heart Journal, 53(5), 483–489.
- Becker, A. E. (1990). Morphology of the right atrial appendage in relation to arrhythmogenesis. European Heart Journal, 11(Suppl E), 59–67.
- Tabata, T. (1997). Right atrial appendage function assessed by transesophageal echocardiography. Journal of the American Society of Echocardiography, 10(7), 790–798.
- Ho, S. Y., Sanchez-Quintana, D., & Becker, A. E. (2002). Atrial structure and the right atrial appendage: Morphological considerations for electrophysiology. Heart Rhythm, 89, 939–947.
- Kuroiwa, A., & Yamamoto, T. (2006). Three-dimensional architecture of the right atrial appendage. Journal of Cardiac Anatomy, 12(3), 145–158.
- Stiles, M. K. (2008). Right atrial appendage conduction properties in atrial flutter. Heart Rhythm, 5(1), 89–95.
- Hołda, M. K., Koziej, M., & Bolechała, F. (2016). Right atrial appendage morphology in high-resolution CT. Clinical Anatomy, 29(6), 789–798.
- Roux, J. F. (2017). Electrophysiological significance of the right atrial appendage in focal atrial tachycardia. Europace, 19(8), 1383–1391.
- Sato, T. (2019). Hemodynamics of the right atrial appendage using 4D flow MRI. Journal of Magnetic Resonance Imaging, 50(4), 1232–1241.
- Liu, X. (2021). Right atrial appendage thrombus formation in atrial fibrillation: CT-based analysis. Journal of Cardiovascular Computed Tomography, 15(2), 101–109.
- Park, D. (2023). Right atrial appendage function and its endocrine contribution in human ANP physiology. Frontiers in Cardiovascular Medicine, 10, 1324421.
- Delgado, A. (2024). Artificial intelligence–based volumetric analysis of the right atrial appendage. European Heart Journal Imaging, 25(1), 89–104.
Kolesterol
- sıkı safra anlamına gelir. (bkz: kole) (bkz: stereos)
- Kolesterol, lipitler grubuna ait polisiklik alkole verilen isimdir.
- Kolesterini hücre zarından alır ve yağ asiti ile esterleşir.
- high density lipoprotein (hdl)
Kimyasal
İsimlendirme
- Kolesterolün kimyasal adı (IUPAC adı) (3β) -kolest-5-en-3-ol’dur.
- Sistematik adı 2,15-dimetil-14- (1,5-dimetilheksil) tetrasiklo [8.7.0.02,7.011,15] heptacos-7-en-5-ol’dir.
- Diğer isimler:
- (10R, 13R) -10,13-dimetil-17- (6-metilheptan-2-il) -2,3,4,7,8,9,11,12,14,15,16,17-dodekahidro- 1H-siklopenta [a] fenantren-3-ol
- Kolesterol
- Cholest-5-en-3β-ol
- 5-kolesten-3β-ol
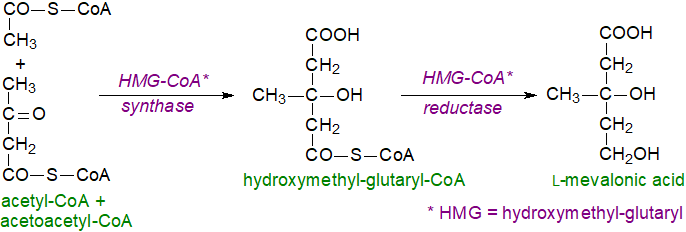
Yapı
Kolesterol molekülü, beş üyeli bir halka ve alifatik bir hidrokarbon radikalinin bağlı olduğu, karakteristik olarak birbirine bağlı üç altı üyeli halkadan oluşur. C5 ve C6 karbon atomları arasındaki çift bağ dışında, moleküldeki tüm bağlar doymuştur. Karbon atomu C3, bir hidroksil grubu taşır. Maddenin moleküler formülü C27H46O’dur. Moleküler kütle (moleküler ağırlık) 386.67 g · mol-1’dir.

Kolesterol, OH grubu üzerinde bir asil kalıntısına sahip olduğu için insan organizmasında serbest veya ester olarak bulunabilir.
biyosentez
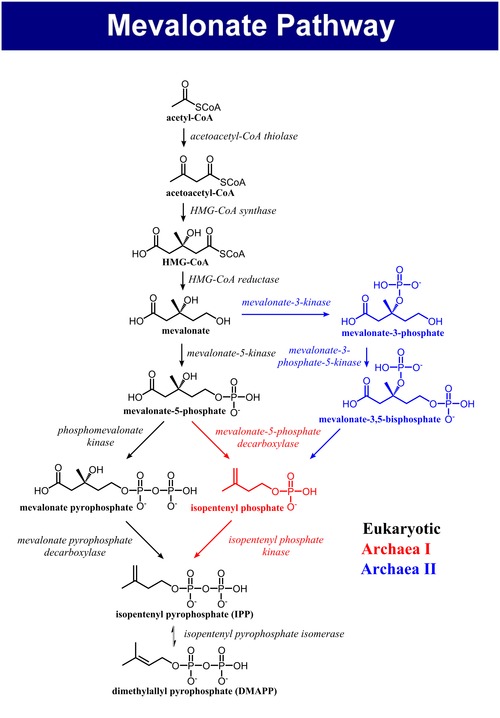
İnsan organizması kolesterolü kendisi sentezleyebilir; karaciğerde her gün 700 mg’a kadar üretilir. Bunun için başlangıç maddesi, asetoasetil-CoA’ya ve daha sonra β-hidroksimetilglutaril-CoA’ya (β-HMG-CoA) metabolize olan asetil-CoA’dır. Bu molekül, sonraki metabolik aşamalarda mevalonata indirgenir ve aktive edilmiş izopren türevleri izopentenil pirofosfat ve dimetilalil pirofosfata dönüştürülür. Kolesterol sentezinin diğer ara ürünleri, farnesil ve geranil pirofosfattır; skualenin döngüsel yapısını oluşturan. Kolesterol nihayet lanosterol yoluyla üretilir.
Bu metabolik yoldaki anahtar enzim, mevalonat oluşumunu katalize eden β-HMG-CoA redüktazdır. Kolesterol eksikliği varsa kolesterol tarafından daha büyük oranda ifade edilir ve baskılanır ve yarı ömrü kısalır. Depolanan enerji eksikliği, enzimin fosforilasyonuna ve dolayısıyla inhibisyona yol açar.
Fizyolojik
Transport
Yüksek düzeyde lipofilik bir madde olan kolesterol, kanda, lenfte ve safrada çözünmez ve bu nedenle ya miseller içinde paketlenmeli ya da lipoproteinlere bağlanarak taşınmalıdır. Besin yoluyla alınan veya karaciğerde sentezlenen kolesterolün taşınması, VLDL ve LDL yoluyla hedef dokulara ve karaciğere ters taşınmada HDL yoluyla gerçekleşir. Lipoproteinler, lipoprotein reseptörlerine bağlanabilir ve bu şekilde, kolesterol miktarına bağlı olarak, biyosentezin diğer reseptörlerinin veya enzimlerinin ekspresyonunu düzenleyen bir sinyal kademesini tetikler.
stereos
Yunancada; sıkı anlamına gelir.
Orikula sinistra
Tanım ve terminoloji
Kalbin atriyal apendiksi (Lat. auricula, “küçük kulak”) atriyum duvarından dışarı doğru uzanan, ince duvarlı, kas çıkıntısıdır. Dış görünümü kulak kepçesini andırdığı için Türkçede kalp kulakçığı olarak da adlandırılır. İki taraflıdır:
- Sağ atriyal apendiks (auricula cordis dextra, İng. right atrial appendage – RAA)
- Sol atriyal apendiks (auricula cordis sinistra, İng. left atrial appendage – LAA)
Klasik anatomi terminolojisinde “auricula” ile “appendage/apendiks” eşdeğer kullanılmaktadır. “(bkz: Orikula)” ve “(bkz: sinistra)” notları sırasıyla kulakçık ve “sol taraf” anlamındaki Latince kökleri işaret eder.
- Auricula: Latince “kulakçık”, genel kullanımda atriyal apendiks anlamındadır.
- Dexter/dextra – sinister/sinistra: Sağ – sol tarafı ifade eder.
- Klinik ve görüntüleme raporlarında “right/left atrial appendage (RAA/LAA)” ile “auricula dextra/sinistra” aynı yapıyı tanımlar.
Makroanatomi ve topografya
Sağ atriyal apendiks (RAA)
- Sınırlar ve bağlantılar: RAA, sağ atriyumun ön-üst bölümünden köken alır ve crista terminalis ile sağ atriyumun düz duvarlı (sinus venarum) kısmından ayrılır.
- Komşuluklar: Önünde ve medialinde çıkan aort (aorta ascendens) yer alır; kök düzeyinde yakın komşuluktur. Yakınında sağ koroner arter başlangıcı bulunur.
- İç yapı: İç yüz pektinat kaslarla (musculi pectinati) belirgin pilili bir morfoloji sergiler; bu kıvrımlar apendiksin kompliyansını artırır.
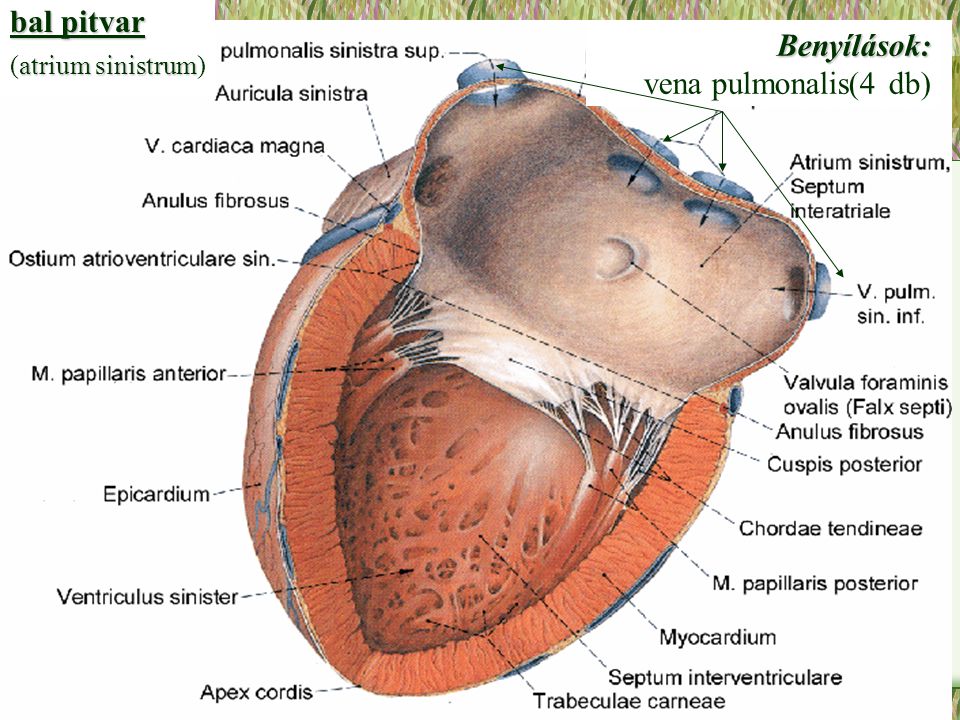
Sol atriyal apendiks (LAA)
- Sınırlar ve bağlantılar: LAA, sol atriyumun superior-anterior duvarından köken alır; ostiyumu sol üst pulmoner ven ve mitral anulus komşuluğundadır.
- Komşuluklar: Ana pulmoner arter boyunca anterolateral yönde uzanır; kalbin ventral yüzünde sol atriyumdan dışarı gözlenebilen tek belirgin kısımdır. Sol ventrikül üst-ön yüzü ve sol ana koroner arter dallarıyla (özellikle sirkumfleks) topografik yakınlık gösterebilir.
- İç yapı: Pektinat kaslar burada da belirgindir; ostiyumdan perifere uzanan trabeküler yapı, akım paternlerini ve tromboz eğilimini etkiler.
Mikroskopik yapı
- Duvar mimarisi: Tek katlı endokard, altında zengin elastik lifli subendokard, onu izleyen ince fakat oldukça kompliyan atriyal miyokard tabakasından oluşur.
- Kas düzeni: Pektinat kaslar longitudinal ve sirküler lif demetleriyle ritim ve hacim değişikliklerine uyum sağlar.
- Nörohümoral hücreler: Atriyal miyositler, özellikle gerilime duyarlı granüllerinde ANP (atriyal natriüretik peptid) sentezler; daha az oranda BNP de üretilebilir.
Embriyoloji ve morfogenez
- Köken: Apendiksler, erken embriyonik ortak atriyum dokusunun kalıntılarıdır. Sağda sinus venarumun gelişimiyle düz duvarlı bölüm ayrışırken, apendiks pektinatlı, “ilkel” atriyal kısmı temsil eder.
- Sol atriyal gelişim: Sol tarafta pulmoner venöz komponentin sol atriyuma inkorporasyonu düz duvarlı alanı oluşturur; LAA, bu sürecin dışında kalıp trabeküler, primitif morfolojisini sürdürür. Bu embriyolojik ayrım, LAA’nın hem şekil çeşitliliğini hem de hemodinamik özelliklerini açıklar.
Morfolojik varyantlar (özellikle LAA)
Görüntüleme serilerinde LAA için dört baskın fenotip tanımlanır; akım ve tromboz riskiyle ilişkili olabilir:
- “Tavuk kanadı (chicken-wing)”
- “Rüzgâr tulumu/windsock”
- “Kaktüs (cactus)”
- “Karnabahar/cauliflower”
Ostiyum çapı, lob sayısı ve boyun uzunluğu, pektinat kas trabekülasyonu ve kulakçık ekseninin bükülme derecesi klinik açıdan önemlidir.
Fizyoloji ve işlev
- Hacim rezervuarı ve kompliyans: Apendiksler, atriyal sistol ve diyastol boyunca genişleyip daralarak atriyal kompliyansa katkı sağlar; venöz dönüş dalgalanmalarını sönümler, mitral-triküspit kapaklara giden akımı “tamponlar”.
- Hormon salgısı: ANP başlıca atriyal miyositlerden salınır; atriyal gerilme arttığında salınım yükselir. ANP; renal sodyum atılımını artırır, diürezi uyarır, RAAS’ı baskılar ve damar düz kasında vazodilatasyon yapar. LAA ve RAA bu endokrin fonksiyona anlamlı katkıda bulunur.
- Elektriksel özellikler: Pektinat kas trabekülasyonu ve fiber yönlenmesi, iletim hızı heterojenliği yaratabilir; özellikle LAA, atriyal fibrilasyon (AF) odaklarının bir kısmına zemin hazırlayabilir.
- Hemodinamik sonuçlar: Cerrahi/kateter-temelli LAA eksklüzyonu sonrası kısa dönemde ANP düzeylerinde azalma ve dolaylı hacim-basınç etkileri bildirilebilir; klinik karşılığı hasta seçimine göre değişir.
Görüntüleme ve değerlendirme
- Transtorasik ekokardiyografi (TTE): Apendiksleri sınırlı çözünürlükle gösterir; özellikle sağ apendiks için bazı pencerelerde değerlendirilebilir.
- Transözofageal ekokardiyografi (TEE): LAA/RAA anatomi, ostiyum çapı, loblar, spontan eko kontrastı ve trombüs açısından altın standart yatakbaşı yöntemdir; kardiyoversiyon veya ablasyon öncesi kritik rol oynar.
- Kardiyak BT (CCTA): 3B anatomiyi, komşulukları ve cihaz planlamasını ayrıntılı gösterir; LAA kapatma (LAAC) öncesi ölçüm ve procedural strateji için sıklıkla kullanılır.
- Kardiyak MR: Doku karakterizasyonu ve fonksiyonel değerlendirme için seçilmiş olgularda yardımcıdır.
- Doppler/CMR akım analizi: LAA içi akım hızlarının düşük olması tromboz riskini artırır; TEE’de LAA boşalma hızı düşükse (örn. <20–25 cm/sn), trombüs ve inme riski artmış kabul edilir.
Klinik önem
Tromboz ve inme
- Patofizyoloji: AF’de atriyal mekanik fonksiyon kaybı, staz, endokardiyal değişiklikler ve hiperkoagülabilite (Virchow triadı) LAA’da trombüs oluşumunu kolaylaştırır.
- Lokalizasyon: Non-valvüler AF olgularında sol atriyal trombüslerin büyük çoğunluğu LAA’da saptanır; bu nedenle LAA, kardiyoembolik inmelerin kilit kaynağıdır.
- Kardiyoversiyon öncesi tarama: Elektriksel kardiyoversiyon ya da sol atriyumu ilgilendiren girişimler (örn. ablasyon) öncesinde TEE ile trombüs dışlama standart yaklaşımdır. Trombüs saptanırsa antikoagülasyonla çözülme beklenir; aksi halde kardiyoembolik inme riski yüksektir.
Antikoagülasyon ve risk katmanlaması
- AF’de CHA₂DS₂-VASc skoru ile inme riski belirlenir ve oral antikoagülasyon (OAK) endikasyonu konur.
- Kontrendikasyon (major kanama, tekrarlayan düşmeler, ileri frajilite, OAK intoleransı) veya hastanın OAK’ı sürdüremeyeceği durumlarda LAA kapatma bir alternatif oluşturur.
Sol atriyal apendiks kapatma (LAAC)
Endikasyonlar
- Yüksek inme riski olup uzun dönem OAK’a kontrendike veya tolere edemeyen AF hastaları.
- Bazen kardiyak cerrahi esnasında ek işlem olarak (örn. mitral cerrahi ile eş zamanlı) yapılır.
Yöntemler
- Perkütan cihazla kapatma:
- Femoral venden transseptal ponksiyonla sol atriyuma geçilir, seçilen cihaz (örn. “tıkayıcı/plug” veya “disk-şemsiye” tasarımları) LAA ostiyumuna yerleştirilir.
- Prosedür öncesi BT-TEE ile ostiyum çapı, boyun uzunluğu, loblanma ölçülerek cihaz boyutu seçilir.
- Cerrahi eksizyon/kapama:
- Açık kalp cerrahisi sırasında rezeksiyon veya dıştan klip (epikardiyal) ile ligasyon yapılabilir.
- Epi-endokardiyal ligasyon sistemleri:
- Seçilmiş olgularda hibrid tekniklerle epikardiyal ligasyon uygulanabilir.
Antitrombotik protokoller
- Cihaz endotelyalizasyonu tamamlanıncaya kadar kısa süreli antitrombotik (ör. DAPT veya kısa OAK) gerekebilir; merkez protokolleri ve cihaz tipine göre değişir.
- Takip TEE’de peridevice sızıntı ve cihaz üstü trombüs kontrolü yapılır.
Olası komplikasyonlar
- Perikardiyal efüzyon/kalp zedelenmesi, cihaz embolizasyonu, inme, vasküler giriş yeri komplikasyonları. Uygun hasta-cihaz seçimi ve görüntüleme ile risk azaltılır.
Diğer klinik durumlar
- Apendiks trombüsü: Sinüs ritminde de (özellikle ciddi sol atriyal dilatasyon veya mitral patolojilerinde) görülebilir; tedavide OAK ve altta yatan nedenin düzeltilmesi esastır.
- Spontan eko kontrastı (“duman”): Düşük akım hızlarının işaretidir; tromboz riskiyle ilişkilidir.
- Apendiks anevrizması (nadir): Özellikle LAA’da raporlanmıştır; ritim bozuklukları ve emboli riski nedeniyle cerrahi düşünülebilir.
- Aritmojenite: LAA odaklı erken uyarılar AF’yi tetikleyebilir; ileri elektrofizyolojik çalışmalarda LAA izolasyonu nadiren başvurulan bir stratejidir.
Cerrahi ve anatomik notlar
- RAA ve LAA’nın trabeküler yapısı, sütür tutuş gücünü artırsa da duvar ince olduğu için perforasyon riski vardır; girişimlerde düşük profilli, yumuşak uçlu kateter sistemleri ve gerçek-zamanlı TEE/BT kılavuzluğu tercih edilir.
- RAA, crista terminalis ile sınırlanan “pektinatlı” bölümün en belirgin uzantısıdır; sinoatriyal düğümün yakın komşuluğu nedeniyle cerrahi ve ablasyonlarda dikkat gerektirir.
Pratik klinik özet noktaları
- Kardiyoversiyon/ablasyon öncesi TEE, LAA/RAA trombüsünü dışlamak için standarttır; saptanırsa girişim ertelenir ve antikoagülasyon optimize edilir.
- Non-valvüler AF’de trombüsün tipik kaynağı LAA’dır; LAA kapatma, uzun dönem OAK uygun değilse kanıta dayalı bir inme önleme seçeneğidir.
- Apendiksler yalnızca “artık” yapılar değildir: atriyal kompliyans ve ANP salınımı yoluyla kardiyovasküler homeostaza katkı sunarlar.
Keşif
1) Erken çizimler ve adlandırma (15.–16. yüzyıl)
- Leonardo da Vinci (≈1510–1513): Erken kalp çizimlerinde atriyumların kulak benzeri çıkıntılarını ayrı hacimler olarak resmeder; “kulakçık” benzetmesinin görsel temeli burada belirginleşir.
- Jacopo Berengario da Carpi (1510’lar–1520’ler): İnsan kalbinin dış şekline dair betimlemeleri aurikulanın ayrı bir çıkıntı olduğunu vurgular.
- Andreas Vesalius (1543): De humani corporis fabrica’da atriyal çıkıntıları tutarlı bir anatomi diliyle yerleştirir; Latince auricula terimi anatomi sözvarlığına kalıcı biçimde girer.
2) Dolaşım devrimi ve işlevsel çerçevenin oluşumu (17. yüzyıl)
- William Harvey (1628): De Motu Cordis ile kapalı devre dolaşımı ispatlayarak atriyumların—dolayısıyla aurikulaların—“pasif çıkıntı” değil, akım düzenleyen odacıklarla bağlantılı yapılar olduğu fikrini sağlam zemine oturtur.
- Richard Lower (1669): Tractatus de Corde; kalbin odacık dinamiklerini deneysel bir düzleme taşır; atriyal yapıların hemodinamik önemine ampirik vurgu yapar.
- Raymond de Vieussens (geç 1600’ler–erken 1700’ler): Atriyal morfoloji, koroner sinus ve komşuluklara ilişkin betimleriyle sağ atriyal bölgenin ayrıntılandırılmasına katkıda bulunur.
3) Sistematik anatomi ve patoloji köprüsü (18. yüzyıl)
- Jean-Baptiste de Sénac (1749): Traité de la structure du cœur…; kalbin yapısı ve hastalıklarını birlikte ele alır, aurikulanın morfolojik özelliklerini klinik gözlemle yan yana getirir.
- Albrecht von Haller (1750’ler): Fizyolojik çerçeve; atriyal dokunun kasılma ve uyumluluk niteliklerinin kuramsallaşması.
- Giovanni Battista Morgagni (1761): De sedibus…; otopsi gözlemleriyle atriyal boşluk ve pıhtılaşma odağını birbirine bağlayan patoloji anlatısını kurar.
4) Kavramların oturması: anatomi atlasları, tromboz düşüncesi ve aritmi (19. yüzyıl)
- Rudolf Virchow (1856): Tromboz ve emboli doktrini; “staz–endotel–hiperkoagülabilite” (Virchow triadı) ile aurikulanın pıhtı için biyomekanik “cep” olabileceği fikri patoloji zemininde mümkün hâle gelir.
- Henry Gray & Henry V. Carter (1858 →): Gray’s Anatomy; aurikulanın makroanatomisi ve pektinat kaslarının düzeni standartlaştırılmış görsellerle ders kitaplarına yerleşir.
- Thomas Lewis (erken 1900’lere köprü): Aritmilerin klinik-elektrofizyolojik betimlemesi; atriyal fibrilasyon kavrayışının sahaya çıkışı (19. yüzyıl sonu–20. yüzyıl başı geçişinde klinik altyapı).
5) Görüntüleme çağının eşiği: ekokardiyografi ve TEE ile “içeriden bakış” (20. yüzyıl ortası–sonu)
- Inge Edler & Hellmuth Hertz (1953): İlk klinik ekokardiyografik kayıtlar; atriyal yapıların canlı görüntülenmesine kapı aralanır.
- Harvey Feigenbaum (1960’lar–1970’ler): Ekokardiyografinin klinik yaygınlaşmasının öncüsü; atriyal yapıların rutin değerlendirilmesi mümkün hâle gelir.
- Werner Aschenberg ve çağdaşları (1980’ler): Transözofageal ekokardiyografi (TEE) ile sol atriyal apendikste trombüs saptanmasının metodolojik standardını kuran erken çalışmalar; kardiyoversiyon/ablasyon öncesi TEE pratiğinin temeli.
6) “Kaynak odak”ın kesinleşmesi ve koruma stratejileri (geç 20. yüzyıl–erken 21. yüzyıl)
- John L. Blackshear & James A. Odell (1990’lar): Atriyal fibrilasyonda inmelerin başlıca kaynağının LAA olduğunu klinik verilerle çerçeveleyen, cerrahi appendiks obliterasyonu fikrini sistematikleştiren öncü yayınlar.
- Kardiyak cerrahinin katkısı (1990’lar): Mitral cerrahiyle eş zamanlı cerrahi LAA eksklüzyonu/ligasyonunun yaygınlaşması; epikardiyal klips ve rezeksiyon tekniklerinin gelişimi.
- İntervansiyonel kardiyolojinin yükselişi (2000’ler): Transseptal yolla perkütan LAA kapatma (PLAATO ile ilk insan serileri; ardından Watchman, Amplatzer/Amulet ailesi).
- David R. Holmes Jr. & Vivek Y. Reddy ve ekipleri: Randomize çalışmalar ve uzun dönem takiplerle LAA kapatmanın antikoagülasyona alternatif/kompleman bir inme profilaksisi yaklaşımı olarak kanıt zemininin oluşturulması.
- Horst Sievert ve ilk-inşan/erken deneyim ekipleri: Cihaz ve teknik evriminin sahadaki öncüleri.
7) Morfoloji–risk eşlemesi ve güncel rafinman (2010’lar →)
Klinik pratiğin standardizasyonu: Kardiyoversiyon/ablasyon öncesi TEE ile LAA trombüs dışlama, antikoagülasyon kararı için CHA₂DS₂-VASc tabanlı katmanlama; OAK kontrendikasyonunda LAA kapatmanın hasta-seçimli uygulanması.
Gelişmiş TEE/BT ekipleri: “Chicken-wing”, “windsock”, “cactus”, “cauliflower” gibi LAA morfotiplerinin tanımlanması; lob sayısı, ostiyum çapı ve boşalma hızının tromboz/inme riskiyle ilişkilendirilmesi.
İleri Okuma
- da Vinci L. (≈1510–1513). Anatomical Manuscripts and Drawings. Royal Collection, Windsor Castle.
- Vesalius A. (1543). De humani corporis fabrica libri septem. Basel: Oporinus.
- Harvey W. (1628). Exercitatio anatomica de motu cordis et sanguinis in animalibus. Frankfurt.
- Lower R. (1669). Tractatus de corde. London.
- Vieussens R. (1706). Traité nouveau de la structure et des causes du mouvement naturel du cœur. Toulouse.
- Sénac J.-B. (1749). Traité de la structure du cœur, de son action, et de ses maladies. Paris.
- Haller A. von (1757–1766). Elementa physiologiae corporis humani. Lausanne.
- Morgagni G.B. (1761). De sedibus et causis morborum per anatomen indagatis. Venice.
- Virchow R. (1856). Gesammelte Abhandlungen zur wissenschaftlichen Medicin. Frankfurt.
- Gray H., Carter H.V. (1858). Anatomy: Descriptive and Surgical. London: J.W. Parker.
- Edler I., Hertz H. (1954). The use of ultrasonic reflectoscope for the continuous recording of the movements of heart walls. Kungl Fysiografiska Sällskapets i Lund Förhandlingar, 24:40–58.
- Aschenberg W., Schlüter M., Kremer P., Schroeder E., Siglow V., Bleifeld W. (1986). Transesophageal two-dimensional echocardiography for the detection of left atrial appendage thrombus. Journal of the American College of Cardiology, 7(1):163–166.
- Blackshear J.L., Odell J.A. (1996). Appendage obliteration to reduce stroke in cardiac surgical patients with atrial fibrillation. Annals of Thoracic Surgery, 61(2):755–759.
- Holmes D.R. Jr., Reddy V.Y., Turi Z.G., Doshi S.K., Sievert H., Buchbinder M., Mullin C.M., Sick P., PROTECT AF Investigators (2009). Percutaneous closure of the left atrial appendage versus warfarin therapy for prevention of stroke in patients with atrial fibrillation: a randomized non-inferiority trial. Lancet, 374(9689):534–542.
- Reddy V.Y., Doshi S.K., Sievert H., Buchbinder M., Neuzil P., Huber K., Halperin J.L., Holmes D.R. Jr., PROTECT AF Investigators (2013). Percutaneous left atrial appendage closure for stroke prophylaxis in patients with atrial fibrillation: 2.3-year follow-up of the PROTECT AF (Watchman Left Atrial Appendage System for Embolic Protection in Patients With Atrial Fibrillation) trial. Circulation, 127(6):720–729.
nota bene
iyi fark edin. (bkz: nota) (bkz: bene).
manus dextra
sağ el. (bkz: manus) (bkz: dextra)
**burdaki istisnada “manus”, sonundaki eke rağmen feminin olarak sayılıp, ona göre çekimlenmiştir “dexter”.
HMG CoA reductase
- -3-hydroxy-3-methylglutaryl-coenzym-a-reduktase açılımıdır.
- -cholesterol sentezi sırasında hız belirleyen enzimdir.
- -çeşitli sentez yolları için hücre zarı bileşenidir, depo yağı ve çıkış maddesidir.