Vascular endothelial growth factor
- Vascular endothelial growth factor (VEGF), orjinali vascular permeability factor (VPF), vasculogenesis ve angiogenesis’i uyarmak için oluşturulan proteindir.
Prostaglandin E2
- prostaglandin E2 (PGE2 or PGE2), tıpta dinoprostone olarak da bilinir.
Prostaglandin endoperoksit sentaz 2
- PTGS2 genin kodladığı bir enzimdir.
- Cox teriminin kullanılmasının sebebi “sitokrom c oksidaz”ailesindeki bir gen olması.
- “PTGS” prostaglandin-endoperoksid sentaz (siklooksigenaz) .
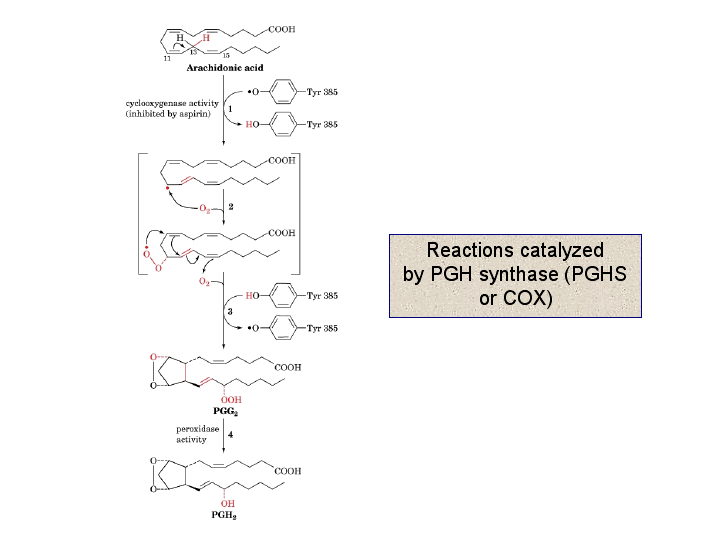
- Siklooksijenaz-2 (COX-2), ayrıca prostaglandin sentaz-2 (PGHS-2), siklooksijenaz-1 (COX-1) gibi, araşidonik asidi iki aşamada eikosanoid prostaglandin H2’ye oksitleyen bir enzimdir.
- COX-1 yapısal olarak eksprese edilirken, COX-2 sentezi sadece hücrelerin yaralanması, iltihaplanması veya filizlenmesi durumunda sitokinler ve mitojenler tarafından indüklenir.
- COX-2’nin spesifik COX-2 inhibitörleri tarafından bloke edilmesi, bu nedenle, steroidal olmayan anti-enflamatuar ilaçlardan bilinen yan etkilerin hiçbirine neden olmaz.
- COX-2 ayrıca plasenta ve fetal erkek genital organlarındaki baskın izoformdur.
- Yeni kan damarlarının oluşumunu düzenleyebilir, bu nedenle kanserde COX-2’nin inhibisyonu şu anda araştırılmaktadır. COX-2, sırayla geniş patojen indüklenebilir oksijenazlar (PIOX’lar) ailesine ait olan siklooksijenazlara aittir.
KRAS
GTPase KRas veya V-Ki-ras2 Kirsten rat sarcoma viral oncogene homolog ve KRAS, KRAS geninin insanda kodladığı proteindir.
Tümör hücreleri
- Kanser hücreleri.
Özellikleri:
- Dış büyüme sinyallerinden bağımsızdırlar.
- Büyüme engelleyicilerine karşı hassiyetlerini kaybetmişlerdir.
- Sınırsız büyüme potansiyeline sahiptir.
- Devamlı olarak yeni Angiogenese gerçekleşerek, hücrelere ihtiyacı olan besinler takviye edilir.
- Dokuları istila ederek, diğer organlarda büyürler.
Gelişimleri:
- Kanser hücreleri, normal vücut hücrelerinden gelişirler.Bu gelişim 3 adımda gerçekleşir.
-
İnisiyasyon( genotoksik maddeler).
- Değişen hücrenin , Tümör promosyonu(Büyüme avantajı)
- değişmiş hücre klonisi → premalig iyi huylu tümör.(kötü huylu maligne hücreleri, premalig iyi huylu hücre topluluklarından oluşur.)

- Karzinogenese yıllar boyunca sürer ve bu süre zarfında yeni mutasyonlar ortaya çıkar.Böylece tümörlerin gelişimi hızlanır.
Suppresörler:
- TGF-α (Bir çok kanserde)
- TGF-β (Kolon kanseri),
- EGFR (Kolon kanseri),
- APC (Kolon kanseri),
- erB2 (Neuroblastome, Mamma, Kolon, Ovarial,..) ,
- SMAD (Kolon, Pankreas) Abl (CML),
- p53 (birçok tümör çeşidinde),
- Ras (Göğüs, Deri, Akciğer, Kolon, Neuroblastom, Leukemien),
- Rb (Retinoblastom, Osteosarkom),
- β-Catenin (Kolon, HCC),
Caretaker (Tümör baskılayıcı gen alt grubudur): DNA hasralarını tamir eder, tamir edilemeyece hücreleri uzaklaştırır.Hasarlar çeşitli tümörlere dönüşebilir:
Fas-Counter-attack:
- Apoptose indüksiyonu azlığı, kanser hücrelerinin Fas-Counterattack yüzünden bağışık sistemine zarar vermesine ve zarar almamasına yol açar.Bunun için hasta hücrelerinin yüzeyindeki death-receptor’leri kullanılır.Kanser hücreleri, düşük Fas ekspressyonu,mutasyonlar ve apoptosenin gerçekleşememesi sayesinde cytotoksik T hücrelerinin ürettiği FasL yüzünden ölmezler. Kanser hücreleri hatta FasL üretirler.(kendilerinde Fas ekspressyonu düzgün olmadığı için ölmezler.)Bu yüzden T hücreleri, kanser hücrelerinden uzaklaşırlar.Buna Fas-Counter-attack denir.
- Apoptose işlevi kaybı, bcl-2 gen ailesinin mutasyonu sonucu oluşur.(pro- ve antiapoptik işleyen bcl-2 proteinleri vardır.)
- Apoptose indüksiyonu direnci oluşmasını sağlayan zararlı moleküller.
- Genel apoptose direncine ek olarak tedavi direncine yol açabilir.ABC taşıyıcı proteinleri, ilacın hücre içine girmesini engelleyebilir.P-Glykoprotein (ABCB1), MRP1 (multi-drug-resistance Protein 1), BCRP (Göğüs kanseri direnç proteini.)
- İlacın etkileşimi değişterecek bir direnç oluşabilir.(CYP, Gluthathiontransferasen,..)
- Yukarıdaki mekanizmaların engellenmesi durumunda, tümör hücrelerine karşı direnç kazanılabilir.Ama p53 hasarlıysa veya ras geni mutasyonluysa yapılacak bir müdahale yoktur.
- Tümör hücrelerinin oluşturduğu direncin bir çok kaynağı olabilir.Örneğin; Kemoterapi sırasında sigara içilmemelidir.Çünkü nikotinin standart kemoterapi ilaçlarının etkisini azalttığı kanıtlanmıştır.
- Hücre içine Substanz taşımanın azalması yada hücre dışına taşımanın artması (Multiple Drug Resistance) da sebebler arasındadır.
- Hücrenin kendisi de inaktifleştirici enzimlere sahip olabilir.
- Damarlarla iyi beslenen bir tümör (Angiogenese) hızlı büyüyüp, kemoterapiye daha iyi cevap verebilir.
- Hücre içinde Cytostatika sayesinde hasarların oluşması için;
- Tümör hücresinde kontrol sistemin(örneğin p53) hala aktif olmalı,
- Bu sistem, oluşan hataları fark etmelidir.
- Tamir mekanizması, bu sisteme karşı çalışmaz, bunun yerine hücre kontrollü ölüme hazırlandırılmak zorundadır.
- Dirençler erkenden tespit edilmelidir, böylece uygun ilaçlar verilip, mutasyonların sıklaşıp tedavinin daha güç olması engellenir.
Oncogene
- Onkogen. normal büyüyen bir hücreden, kontrolsüz gelişen tümör büyümesine geçmeyi sağlayan genlerdir.
Tumor suppressor gene
- antioncogene,Tümör baskılayıcı gen veya tümör supresör gen.
- hücre dönügüsünü kontrol eden veya apoptoseyi uyaran protein.
- Büyüme engelleyen sinyaller üretirler.
- Eksikliğinde hücreler kontrolsüzce büyür ve genetik kararsızlık oluşur.Bu gelişmeleri ek olarak mutasyonlar takip eder ve tümörler gelişir.
BRCA
- BReast CAncer gene
- BRCA genleri, mutasyonları meme kanseri gelişme riskinin artmasıyla ilişkili olan tümör baskılayıcı genlerdir.

Sınıflandırma
- Tümör baskılıyıcı genlerdir, mutasyon olması durumunda patolojiden bahsedilir.
- BRCA1 (BReast CAncer 1, early-onset) kromozom 17
- BRCA2 (BReast CAncer 2, early-onset) kromozom 13
- BRCA3

Patogenez için önemi
Mutasyona uğramış bir durumda, BRCA genleri, hücreler kontrolsüz bir şekilde büyüyebildiğinden, meme ve/veya yumurtalık karsinomlarının gelişimini desteklemektedir. BRCA2 genindeki mutasyonlar ayrıca diğer neoplazmaların (pankreas karsinomu, kolon karsinomu, lenfoma dahil) gelişimini de destekler.
Tüm meme kanserlerinin yaklaşık %5’inin kalıtsal olduğu ve kalıtsal meme kanserlerinin yarısının BRCA genlerindeki mutasyonlardan kaynaklandığı tahmin edilmektedir.
Riskte artış
Meme kanseri riskindeki artış şu şekilde gösterilebilir: Bir hastada BRCA genlerinden birinde mutasyon tespit edilirse, 85 yaşına kadar meme kanserine yakalanma nispi riski %80 civarında yükselir. BRCA olmayan taşıyıcılar için göreceli risk %10 civarındadır. Meme kanseri riskine ek olarak yumurtalık kanseri riski %60’lara kadar çıkmaktadır.
Riskteki artışın boyutu çalışmalarda farklı şekilde verilmektedir. Son bir değerlendirme ve patofizyolojik arka planın daha derinden anlaşılması şu anda hala beklemededir.
Teşhis
İki meme kanseri geni çok büyük olduğu için genlerin incelendiği ve anormal bölümlerin tam olarak sıralandığı bir test ortalama dört ay sürer. Genin tamamı dizilenirse, bir test sonucunun elde edilmesi 18 ay kadar sürebilir.
Genetik teşhisin önemi tartışmalıdır; rutin tarama yaygın değildir. Kalıtsal meme kanseri formları için risk sınıflandırması klinik olarak özel bir aile öyküsüne dayanmaktadır.
Melanocyte-stimulating hormone
- melanocyte-stimulating hormones (α-MSH, β-MSH, γ-MSH, topluca MSH veya intermedins denir)