Halk dilinde: kuşpalazı,

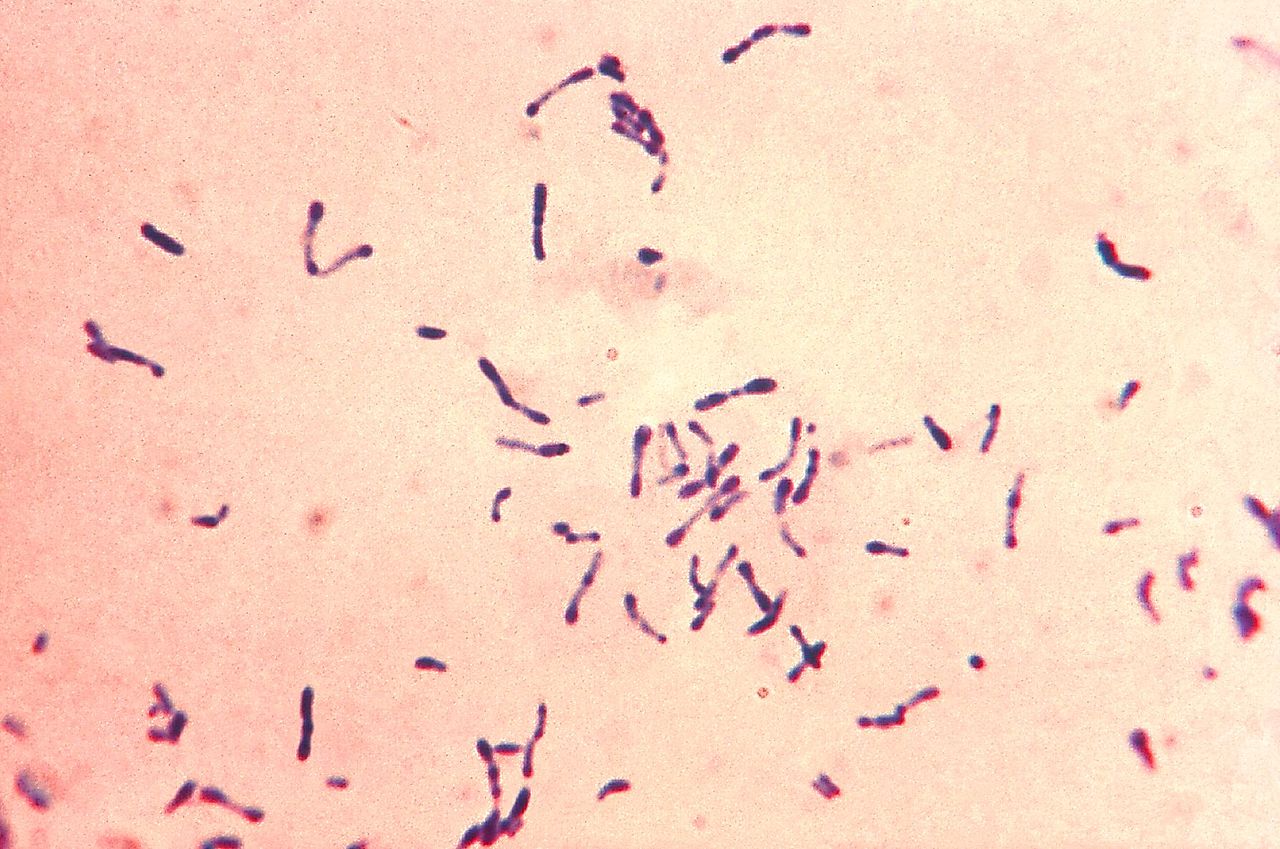
Hastalık difteri adını Yunanca “post” veya “deri” anlamına gelen diphthera kelimesinden alır ve enfekte bireylerin boğazında oluşan sert, kösele gibi yalancı zara atıfta bulunur. Difteri, boğaz, burun, deri, gözler ve diğer mukozal yüzeyleri enfekte edebilen gram-pozitif çubuk şeklinde bir organizma olan Corynebacterium diphtheriae bakterisinden kaynaklanır.
Enfeksiyon Özellikleri
- İnkübasyon Süresi**: Tipik olarak, bakteriye maruz kaldıktan 2-6 gün sonra.
- Enfektivite**:
- Antibiyotik tedavisi ile: enfektivite yaklaşık 2 gün sürer.
- Antibiyotik tedavisi olmadan: 4 haftaya kadar devam edebilir, bu da tedavi edilmemiş vakaları oldukça bulaşıcı hale getirir.
Klinik Sunum
- Erken Belirtiler (Prodromal Faz)** (1-2 gün):
- Genel halsizlik, düşük dereceli ateş ve boğaz ağrısı.
- Hastalar yutma güçlüğü (disfaji), bulantı, baş ağrısı, baş dönmesi ve çarpıntı yaşayabilir.
- Tatlı, donuk veya kokuşmuş karakteristik bir kötü nefes sıklıkla görülür.
- Boyundaki lenf düğümlerinde ağrılı şişme (şiddetli olduğunda genellikle “boğa boynu difterisi” olarak adlandırılır).
- Pseudomembranöz kaplamalar: Difterinin ayırt edici özelliği bademcikler, farinks, larinks veya burun mukozası üzerinde oluşan ve kazındığında kanayan kalın, grimsi psödomembranlardır.
- Şiddetli Belirtiler**:
- Güçlü bir genel hastalık hissi ve önemli rahatsızlık yaygındır.
- Tedavi edilmezse, bu psödomembranlar hava yolunu tıkayarak suffokasyona yol açabilir.
Komplikasyonlar
- Kardiyak Komplikasyonlar: Bakteri tarafından üretilen toksin nedeniyle, özellikle tedavi edilmezse ciddi kardiyak sorunlar ortaya çıkabilir:
- Kas hücresi tahribatına yol açan Toksik miyokardiyal hasar.
- Aritmiler**, *hipotansiyon*, *taşikardiler* ve AV blok ve bundle-branch blok gibi çeşitli kalp bloğu modelleri yaygındır.
- Elektrokardiyografik değişiklikler (ST-segment değişiklikleri)** kardiyak etkinin şiddetini yansıtır.
- Nörolojik Komplikasyonlar**: Difteri toksini sinir sistemini de etkileyerek aşağıdakilere yol açabilir:
- Yumuşak damak parezisi** (erken başlangıçlı).
- 4-6. haftadan itibaren: Disfaji (yutma güçlüğü), burundan sıvı kusması, göz kası felci ve akomodasyon bozuklukları.
- Tek bir uzvu etkileyen polinöritik paralizi, diyafram paralizisi ve potansiyel olarak solunum fonksiyonunu tehlikeye atan abdominal veya torasik kas paralizisi.
Tanı
- Klinik Tanı: Karakteristik psödomembran ve klinik semptomlara dayanır.
- Laboratuvar Tanı**:
- Corynebacterium diphtheriae kültürü için özellikle zarın altından alınan boğaz ve nazofarengeal sürüntü örnekleri**.
- Mikroskobik inceleme**: Bakterileri tanımlamak için *Neisser boyaması* kullanılması.
- Kültür teknikleri**: Difteri bakterileri için seçici bir besiyeri olan *Tellurite Agar* üzerinde üreme.
- Toksin Tespiti: Elek testi (immün difüzyon testi) gibi yöntemlerle.
- PCR: Toksin üreten suşların kesin tanımlanması için polimeraz zincir reaksiyonu kullanılabilir.
Tedavi
- Difteri Antitoksini**: Dolaşımdaki difteri toksinini nötralize eden heterolog bir serum. Toksinin etkilerini sınırlamak için tanı konulduktan sonra mümkün olan en kısa sürede uygulanmalıdır.
- Antibiyotikler:
- Penisilin: Bakterileri yok etmek için en az 2 hafta boyunca 100.000 IU/kg/gün uygulanır.
- Makrolidler: Eritromisin gibi, hastaların penisiline alerjisi varsa alternatif olarak kullanılır.
- Antibiyotiklerle erken müdahale mortaliteyi önemli ölçüde azaltır. Semptomların görüldüğü 1. günde yapılan tedavi %1 civarında bir ölüm oranıyla sonuçlanırken, tedavinin 4. güne kadar geciktirilmesi ölüm riskini yirmi kata kadar artırabilir.
- Semptomatik Tedavi:
- Yatak istirahati**, sedasyon ve anksiyoliz tedavinin kritik bileşenleridir.
- Hava yolu tıkanıklığına yol açabilen laringeal difteri için trakeotomi gerekli olabilir.
- Ciddi kardiyak komplikasyon gelişme riski nedeniyle EKG’ler ile sürekli izleme (4-6 hafta boyunca haftada 2-3 kez) önemlidir.
Profilaksi
- Aktif Bağışıklama:
- Difteriye karşı en etkili korunma stratejisi aşılamadır. Difteri toksoid aşısı** tipik olarak karma aşıların (çocuklar için DTaP, yetişkinler için Tdap veya Td gibi) bir parçası olarak uygulanır. Rutin çocukluk aşılama programları, dünya çapında difteri vakalarında dramatik bir düşüşe yol açmıştır.
- Temas Profilaksisi:
- Difteri hastalarının yakın temaslıları, enfeksiyonun yayılmasını önlemek için pasif bağışıklama (difteri antitoksini) ve penisilin profilaksisi almalıdır.
Keşif
Bir zamanların korkunç bulaşıcı hastalığı difteri, önemli anların ve ilgi çekici hikayelerin damgasını vurduğu zengin bir tarihe sahiptir. Eski salgınlardan modern tıbbi buluşlara kadar, bu ölümcül hastalığa karşı verilen mücadele, insan direncinin, bilimsel ilerlemenin ve halk sağlığı önlemlerinin gücünün hikayesini anlatıyor.
Erken modern dönemde difteri birçok kişi tarafından “boğucu melek” olarak bilinirdi. 1613 yılında İspanya, “El Año de los Garrotillos” ya da “Boğulma Yılı” olarak bilinen ilk büyük salgınlardan birini yaşadı. Hastalık, boğazlarında oluşan kalın, kösele gibi psödomembranların hava akışını keserek kurbanlarını, genellikle de çocukları, boğması nedeniyle özellikle korkulan bir durumdu. O zamanlar hastalık hakkında çok az bilgi vardı ve ebeveynler çocuklarının boğulmaya yenik düşmesini çaresizce izliyordu. Bu terör Avrupa’yı yüzyıllar boyunca etkisi altına almış, salgınlar düzenli olarak ortaya çıkmış ve toplumları harap etmiştir.
19. yüzyıl difterinin anlaşılmasında kritik bir dönüm noktası oldu. 1883 yılında Alman bilim adamı Edwin Klebs difteriden sorumlu bakteriyi, Corynebacterium diphtheriae, tanımladı. Bir yıl sonra Friedrich Löffler bakteriyi izole etmeyi ve etkilerini göstermeyi başardı. Bu çok önemli bir başarıydı çünkü difteriyi gizemli bir hastalık olarak görmekten spesifik bir bakteriyel enfeksiyon olarak anlamaya geçişi işaret ediyordu. Bakterinin tanımlanması, bilim insanlarının bakterinin davranışını incelemesine olanak sağlayarak gelecekteki tedaviler için zemin hazırladı.
Bu bilgi yayıldıkça, bilim insanları hastalıkla mücadele yolları geliştirmek için yorulmadan çalıştılar. En dramatik atılımlardan biri 1890 yılında Emil von Behring ve Shibasaburo Kitasato’nun difteri antitoksini keşfetmesiyle gerçekleşti. Çalışmaları, hayvanlara küçük dozlarda difteri toksini enjekte etmeyi içeriyordu, bu da hayvanların antikor üretmesini sağladı. Bu antikorlar daha sonra çıkarıldı ve bakteriler tarafından üretilen ölümcül toksini nötralize ederek insanları tedavi etmek için kullanıldı. Antitoksinin keşfi çığır açıcı oldu. Dramatik bir vakada, Berlin’deki bir hastanede ölmek üzere olan bir çocuğa yeni keşfedilen serum enjekte edildi ve hem doktorları hem de ebeveynleri hayrete düşüren bir şekilde çocuk saatler içinde iyileşmeye başladı. Difteriyi tedavi etmek için yeni keşfedilen bu yetenek sayısız aileye umut verdi ve von Behring’e 1901 yılında tıp alanında verilen ilk Nobel Ödülü’nü kazandırdı.
1920’lerde Fransız bilim insanları Gaston Ramon ve Alphonse Dochez tarafından difteri aşısının geliştirilmesiyle difterinin öyküsü bir başka önemli dönemece girdi. Aşı, hastalığa neden olmadan bağışıklık sistemini uyarmak için toksinin inaktive edilmiş bir formunu kullanarak önlemede büyük bir adımdı. Bu keşif, difteri tarihinin en ünlü olaylarından biri olan 1925’te Alaska’nın Nome kentinde yaşanan salgın için tam zamanında geldi. Ölümcül bir salgının kasabayı kasıp kavurduğu ve antitoksin stoklarının tükendiği Nome halkı büyük bir sıkıntı içindeydi. En yakın antitoksin 600 milden daha uzaktaydı ve şiddetli kış koşulları kasabanın dünyanın geri kalanıyla bağlantısını kesmişti. Kahramanca bir çabayla, kar fırtınalarına ve aşırı soğuğa göğüs geren bir kızak-köpek ekibi, hayat kurtaran serumu ulaştırmak için Alaska boyunca yarıştı. Balto adlı bir köpeğin liderliğindeki ekipler 674 millik yolculuğu sadece beş buçuk günde tamamladı. Cesaretleri sayısız hayat kurtardı ve Balto’yu New York Central Park’ta bir heykelle ölümsüzleştirilen ulusal bir kahramana dönüştürdü.
20. yüzyılın ortalarına gelindiğinde difteri, yaygın aşılama kampanyaları sayesinde dünyanın büyük bölümünde büyük ölçüde kontrol altına alınmıştı. Kombine DTP (difteri, tetanos, boğmaca) aşısının 1940’larda piyasaya sürülmesi milyonlarca çocuğun aşılanmasını mümkün kılarak difteri vakalarını ve ölümleri büyük ölçüde azalttı. Ancak, İkinci Dünya Savaşı sonrası Avrupa’da difterinin yeniden ortaya çıkması, dünyaya uyanık olmanın gerekli olduğunu hatırlattı. Savaşın harap ettiği Almanya’da aşırı kalabalık, kötü sağlık koşulları ve yetersiz beslenme nedeniyle hastalık ölümcül bir şekilde yeniden ortaya çıkmıştır. Müttefik kuvvetler, savaş sonrası ilk halk sağlığı çabalarından birinde, salgını kontrol altına almak için toplu bir aşılama kampanyası başlattı. Bu kampanya, halk sağlığında uluslararası işbirliğinin ilk örneklerinden biriydi ve aşıların bir hastalığı izinde durdurma gücünü gösterdi.
Difterinin hikayesi 1990’larda Sovyetler Birliği’nin çöküşünün ardından beklenmedik bir geri dönüş yapmasıyla sarsıcı bir hal aldı. Ekonomik zorluklar, sağlık hizmetlerindeki aksaklıklar ve aşılama oranlarındaki düşüş, başta Rusya ve Ukrayna olmak üzere eski Sovyet ülkelerinde büyük bir salgına yol açtı. Yüz binlerce vaka rapor edildi ve binlerce kişi öldü. Salgın, aşılama oranları düştüğünde neler olabileceğinin çarpıcı bir hatırlatıcısı oldu ve hızlı bir uluslararası müdahaleyi teşvik etti. Dünyanın dört bir yanından halk sağlığı kuruluşları aşı ve antitoksin dağıtmak için acele ederek daha fazla yayılmayı önledi. Bu kriz, bir hastalık kontrol altına alınmış gibi görünse bile sağlam aşılama programlarının sürdürülmesinin önemi konusunda güçlü bir ders oldu.
Son yıllarda, devam eden küresel aşılama çalışmaları sayesinde difteri salgınları nadiren görülmüştür. Ancak 2018’de Bangladeş’teki Rohingya mülteciler arasında görülen difteri salgını, aşırı kalabalık ve sağlık hizmetlerine erişimin yetersiz olduğu mülteci kamplarındaki kırılganlıkların hastalığın gelişmesine hala izin verebileceğinin altını çizdi. Uluslararası yardım kuruluşları hızlı bir şekilde müdahale ederek aşı uyguladı ve enfekte olanları tedavi etti, ancak salgın, büyük ölçüde kontrol altına alınmış olsa da difterinin aşılama kapsamının düşük ve yaşam koşullarının kötü olduğu bölgelerde bir tehdit olmaya devam ettiğini hatırlattı.
Difterinin tarihi, yüzyıllar önce halkları dehşete düşürmesinden günümüzde neredeyse yok edilmesine kadar, bilimsel keşiflerin ve halk sağlığının gücünün bir kanıtıdır. Bakterinin tanımlanmasından antitoksin ve aşıların geliştirilmesine ve kurtarılan hayatların dramatik hikayelerine kadar, difteri ile mücadele tıbbın en büyük zaferlerinden biri olarak duruyor. Bununla birlikte, bir zamanlar ölümcül olan bu hastalıktan korunmak için sürekli tetikte olmanın önemini ve aşılamanın kritik rolünü de hatırlatmaktadır.
İleri Okuma
- Behring, E. V. (1890). “Studies on Diphtheria: The Development of the Antitoxin.” Deutsche Medizinische Wochenschrift, 16, 1145-1150.
- Vitek, C. R., & Wharton, M. (1998). “Diphtheria in the Former Soviet Union: Reemergence of a Pandemic Disease.” Emerging Infectious Diseases, 4(4), 539-550.
- Holmes, R. K. (2000). “Biological and Biochemical Properties of Corynebacterium diphtheriae.” Clinical Microbiology Reviews, 13(2), 256-282.
- Rappuoli, R., & Malito, E. (2019). “Historical and Scientific Advances in the Development of the Diphtheria Toxoid Vaccine.” Journal of Vaccine Research, 5(1), 1-6.










Yorum yazabilmek için oturum açmalısınız.