
Kuramsal fizikçiler, kim olduğumuzu belirleyenin sadece DNA’mıza kodlanmış enformasyondan ibaret olmadığını doğruladı. DNA’nın kendi üzerine katlanma biçiminin de hangi genlerin bedenlerimizde ifadesinin (ekspresyonunun) olacağı üzerinde etki yaptığı ortaya kondu.
Bu biyologların yıllardan beri bildiği bir şeydi1. Hatta DNA’nın katlanmasından sorumlu olan proteinlerin bir kısmını belirlemeyi de başarmışlardı2. Şimdi ise bir grup fizikçi, simülasyonlar kullanarak bu gizli bilginin evrimimizi nasıl kontrol ettiğini ilk kez olarak gösterdi.
Bu gelişme pek çok bilimcinin kulağına yeni bir haber olarak gelmeyebilir ama konuya aşina olmayanlar için ikinci düzey DNA enformasyonu hakkında kısa bir özet geçelim. Muhtemelen lise yıllarında, Watson ile Crick’in 1953’te kimliğimizi belirleyen DNA kodunun G, A, S ve T harflerinin bir dizisinden oluştuğunu keşfettiklerini öğrenmişsinizdir. Guanin, adenin, sitozin ve timini simgeleyen bu harflerin sıralaması, hücrelerimizde hangiproteinlerin üretileceğini belirler. Yani eğer gözleriniz kahverengiyse, bunun nedeni DNA’nızda irisinizin içinde koyu renk pigment üretecek bir proteini kodlayan belli bir harf dizisi olmasıdır.
Ama öykü bu kadarla kalmıyor. Çünkü bedeninizdeki tüm hücreler tıpatıp aynı DNA kodu ile işe başlıyor olmasına rağmen, her organ başka bir işleve sahip oluyor. Örneğin mide hücrelerinizin kahverengi göz proteini üretmesi gerekmez, ama sindirim enzimleri yapmaları lazımdır. Peki bu nasıl oluyor?
80’li yıllardan beri bilimciler bu süreci kontrol edenin, DNA’nın hücrelerimiz içindeki katlanış biçimi olduğunu biliyor3. Çevresel etkenlerin de bu süreçte payı olabiliyor. Mesela stresin epigenetik yoluyla bazı genleri açık veya kapalı konuma getirebildiği biliniyor. Fakat asıl kontrol mekanizması DNA katlanmasının mekaniğinden kaynaklanıyor. Bedenimizdeki herbir hücre yaklaşık 2 metre uzunluğunda DNA taşıdığında, sığabilmek için DNA’nın nükleozom adı verilen bir öbek biçiminde sıkıca paketlenmesi gerekiyor.
İşte DNA’nın bu paketlenişi, hücre tarafından hangi genlerin okunacağını yönetiyor. Paketin içinde kalan genler proteinler tarafından ifade edilmiyor; sadece dışta kalanların ekspresyonu gerçekleşiyor. Bu durum, aynı DNA’yı taşıyan hücrelerin nasıl olup da farklı işlevleri olabildiğini açıklıyor.
Son yıllarda biyologlar DNA’nın katlanış yöntemini belirleyen mekanik yönergeleri ortaya çıkarmaya başladı. Gelelim kuramsal fizikçilerin bu konuyla ne ilgisi olduğuna… Hollanda’da bulunan Leiden Üniversitesi’nden bir ekip, bir adım geriye gidip sürece genom ölçeğinden bakarak, bu mekanik yönergelerin de aslında DNA içinde kodlanmış durumda olduğunu bilgisayar simülasyonları ile doğruladı.
Helmut Schiessel liderliğindeki fizikçiler, ekmek mayasının ve fisyon mayasının genomlarını simüle etti ve sonra onlara tüm mekanik yönergeleri içeren rastgele ikinci düzey DNA bilgisi atadı. Bu yönergelerin DNA’nın nasıl katlanacağını etkilediğini ve hangi proteinlerin ifade edileceğini belirlediklerini gördüler. Böylece DNA mekaniğinin de DNA’nın içinde gizli olduğu ve evrimsel açıdan kodun kendisi kadar önemli olduğu anlaşılmış oldu. Bunun anlamı, DNA mutasyonlarının canlıyı etkilemesinin birden fazla yolu olduğu demek oluyor. DNA’daki harfler değiştirilerek de farklılık yaratılabilir, DNA’nın katlanışını belirleyen mekanik yönergeler değiştirilerek de farklılık yaratılabilir.
Sonuçları PLOS One dergisinde yayımlanan bu çalışma, biyologların zaten bildiği birşeyi doğrulamış oldu. Fakat işin heyecan verici yanı, bilgisayar simülasyonlarının devreye girmesiyle birlikte DNA’yı biçimlendiren mekanik yönergelerin kontrolünde bilimcilere yeni olasılıklar doğmuş olması. Belki bir gün istenmeyen genlerin ifadelerinden korunmak için DNA’nın katlanma biçimini değiştirebiliriz.
Kaynaklar:
- Bilimfili,
- Leiden Üniversitesi, “Second layer of information in DNA confirmed”
< http://www.physics.leidenuniv.nl/index.php?id=11573&news=889&type=LION&ln=EN > - Science Alert, “Physicists confirm there’s a second layer of information hidden in our DNA”
< http://www.sciencealert.com/scientists-confirm-a-second-layer-of-information-hiding-in-dna >
İlgili Makale: Behrouz Eslami-Mossallam, Raoul D. Schram, Marco Tompitak, John van Noort, Helmut Schiessel Multiplexing Genetic and Nucleosome Positioning Codes: A Computational Approach PLOS ONE Published: June 7, 2016http://dx.doi.org/10.1371/journal.pone.0156905
Notlar:
[1] Eran Segal, Yvonne Fondufe-Mittendorf, Lingyi Chen, AnnChristine Thåström, Yair Field, Irene K. Moore, Ji-Ping Z. Wang and Jonathan Widom A genomic code for nucleosome positioning Nature 442, 772-778 (17 August 2006) | doi:10.1038/nature04979; Received 16 March 2006; Accepted 14 June 2006; Published online 19 July 2006
[2] https://en.m.wikipedia.org/wiki/Trithorax-group_proteins
[3] http://www.nature.com/milestones/geneexpression/milestones/articles/milegene16.html

 Yeni bulunan bakteri E.coli’yi sadece 30 saniyede öldürebiliyor. Gün geçtikçe antibiyotik direncin artmasıyla süper bakterilerden kaynaklı endişe büyüyor. Bu nedenle antibiyotiklere direnç kazanan güçlenmesi nedeniyle , başa gelebilecek en kötü senaryoyu engellemek için daha fazla araştırma yaparak yeni ilaçların geliştirilmesi gerekiyor. Neyse ki, Singapur’dan bilim insanlarının katkılarıyla geçtiğimi yıllarda umut vadeden gelişimler yaşanıyor. Yeni geliştirilen madde sadece mikropları çabucak öldürmekle kalmıyor, aynı zamanda antibiyotik dirençli bakteri üremesini engelliyor.
Yeni bulunan bakteri E.coli’yi sadece 30 saniyede öldürebiliyor. Gün geçtikçe antibiyotik direncin artmasıyla süper bakterilerden kaynaklı endişe büyüyor. Bu nedenle antibiyotiklere direnç kazanan güçlenmesi nedeniyle , başa gelebilecek en kötü senaryoyu engellemek için daha fazla araştırma yaparak yeni ilaçların geliştirilmesi gerekiyor. Neyse ki, Singapur’dan bilim insanlarının katkılarıyla geçtiğimi yıllarda umut vadeden gelişimler yaşanıyor. Yeni geliştirilen madde sadece mikropları çabucak öldürmekle kalmıyor, aynı zamanda antibiyotik dirençli bakteri üremesini engelliyor.

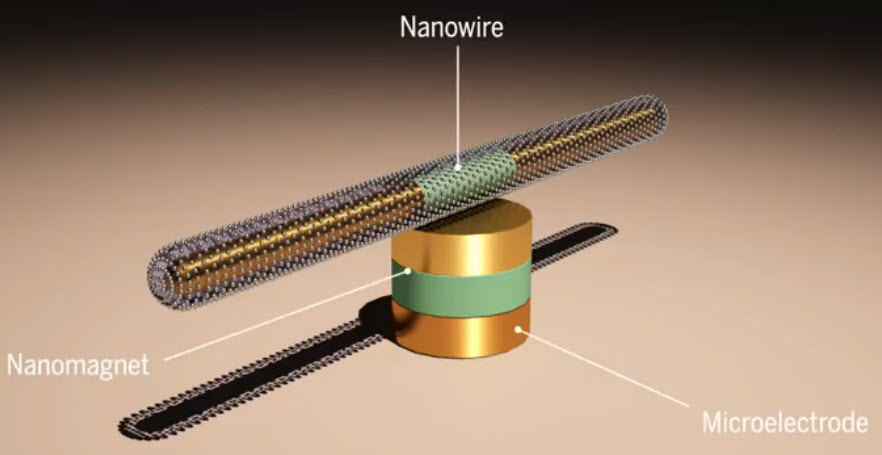
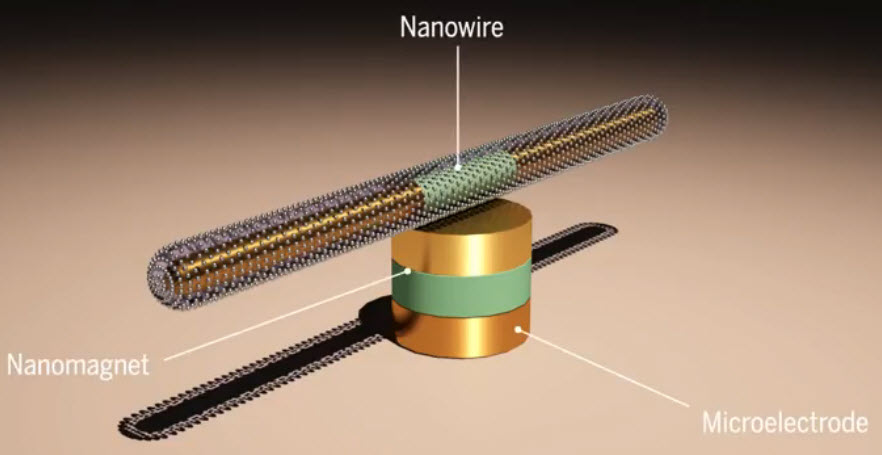 Hayatınızda gördüğünüz ve kullandığınız en küçük motorun boyutlarını sorsam ne söylersiniz? peki bir motor hayal etmenizi isteseler, ne kadar küçük bir motor hayal edebilirsiniz? Hayal ettiğiniz bu motoru siz olsanız ne için kullanırdınız?
Hayatınızda gördüğünüz ve kullandığınız en küçük motorun boyutlarını sorsam ne söylersiniz? peki bir motor hayal etmenizi isteseler, ne kadar küçük bir motor hayal edebilirsiniz? Hayal ettiğiniz bu motoru siz olsanız ne için kullanırdınız?
 Gelelim ikinci ve asıl sorumuza, bu kadar küçük bir motor bizim için ne gibi işler yapabilir, nerelerde kullanılabilir? 15 saat boyunca durmadan çalışabilen, hızı bir jet uçağının motorunun hızını bile geçebilen bu motor sayesinde nano-elektromekanik sistemlerde büyük ilerleme kaydedilebilecek. Fakat daha da önemlisi, canlı hücrelerimize kadar müdahale ederek birçok hastalığın teşhisi ve tedavisinde önemli bir rol oynayacak. Hemen herkes ilaç içtiği zaman, ilacın gitmesi gereken yere nasıl ulaştığı, midemize doğru yol aldığını bildiğimiz ilacın başımızın ağrısını nasıl iyileştirdiğini merak etmiştir. Nanomotorlar bu konu da tam da düşündüğümüz gibi davranıp, vücudun ilaca ihtiyacı olan kısmına, parklarda kullanılan dönen fıskiyeler gibi ilacı yayarak hızlı ve etkili bir tedavi imkanı sunacak. (Motorun dönme hızını ve yönünü ayarlayarak verilecek olan ilaç miktarı ayarlanabiliyor. Araştırmacılar birden fazla nanomoturu belli bir düzen ile dizerek senkronize bir yapı oluşturarak daha güçlü ve fonksiyonel araçlar elde edebiliyorlar.)
Gelelim ikinci ve asıl sorumuza, bu kadar küçük bir motor bizim için ne gibi işler yapabilir, nerelerde kullanılabilir? 15 saat boyunca durmadan çalışabilen, hızı bir jet uçağının motorunun hızını bile geçebilen bu motor sayesinde nano-elektromekanik sistemlerde büyük ilerleme kaydedilebilecek. Fakat daha da önemlisi, canlı hücrelerimize kadar müdahale ederek birçok hastalığın teşhisi ve tedavisinde önemli bir rol oynayacak. Hemen herkes ilaç içtiği zaman, ilacın gitmesi gereken yere nasıl ulaştığı, midemize doğru yol aldığını bildiğimiz ilacın başımızın ağrısını nasıl iyileştirdiğini merak etmiştir. Nanomotorlar bu konu da tam da düşündüğümüz gibi davranıp, vücudun ilaca ihtiyacı olan kısmına, parklarda kullanılan dönen fıskiyeler gibi ilacı yayarak hızlı ve etkili bir tedavi imkanı sunacak. (Motorun dönme hızını ve yönünü ayarlayarak verilecek olan ilaç miktarı ayarlanabiliyor. Araştırmacılar birden fazla nanomoturu belli bir düzen ile dizerek senkronize bir yapı oluşturarak daha güçlü ve fonksiyonel araçlar elde edebiliyorlar.) özellikle diyabet hastaları için insülin hormonunu yöneterek birçok hastaya umut olabilecek bir gelişme.
özellikle diyabet hastaları için insülin hormonunu yöneterek birçok hastaya umut olabilecek bir gelişme.


 Yediğimiz ve içtiğimiz her şey bize gaz yapar. Aslında, günde 1,9 litre veya yaklaşık 15-20 kadar gaz çıkarmak gayet normaldir.
Yediğimiz ve içtiğimiz her şey bize gaz yapar. Aslında, günde 1,9 litre veya yaklaşık 15-20 kadar gaz çıkarmak gayet normaldir.



Yorum yazabilmek için oturum açmalısınız.