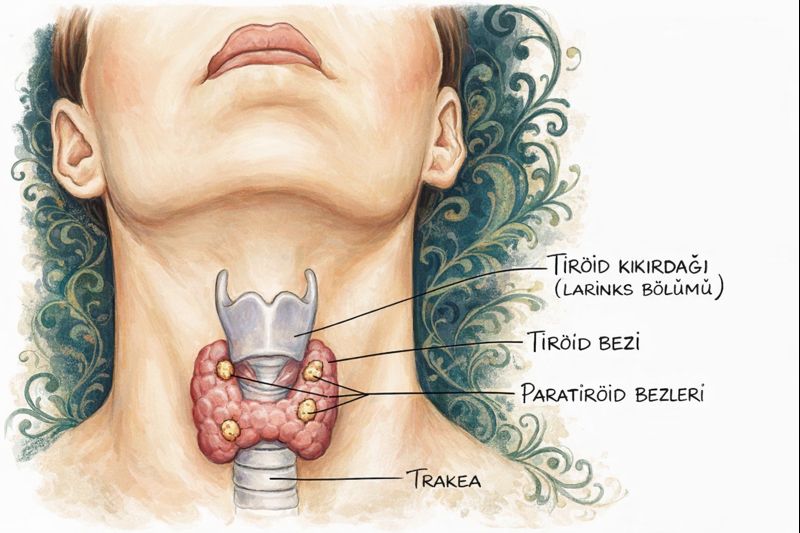
Paratiroid bezleri, anatominin tuhaf bir ironisi gibi durur: dört küçük doku adacığı, çoğu zaman tiroidin arka yüzünde yağ dokusuna karışmış, cerrahın ışığında bir an parlayıp bir an kaybolan, fakat yokluğu dakikalar–saatler içinde bütün organizmayı altüst edebilen bir endokrin kumanda merkezi.
1) Sahne hazırlanıyor: tiroid cerrahisi, tetani ve “anlaşılamayan felaket”
19. yüzyılın ikinci yarısında tiroid cerrahisi hızla yaygınlaşırken hekimler aynı ürkütücü tabloyu tekrar tekrar görmeye başladı: bazı hastalar ameliyattan kısa süre sonra kasılmalar, paresteziler, spazmlar ve bazen ölümle sonuçlanan nöromüsküler bir fırtınaya giriyordu. Bu tabloya “tetani” deniyor, fakat nedenini kimse kesin olarak açıklayamıyordu. Bazıları bunun “kanda biriken toksinler” ya da tiroidin “temizleyici” bir işlevinin kaybı olduğunu düşünüyordu. Sorun şuydu: ameliyat edilen organ tiroiddi; klinik felaket ise sanki sinir–kas sistemini hedef alıyordu. Bu çelişki, tıp tarihinde sık görülen o dönüm noktalarından birini yaratacaktı: anatomik bir ayrıntı, fizyolojik bir kanuna dönüşecekti.
2) “Küçük, ayrı, inatçı”: Sandström ve paratiroidin anatomik keşfi
Bu düğümün ilk somut ipliği, Uppsala’da genç bir anatomistin disseksiyon masasından çıktı. Ivar Sandström, tiroidin yakınında, ondan belirgin biçimde farklı, küçük bezsel yapılar tarif etti. Önemli olan yalnızca “bir şey bulmuş” olması değildi; onu asıl ayırt eden, bu dokuların tiroidin bir parçası olmadığını ısrarla göstermesiydi: ayrı bir kapsül, ayrı bir doku karakteri, ayrı bir topografik kimlik… Bu nedenle paratiroid bezleri, modern anatomi literatüründe sık sık “son büyük anatomik keşif” diye anılır. Keşif, ilk bakışta sessizdi; fakat cerrahi sahnede tetani gibi bir dram varken bu sessizlik uzun sürmeyecekti.
Sandström, insan ve çeşitli memelilerde bu küçük bezleri tanımladı. Adlandırma da bu “yanında olma” gerçeğini taşıdı: para- (yanında) + thyroidea (tiroid). Böylece “paratiroid” kelimesi, hem yerleşimi hem de tarihsel kaderi içinde bir tür gölge kavram oldu: hep tiroidin yanında, hep tiroidin gölgesinde, ama sonunda tiroidin ötesine geçen bir fizyolojiyle.
3) İlk işlev arayışı: Gley, Vassale, Generali ve tetaninin izi
Anatomik keşif, tek başına klinik felaketi açıklamaz. İşlev bulunmadan organ “susar”. 1890’larda fizyologlar, özellikle hayvan deneyleri üzerinden, tiroid ameliyatlarından sonra görülen tetaninin aslında tiroidin değil, bu küçük bezlerin zedelenmesiyle bağlantılı olabileceğini düşündüler.
Eugène Gley’nin çalışmaları burada kritik bir eşik oluşturdu. Farklı deney düzenekleriyle, tetaninin yalnızca tiroidin alınmasına bağlı olmadığını; paratiroid dokusunun kaybı veya hasarıyla belirginleştiğini işaret eden bulgular ortaya koydu. Gley’nin dönemi için zorluk şuydu: paratiroid bezleri çok küçüktü, sayıları ve yerleri değişkendi, disseksiyon ve cerrahi teknikler bugünkü kadar rafine değildi. Bu nedenle aynı deneyin farklı laboratuvarlarda farklı sonuçlar vermesi şaşırtıcı değildi. Yine de tablo giderek netleşti: “tetani” denen şey, büyük olasılıkla bu küçük bezlerin kaybıyla ilgiliydi.
Giuillo Vassale ve Francesco Generali’nin deneyleri ise paratiroidin “hayati” bir işlev taşıdığı fikrini güçlendirdi. Dönemin kavramsal çerçevesi henüz kalsiyum fizyolojisini bugünkü gibi merkezde görmüyordu; bu yüzden bazı yorumlar “antitoksik” bir görev gibi bugün tarihsel bir ara durak saydığımız hipotezlere yaslandı. Fakat bilim tarihinde sık görülen bir durum tekrarlandı: yanlış açıklama bile doğru gözlemi ileri taşır. Paratiroid çıkarılınca tetani oluyordu; bunun neden olduğu daha sonra bulunacaktı.
4) Kalsiyum sahneye giriyor: MacCallum–Voegtlin ve tetaninin kimyası
- yüzyılın başında bir şey değişti: tetani artık yalnızca bir klinik “belirti” değil, ölçülebilir bir metabolik dengesizlik olarak düşünülmeye başlandı. William G. MacCallum ve çalışma arkadaşları, paratiroidin kalsiyum metabolizmasıyla ilişkisini deneysel olarak daha açık biçimde kuran çizgiyi temsil eder. Tetani ile hipokalsemi arasındaki bağlantının netleşmesi, paratiroidin işlevini modern homeostaz diliyle yazmaya başladı.
Bu aşama, hikâyenin en dramatik dönüşlerinden biridir: Bir organın işlevi, “organın ne yaptığı” sorusundan, “organizmanın neyi sabit tuttuğu” sorusuna taşınır. Paratiroid, artık “bir bez” değil, kalsiyumun kan düzeyini dar bir aralıkta koruyan bir kontrol düğümü olarak görülmeye başlanır. Bu, endokrinolojinin olgunlaşma anıdır: küçük bir doku parçası, bütün sinir–kas eksitabilitesinin kimyasal zeminini belirler.
5) Patoloji ve cerrahi kahramanlığı: Erdheim’in düşüncesi, Mandl’in ameliyatı
Paratiroidin yalnızca “yokluğu” değil, “fazlalığı” da bir hastalık üretir. Kemiklerde ağrı, deformite, kırıklar; böbrek taşları; kas güçsüzlüğü; psikiyatrik dalgalanmalar… Bu tablo, daha sonra primer hiperparatiroidizm olarak kavramsallaşacak olan hastalık spektrumunun erken yüzleridir. O dönemde kemik lezyonları “osteitis fibrosa cystica” gibi adlarla tariflenir; paratiroidin kemik üzerindeki etkisi yavaş yavaş anlaşılır.
Felix Mandl’in 1925’te yaptığı paratiroid adenomu çıkarımı, yalnızca bir ameliyat başarısı değildir; aynı zamanda bir “neden–sonuç” iddiasıdır: Eğer bu küçük bezin aşırı çalışması kemik yıkımına yol açıyorsa, o bezi çıkarınca hastalık gerilemelidir. Mandl’in girişimi, paratiroid cerrahisinin tarihini başlatan temel dramatik hamlelerden biri olarak kabul edilir. Cerrah burada, anatomiyi ve yeni doğan fizyoloji bilgisini tek bir noktada birleştirir: boynu açar, küçük bir dokuyu bulur ve bir sistem hastalığını geri çevirir.
6) Hormonun doğuşu: Collip ve “parathormone” fikrinin kesinleşmesi
Bir organın işlevinin “hormonla” anlatılması, endokrinolojinin dilini tamamlar. James B. Collip’in 1920’lerde paratiroid özütleriyle yaptığı çalışmalar, paratiroidin etkisinin bir “kimyasal haberci” üzerinden yürüdüğünü netleştiren dönüm noktalarındandır. Buradaki zorluk, o dönemin biyokimya teknikleri düşünüldüğünde büyüktür: proteinler kırılgandır, özütler inaktiftir, doz–yanıt ilişkisi belirsizdir ve deney hayvanlarında tetani gibi dramatik bir sonlanım, küçük hataları bile büyütür.
Collip’in başarısı, yalnız “aktif madde” elde etmek değil, aynı zamanda şu fikri sağlamlaştırmaktır: Paratiroidin etkisi, kanla taşınan bir hormon aracılığıyla olur; bu hormon kalsiyum düzeyini düzenler ve tetaniyi önler. Böylece “parathormone / parathyroid hormone (PTH)” kavramı, anatomi ve fizyoloji arasındaki köprüyü tamamlar.
7) Moleküler arınma: Rasmussen–Craig ve PTH’nin biyokimyasal saflaşması
Hormon kavramı yerleşse bile, hormonun kendisini saflaştırmak ve tanımlamak ayrı bir çağ gerektirir. 1950’ler–1960’larda Howard Rasmussen ve Lyman C. Craig’in çalışmaları, paratiroid hormonunun biyokimyasal saflaştırılmasına giden yolu temsil eder. Bu dönem, endokrinolojinin “özütlerden moleküllere” geçiş dönemidir. Artık soru şudur: Hangi peptid? Hangi parça aktif? Hangi sekans hangi reseptörü uyarır?
Bu çizgi ilerledikçe PTH’nin parçaları, fragmanlarının farklı biyolojik etkileri ve özellikle PTH(1–34) gibi biyolojik olarak güçlü bölümler klinik farmakolojide giderek önem kazanacaktır. Modern osteoporoz tedavilerinin bir kısmı da bu moleküler parçalanmış bilginin ürünüdür.
8) Hücrenin kulağı: Kalsiyum-duyarlı reseptör (CaSR) ve geri bildirim devrimi
Paratiroid hikâyesinin en zarif bölümlerinden biri, bezin “neyi dinlediğinin” bulunmasıdır. Çünkü paratiroid yalnız hormon salgılayan bir fabrika değil, aynı zamanda kanın iyonik kompozisyonunu anbean izleyen bir sensördür. 1990’larda kalsiyum-duyarlı reseptörün (CaSR) tanımlanmasıyla şu muhteşem fikir moleküler bir gerçekliğe dönüşür: Paratiroid hücresi, kandaki iyonize kalsiyumda çok küçük değişimleri algılar ve PTH salgısını saniyeler–dakikalar ölçeğinde ayarlar.
Bu keşif, klinikte iki büyük kapı açar:
- Genetik hastalıkların anlaşılması: CaSR yolundaki bozukluklar, kalsiyum set noktalarını kaydırarak hipokalsemi–hiperkalsemi spektrumlarında ailevi tablolar oluşturabilir.
- Hedefe yönelik ilaçlar: Calcimimetic (ör. cinacalcet, bazı intravenöz ajanlar) gibi tedaviler, paratiroidin “duyma” mekanizmasını farmakolojik olarak modüle ederek PTH salınımını düşürebilir.
Böylece paratiroid artık yalnızca “PTH üreten bez” değil, “kalsiyumu algılayan ve buna göre PTH üreten bez” olarak tam bir geri bildirim sistemi şeklinde anlaşılır.
9) Görüntüleme ve operasyonun incelmesi: minimal invaziv paratiroidektomi, intraoperatif PTH ve NIRAF
Paratiroid cerrahisi, tarihte en çok “küçük organı bulma sanatı”yla anılır. Klasik bilateral boyun eksplorasyonu, yıllarca standart yaklaşım oldu. Zamanla görüntüleme teknikleri ve intraoperatif biyokimya oyunu değiştirdi:
- İntraoperatif PTH ölçümü ile, çıkarılan dokunun gerçekten “sorunlu paratiroid” olup olmadığı dakikalar içinde biyokimyasal olarak teyit edilebilir hâle geldi.
- Sestamibi temelli nükleer görüntüleme ve SPECT/CT, özellikle tek adenom olgularında hedefe yönelik cerrahiyi kolaylaştırdı.
- 4D-CT ve gelişmiş kesitsel yöntemler, özellikle reoperasyon ve ektopik bez arayışında önemli rol üstlendi.
Daha yeni ve görsel olarak da etkileyici bir kırılma ise yakın kızılötesi otofloresans (NIRAF) teknolojileriyle geldi. Paratiroid dokusunun, bazı dalga boylarında kendine özgü bir otofloresans sinyali vermesi, cerrahın ameliyat sırasında “bu doku paratiroid olabilir” sezgisini bir optik geri bildirimle güçlendiriyor. Bu yaklaşımın hedefi yalnız bezleri bulmak değil; tiroid cerrahisinde paratiroidlerin korunmasını artırarak postoperatif hipokalsemi riskini azaltmak. Son yıllarda bu alanda klinik çalışmaların belirgin biçimde hızlandığı görülüyor; fiber tabanlı sistemlerden kamera tabanlı platformlara uzanan bir teknoloji ekosistemi oluşmuş durumda.
10) Paratiroidin yeni dili: tek-hücre atlasları, epigenetik haritalar ve oksifil hücrenin sırrı
Paratiroid histolojisi, uzun süre iki ana hücre tipinin (chief ve oksifil) “klasik” betimlemesiyle yetindi. Fakat modern biyoloji artık dokuları “hücre kümeleri” değil, hücrelerin durumları ve geçişleri olarak okuyor. Son yıllarda:
- Tek-hücre RNA dizileme ile insan paratiroid dokusunun hücre atlasları çıkarılmaya, chief–oksifil ayrımının dinamikleri anlaşılmaya başlandı. Oksifil hücrelerin yalnız “yaşla artan” pasif bir fenomen olmayabileceği; metabolik, mitokondriyal ve farklılaşma eksenlerinde belirli geçişlerle oluşabileceği fikri güçleniyor.
- Epigenetik ve kromatin mimarisi haritaları, paratiroidin gen düzenleyici ağlarını, hastalık durumlarında hangi düğümlerin kırıldığını, hangi enhancer bölgelerinin aktifleştiğini daha sistematik biçimde göstermeye başladı.
Bu çizgi, hiperparatiroidizm adenomlarının neden belirli gen ağlarına saplandığı, neden bazı olguların agresifleştiği ve neden bazı bezlerin “set noktası” değiştirdiği gibi soruları artık daha sofistike bir düzlemde tartışmaya imkân veriyor.
11) Yeniden yapım hayali: organoidler, kök hücreler, hücre nakli ve “işlevsel bez” üretimi
Paratiroidin biyoteknolojideki en heyecan verici cephesi, son birkaç yılda giderek belirginleşti: Paratiroid dokusunu kültürde uzun süre yaşatmak, hatta organoid düzeyinde “bez benzeri” yapılar üretmek. Bu alanın itici gücü özellikle kronik hipoparatiroidi: yaşam boyu kalsiyum–D vitamini dengesiyle yürüyen, böbrek taşı ve hiperkalsiüri riskiyle uğraşan, kalite-of-life yükü yüksek bir hastalık alanı.
Kök hücre kökenli paratiroid organoidleri ve deneysel modellerde fonksiyon gösteren “bez üretimi” çalışmaları, endokrin replasmanın bir sonraki aşamasını ima ediyor: yalnız hormon vermek değil, hormon üreten ve geri bildirim kuran bir doku sistemini geri kazandırmak. Bugün için bunlar çoğunlukla araştırma düzeyinde; fakat yön net: endokrinoloji, doku mühendisliğiyle birleşiyor.
12) Klinik tedavide güncel eşik: PTH replasmanında uzun etkili moleküller ve Yorvipath dönemi
Hipoparatiroidi tedavisinde uzun yıllar temel yaklaşım, kalsiyum ve aktif D vitaminiyle “yerine koyma”ydı; fakat bu yaklaşım, fizyolojik PTH dalgalanmasını ve böbrek kalsiyum işlenmesini tam taklit edemez. Rekombinant PTH tedavileri bu nedenle önemli bir paradigmaydı.
Son dönemde ise uzun etkili PTH prodrug stratejileri öne çıktı. Palopegteriparatide (TransCon PTH) bu hattın en görünür örneklerinden biri hâline geldi ve düzenleyici onaylarla klinik pratiğe güçlü bir giriş yaptı. Bu gelişme, paratiroid hikâyesinin modern çağdaki simgesel tamamlanması gibi okunabilir: 19. yüzyılda “küçük bez kaybolduğunda tetani oluyor” gözlemiyle başlayan yol, 21. yüzyılda “fizyolojiye yakın PTH replasmanı”na doğru rafine bir terapötik mimariye evrildi.