İçindekiler
1. Kavramsal Çerçeve ve Tanım
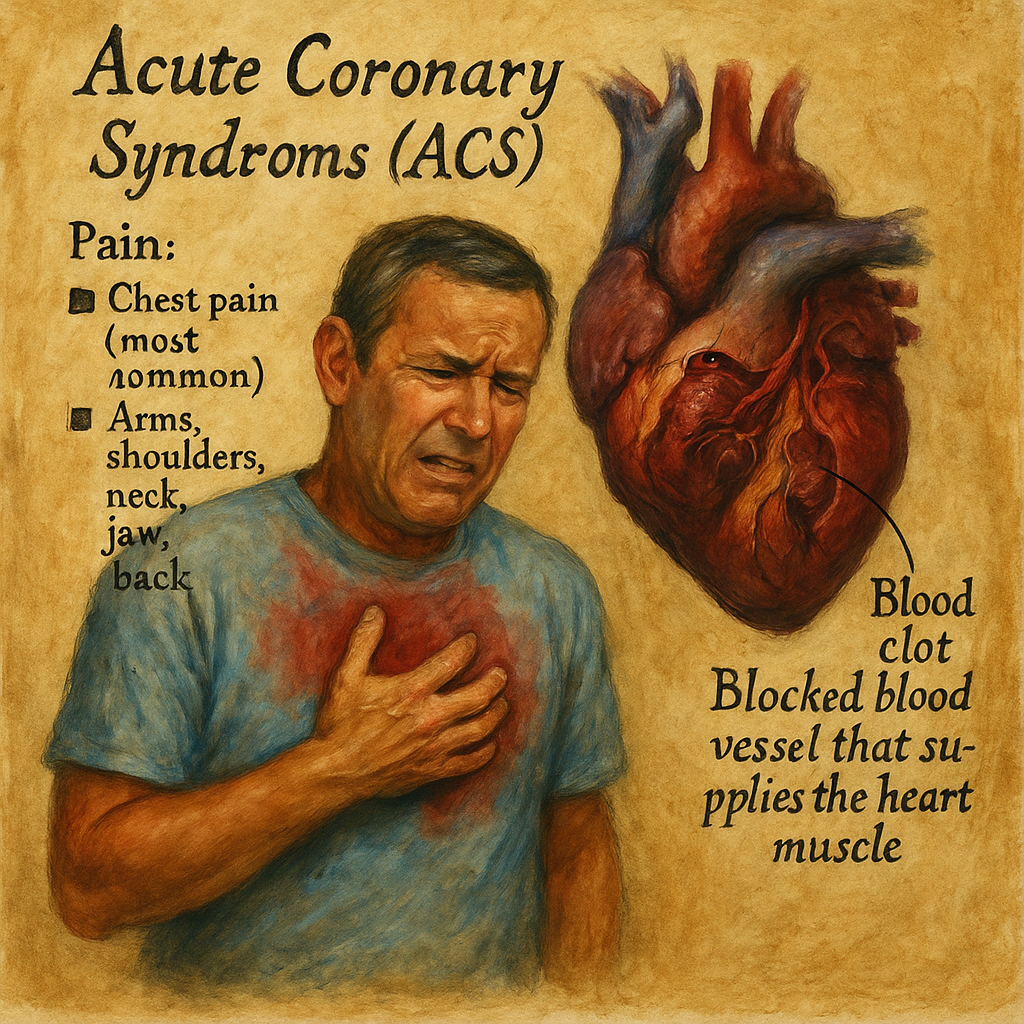
Akut Koroner Sendrom (AKS), kalbi besleyen koroner arterlerin aniden daralması veya tamamen tıkanması sonucunda ortaya çıkan, miyokardiyal iskemi ile karakterize kritik bir klinik durumdur. Temel mekanizma, kalp kasına yeterli oksijen ve besin maddesi ulaştırılamaması nedeniyle gelişen akut iskemik hasar sürecidir.
AKS şunları kapsar:
- ST-segment elevasyonlu miyokard enfarktüsü (STEMI)
- ST-segment elevasyonsuz miyokard enfarktüsü (NSTEMI)
- Stabil olmayan angina pektoris (SAP / IAP)
Bu üç tablo arasındaki fark, trombus miktarı, oklüzyon derecesi, iskeminin süresi, myokard nekrozunun varlığı ve EKG bulgularının özellikleri ile belirlenir.
2. Etimoloji: Kavramların Tarihsel ve Dilbilimsel Serüveni
Tıbbi terimlerin dilsel kökeni, AKS’nin klinik hissiyatını şaşırtıcı bir doğrulukla yansıtır.
Akut
- Latince acutus: “keskin, sivri, ani başlayan”.
- Tıbbi kullanımda hızlı başlangıçlı, dramatik seyirli patolojileri tanımlar.
Koroner
- Latince corona: “taç, çember”.
- Kalbi bir taç gibi saran arterlere “koroner” denilmesi bu görsel benzetmedendir.
Sendrom
- Eski Yunanca syn-dromos: “birlikte koşan / birlikte ortaya çıkan”.
- Bir hastalık değil, ortak bir mekanizmadan kaynaklanan semptom ve bulgu kümesi anlamına gelir.
Angina pectoris
- Angina: Latince angere (“boğmak, sıkıştırmak”) kökünden gelen “boğucu, daraltıcı ağrı”.
- Pectoris: Latince pectus (“göğüs”).
Kombinasyon olarak “göğüs sıkışması / göğüs boğulması” anlamına gelir. Bu terim, hastaların yüzyıllardır neredeyse aynı hisleri tarif etmesiyle dikkat çekicidir.
3. Tarihsel Çizgi: “Göğüs Enfesasyonu”ndan Modern AKS Kavramına
- yüzyılda William Heberden, hastaların yürürken aniden durmak zorunda bırakan, göğüste baskı hissi ile karakterize bir tabloyu “angina pectoris” olarak tanımladı.
- yüzyılda elektrokardiyogramın, ardından koroner anjiyografinin gelişmesiyle şu fark edildi:
- Her göğüs ağrısı enfarktüs değildir.
- Her enfarktüs klasik göğüs ağrısı vermeyebilir.
- Bazı koroner oklüzyonlarda ST elevasyonu olmayabilir (bugün Dr. Smith ve OMI yaklaşımının merkezinde olan keşif).
Bu gözlemler, modern Akut Koroner Sendrom paradigmasını oluşturdu.
4. Patofizyoloji: Aterosklerozdan Akut Tıkanmaya Uzanan Zincir
4.1 Ateroskleroz: Kronik İnflamatuvar Bir Arteriyel Hastalık
Ateroskleroz, yalnızca lipid birikiminden ibaret değildir; kronik, düşük dereceli inflamasyon süreciyle ilerleyen dinamik bir damar duvarı hastalığıdır.
Başlıca risk faktörleri:
- Sigara
- Hipertansiyon
- Diabetes mellitus
- LDL yüksekliği
- Fiziksel inaktivite
- Obezite
- Ailevi yatkınlık
Bu faktörler aşağıdaki olayların başlamasına neden olur:
- Endotel disfonksiyonu
– Damarın iç yüzeyi geçirgenleşir, vazodilatasyon kaybolur, inflamasyon artar. - LDL’in intimaya giriş ve oksidasyonu
– Makrofajlar tarafından fagosite edilerek köpük hücreleri oluşur. - Fatty streak → fibroaterom oluşumu
– Lipid çekirdeği (lipid core) ve fibröz başlık (fibrous cap) gelişir.
4.2 “Initial inflammation çözülebilir”: Patolojik sürecin geri dönüşebilirliği
Erken evre inflamatuvar süreçler belirli ölçüde:
- yoğun statin tedavisi,
- yaşam tarzı değişiklikleri,
- glisemik ve kan basıncı kontrolü
ile stabilize edilebilir veya gerileyebilir.
Yani notundaki ifade bilimsel olarak doğrudur:
“Başlangıç inflamasyonu” gerçekten modüle edilebilir.
Ancak ileri evre plak tamamen kaybolmaz; stabil hâle gelir.
4.3 Vulnerabl (Kırılgan) Plağın Doğası
“Vulnerabl plak” üç ana özellik taşır:
- Geniş, yumuşak lipid çekirdeği
- İnce, kollajen fakiri fibrous cap
- Yoğun makrofaj infiltrasyonu
Bu yapı mekanik olarak kırılgandır. Sonuç:
- Plaque rupture (kırılma)
- Plaque erosion (erozyon, endotel kaybı)
4.4 Trombus Oluşumu ve AKS’nin başlangıcı
Plak yüzeyi bozulduğunda:
- Trombositler plağa yapışır.
- Aktivasyon ve agregasyon başlar.
- Koagülasyon sistemi devreye girer.
- İntraluminal trombus gelişir.
Bu trombus:
- Tam tıkanma → STEMI
- Kısmi tıkanma → NSTEMI
- Geçici / sınırlı → İnstabil angina
ile sonuçlanır.
5. AKS’nin Klinik Görünümü
5.1 Semptomlar
Metindeki semptom listesi oldukça doğru biçimde klinik tabloyu özetlemektedir:
- Göğüste baskı, sıkışma, yanma
- Kola, çeneye, sırta, epigastrik bölgeye yayılım
- Nefes darlığı
- Bulantı, kusma
- Soğuk terleme
- Baş dönmesi, presenkop
Ayrıca şu önemli klinik not eklenmelidir:
- Kadınlarda, yaşlılarda ve diyabetiklerde semptomlar sıklıkla atipiktir: halsizlik, dispne, epigastrik rahatsızlık, çarpıntı.
5.2 Ani ölüm, mekanik komplikasyonlar
AKS’nin en ağır formu akut tam oklüzyon sonucu gelişen:
- ventriküler fibrilasyon,
- kardiyojenik şok,
- veya mekanik yırtılma komplikasyonlarıdır.
6. Tanı: EKG, Troponin, Görüntüleme ve Risk Sınıflaması
6.1 Elektrokardiyografi (EKG)
İlk dakikalarda çekilmelidir. EKG:
- STEMI’yi doğrudan gösterebilir (ST elevasyonu, QRS değişiklikleri).
- NSTEMI’de ST depresyonu veya T dalga inversiyonu görülebilir.
- Normal olabilir (özellikle erken dönemde veya posterior MI’de).
Dr. Steven W. Smith’in OMI (Occlusion MI) yaklaşımı, STEMI-NSTEMI ayrımının bazı okklüzyonları kaçırabileceğini vurgular.
Bu nedenle şu paternler çok kritiktir:
- Hiperakut T dalgaları
- de Winter paterni
- Wellens işaretleri
- Subtil ST değişiklikleri
- Reciprocal değişiklikler
Life in the Fast Lane (LITFL) gibi kaynaklar bu paternlerin global tanınırlığını artırmıştır.
6.2 Biyobelirteçler
- Yüksek duyarlılıklı troponin (hs-cTn) AKS tanısının temel taşıdır.
- Troponin pozitifliği → miyokard nekrozu (NSTEMI / STEMI).
- Troponin negatifliği → instabil angina veya çok erken evre.
6.3 Ek tetkikler
- Ekokardiyografi (wall motion analizi)
- Koroner anjiyografi (altın standart)
- Gerektiğinde CT koroner anjiyografi
6.4 Risk değerlendirme
- GRACE ve TIMI skorları rutin kullanılır.
Metindeki ACS NSQIP değerlendirme aracı, aslında cerrahi sonrası mortalite/morbidite öngörüsü için kullanılan perioperatif risk hesaplayıcısıdır; AKS’nin cerrahi bağlamdaki risk profilini belirlemede kullanılır.
7. Tedavi: Akut Yönetimden Uzun Dönem Bakıma
7.1 Acil Yönetim
Notunda sıralanan tedbirler klinik açıdan doğrudur ve sistematik olarak şöyle sınıflandırılabilir:
A. Destek Tedavileri
- Oksijen (sadece hipoksi varsa)
- Yatak başının yükseltilmesi
- Analjezi / sedasyon
B. Antitrombotik Tedavi
- ASS: 250–300 mg PO veya Aspisol 125 mg IV
- P2Y12 inhibitörü:
- Clopidogrel 600 mg yükleme (örneğin 2 × 300 mg),
- Prasugrel 60 mg (6 tablet × 10 mg)
- Antikoagülan: Heparin veya benzeri ajanlar
C. Anti-iskemik Tedaviler
- Beta-bloker (Metoprolol / Beloc):
Kalp hızını düşürerek oksijen tüketimini azaltır. Doz, nabız ve tansiyona göre ayarlanır. - Nitrogliserin (Perlinganit):
Venodilatasyon ve preload azaltımı, ağrı kontrolü, kan basıncı yönetimi.
7.2 STEMI’de reperfüzyon
- Birincil PCI: Altın standart
- Fibrinoliz: PCI yapılamıyorsa
- CABG: Kompleks lezyonlarda veya sol ana koroner tutulumunda
7.3 Uzun Dönem Tedavi ve Sekonder Korunma
- Dual antiplatelet therapy (DAPT) 6–12 ay
- Yüksek potent statin tedavisi
- ACEİ/ARB/ARNI
- Beta-bloker
- MRA (kalp yetmezliği varsa)
- Yaşam tarzı değişikleri (sigara bırakma, beslenme düzeni, hareket, kilo kontrolü)
8. Evrimsel Tıp Perspektifi: AKS bir “Uyumsuzluk Hastalığıdır”
Modern yaşam tarzı, insan türünün genetik evrimiyle tam bir uyumsuzluk içindedir.
Atalarımız:
- düşük yağlı, yüksek lifli diyetle besleniyor,
- günde onlarca kilometre yürüyordu,
- kısa stres epizodları yaşıyordu (avlanma, kaçma vs.),
- enfeksiyonlarla mücadele için güçlü inflamatuvar yanıt taşıyordu.
Günümüz:
- yüksek kalorili ve yağlı diyet,
- fiziksel hareketsizlik,
- kronik psikososyal stres,
- obezite, insülin direnci,
- aterosklerotik inflamasyon.
Ateroskleroz ve AKS, biyolojik tasarımın modern çevreyle çatışmasının dramatik bir sonucudur.
Eski avantajlı mekanizmalar (yağ depolama, güçlü inflamasyon) bugünün ortamında dezavantaja dönüşmektedir.
Keşif
İnsanın göğsünü sanki görünmeyen bir elin sıkıştırdığı o an, tıbbın tarihine çok geç girdi; ama girdikten sonra, kardiyolojinin bütün dilini değiştirdi. Bugün “Akut Koroner Sendrom (AKS)” dediğimiz kavram, aslında yüzyıllar boyunca parça parça gözlenmiş, yanlış yorumlanmış, korkuyla karışık saygıyla izlenmiş bir fenomenin, yavaş yavaş bilimsel bir dile kavuşmasının tarihidir.
1. Göğüste “baskı” hissi: Antik çağlardan isimsiz bir düşman
Antik Mısır papirüslerinde, Roma yazarlarının satır aralarında, eforla gelen göğüs ağrısından, kola ve boyna yayılan, dinlenince geçen bir rahatsızlıktan söz edilir. Hekimler bu tabloyu çeşitli şekillerde yorumlar: kimine göre “göğse yerleşmiş melankoli”, kimine göre “kötü hava, kötü mizacın dışa vurumu”…
Kalbi besleyen damarlar, o dönem için soyut bir fikirdir; koroner arterler anatomik olarak bilinse bile, göğüs ağrısı – damar tıkanması – ani ölüm üçlüsünü tek bir patofizyolojik eksende birleştirecek bilgi henüz yoktur.
Göğüs ağrısı, bir semptomdur; ama henüz ismi yoktur, henüz “angina pectoris” olmamıştır.
2. William Heberden sahneye çıkar: “Angina pectoris” adını koyan hekim
18. yüzyıl Londrası’nda, Kraliyet Hekimler Koleji’nin saygın üyelerinden William Heberden (1710–1801), klinik gözlemlerini titizlikle not eden bir iç hastalıkları hekimidir. 21 Temmuz 1768’de, kolejde yaptığı bir sunumda, daha önce kimsenin bu kadar berrak tarif etmediği bir sendromdan söz eder:
- Eforla gelen göğüs sıkışması,
- Kola, boyna yayılan ağrı,
- Durunca hızla hafifleyen ama zamanla ilerleyen bir tablo,
- Bazı hastalarda gece uykudan uyandıran ve oturunca azalan ağrı.
Bu tabloya, Latince “boğucu göğüs” anlamına gelen bir ad verir: angina pectoris.
Tanımı 1772’de yayımlandığında, modern KHK (koroner kalp hastalığı) ders kitaplarının girişine konabilecek kadar net bir klinik tablo çizmiştir. Heberden, koroner arter trombozu ile anatomik bağlantıyı tam olarak kurmasa da, göğüs ağrısının öngörülebilir, tipik ve ölümcül yönünü tıp camiasının zihnine yerleştirir.
Angina pectoris, ilk kez kendi adıyla tanınmış olur; ama henüz Akut Koroner Sendrom kavramı doğmamıştır.
3. 19. yüzyıl: Patologlar sahnede – kalp kasındaki “infarkt” fikri
Heberden’in klinik tarifinin ardından 19. yüzyıl boyunca, otopsi salonlarında yeni bir kavram şekillenir: miyokard enfarktüsü. Patologlar, kalp kası dokusunda:
- Soluk, sarı-beyaz alanlar,
- Nekroz, fibrozis,
- Ve bazen de koroner arter içinde pıhtı ile birlikte bu alanları ilişkilendirmeye başlarlar.
Fransız patolog René Marie ve çağdaşları, “miyokard infarktı”nı ayrıntılı tarif ederken, koroner arterlerdeki trombozu da giderek daha sık not ederler. Yine de, bu bulgular uzun süre “istisna” olarak görülür; “kalp krizi” çoğu hekim için hâlâ ani, açıklanamaz bir ölüm nedenidir.
- yüzyılın sonuna gelindiğinde, arteriyoskleroz ve kalp kası nekrozu arasında bağ kurulmaya başlanmıştır; ama yaşayan hastada tanı koymak hâlâ neredeyse imkânsızdır.
4. James B. Herrick: Miyokard enfarktüsünü yaşayan hastaya “yakıştırmak”
- yüzyılın başında, Chicago’da çalışan James Bryan Herrick (1861–1954), tıbbi düşünceyi kökten değiştiren iki büyük katkıda bulunur: biri orak hücreli anemi, diğeri ise miyokard enfarktüsü üzerinedir.
Herrick 1912’de, Amerikan Hekimler Birliği’ne yaptığı bir sunumda ve JAMA’da yayımladığı yazıda, o güne dek çoğunlukla “post-mortem sürpriz” olarak kabul edilen koroner trombozun:
- Her zaman ani ölümle sonuçlanmadığını,
- Uzun süre yaşayabilen hastalarda da görülebileceğini,
- Klinik göğüs ağrısı, EKG bulguları ve otopsi ile aynı tabloyu oluşturduğunu
ortaya koyar.
Herrick’in en çarpıcı yeniliği şudur:
Kalp krizi, yalnızca otopside adı konan, “gizli ve ani bir kader” değildir; tanınabilir, izlenebilir, yönetilebilir bir klinik sendromdur.
Bu fikir, koroner trombozun ve miyokard enfarktüsünün, ilk kez yaşayan hastanın yatağında anlam kazanmasını sağlar. AKS kavramının tohumları, işte burada atılır.
5. Elektrokardiyografi ve “kalbin yazısı”: Görünmeyeni görünür kılan devrim
- yüzyıl sonu – 20. yüzyıl başında Willem Einthoven ve meslektaşları, kalbin elektriksel aktivitesini kayıt edebilmek için string galvanometreyi geliştirirler. Einthoven, EKG derivasyonlarını tanımlar ve kalbin “elektriksel imzası”nı ortaya koyar.
Bir süre sonra, klinisyenler şu bağlantıyı kurar:
- Göğüs ağrısı sırasında EKG’de ST segmenti yükseliyor,
- Kriz geçince veya nekroz tamamlanınca bu değişiklikler farklılaşıyor,
- Bu paternler, Herrick’in anlattığı koroner tromboz vakalarıyla örtüşüyor.
Böylece:
- Angina pectoris → klinik semptom,
- Miyokard enfarktüsü → patolojik ve klinik sendrom,
- EKG → bu süreci gerçek zamanlı gözleyen pencere
olarak birleşir.
Artık kalp krizi yalnızca otopside değil, ekranın çizgilerinde de görülebilmektedir.
6. Koroner arterlerin ilk kez “yaşarken izlenmesi”: Sones ve anjiyografi
1958 yılına gelindiğinde, Ohio’daki Cleveland Clinic’te çalışan bir kardiyolog, tarihin akışını değiştirecek bir hata yapar.
F. Mason Sones Jr., rutin bir kardiyak kateterizasyon sırasında, kontrast maddeyi sol ventriküle vermesi gerekirken, kateter ucu istemeden sağ koroner artere kayar. Sones, enjeksiyonu durdurmaya çalışsa da yaklaşık 30 ml kontrast doğrudan koroner artere verilir.
O an, ekranda ilk kez koroner arterlerin kendisi belirir: canlı, hareketli, daralan, genişleyen damarlar… Hasta, beklenenin aksine ani aritmi ile ölmez; bu da yöntemin dikkatli uygulamayla güvenli olabileceğini düşündürür.
Bu “hata”, kısa sürede kasıtlı bir tekniğe dönüşür:
- Sones, selektif koroner anjiyografi tekniğini geliştirir,
- Melvin Judkins, koroner arterlere uygun şekillendirilmiş kateterler tasarlar,
- Cerrahlar ve girişimsel kardiyologlar, artık daralmanın yeri ve derecesini doğrudan görebilmektedir.
AKS’nin patofizyolojisi artık sadece teorik değildir; gözle görülen bir anatomiye kavuşur.
7. Koroner bakım üniteleri, tromboliz ve revaskülarizasyon çağı
1950’ler ve 60’lar, kalp krizinin yalnızca “kaçınılmaz ölüm” olmadığının, iyi izlenirse ve hızlı müdahale edilirse dönüştürülebileceğinin keşfedildiği yıllardır.
- Koroner bakım üniteleri (Coronary Care Units) kurulur,
- Sürekli EKG izlemi ile aritmiler hızla fark edilip tedavi edilir,
- Mortalitenin, sadece bu organizasyonel değişiklikle bile ciddi oranda azaldığı gösterilir.
1960’lar ve 70’lerde, antikoagülan tedaviler ve trombolitik ilaçlar (streptokinaz, daha sonra alteplaz vb.) miyokard enfarktüsünde kullanılmaya başlanır. 1977’de Andreas Grüntzig, Zürich’te ilk başarılı perkütan translüminal koroner anjiyoplasti (PTCA) girişimini yapar; aynı dönemde Werner Porstmann da benzer teknikler geliştirir. Koroner damarları içeriden balonla genişletmek, birkaç yıl önce hayal bile edilemeyen bir fikirdir. (CIRSE)
Bu dönemde artık üç şey nettir:
- Göğüs ağrısı sendromları klinik olarak tanımlanabilmekte,
- Koroner arter darlıkları anjiyografiyle görüntülenebilmekte,
- Tıkanan damar ilaçla veya mekanik yöntemle yeniden açılabilmektedir.
Ancak klinik sınıflama hâlâ “angina – enfarktüs” ekseninde, biraz kaba ve ikili bir yapıya sahiptir; Akut Koroner Sendrom ifadesi henüz yaygınlaşmamıştır.
8. AKS kavramının doğuşu: STEMI, NSTEMI ve instabil angina
- yüzyılın son çeyreğine gelindiğinde, klinisyen ve araştırmacılar şunu fark eder:
- Göğüs ağrısı ile gelen hastaların bir kısmında ST elevasyonu var,
- Bir kısmında yok ama troponin (o dönemde CK-MB) ve klinik tablo nekrozu düşündürüyor,
- Bir kısmında ise troponin yükselmemiş, ama tablo stabil olmayan, sık tekrar eden, dinlenmekle bile gelen angina.
Bu durum, klinik yaklaşımı “infarkt var – yok” ikiliğinden çıkarıp daha rafine bir sınıflamaya zorlar.
Yavaş yavaş şu çerçeve yerleşir:
- STEMI (ST Elevasyonlu Miyokard Enfarktüsü)
→ Genellikle tam damar oklüzyonu, transmural nekroz, belirgin ST elevasyonu. - NSTEMI (ST Elevasyonsuz Miyokard Enfarktüsü)
→ Kısmi veya geçici oklüzyon, subendokardiyal nekroz, ST depresyonu / T dalga değişiklikleri. - İnstabil Angina Pektoris
→ Klinik olarak “dinlenme veya minimal eforla gelen, yeni başlayan veya belirgin kötüleşen angina”, fakat biyobelirteç yükselmesi yok.
Bu üçlük, patofizyolojik olarak aynı süreklilik üzerinde dizilir; hepsi birer Akut Koroner Sendromdur, ama nekrozun derecesi ve EKG bulgusu farklıdır.
Bu sırada troponin testlerinin duyarlılığı artar; bazı “eski tip instabil angina” vakalarının aslında küçük NSTEMI olduğu anlaşılır. “AKS” terimi böylece kılavuzlara ve ders kitaplarına girer; yalnızca semptomu değil, damar içi sürecin çerçevesini anlatan bir üst kavrama dönüşür.
9. Plak rüptürü, plak erozyonu ve ötesi: Patofizyoloji derinleşiyor
- yüzyılın ortasında, AKS’nin ana mekanizması, basitçe “aterosklerotik plak + trombus = enfarktüs” şeklinde özetlenebilirken, 21. yüzyıla gelindiğinde bu resim belirgin biçimde karmaşıklaşır.
İleri patoloji, intravasküler görüntüleme (IVUS, OCT) ve klinik çalışmalar sayesinde şu ayrımlar yapılır:
- Plak rüptürü: İnce fibröz başlığın yırtılması, altındaki lipid çekirdeğinin kanla temas etmesi, yoğun tromboz.
- Plak erozyonu: Fibröz başlık sağlam kalırken yüzeysel endotel kaybı, nispeten daha az lipidik ve daha fibrotik plaklar; sıklıkla daha genç, çoğu zaman kadın hastalarda.
- Kalsifiye nodül: Kalsifik kitlelerin lümene doğru protrüzyonu ve bunların etrafında trombus oluşumu.
- Non-aterosklerotik nedenler: Koroner vazospazm, spontan koroner arter diseksiyonu (SCAD), emboli vb.
Güncel çalışmalar, özellikle plak erozyonunun AKS vakalarının hatırı sayılır bir kısmından sorumlu olduğunu ve bu hastaların klasik “büyük lipid çekirdekli, ince başlıklı” rüptür plaklarından klinik ve biyolojik olarak ayrılabileceğini gösteriyor. (OUP Academic)
Böylece AKS, artık sadece “tıkandı – açalım” basitliğindeki bir damar olayı değil; çeşitli mikro-anatomik ve inflamatuvar yolların ortak klinik ifadesi olarak anlaşılmaya başlanıyor.
10. Dr. Smith, OMI ve “göze görünmeyen” oklüzyonlar
Klasik kılavuzlar STEMI’yi ST elevasyonu üzerinden tanımlarken, acil tıp ve kardiyoloji pratiğinde çalışan bazı hekimler, akut tam damar oklüzyonu olan ama STEMI kriterlerini karşılamayan hastaları tekrar tekrar görmeye başladı.
Bu bağlamda, özellikle Stephen W. Smith ve ekibinin yaptığı çalışmalar, OMI (Occlusion MI) kavramını öne çıkarır:
- Her ST elevasyonu olan enfarktüs değildir,
- Ama her tam damar oklüzyonu da STEMI kriterlerini karşılamak zorunda değildir.
Hiperakut T dalgaları, de Winter paterni, Wellens bulguları, “subtil” ön duvar değişiklikleri gibi paternler, artık STEMI dışı OMI göstergeleri olarak kabul görmeye başlar. FOAMed ekosisteminde “Dr. Smith’s ECG Blog” ve Life in the Fast Lane (LITFL) gibi kaynaklar, bu bilgi birikimini dünya çapında yayar.
Böylece AKS kavramının bir başka evrimi ortaya çıkar:
Sadece ST segmentine değil, bütün EKG morfolojisine, klinik bağlama ve troponin dinamiğine bakan, daha “zihinli” bir tahlil.
11. 21. yüzyılda AKS araştırmaları: Moleküler, görüntüleme, biyomekanik ve kişiselleştirilmiş tıp
Günümüzde AKS araştırması birkaç ana eksende ilerliyor:
11.1 İntravasküler görüntüleme ve biomekanik modelleme
IVUS, OCT ve yeni nesil görüntüleme teknikleri, koroner damar içini adeta histoloji kesiti gibi görmemizi sağlıyor. Bu veriler:
- Plak başlığının kalınlığı,
- Lipid çekirdeğinin büyüklüğü,
- Mikrokalsifikasyonlar,
- Lokal kesme gerilimi (shear stress)
gibi parametrelerin sayısal olarak değerlendirilmesine yol açtı.
Son yıllarda yayımlanan çalışmalar, bu görüntüleri bilgisayar temelli biomekanik modellerle birleştirerek, hangi plağın ne zaman ve hangi koşullar altında rüptüre uğrayacağını öngörmeye çalışıyor.
11.2 Plak erozyonu ve farklı tedavi stratejileri
Plak erozyonunun, bazı hastalarda tam stentleme yerine sadece farmakolojik tedaviyle yönetilebileceği, böylece stent ilişkili komplikasyonların azaltılabileceği yönünde çalışmalar yürütülüyor. Özellikle OCT rehberli stratejiler, “stentsiz” AKS tedavisinin güvenli olup olamayacağını test ediyor.
11.3 İnflamasyon, lipidler ve genetik
- Yüksek potent statinler,
- PCSK9 inhibitörleri,
- İnflamasyonu hedefleyen ajanlar (örneğin IL-1β blokajı, colchicine çalışmaları)
AKS riskini azaltmada, artık yalnızca LDL düşürmenin değil, damar duvarındaki inflamatuvar ortamı değiştirmeyi de hedefliyor.
Genom düzeyinde, hangi bireylerin daha “vulnerabl plak” geliştirmeye meyilli olduğunu, hangi inflamatuvar imzaların yüksek riskle ilişkili olduğunu araştıran çok sayıda çalışma sürüyor.
12. Bir kavramın olgunlaşması: Göğüs ağrısından moleküler AKS’ye
Heberden’in “göğüste tuhaf bir sıkışma” diye anlattığı tablo ile, bugün OCT görüntüsünde fibröz başlığı mikron düzeyinde ölçülen bir plak arasındaki mesafe ilk bakışta çok büyük görünebilir. Ama tarihsel çizgiye baktığımızda, bu aslında son derece tutarlı bir evrimdir:
- Antik çağ: İsimsiz göğüs ağrısı.
- yüzyıl: Heberden ile angina pectoris adlı bir klinik sendrom.
- yüzyıl: Patologlarla miyokard enfarktüsü kavramı.
- yüzyılın başı: Herrick ile koroner tromboz ve enfarktüsün yaşayan hastada tanınması.
- yüzyıl ortası: EKG ve koroner anjiyografi ile görünür hale gelen damarlar.
- yüzyıl sonu: STEMI, NSTEMI, instabil angina üçlüsüyle Akut Koroner Sendrom çatısı.
- yüzyıl: Plak rüptürü, erozyonu, kalsifiye nodüller, OMI, intravasküler görüntüleme, biomekanik modelleme ve kişiselleştirilmiş antitrombotik ve lipid düşürücü tedaviler.
Bugün AKS dendiğinde, artık yalnızca göğüs ağrısını değil; genlerden damar duvarına, inflamasyondan EKG morfolojisine, yaşam tarzından sağlık sistemlerinin organizasyonuna kadar uzanan çok katmanlı bir biyolojik ve toplumsal fenomeni kast ediyoruz.
İleri Okuma
- Greenslit, F.F. (1941). Origins of a clinical concept of coronary thrombosis. MD Thesis, University of Nebraska (digitalcommons.unmc.edu).
- Segall, H.N. (1945). The first clinico-pathological case history of angina pectoris. Bulletin of the History of Medicine, 18(1), 47–57 (JSTOR).
- Leach, M.A. (1967). History of Angina. Res Medica, 6(3), 25–32 (journals.ed.ac.uk).
- Roberts, C.S. (1990). Herrick and Heart Disease. In: Clinical Methods (3rd ed.). NCBI Bookshelf (NCBI).
- Jay, V. (2000). The Legacy of William Heberden. Archives of Pathology & Laboratory Medicine, 124(12), 1750–1753 (meridian.allenpress.com).
- Khan, I.A. (2002). Initial historical descriptions of the angina pectoris. Annals of Emergency Medicine, 40(2), 216–223 (ScienceDirect).
- Antman, E.M., et al. (2004). ACC/AHA guidelines for the management of patients with ST-elevation myocardial infarction. Journal of the American College of Cardiology, 44(3), E1–E211.
- Bruschke, A.V.G., et al. (2009). A Half Century of Selective Coronary Arteriography. Journal of the American College of Cardiology, 54(22), 2139–2151 (ScienceDirect).
- Amsterdam, E.A., Wenger, N.K., Brindis, R.G., Casey, D.E., Ganiats, T.G., Holmes, D.R., … Levine, G.N. (2014). 2014 AHA/ACC guideline for the management of patients with non–ST-elevation acute coronary syndromes. Journal of the American College of Cardiology, 64(24), e139–e228.
- Roffi, M., Patrono, C., Collet, J.P., Mueller, C., Valgimigli, M., Andreotti, F., … Aboyans, V. (2016). 2015 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. European Heart Journal, 37(3), 267–315.
- Harold, J.G. (2019). Myocardial Infarction: Evolution in Diagnosis, Care, Prognosis. American College of Cardiology – Harold on History (American College of Cardiology).
- Pfeiffer, D. (2020). Coronary Balloon Angioplasty is due to two physicians born in Saxony, Germany. European Heart Journal (CIRSE).
- Bruschke, A.V.G., et al. (2009). A Half Century of Selective Coronary Arteriography. Journal of the American College of Cardiology, 54(22), 2139–2151 (ScienceDirect).
- Yuan, D., et al. (2023). New Concepts on the Pathophysiology of Acute Coronary Syndrome. Journal of Clinical Medicine, 12(9), 3127 (PMC).
- Mohyeldin, M., et al. (2024). F. Mason Sones Jr.: The serendipitous discovery of coronary angiography and its lasting impact on cardiology. Current Problems in Cardiology (PMC).
- Al-Ammash, M.S.J. (2024). Advances in understanding and managing acute coronary syndrome: Pathophysiology, diagnostic innovations and therapeutic strategies. Journal of Research in Cardiology (Journal of Rare Cardiovascular Diseases).
- Kraler, S., et al. (2025). Acute coronary syndromes: mechanisms, challenges, and new frontiers. European Heart Journal, 46(29), 2866–2883 (OUP Academic).
- Riascos-Bernal, D.F., et al. (2025). Pathogenesis of plaque erosion. Progress in Cardiovascular Diseases (ScienceDirect).
- Buonpane, A., et al. (2025). Uncovering Plaque Erosion: A Distinct Pathway in Acute Coronary Syndromes. Journal of Clinical Medicine, 14(15), 5456 (MDPI).
- Wang, L., et al. (2025). Role of biomechanical factors in plaque rupture and erosion. Coronary Artery Disease (Nature Partner Journal) (Nature).
Yorum yazabilmek için oturum açmalısınız.