Albiglutid iki temel unsurdan oluşan bir isimdir:
- “Albi-“: Bu önek muhtemelen “albumin”den türemiştir ve ilacın yapısını, iki modifiye edilmiş glukagon benzeri peptid-1 (GLP-1) molekülünü insan albüminine bağlayan bir füzyon proteini olarak yansıtır. Albümin, insan kan plazmasındaki önemli bir proteindir ve dahil edilmesi ilacın vücuttaki yarı ömrünü uzatır.
- “-glutid”: Bu ek, genellikle glikoz düzenlemesinde rol oynayan bir hormon olan glukagon benzeri peptid-1’in (GLP-1) analogları veya taklitleri olan ilaçlar için kullanılır. “-glutid” eki, bu ilaç sınıfı için standarttır ve bir GLP-1 reseptör agonisti olarak mekanizmasını gösterir.
Yani, “albiglutid” ismi esasen “albumin-GLP-1 analoğu” anlamına gelir ve doğrudan moleküler yapısına ve farmakolojik etkisine atıfta bulunur.
Önemli Noktalar
- Tip 2 diyabet için bir GLP-1 reseptör agonisti olan Albiglutid, 2014 yılında onaylandı ancak güvenlik endişelerinden değil ekonomik nedenlerden dolayı 2017 yılında üretimi durduruldu.
- Araştırmalar, 2018 Harmony Outcomes çalışmasında gösterildiği gibi kardiyovasküler riskleri azalttığını öne sürüyor ancak artık mevcut değil.
- Eksenatid, liraglutid ve semaglutid gibi mevcut alternatifler, benzer faydalarla diyabet yönetimi için yaygın olarak kullanılıyor.
Genel Bakış
Albiglutid, bir zamanlar tip 2 diyabet için bir tedaviydi ve GLP-1 hormonunu taklit ederek kan şekerini kontrol etmeye yardımcı oluyordu. Haftalık enjeksiyon olarak veriliyordu ve insülini artırarak, glukagonu azaltarak ve mide boşalmasını yavaşlatarak çalışıyordu. Ancak, 2017 yılında üretimi durdurulduğu için artık piyasada değil. Buna rağmen, Harmony Outcomes çalışması gibi onayından sonra yapılan çalışmalar, kalp riski taşıyan diyabet hastaları için önemli olan kardiyovasküler faydaları olduğunu öne sürüyor.
Güncel Durum ve Alternatifler
Bugün, exenatide (StatPearls), liraglutide ve semaglutide gibi diğer GLP-1 reseptör agonistleri standart tedavilerdir. Bu ilaçlar daha iyi kan şekeri kontrolü ve potansiyel kilo kaybı gibi benzer faydalar sunar ve genellikle diyet, egzersiz veya diğer diyabet ilaçlarıyla birlikte kullanılır.
Yan Etkiler ve Güvenlik
Yaygın yan etkiler arasında mide bulantısı, ishal ve enjeksiyon yeri reaksiyonları bulunurken pankreatit gibi nadir ciddi riskler de vardır. Kanıtlar bunların yönetilebilir olduğuna doğru eğilmektedir, ancak hastalar özellikle kesilmesi göz önüne alındığında doktorlarıyla görüşmelidir.
Giriş
Glukagon benzeri peptid-1 (GLP-1) reseptör agonisti olan Albiglutid, tip 2 diabetes mellitus (T2DM) tedavisi için geliştirilmiş ve 2014 yılında sırasıyla Eperzan ve Tanzeum marka adları altında hem AB’de hem de ABD’de onaylanmıştır. GlaxoSmithKline (GSK) tarafından pazarlanan bu ilaç, 8. pozisyondaki alanini glisin ile değiştirerek elde edilen dipeptidil peptidaz-4 (DPP-4) bozunumuna karşı direnci nedeniyle 6 ila 8 günlük yarı ömre sahip, haftada bir kez deri altına uygulanan uzun etkili bir enjekte edilebilir ilaç olarak tasarlanmıştır. Bu anket notu, Albiglutide’in mekanizması, klinik kullanımı, kesilmesi ve 20 Nisan 2025 itibarıyla GLP-1 reseptör agonistlerinin daha geniş manzarası içindeki yeri hakkında ayrıntılı bir inceleme sunmaktadır.
Etki Mekanizması ve Klinik Kullanım
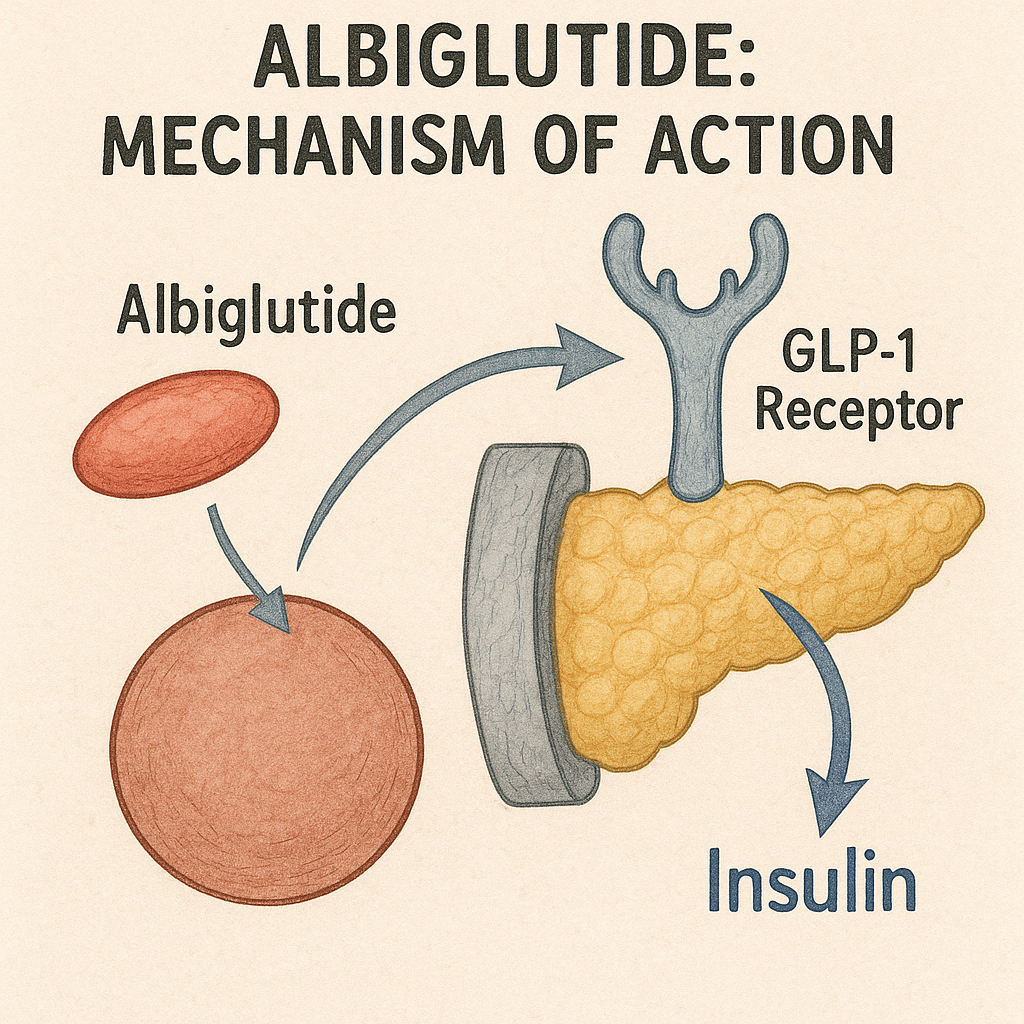
Albiglutide, insan albüminine bağlı bir GLP-1 dimerinden oluşan ve vücuttaki ömrünü uzatan bir rekombinant füzyon proteinidir. Glikoz metabolizması için çok önemli olan inkretin hormonu GLP-1’in etkisini taklit eder. Etkileri şunlardır:
- İnsülin salgılanmasını uyarma: Yüksek kan şekeri seviyelerine yanıt olarak pankreas beta hücrelerinden insülin salınımını artırır.
- Glukagon salgılanmasını azaltma: Glukagon salınımını baskılayarak hepatik glikoz üretimini azaltır.
- Mide boşalmasını yavaşlatma: Mide boşalmasını geciktirir, yemek sonrası glikoz yükselmelerini azaltır ve tokluk hissini artırarak potansiyel olarak kilo yönetimine yardımcı olur.
Diyet ve egzersizin tek başına veya diğer oral antidiyabetik ilaçlar veya insülinle birlikte yeterli glisemik kontrol sağlamadığı durumlarda T2DM’li yetişkinler için endikedir. Haftada bir kez uygulanması hasta rahatlığı açısından önemli bir avantajdı.
Yan Etkiler ve Güvenlik Profili
Klinik çalışmalarda belgelendiği gibi en yaygın yan etkiler şunlardır:
- Mide bulantısı
- İshal
- Enjeksiyon bölgesi reaksiyonları (kızarıklık, şişlik veya ağrı)
Nadir de olsa ciddi yan etkiler şunları içerir:
- Pankreatit (pankreas iltihabı)
- Hipoglisemi, özellikle sülfonilüreler veya insülin ile kullanıldığında
- İnsanlarda kesin olarak bağlantılı olmasa da tiroid C hücreli tümörler için potansiyel risk
- Döküntü, nefes alma zorluğu veya şişlik gibi alerjik reaksiyonlar
Kontrendikasyonlar arasında Albiglutide’e karşı şiddetli aşırı duyarlılık öyküsü, medüller tiroid karsinomu veya multipl endokrin neoplazi sendromu tip 2 yer alır. Hastalara, özellikle uzun vadeli kullanım etkileri göz önüne alındığında, sağlık hizmeti sağlayıcılarıyla riskleri ve faydaları tartışmaları önerildi.
Üretimin Durdurulması ve Ekonomik Faktörler
Onaylanmasına rağmen, Albiglutide 2017 yılında üretimi durduruldu ve GSK, özellikle sınırlı reçeteleme ve düşen satışlar gibi ekonomik nedenlerle dünya pazarından çekildiğini duyurdu (Drugs.com). 2018’e gelindiğinde, kalan stoklar tükendi ve 2025 itibarıyla temin edilemez hale geldi. Bu karar, güvenlik veya etkinlik endişelerinden değil, ticari uygulanabilirlikten kaynaklandı; 2015 tarihli bir analiz, glikozlanmış hemoglobini (HbA1c) düşürme ve kilo kaybını teşvik etme konusunda liraglutid gibi diğer GLP-1 agonistlerinden daha az etkili olduğunu, ancak enjeksiyon yeri reaksiyonları dışında daha az gastrointestinal yan etkiye sahip olduğunu gösteriyordu (Wikipedia).
Tedavinin Sonlandırılmasından Sonraki Çalışmalar: Harmony Sonuçları
İlacın kesilmesinden sonra bile, Albiglutide’in klinik verileri analiz edilmeye devam etti, özellikle 2018’de The Lancet‘te yayınlanan Harmony Sonuçları çalışması aracılığıyla (The Lancet). Bu çift kör, randomize, plasebo kontrollü çalışma, T2DM ve kardiyovasküler hastalığı olan hastalarda kardiyovasküler (KV) güvenliğini ve etkinliğini değerlendirdi. Temmuz 2015’te başlatılan ve tedavinin kesilmesinden sonra tamamlanan çalışma, Albiglutide’in KV ölüm, miyokard enfarktüsü ve felç dahil olmak üzere majör olumsuz kardiyovasküler olayları (MACE) azaltmada plasebodan üstün olduğunu buldu. Bu bulgu, Albiglutide’in 2014 onayı sırasında daha az belirgin olan GLP-1 reseptör agonistlerinin kardiyovasküler faydalarına ilişkin kanıt tabanına katkıda bulunduğu için önemliydi.
Harmony Outcomes denemesi, 28 ülkede 611 merkezde randomize edilen 9.463 hastayı içeriyordu ve sonuçlar 2018 Avrupa Diyabet Çalışmaları Derneği kongresinde sunuldu (GSK Basın Bülteni). Albiglutide’in CV güvenlik profilini belirleyerek, glisemik kontrolün yanı sıra sert CV sonuçlarında iyileşmeler gösterdi, ancak bu faydaların mekanizmaları daha fazla araştırma gerektiriyor (American College of Cardiology).
Güncel Alternatifler: 2025’te GLP-1 Reseptör Agonistleri
Albiglutide’in kesilmesiyle birlikte, diğer GLP-1 reseptör agonistleri T2DM için standart tedaviler haline geldi. 2025 itibarıyla, son klinik kılavuzlara ve araştırmalara göre, aşağıdakiler yaygın olarak reçete edilmektedir:
| İlaç | Dozaj Sıklığı | Temel Faydalar | Önemli Çalışmalar |
|---|---|---|---|
| Eksenatid | Günde iki kez veya haftada bir kez | Glisemik kontrolü ve kilo kaybını iyileştirir | StatPearls |
| Liraglutid | Günde bir kez | Kardiyovasküler faydalar, kilo kaybı | ScienceDirect |
| Lixisenatid | Günde bir kez | Yemek sonrası glikoz kontrolü | Vikipedi |
| Dulaglutid | Haftada bir kez | Kardiyovasküler risk azaltma | PMC |
| Semaglutid | Haftada bir kez (enjekte edilebilir) veya günlük (oral) | Güçlü glisemik ve kilo kaybı etkileri | Cleveland Clinic |
Bu ilaçlar, insülin salgılanmasını artırma, glukagonu baskılama ve mide boşalmasını yavaşlatma gibi ortak mekanizmalara sahiptir ve gerektiğinde genellikle metformin, sülfonilüreler veya bazal insülin ile birlikte kullanılır. GLP-1 agonistleriyle ilgili son tedarik sorunları 2024’ün sonlarında çözüldü ve hastalar için bulunabilirlik sağlandı (Diabetes UK).
Karşılaştırmalı Etkinlik ve Güvenlik
Albiglutide ile karşılaştırıldığında, semaglutide gibi mevcut GLP-1 reseptör agonistleri, obezite yönetimi için STEP gibi denemelerde görüldüğü gibi, HbA1c’yi düşürmede ve kilo kaybını teşvik etmede üstün etkinlik göstermiştir. Albiglutide’in olumsuz olay profili olumluydu ve enjeksiyon bölgesi reaksiyonları dışında, plasebodan biraz daha fazla gastrointestinal sorun ancak liraglutide gibi bazı rakiplerinden daha azdı. Sınıf bir bütün olarak düşük hipoglisemi riski ile ilişkilidir ve bu da onu kardiyovasküler komorbiditeleri olan hastalar için uygun hale getirir.
Henüz Bilinmeyen Noktalar ve Gelecekteki Araştırmalar
Albiglutide’in 2014’teki onayında, uzun vadeli etkiler, diğer ilaçlarla olası etkileşimler ve nadir görülen yan etkiler belirsizlik alanlarıydı. Harmony Outcomes çalışması bazı kardiyovasküler bilinmeyenleri ele aldı, ancak durdurulmasıyla birlikte Albiglutide ile ilgili daha fazla araştırma sona erdi. Mevcut araştırmalar, daha yeni GLP-1 reseptör agonistlerine odaklanıyor, alkolsüz yağlı karaciğer hastalığı ve bağımlılık gibi endikasyonları araştırıyor ve geliştirilmiş etkinlik için ikili agonistleri (örn. GLP-1/GIP) optimize ediyor.
İleri Okuma
- Madsen, K., Knudsen, L. B., Agersø, H., et al. (2007). Structure–activity and protraction relationship of long-acting glucagon-like peptide-1 derivatives: importance of fatty acid length, polarity, and bulkiness.
Journal of Medicinal Chemistry, 50(24), 6126–6132.
https://doi.org/10.1021/jm070709s - Matthews, J. E., Stewart, M. W., De Boever, E. H., et al. (2008). Pharmacodynamics, safety, and tolerability of albiglutide, a long-acting GLP-1 mimetic, in patients with type 2 diabetes.
Journal of Clinical Endocrinology & Metabolism, 93(12), 4810–4817.
https://doi.org/10.1210/jc.2008-1162 - Wang, Y., Liu, J., Xiang, G. (2009). Human GLP-1-Fc fusion protein with prolonged activity on glucose tolerance control.
Journal of Pharmacy and Pharmacology, 61(3), 389–394.
https://doi.org/10.1211/jpp.61.03.0011 - Bush, M. A., Matthews, J. E., Han, J., et al. (2009). Pharmacokinetics and pharmacodynamics of albiglutide, a long-acting GLP-1 receptor agonist, in healthy subjects and subjects with type 2 diabetes mellitus.
Journal of Clinical Pharmacology, 49(8), 879–888.
https://doi.org/10.1177/0091270009335762 - Rosenstock, J., Reusch, J., Bush, M. A., Yang, F., Stewart, M. W. (2010). Potential of albiglutide, a long-acting GLP-1 receptor agonist, in type 2 diabetes: A randomized controlled trial.
Diabetes, Obesity and Metabolism, 11(11), 1000–1007.
https://doi.org/10.1111/j.1463-1326.2009.01098.x - Pratley, R. E., Nauck, M., Barnett, A. H., et al. (2014). Once-weekly albiglutide versus liraglutide in patients with type 2 diabetes inadequately controlled on oral drugs (HARMONY 7): a randomised, open-label, multicentre, non-inferiority phase 3 study.
The Lancet Diabetes & Endocrinology, 2(4), 289–297.
https://doi.org/10.1016/S2213-8587(13)70160-3 - Tanzeum [Albiglutide] FDA Approval Package (2014).
United States Food and Drug Administration (FDA).
NDA 125431 Approval Letter and Clinical Pharmacology Review.
https://www.accessdata.fda.gov - Nauck, M. A., Petrie, J. R., Sesti, G., et al. (2016). A phase 3, randomized, open-label trial comparing the efficacy and safety of once-weekly albiglutide with thrice-daily insulin lispro added to titrated insulin glargine in patients with type 2 diabetes (HARMONY 6).
Diabetes Care, 39(2), 230–238.
https://doi.org/10.2337/dc15-1247













Yorum yazabilmek için oturum açmalısınız.