2021’de ABD ve AB’de enjeksiyon için bir çözüm olarak onaylandı (ABD: Adbry®, AB: Adtralza®).

- Tralokinumab, atopik dermatit tedavisi için monoklonal antikorlar grubundan bir anti-inflamatuar ve immünomodülatör ilaçtır.
- Etkiler, sitokin interlökin-13’ün bağlanmasına ve inaktivasyonuna dayanır.
- İlaç deri altına enjekte edilir.
- En yaygın olası advers reaksiyonlar arasında üst solunum yolu enfeksiyonu, konjonktivit, enjeksiyon bölgesi reaksiyonları ve eozinofili yer alır.

Kimyasal
Yapı ve özellikler
Tralokinumab, biyoteknolojik yöntemler kullanılarak üretilen bir insan monoklonal IgG4 antikorudur. 1326 amino asitten oluşur ve moleküler kütlesi 147 kDa’dır.
Etkileri
- Tralokinumab, anti-inflamatuar ve immünomodülatör özelliklere sahiptir.
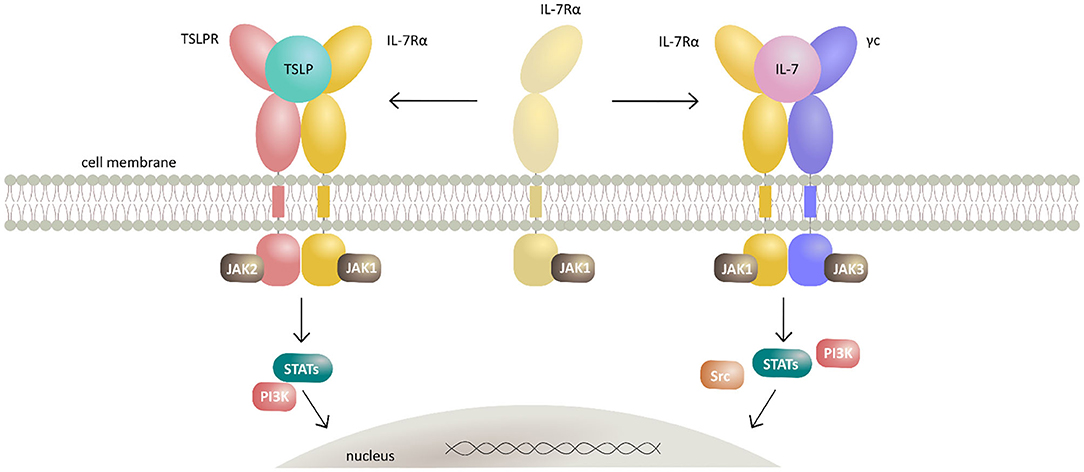
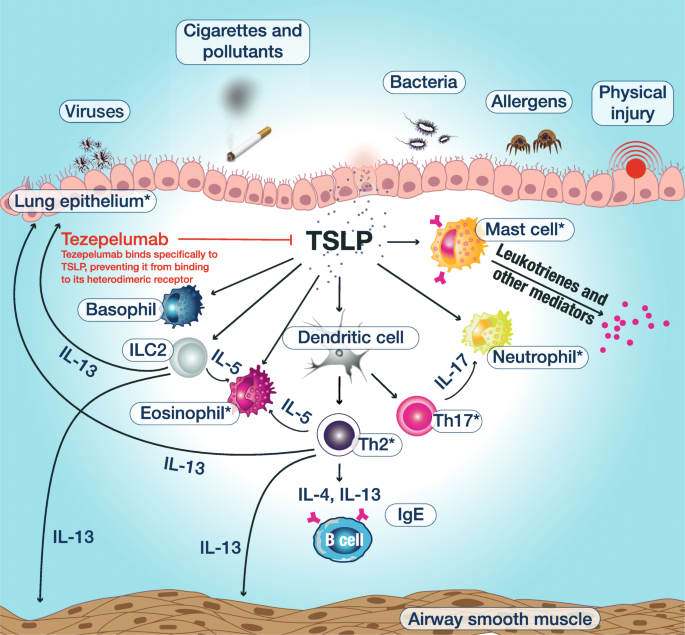
- Etkiler, sitokin interlökin-13’e (IL-13) bağlanmaya dayanır.
- Bu, IL-13 reseptörünün a1 ve a2 alt birimleri ile etkileşimi engeller. Tralokinumab, IL-13’ün etkilerini ve diğer sitokinlerin, kemokinlerin ve IgE’nin salınımını inhibe eder.
- Antikorun 3 haftalık uzun bir yarı ömrü vardır.

Endikasyonlar
Atopik dermatit tedavisi için.
Teknik bilgilere göre dozajlanır. İlaç deri altına enjekte edilir.
Kontrendikasyonlar
- aşırı duyarlılık
Tam önlem önlemleri, profesyoneller için ilaç bilgilerinde bulunabilir.
Etkileşimler
Canlı aşılarla kombinasyon önerilmez.
istenmeyen etkiler
En yaygın olası advers reaksiyonlar arasında üst solunum yolu enfeksiyonu, konjonktivit, enjeksiyon bölgesi reaksiyonları ve eozinofili yer alır.