Ticari isimler: Brilique®
Ticagrelor adı ilacın kimyasal adından türetilmiştir: (1S,2S,3R,5S)-3-[7-[(1R,2S)-2-(3,4-diflorofenil)siklopropilamino]-5-( propiltiyo)-3H-[1,2,3]triazolo[4,5-d]pirimidin-3-il]-5-(2-hidroksietoksi)siklopentan-1,2-diol.
İsminin ilk kısmı olan tica, ilacın çekirdek yapısı olan triazolopirimidin halka sisteminin kimyasal adından gelmektedir. İsmin ikinci kısmı olan grelor, proteinlerin etkisini bloke ederek çalışan ilaçlar için kullanılan yaygın bir ektir.
Ticagrelor ilk olarak 2000’li yılların başında AstraZeneca tarafından keşfedildi. Amerika Birleşik Devletleri’nde Gıda ve İlaç İdaresi (FDA) tarafından 2011 yılında kullanılması onaylanmıştır. Ticagrelor, Brilinta markası altında pazarlanmaktadır.
Ticagrelor, kan pıhtılarını önlemek için kullanılan diğer ilaçlar olan klopidogrel ve prasugrel’den daha yeni bir ilaçtır. Ticagrelor’un kalp krizi ve felçleri önlemede klopidogrel ve prasugrel’den daha etkili olduğu gösterilmiştir.
Ticagrelor kan pıhtılarını önlemek için güvenli ve etkili bir ilaçtır. Ancak ciddi olabilecek kanama risklerinin farkında olmak önemlidir. Ticagrelor kullanıyorsanız kanama riskiniz ve bunu nasıl yönetebileceğiniz konusunda doktorunuzla konuşmalısınız.

Hareket mekanizması:
Ön ilaç olan klopidogrel ve prasugrelin aksine tikagrelor, metabolik aktivasyon gerektirmeyen aktif bir ilaçtır. Trombositlerin üzerindeki P2Y12 reseptörüne geri dönüşümlü olarak bağlanarak trombositlerin toplanıp pıhtı oluşturmasını önler. Etkileri diğer P2Y12 inhibitörleriyle karşılaştırıldığında daha hızlıdır ve ilaç kesildiğinde daha çabuk geçer.
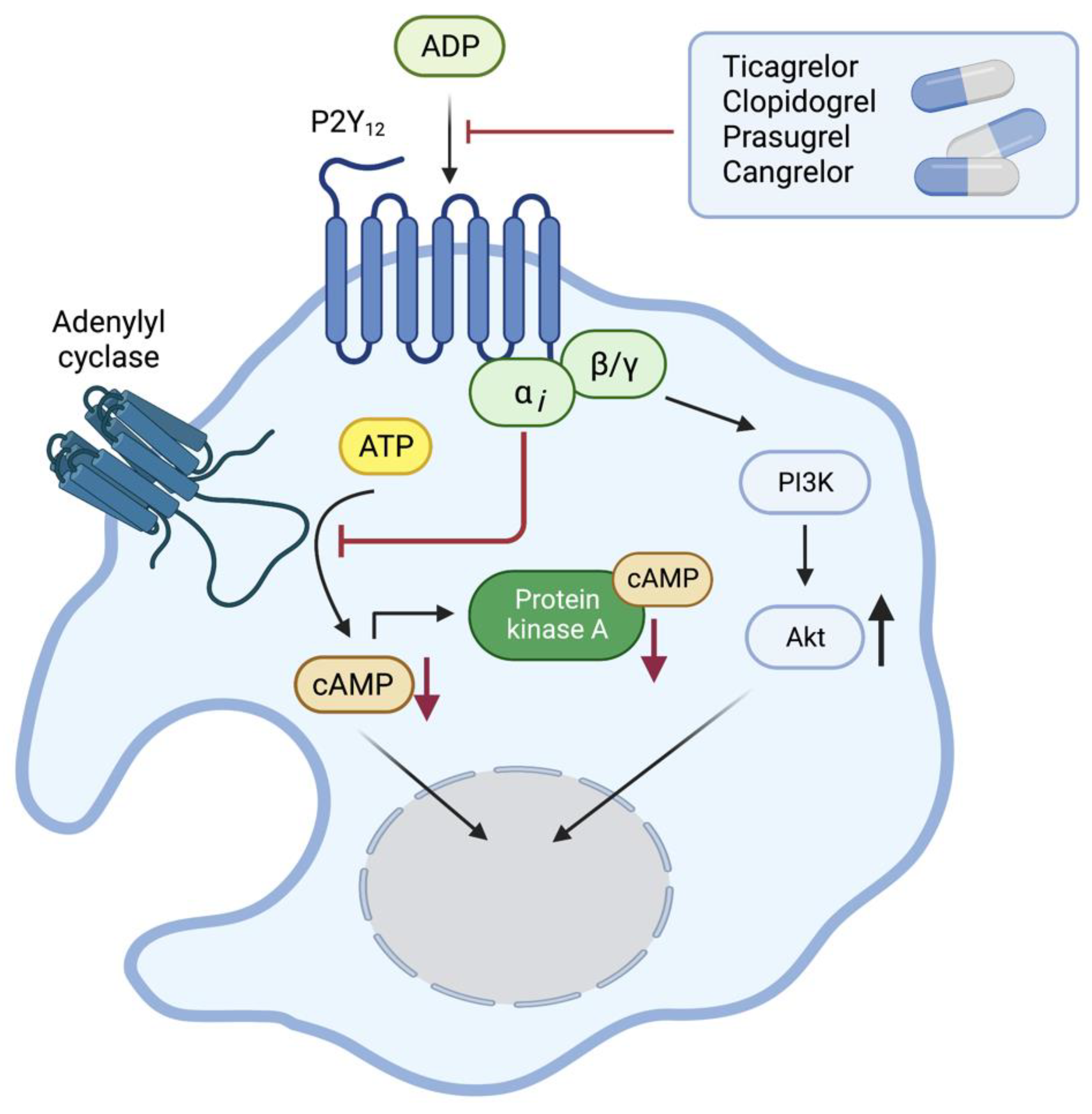
P2Y12 Reseptöründe Ticagrelorun Mekanizma Basamağı:
- Reseptör Hedefleme: Ticagrelor, trombosit yüzeyindeki ADP (adenosin difosfat) reseptörlerinin P2Y12 alt tipine seçici ve geri dönüşümlü olarak bağlanır.
- ADP Blokajı: Ticagrelor, P2Y12 reseptörüne bağlanarak ADP’nin reseptörüne bağlanmasını engeller. ADP, trombosit aktivasyonunu ve agregasyonunu destekleyen anahtar bir moleküldür.
- G-Protein Sinyallemesinin İnhibisyonu: P2Y12, G-proteinine bağlı bir reseptördür. Normal koşullarda, ADP’nin P2Y12’ye bağlanması trombosit içindeki bir G-proteinini aktive eder ve bu daha sonra başka sinyal olaylarına yol açar.
- Azalan cAMP Bozunması: G-protein sinyalinin inhibisyonu, adenilat siklaz enziminin aktivasyonunun azalmasına yol açar, bu da siklik AMP’nin (cAMP) bozunmasının azalmasına yol açar.
- İntegrin αIIbβ3 Aktivasyonunun Azaltılması: Trombosit içindeki yüksek cAMP seviyeleri, trombositlerin dinlenme durumunda kalmasına yardımcı olur ve trombosit agregasyonunun son ortak yolu olan integrin αIIbβ3’ün aktivasyonunu azaltır.
- Azalan Trombosit Toplanması: Azalan integrin aktivasyonu nedeniyle, trombositler daha az yapışkandır ve bir araya gelme olasılıkları daha düşüktür, bu da pıhtı oluşturma yeteneklerini azaltır.
- Tersine çevrilebilirlik: Klopidogrel ve prasugrel gibi diğer P2Y12 inhibitörlerinin aksine, tikagrelor bağlanması geri dönüşümlüdür, bu da ilacın kesilmesi üzerine trombosit fonksiyonunun daha hızlı iyileşmesine olanak tanır.
Belirteçler:
- Akut Koroner Sendrom (AKS)
- Perkütan koroner girişim (PCI) uygulanan hastalar
- Kardiyovasküler olayların ikincil önlenmesi
Yan etkiler:
Yaygın yan etkiler şunlardır:
- Kanama
- Nefes darlığı
- Morarma
- Baş ağrısı
- Mide bulantısı
Kontrendikasyonlar:
- Aktif patolojik kanama
- Kafa içi kanama öyküsü
- Şiddetli karaciğer yetmezliği
İlaç etkileşimleri:
Ticagrelor, aspirin, antikoagülanlar ve bazı antifungal ilaçlar gibi ilaçlarla etkileşime girebilir. Etkileşimlerin ve uygun dozajların tam listesi için daima bir sağlık uzmanına danışın.
Dozaj:
Genellikle yükleme dozu ve ardından idame dozu olarak uygulanır. Ancak spesifik doz rejimi bir sağlık uzmanı tarafından belirlenmelidir.
Ticagrelor’un Tarihi
Ticagrelor, 2001 yılında AstraZeneca tarafından keşfedilen bir trombosit agregasyon inhibitörüdür (P2Y12 reseptör antagonisti). Amerika Birleşik Devletleri’nde 2011’de ve Avrupa’da 2010’da tıbbi kullanım için onaylandı.
Ticagrelor, başka bir tiyenopiridin sınıfı antitrombosit ilaç olan klopidogrelin halefi olarak geliştirildi. Klopidogrel etkiliydi ancak kanama ve morarma gibi çok sayıda ciddi yan etkiye sahipti. Ticagrelor daha olumlu bir yan etki profiline sahip olacak şekilde tasarlandı.
- Ticagrelor başlangıçta AZD6140 olarak biliniyordu. Adı 2009 yılında Tinospora Crispa bitkisinde bulunan “ticagrel” ve altın anlamına gelen “or” kelimelerinin birleşiminden oluşan ticagrelor olarak değiştirildi.
- Ticagrelor başlangıçta akut koroner sendromun tedavisi için geliştirildi. Ancak kısa sürede stabil koroner arter hastalığı olan hastalarda kalp krizi ve felç gibi aterosklerotik olayların önlenmesinde etkili olduğu anlaşıldı.
- Ticagrelor, akut koroner sendromu, stabil koroner arter hastalığı ve periferik arter hastalığı olan hastalar için yaygın olarak reçete edilmektedir. Ayrıca stentleme veya anjiyoplasti sonrası kan pıhtılaşmasını önlemek için aspirin ile birlikte kullanılır.
- Ticagrelor, karakteristik pembe renginden dolayı bazen “pembe hap” olarak da anılır.
- Ticagrelor kanama, morarma ve nefes darlığı gibi bir dizi yan etkiye neden olabilir. Bununla birlikte, en olağandışı yan etkilerden biri eforla nefes darlığı (DOE) veya eforla nefes almada zorluktur. Heart dergisinde yayınlanan bir çalışma, tikagrelor alan hastaların DOE bildirme olasılığının klopidogrel alan hastalara göre daha yüksek olduğunu buldu.
- Ticagrelorun bir başka alışılmadık yan etkisi de bradikardi veya yavaş kalp atış hızıdır. Circulation dergisinde yayınlanan bir çalışma, tikagrelor alan hastaların bradikardi yaşama olasılığının klopidogrel alan hastalara göre daha yüksek olduğunu buldu.
Tarihsel Anekdotlar
- 2009 yılında PLATO çalışmasının sonuçları yayınlandı. Çalışma, akut koroner sendromlu hastalarda aterosklerotik olayların önlenmesinde aspirin ile kombinasyon halindeki tikagrelorun, aspirin ile kombinasyon halinde klopidogrele göre üstün olduğunu gösterdi. PLATO çalışması, tikagrelorun akut koroner sendromlu hastalar için yeni bir bakım standardı haline gelmesini sağlayan dönüm noktası niteliğinde bir çalışmaydı.
- 2013 yılında PEGASUS-TIMI 54 çalışmasının sonuçları yayımlandı. Çalışma, stabil koroner arter hastalığı olan hastalarda aterosklerotik olayların önlenmesinde aspirin ile kombinasyon halinde tikagrelorun, aspirin ile kombinasyon halinde klopidogrele göre üstün olduğunu gösterdi. PEGASUS-TIMI 54 çalışması, tikagrelorun kardiyovasküler hastalığın tedavisindeki rolünü daha da genişletti.
- 2019 yılında THEMIS çalışmasının sonuçları yayınlandı. Çalışma, periferik arter hastalığı olan hastalarda aterosklerotik olayların önlenmesinde aspirin ile kombinasyon halindeki tikagrelorun, aspirin ile kombinasyon halinde klopidogrele göre üstün olduğunu gösterdi. THEMIS çalışması, tikagrelorun kardiyovasküler hastalığın tedavisindeki rolünü daha da genişletti.
- Ticagrelor, kardiyovasküler hastalıkların tedavisinde ve önlenmesinde devrim yaratan dikkate değer bir ilaçtır. Milyonlarca hayatın kurtarılmasına yardımcı olan güvenli ve etkili bir ilaçtır.
Tromboz Araştırması dergisinde yayınlanan bir araştırma, tikagrelor alan hastaların öfkeli ve sinirli hissetme olasılığının daha yüksek olduğunu buldu. Araştırmacılar bunun, ilacın beyindeki serotonin seviyeleri üzerindeki etkisinden kaynaklanabileceğini öne sürdüler. Yani, eğer tikagrelor alıyorsanız ve kendinizi biraz huysuz hissediyorsanız endişelenmeyin, bu tamamen normaldir.
Kaynak:
- Wallentin, L., Becker, R. C., Budaj, A., et al. (2009). Ticagrelor versus Clopidogrel in Patients with Acute Coronary Syndromes. New England Journal of Medicine, 361(11), 1045–1057.
- James, S., Angiolillo, D. J., Cornel, J. H., et al. (2010). Ticagrelor vs. Clopidogrel in Patients with Acute Coronary Syndromes and Diabetes: A Substudy from the PLATO Trial. European Heart Journal, 31(24), 3006–3016
- Storey, R. F., Husted, S., Harrington, R. A., et al. (2010). Inhibition of platelet aggregation by AZD6140, a reversible oral P2Y12 receptor antagonist, compared with clopidogrel in patients with acute coronary syndromes. Journal of the American College of Cardiology, 50(19), 1852-1856.
- van Giezen, J. J., Nilsson, L., Berntsson, P., et al. (2009). Ticagrelor binds to human P2Y(12) independently from ADP but antagonizes ADP-induced receptor signaling and platelet aggregation. Journal of Thrombosis and Haemostasis, 7(9), 1556–1565.









Yorum yazabilmek için oturum açmalısınız.