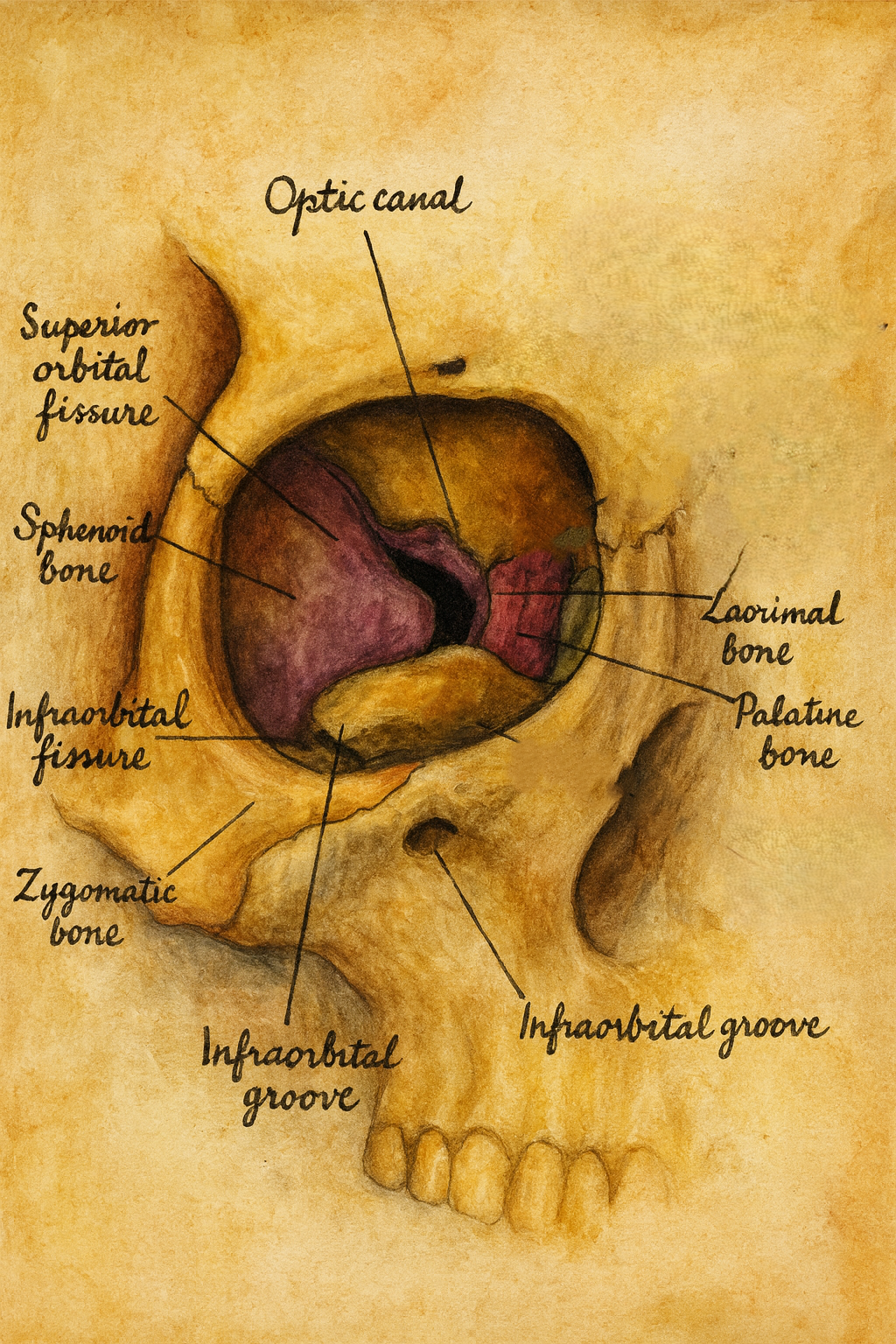
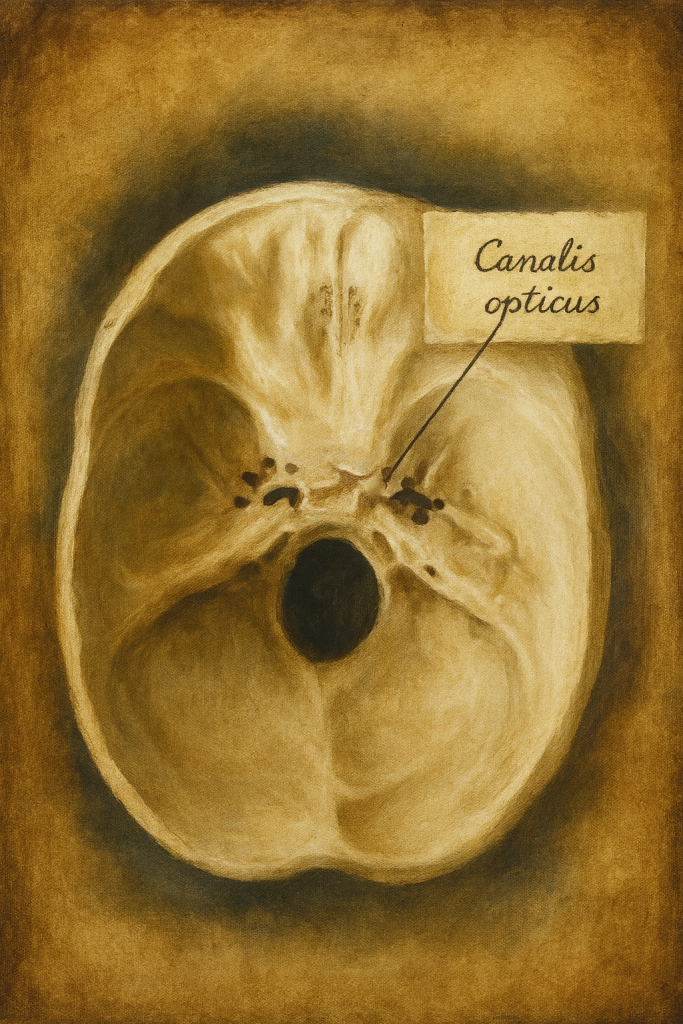
Optik kanal, canalis opticus, insan kafatasının sfenoid kemiği içinde yer alan dar ama son derece kritik bir kemik kanaldır. Optik sinir (n. opticus, kranial sinir II) ve oftalmik arter için tek fizyolojik geçit olması nedeniyle, görsel bilginin iletiminden göz küresinin kanlanmasına kadar uzanan bir dizi yaşamsal işlevin anatomik “şişe boynu”nu oluşturur.
İçindekiler
1. Tanım ve genel bakış
Optik kanal, sfenoid kemiğin küçük kanadının (ala minor ossis sphenoidalis) içinde, kafatası tabanının ön-orta bölümünde yer alan, kemikten oluşmuş tüp şeklinde bir yapıdır. Medialde sfenoid korpusu, lateralde küçük kanadın kortikal lamelleri ile sınırlanır ve arkada orta kranial fossadaki optik foramen’den, önde orbita apeksine doğru uzanır.
Kanal, içinden geçen iki ana yapı ile tanımlanır:
- Optik sinir (CN II): Retinadan çıkan miyelinli akson demetlerini beynin optik kiazma ve traktus optikusuna taşıyarak görsel iletimi sağlar.
- Oftalmik arter: İnternal karotid arterin intrakraniyal segmentinden doğan ana orbital arterdir; orbita içindeki kas, sinir, retina ve yardımcı göz yapılarına arteriyel kan götürür.
Bu iki yapının aynı dar kemik kanaldan geçmesi, optik kanalı hem normal fizyoloji hem de patolojik süreçler açısından son derece hassas bir bölge hâline getirir: Küçük hacim değişiklikleri dahi, sinir iletimi ve kan akımı üzerinde dramatik etkiler yaratabilir.
2. Etimoloji ve tarihsel notlar
“Optik” terimi, Antik Yunanca’da “görme ile ilgili, görmeye ait” anlamına gelen ὀπτικός (optikos) sıfatından gelir; bu sözcük kökenini “göz, bakış” anlamındaki ὤψ (ōps) kökünden alır. Aynı kök, “opsiyon”, “opisiyal” gibi Latince üzerinden diğer Batı dillerine de yansımıştır.
“Canalis” ise Latince’de “kanal, oluk, boru” anlamına gelir ve “kamış, içi boş sap” anlamındaki canna sözcüğü ile ilişkilidir. “Canalis opticus” tamlaması, kelime anlamıyla “görmeye ait (yapıların) kanalı” demektir.
Klasik anatomi metinlerinde, kanalın kranial yüzeye açılan deliği için foramen opticum, kanalın kendisi için ise canalis opticus ossis sphenoidalis terimi kullanılmış; bu nomenklatür modern Terminologia Anatomica’da da korunmuştur.
3. Makroanatomi
3.1 Lokalizasyon ve sınırlar
Optik kanal, sfenoid kemiğin üst yüzünde, optik kiazmanın hemen anteriorunda yer alan sulkus chiasmatis (chiasmaticus)’un iki ucunda başlayan optik foramenden başlar. Bu foramen, kanalın intrakraniyal girişidir. Arkada orta kranial fossa ile, önde orbita apeksiyle ilişkilidir.
Kanal:
- Süperiorunda: Ön klinoid çıkıntı (processus clinoideus anterior) ve ona komşu dura kıvrımları,
- İnferiorunda: Sfenoid korpus ve kısmen parassellar bölge,
- Lateralde: Kavernöz sinüs ve içinden geçen internal karotid arterin supraklinoid segmenti,
- Medialde: Sfenoid korpus ve planum sphenoidale
ile komşudur. Bu yakın komşuluk, hem kavernöz sinüs patolojilerinin hem de karotid- oftalmik segment anevrizmalarının optik kanal içeriğini etkilemesine zemin hazırlar.
Orbita içinde optik kanal, üst orbital fissürün medialinde ve biraz superiorunda yer alır; böylece orbita apeksinde sinir, damar ve kasların karmaşık bir şekilde kesiştiği bir “nörvovasküler kavşak” oluşturur.
3.2 Şekil ve boyutlar
Klasik tarifte optik kanal “kısa silindirik” olarak anlatılsa da, detaylı morfometrik ve kesit çalışmalarında kanalın huni biçimli (funnel-like) olduğu, kranial uca göre orbital uçta daha daraldığı gösterilmiştir.
Farklı popülasyonlarda BT ve kadavra çalışmaları:
- Uzunluk: Ortalama ~8–11 mm (çoğu çalışmada 9–10 mm civarı),
- Kranial açıklık çapı: Yaklaşık 4–5,5 mm,
- Orbital açıklık çapı: Yaklaşık 3–4 mm,
- Posterior uçlar arası mesafe: ~25 mm,
- Anterior uçlar arası mesafe: ~30 mm
olduğunu göstermektedir.
Bu ölçüler, popülasyona, cinsiyete ve bireysel kraniyofasiyal morfolojiye göre değişkenlik gösterebilir; erkeklerde kanal uzunluğunun ve kranial açıklık çapının kadınlardan hafifçe daha büyük olduğu bildirilmiştir.
3.3 Komşuluk ilişkileri
Optik kanalın klinik açıdan en önemli komşulukları şunlardır:
- Optik kiazma: Kanalın kranial girişinin hemen posterior-superiorunda yer alır; kiazma patolojileri (ör. kraniofaringiom, hipofiz adenomu) optik kanal girişinde sinir liflerini etkileyebilir.
- Kavernöz sinüs ve ICA: İç karotid arterin oftalmik segmenti, optik kanalın inferolateralinde seyreder; bu segment anevrizmaları kanala ve optik sinire bası yapabilir.
- Üst orbital fissür: Lateralde yer alır; III, IV, V1 ve VI. kranial sinirler ile superior oftalmik ven için geçit sağlar. Optik kanal ve üst orbital fissür birlikte, orbital apeks sendromlarının anatomik temelini oluşturur.
4. Mikroskobik anatomi ve nörovasküler içerik
Optik kanal içinden geçen optik sinir, teknik olarak bir “duyusal sinir”den çok, merkezi sinir sisteminin uzantısı olan bir beyin traktusudur. Bu nedenle:
- Üç tabakalı meninks (dura, araknoid, pia) ile sarılıdır,
- Subaraknoid boşluğu, kranial subaraknoid boşluk ile doğrudan devamlıdır,
- İçinden geçen aksonlar oligodendrosit kaynaklı miyelinle örtülüdür.
Bu özellikler, özellikle artmış intrakraniyal basınç ve demiyelinizan hastalıkların optik kanalda bulunan sinir segmentini doğrudan etkilemesine zemin hazırlar.
Optik sinir kılıfı boyunca seyreden başlıca damar ve yapılar:
- Oftalmik arter: Genellikle internal karotid arterin ön klinoid çıkıntı hizasındaki segmentinden doğar; kısa intrakraniyal segmentin ardından durayı delerek optik kanal girişinden optik sinirle birlikte kanala girer. Kanal içinde, optik sinirin inferolateralinde konumlanır.
- Santral retinal arter: Çoğu olguda oftalmik arterden ayrıldıktan sonra, optik sinirin dural kılıfına girer ve kanal içinde veya hemen orbital çıkış civarında sinir içine penetre olur; retinanın iç katmanlarının ana arteridir.
- Optik sinir etrafında dura ve periost arasında yer yer küçük venöz pleksuslar ve sempatik lifler bulunur; bunlar oftalmik arter boyunca uzanan pleksuslarla bağlantılıdır.
Bu mikroanatomi, özellikle optik sinir kılıfı dekompresyonu, optik sinir kılıfı meningiomları ve vasküler cerrahi için kritik önem taşır.
5. Embriyoloji ve evrimsel bağlam
5.1 Embriyolojik gelişim
Embriyolojik olarak optik sinir, optik sap (optic stalk) adı verilen, diensefalondan göze uzanan nöral tüp çıkıntısından gelişir. Sfenoid kemik ise kranial tabanın kondral iskeleti içinde yer alan presfenoid ve basisfenoid kıkırdak merkezlerinin endokondral kemikleşmesi sonucu oluşur.
- Optik sinir aksonları retina gangliyon hücrelerinden beyne doğru büyürken,
- Sfenoid kondral iskeleti etrafında kemikleşme odakları meydana gelir ve
- Gelişen sinir ve oftalmik arterin etrafı kemik ile sarılarak optik kanal şekillenir.
Bu süreçteki bozukluklar, kanalın darlığı, şekil anomalileri veya optik sinir hipoplazisi gibi tablolarla sonuçlanabilir. Optik sinir hipoplazisinde çoğu zaman optik disk küçük ve çukursuz, optik kanal ise dar veya displastiktir; bu durum ciddi görme kayıplarına ve sıklıkla eşlik eden orta hat beyin anomalilerine (septum pellusidum agenezisi, korpus kallosum defektleri, hipopituitarizm vb.) eşlik edebilir.
5.2 Evrimsel perspektif
Omurgalılarda göz ve optik sinir, erken evrimsel süreçlerden itibaren merkezi sinir sisteminin uzantısı olarak şekillenmiştir. Kuru kafatası üzerinde optik kanala karşılık gelen açıklık, çoğu kara omurgalısında mevcuttur; ancak:
- Orbita konfigürasyonu,
- Kafatasının bazal açısı,
- Optik kanalların birbiriyle yaptığı açı
türlere göre önemli ölçüde değişir.
Özellikle primatlarda ve insanda, orbitaların öne dönmesi ve gözler arası mesafenin optimize edilmesi, binoküler ve stereoskopik görmeyi geliştirmiştir. Bu süreçte optik kanalların uzanımı ve birbirlerine göre konumları, optik kiazmanın yerleşimiyle birlikte, görme alanlarının örtüşme derecesini etkileyen yapısal bir “ayar” mekanizması gibi düşünülebilir. İnsan kafatasında optik kanalların posterior ve anterior uçlarındaki mesafelerin farklı olması, kanalın hafif diverjan yerleşiminin bir yansımasıdır.
6. Anatomik varyasyonlar
Optik kanal anatomisi çoğu bireyde oldukça öngörülebilir olsa da, cerrahi ve radyolojik açıdan önemli olabilecek birtakım varyasyonlar tanımlanmıştır:
- Boyut ve şekil varyasyonları: BT ve morfometrik çalışmalar, kanalın dairesel, oval ya da yarı üçgensi kesitli olabildiğini; en dar segmentin genellikle orta veya orbital kısımda yer aldığını göstermektedir.
- Çift optik kanal / aksesuar kanal: Nadir olgularda, optik kanal bir kemik septum ile iki lümene ayrılabilir; bu durumda oftalmik arter ve optik sinir farklı lümenlerden geçebilir ve cerrahi girişimler için önemli bir varyasyon oluşturur.
- Cinsiyet ve popülasyon farkları: Farklı etnik popülasyonlarda kanal uzunluğu ve açıklık çaplarında anlamlı ancak küçük farklılıklar bildirilmiş; erkeklerde daha geniş ve uzun kanallar daha sık rapor edilmiştir.
- Patolojik daralma: Özellikle osteopetrozis gibi genetik kemik hastalıklarında sfenoid kemikte aşırı kemikleşme ve kanal darlığına bağlı kompresif optik nöropati gelişebilir; bu olgularda cerrahi dekompresyon yaşam boyu görmenin korunması için kritik hâle gelir.
7. Fonksiyonel önem
Optik kanal, yapısal olarak küçük olsa da işlevsel açıdan üç temel rol üstlenir:
- Görsel bilginin iletimi
Optik sinir lifleri, retinadaki fotoreseptörlerden başlayan görsel bilgiyi, sinaptik istasyonlar üzerinden (nukleus geniculatus lateralis, superior kollikulus vb.) oksipital korteksteki birincil görsel alanlara taşır. Kanal segmenti, bu iletim hattının, kemikle sınırlanmış en dar bölümüdür; burada oluşabilecek her türlü bası, hem aksoplazmik akımı hem de iyonik iletimi bozarak ani veya yavaş ilerleyen görme kayıplarına yol açabilir. - Oküler ve orbital kan akımı
Oftalmik arter, orbita ve içindeki yapılara kan sağlayan ana arteriyel giriştir. Santral retinal arter, posterior siliyer arterler, kas dalları ve supraorbital-supratroklear dallar üzerinden retina, koroid, ekstraoküler kaslar, göz kapakları ve alın derisi beslenir. Optik kanal, bu arteriyel sistemin kranial boşluk ile orbita arasındaki tek yolu olduğundan, kanal içi patolojiler, gözün hem sinirsel hem de vasküler bütünlüğünü aynı anda tehdit eder. - BOS ve basınç iletimi
Optik sinir kılıfı içindeki subaraknoid boşluk, kranial subaraknoid boşluk ile devamlıdır. Bu nedenle artmış intrakraniyal basınç, optik sinir kılıfına ve dolayısıyla kanal içindeki sinir segmentine doğrudan iletilir; papilödem ve kronik basıya bağlı optik atrofi bu mekanizmanın klinik sonuçlarıdır.
8. Klinik anatomi ve patoloji
8.1 Travma ve travmatik optik nöropati
Sfenoid kemik kırıkları, özellikle orbital apeks ve kanatları içeren yüksek enerjili kafa travmalarında optik kanalı tutabilir. Bu durumda:
- Kemik fragmanları doğrudan optik sinire bası yapabilir,
- Kanal içinde hematom veya ödem gelişebilir,
- Oftalmik arter veya dalları etkilenerek iskemi eklenebilir.
Travmatik optik nöropati, ani görme kaybı, afferent pupil defekti ve fundusta başlangıçta minimal değişiklikle seyredebilir; optik kanalın darlığı ve kırığın konfigürasyonu, prognozu etkileyen önemli anatomik değişkenlerdir. Seçilmiş olgularda kanal dekompresyonu (kraniotomi ya da endoskopik endonazal yaklaşımlar) gündeme gelebilir.
8.2 Tümörler
Optik kanal bölgesini tutabilen başlıca lezyonlar:
- Optik sinir gliomları: Çoğunlukla çocukluk çağında, özellikle nörofibromatozis tip 1 ile ilişkili; siniri diffüz kalınlaştırarak kanalda bası yapar.
- Optik sinir kılıfı meningiomları: Sinir kılıfından gelişir, “tram-line” görünümüyle MR’da izlenir, kanal segmentini daraltabilir.
- Sfenoid kanat meningiomları: Sfenoidin küçük kanadı üzerinden komşu olarak optik kanal girişine uzanarak siniri yukarı veya laterale itebilir.
- Vasküler lezyonlar (ör. kavernöz hemanjiom, oftalmik segment anevrizmaları) ve metastatik lezyonlar da kanala sekonder bası yapabilir.
Bu lezyonlarda erken tanı, yüksek çözünürlüklü BT ve MR ile komşu yapıların dikkatli analizi, sinir fonksiyonunun korunması açısından belirleyicidir.
8.3 Enflamatuvar ve demiyelinizan süreçler
Optik nevrit, sıklıkla multipl skleroz ile ilişkili, optik sinirin enflamatuvar-demiyelinizan bir hastalığıdır. Lezyon segmenti intraorbital, intrakanaliküler veya intrakraniyal olabilir. İntrakanaliküler tutulum, dar kemik yapı nedeniyle semptomların daha ağır seyretmesine yol açabilir; MR’da kontrast tutan sinir kalınlaşması şeklinde izlenir.
Bu grup hastalıklarda kanalın kendisi yapısal olarak değişmese de, dar bir kemik kılıf içindeki ödemli sinir, iletim bloğu ve ağrıya yol açabilir.
8.4 Vasküler patolojiler
- Oftalmik segment (C6) ICA anevrizmaları, optik kanal girişine komşu yerleşimleri nedeniyle optik sinir ve oftalmik arter üzerinde basıya neden olabilir.
- Oftalmik arter veya dallarındaki tıkanmalar, özellikle santral retinal arter tıkanması, retinada ani ve ağır iskemi ile seyreden akut görme kaybı oluşturur; burada kanal anatomisi, arterin kranial ve orbital segmentlerinin cerrahi veya endovasküler müdahalelerinde önem kazanır.
8.5 Artmış intrakraniyal basınç ve papilödem
İdiyopatik intrakraniyal hipertansiyon gibi durumlarda, BOS basıncının artışı optik sinir kılıfını genişletir ve kanal segmentinde sinire bası yapar. Klinik olarak:
- Baş ağrısı,
- Geçici görme bulanıklıkları,
- Fundusta bilateral papilödem
ile kendini gösterir.
Görüntülemede, optik sinir kılıfının genişlemesi, “boş sella”, posterior göz küresinde yassılaşma gibi bulgular eşlik eder; bunların anatomik temeli, optik kanal ve etrafındaki meningeal yapılar arasındaki basınç iletimine dayanır. Gerekli olgularda optik sinir kılıfı dekompresyonu (optik sinir kılıf fenestrasyonu) uygulanabilir.
8.6 Konjenital anomaliler
Optik kanal ve optik sinirin doğuştan anomalileri geniş bir spektrum oluşturur:
- Optik sinir hipoplazisi: Azalmış akson sayısı ile karakterizedir; optik disk küçük, kanal ise dar olabilir. Sıklıkla orta hat beyin anomalileri ve endokrin bozukluklarla birliktedir.
- Optik disk koloboması, “morning glory” sendromu, peripapiller stafilom: Embriyolojik fissürün tam kapanmamasına bağlı “kazıksı” optik disk anomalileridir; kanal çıkışındaki kemik ve sinir konfigürasyonunda da değişiklikler eşlik edebilir.
- Optik disk drüzenleri: Bazı çalışmalarda temel patolojinin optik kanal veya lamina kribroza displazisi olduğu, aksonların çıkış alanının daralmasına bağlı “axon crowding” ve kalsifik depozitlerle seyrettiği öne sürülmüştür.
Bu anomalilerde erken tanı, çocukluk çağında görsel rehabilitasyon ve eşlik eden sistemik anomalilerin yönetimi açısından önemlidir.
9. Görüntüleme ve cerrahi yaklaşımlar
9.1 Görüntüleme teknikleri
- Bilgisayarlı tomografi (BT):
Yüksek rezolüsyonlu ince kesit BT ve multiplanar rekonstrüksiyonlar, optik kanalın kemik duvarlarını, genişliğini ve travma sonrası kırık fragmanlarını değerlendirmede altın standart yöntemdir. Morfometrik çalışmalarda da BT ölçümleri referans alınmıştır. - Manyetik rezonans görüntüleme (MRG):
Yumuşak doku kontrastı sayesinde optik sinir, sinir kılıfı, meningiomlar, gliomlar, inflamasyon ve demiyelinizan plaklar ayrıntılı olarak değerlendirilebilir. Yağ baskılı T1 ve T2 kesitler, orbital apeks ve kanal segmentindeki lezyonları ortaya koymada özellikle yararlıdır.
9.2 Optik kanal/optik sinir dekompresyonu
Optik kanal dekompresyonu; travmatik optik nöropati, osteopetrozis ilişkili kompresif nöropati, bazı tümörler ve seçilmiş idiyopatik intrakraniyal hipertansiyon olgularında gündeme gelen, yüksek riskli ancak görmeyi kurtarıcı olabilen bir girişimdir.
Başlıca cerrahi yaklaşımlar:
- Transkranial (frontotemporal veya pterional kraniotomi):
Sfenoid küçük kanadı ve optik kanal tavanı yüksek hızlı frezle inceltilip kaldırılarak kanal çevresi açılır; özellikle tümörlere eşlik eden bası durumlarında tercih edilebilir. - Endoskopik endonazal yaklaşım:
Sfenoid sinüs üzerinden minimal invaziv girişle kanalın medial ve inferior duvarı tıraşlanır; özellikle osteopetrozis ve travmatik optik nöropati olgularında kanalın medial tarafındaki hipertrofik kemiğin alınması ile sinir dekomprese edilir. - Transkarunküler/medial orbitotomi yaklaşımları:
Orbital apeks ve optik kanalın ön segmentine, konjonktival veya cilt kesileriyle ulaşılarak sinir kılıfı veya kanal tavanı dekomprese edilebilir; özellikle orbital apex sendromu ve bazı tümörlerde kullanılır.
Bu cerrahilerde optik sinir ve oftalmik arterin kanal içindeki göreceli konumu, kemik duvarın kalınlığı, varsa septalar ve kanal varyasyonları önceden BT ve MRG ile ayrıntılı planlanmalıdır; aksi takdirde kalıcı körlük, orbital iskemi veya karotid yaralanma gibi majör komplikasyonlar ortaya çıkabilir.
10. Oftalmik arter ve orbital cerrahi açısından önem
Optik kanal, oftalmik arterin intrakraniyal sistemden orbita içine geçtiği tek kemik geçittir. Bu nedenle:
- Orbital tümör cerrahisi,
- Aneurizma klipleme veya endovasküler girişimler,
- Endoskopik sinüs cerrahileri,
- Optik sinir kılıf cerrahileri
sırasında kanal anatomisinin hassas bir şekilde bilinmesi gerekir. Oftalmik arterin genellikle optik sinirin inferolateralinde, nadiren de superiorunda seyrettiği; santral retinal arterin ise kanal segmenti boyunca sinir kılıfına girerek yaklaşık 10–15 mm posteriorunda sinir içine penetre olduğu akılda tutulmalıdır.
Bu ilişkilerin küçük bir sapma ile bile değişebildiği olgularda, damar yaralanması dramatik görme kayıplarına yol açabileceğinden, preoperatif görüntüleme ve cerrahi navigasyon güncel pratiğin vazgeçilmez bir parçası hâline gelmiştir.
Keşif
Optik kanalın hikâyesi, aslında insanın “görmenin ne olduğu” sorusunu cevaplamaya çalışırken kafatasının içine bakma çabasının tarihidir. Her yüzyılda, yeni bir teknoloji (diseksiyon, mikroskop, X-ışını, BT, MRI, endoskopi, 3B görüntüleme) ortaya çıkar ve her seferinde aynı dar kemik tünel –canalis opticus– yeniden keşfedilir, yeniden tanımlanır.
Antik Çağ: “Görsel ruh” için bir kanal
Antik dünyada görme, yalnızca fiziksel bir süreç değil, aynı zamanda felsefi ve metafizik bir tartışma konusuydu. M.S. 2. yüzyılda Galen, hayvan kadavraları üzerinde yaptığı diseksiyonlarla beyin, sinirler ve duyu organları arasındaki ilişkileri betimlerken, gözden beyne uzanan kalın bir “kordon”u –bugün optik sinir dediğimiz yapı– tarif etti.
Galen, gözden beyne doğru taşındığını düşündüğü “pneuma opticum” (görsel ruh) kavramını ortaya koydu ve kafatası tabanında bu iletinin geçtiği bir “kanaldan” söz etti. Elinde ne ayrıntılı insan kadavrası ne de modern görüntüleme vardı; göz çukuru ile beyin tabanı arasında, sert kemiğin içindeki bu geçidi daha çok kavramsal ve hayvan diseksiyonlarına dayalı bir şema üzerinden tasvir edebildi. Buna rağmen, optik sinirin kafatası tabanını delerek geçtiği fikrini yerleştirmesi, optik kanalın tarihindeki ilk büyük eşiklerden biriydi.
O dönemde “kanal”ın kendisi ayrı bir kemik yapı olarak değil, görsel ruhun geçtiği bir tünel olarak düşünülüyordu. Yine de Galen’in çizdiği bu kaba şema, yüzyıllarca Avrupa ve İslam dünyasında anatomi kitaplarının temel referansı olarak kaldı.
Orta Çağ ve İslam tıbbı: Metnin gölgesinde anatomik gözlemler
Avrupa’da skolastik düşünce dönemi boyunca, Galen’in otoritesi nadiren sorgulandı. Buna karşın İbn Sînâ ve diğer İslam hekimleri, görme yollarını tartışırken gözden beyne uzanan sinirlerin geçtiği kemik yapılardan söz ettiler; optik kanal terimi kullanılmasa da, göz çukurunu beyne bağlayan kemikli geçit, metinlerde yerini aldı. Ancak disseksiyon kısıtlı olduğundan, ayrıntılı morfoloji henüz sahneye çıkmamıştı; optik kanal, daha ziyade teorik bir “geçit” olarak kaldı.
Rönesans: Kafatası tabanının gerçek haritaları
Vesalius ve insan kafatasının yeniden çizimi
- yüzyılda insan bedenine yeniden, üstelik eleştirel bir gözle bakma cesareti ortaya çıktığında, optik kanal da ilk kez insan üzerinde net biçimde betimlenmeye başladı.
Andreas Vesalius, 1543’te yayımlanan De humani corporis fabrica adlı eserinde, insan kafatası tabanını ayrıntılı gravürlerle çizdi ve optik sinirin geçtiği kemik geçidi belirgin biçimde gösterdi. Galen’in hayvanlara dayalı tasvirlerinin aksine Vesalius, insanda optik sinirin spesifik bir kemik kanaldan geçtiğini, bunun sfenoid kemik üzerinde yer aldığını net biçimde ortaya koydu.
Artık optik kanal, yalnızca soyut bir kavram değil, kuru kafatası üzerinde gösterilebilen somut bir yapı idi. Bu, ileride nöroşirürjinin ve kraniyofasiyal cerrahinin üzerine inşa edileceği anatomik zemini oluşturdu.
Kafatası tabanı anatomisinin kurumsallaşması
Rönesans sonrasında, 16.–17. yüzyıllarda Thomas Willis ve çağdaşları, beyin ve damar anatomisini ayrıntılandırırken, optik sinirlerin geçişini de kafatası tabanı üzerindeki foraminal mimariyle birlikte ele aldılar. Willis’in beyin damarları şemaları, optik sinirlerin kafatası tabanından geçişi ve karotid arterlerle ilişkisini göstermesi açısından önemliydi; bu çizimler, ileride oftalmik arter ve optik kanal komşuluklarının daha sistematik incelenmesine zemin hazırladı.
18. yüzyıl: Winslow ve kanalın fonksiyonel çerçevesi
- yüzyılda, anatomi giderek daha sistematik, daha “atlas benzeri” hâle geldi. Jacob Benignus Winslow, kafatası tabanını anlattığı eserlerinde optik kanalı ayrı bir entite olarak tarif etti; yalnızca optik sinirin değil, oftalmik arterin de bu dar kemik tünelden geçtiğine dikkat çekti.
Bu vurgu, önemli bir teorik dönüşüme işaret ediyordu: Optik kanal artık sadece bir sinir geçidi değil, nörovasküler bir tünel olarak kavranıyordu. Bu bakış açısı, daha sonra kafa içi basınç, damar akımı ve görme arasındaki ilişkilerin kurulmasında kritik rol oynayacaktı.
19. yüzyıl: Patoloji, deformite ve optik kanal
Virchow ve kraniyosinostoz: Kemik dikişleri, kanal ve görme
- yüzyılda anatomiye patoloji eklendiğinde, optik kanal yalnızca “normal” bir yapı olmaktan çıkıp, hastalıklarla ilişkili bir odak hâline geldi.
Rudolf Virchow, kraniyosinostoz ve diğer kafatası deformiteleri üzerine yaptığı çalışmalar sırasında, bazı çocuklarda optik kanalın daraldığını, bunun da optik sinirin sıkışmasına ve görme kaybına yol açtığını gösterdi. Kafatası sütürlerinin erken kapanması, sfenoid kemik ve çevresini şekil olarak değiştirdiğinde, optik kanalın iç hacmi azalıyor, bu da sinir ve damarı tehdit eden kronik bir basıya yol açıyordu.
Bu gözlemler, optik kanalı gelişimsel kraniyofasiyal anomaliler bağlamında düşünmenin kapısını açtı. Artık kanal, yalnızca erişkin anatomi kitabının bir satırı değil, pediatrik nöroloji ve cerrahi açısından da kritik bir yapıydı.
Papilödem ve intrakraniyal basınçla ilişki
- yüzyılın sonlarına doğru, Henri Parinaud gibi klinisyenler fundus muayenesiyle saptanan papilödemi, artmış intrakraniyal basınçla ilişkilendirdiler. Papilödemin, optik sinir kılıfındaki BOS basıncının artışına bağlı olduğunu fark etmek, dolaylı olarak optik kanal içindeki sinir segmentinin basınç değişimlerine ne kadar duyarlı olduğunu da gündeme getirdi.
Bu dönemde hâlâ kanalı doğrudan “canlı” olarak görmek mümkün değildi; ancak klinik bulguların anatomik yerleşimle eşleştirilmesi, optik kanalı intrakraniyal hipertansiyonun ana kavşaklarından biri hâline getirdi.
20. yüzyılın başı: Cushing, Dandy ve cerrahi perspektif
Cushing: Optik yol ve hipofiz cerrahisi
- yüzyılın başında Harvey Cushing, hipofiz adenomlarının cerrahisiyle uğraşırken, optik kiazma ve optik kanal çevresindeki anatomiyi olağanüstü ayrıntıyla tanımladı. Hipofiz bezinin hemen üzerinde konumlanan kiazmanın, optik kanaldan çıkan sinirlerle olan ilişkisini, tümörlerin bu yapıların üzerine yaptığı basıyı ve cerrahi girişimlerde optik kanalın ne kadar kırılgan bir sınır olduğunu vurguladı.
Cushing’in gözlemleri, optik kanalın yalnızca anatomi atlasında değil, ameliyathanede de kritik bir referans noktası hâline geldiğini gösteriyordu.
Dandy: İlk görüntüleme girişimleri
Walter Dandy, 1930’larda geliştirdiği hava ventrikülografisi ve pneumoensefalografi teknikleriyle beyin boşluklarını ve kitle lezyonlarını görüntülemeye çalıştı. Optik kanal doğrudan gösterilmese de, bu yöntemler cerrahların kafatası tabanındaki ilişkileri, özellikle hipofiz ve kiazma çevresini daha iyi anlamasını sağladı. Optik kanalın cerrahi planlama içindeki önemi, böylece ilk kez görüntüleme temelli bir boyut kazandı.
20. yüzyıl ortası: Radyoloji, X-ışınları ve kanalın “görünür” hâle gelmesi
1950’lerden itibaren radyoloji klinik pratiğe yerleştiğinde, kafatası tabanının X-ışını görüntüleri optik kanalı da seçilebilir hâle getirdi. Özellikle:
- Orbita ve sfenoid bölge kırıkları,
- Tümörler veya kalınlaşmış kemik bölgeleri,
- Kraniyosinostoz ve diğer deformiteler
X-ışını ile değerlendirilmeye başlandı; optik kanal, bu filmlerde incelenen ana referans noktalarından biri hâline geldi.
Konvansiyonel radyoloji, kanalı üç boyutlu değil, ancak projeksiyon halinde gösterebildiği için, ayrıntılı cerrahi planlama hâlâ sınırlıydı. Büyük sıçrama, 1970’lerde gelecekti.
1970’ler–1980’ler: BT ve MRI ile devrim
BT: Kemik kanalın üç boyutlu yeniden keşfi
Bilgisayarlı tomografinin (BT) klinik kullanıma girmesi, optik kanal anatomisinde ikinci büyük devrimdi. Artık:
- Kanalın uzunluğu, çapı ve şekli milimetrik hassasiyetle ölçülebiliyor,
- Sfenoid kırıkları ve kanal içi kemik fragmentleri net biçimde gösterilebiliyor,
- Meningiom, gliom gibi lezyonların kanal duvarı ve sinirle ilişkisi çok daha iyi anlaşılabiliyordu.
BT, 20. yüzyılın son çeyreğinde yayımlanan çok sayıda morfometrik çalışmanın temelini oluşturdu. Optik kanalın ortalama uzunlukları, çapları, popülasyonlar arası farkları, cinsiyet farklılıkları bu dönemde sistematik olarak rapor edilmeye başlandı.
MRI: Sinirin ve yumuşak dokunun sahneye çıkışı
1980’lerde manyetik rezonans görüntüleme (MRI) devreye girdiğinde, bu kez optik kanalın içinden geçen sinir dokusunun ve sinir kılıfının ayrıntılı görüntüleri elde edildi:
- Optik nevrit, optik sinir gliomu, optik sinir kılıfı meningiomu,
- Papilödem ve kronik intrakraniyal hipertansiyona bağlı sinir kılıf genişlemeleri,
- Kanal içi tümörler ve enflamatuvar süreçler
ilk kez doğrudan, noninvazif şekilde izlenebildi.
Artık optik kanal, yalnızca kemik bir tünel değil, içinde seyreden sinir ve damar demetinin dinamik patolojileriyle birlikte değerlendirilmesi gereken fonksiyonel bir alan olarak görülüyordu.
1980’ler–1990’lar: Mikrocerrahi ve orbital dekompresyon
Radyolojik ilerlemeler, cerrahların optik kanala çok daha cesur ve hedefli biçimde yaklaşmasını sağladı. 1980’lerden itibaren:
- Orbitotomi ve kraniotomiyle optik kanal dekompresyonu, travmatik optik nöropati, osteopetrozis, meningiomlar ve fibroz displazilerde uygulanmaya başlandı.
- Tiroid göz hastalığında orbital dekompresyon sırasında, özellikle apeks ve optik kanal çevresindeki kemiklerin alınmasıyla görme korunmaya çalışıldı.
Bu dönemde mikrocerrahi tekniklerin gelişmesi, optik kanalın tavanı ve duvarlarının mikroskop altında parsiyel alınması gibi son derece ince manevraları mümkün kıldı. Optik sinirin milimetrelerce yakınından geçen frezler, artık modern nöroşirürjinin günlük pratiğinin bir parçasıydı.
21. yüzyıl: Endoskopik çağ ve minimal invaziv optik kanal cerrahisi
Endonazal ve transorbital endoskopik yaklaşımlar
2000’lerden itibaren, kafatası tabanına endoskopik transnazal yaklaşımlar yaygınlaştı. Bu teknikler, özellikle:
- Tuberkulum sellae ve planum sphenoidale meningiomları,
- Hipofiz ve parasellar tümörler,
- Travmatik optik nöropati ve bazı kraniyosinostoz olguları
için optik kanalın medial ve inferior duvarından dekompresyon yapılmasına olanak tanıdı.
Daha yakın dönemde, endoskopik transorbital yaklaşımlar da (örneğin lateral orbitadan veya üst göz kapağı kıvrımından girilerek) anterior klinoidektomi ve optik kanal dekompresyonu yapmak için kullanılmaya başlandı. Bu yöntem, özellikle sfeno-orbital meningiomlar ve anterior klinoid süreci tutan lezyonlar için alternatif bir yol sunuyor.
Son yıllarda yayımlanan çalışmalar, endoskopik tekniklerle yapılan optik kanal dekompresyonunun:
- Travmatik optik nöropati,
- Tümöre bağlı kompresif nöropati
olgularında anlamlı oranda görme artışı sağlayabildiğini, özellikle erken dönemde uygulandığında sonuçların daha iyi olduğunu gösteriyor.
Bu noktada, optik kanal cerrahisi çok merkezli bir uzmanlık alanına dönüşmüş durumda; “skull base” eğitimi almış cerrahlar ile genel nöroşirürjiyenler arasında, özellikle görme sonuçları açısından anlamlı farklar bildiren çalışmalar yayımlanıyor.
Genetik ve gelişimsel anatomi: Optik kanalın moleküler arka planı
Optik kanalın yalnızca kemik ve sinir düzeyinde değil, genetik ve embriyolojik düzeyde de anlaşılması, 21. yüzyılın önemli temalarından biri hâline geldi.
Optik sinir hipoplazisi ve septo-optik displazi
Optik sinir hipoplazisi ve septo-optik displazi olgularında, son 20 yılda yapılan genetik çalışmalar:
- HESX1, SOX2, SOX3, OTX2, NR2F1, ATOH7 gibi transkripsiyon faktörlerinin,
- Beyin orta hat yapıları, hipofiz ve optik sinir gelişiminde kritik rol oynadığını,
- Bu genlerdeki nadir mutasyonların optik sinir hipoplazisi, midline beyin anomalileri ve endokrin bozukluklarla bağlantılı olabileceğini
ortaya koydu.
Bu sendromlarda optik kanal sıklıkla normalden dar, optik sinir ise küçük ve az sayıda akson içeriyor; yakın tarihli nöro-radyolojik seriler, kanal morfolojisi ile sinir hacmi arasındaki ilişkinin daha sistematik şekilde incelendiği çalışmalar yayımlamaya başladı.
Kraniyosinostoz, kanal darlığı ve cerrahi zamanlama
Özellikle FGFR2, FGFR3 ve benzeri genler ile ilişkili kraniyosinostoz sendromlarında, sfenoid kemik ve optik kanal morfolojisinin bozulduğu, kanalın daraldığı ve erken dönemde görme tehdidi ortaya çıktığı biliniyor. Son yıllarda kraniyosinostoz cerrahisinde:
- Kanal boyutlarının BT ile dikkatlice ölçülmesi,
- Gerekirse eş zamanlı kanal dekompresyonu yapılması,
- Cerrahi zamanlamanın görme fonksiyonuna göre ayarlanması
gündemde. Bu, optik kanalın bir kez daha embriyolojik bozukluk ile klinik sonuç arasındaki kilit halka rolünü üstlenmesi anlamına geliyor.
3B görüntüleme, sanal gerçeklik ve “dijital optik kanal”
- yüzyılın ikinci on yılı, optik kanalın hikâyesine yeni bir katman daha ekledi: 3B görüntüleme, sanal gerçeklik (VR) ve 3B baskı.
CBCT, yüksek çözünürlüklü BT ve 3B morfometri
Konik ışınlı BT (CBCT) ve yüksek çözünürlüklü kraniyofasiyal BT’ler sayesinde:
- Optik kanalın 3B sanal modelleri oluşturulabiliyor,
- Kanalın eğimi, çapı, en dar segmentinin yeri gibi parametreler ayrıntılı bir şekilde ölçülebiliyor,
- Farklı popülasyonlarda ve patolojilerde morfometrik karşılaştırmalar yapılabiliyor.
Yakın tarihli çalışmalar, optik kanal ve orbita modellerinin, cerrahi planlamada ve implant tasarımında kullanılabilecek kadar yüksek doğrulukla üretilebildiğini gösteriyor.
Sanal gerçeklik ve hasta özgül planlama
Son yıllarda, kraniyofasiyal ve kafa tabanı cerrahisinde hasta özgül 3B modellerin ve VR platformlarının kullanımı hızla arttı. Optik kanal ve çevre yapılar:
- Sanal ortamda büyütülebiliyor,
- Tümörle veya kırık hatlarıyla ilişkisi üç boyutlu olarak incelenebiliyor,
- Cerrah, ameliyat öncesi “simülasyon” yaparak hangi kemik segmentlerini ne kadar kaldıracağını planlayabiliyor.
Bu yaklaşım, özellikle tuberkulum sellae meningiomları, anterior klinoid lezyonları ve travmatik optik kanal kırıklarında komşu damar ve sinir yapılarının korunması açısından yeni bir güvenlik katmanı ekliyor.
Güncel araştırma eksenleri: Optik kanal nereye doğru “açılıyor”?
Bugün optik kanal üzerine yapılan çalışmalar birkaç ana hat üzerinde yoğunlaşıyor:
- Cerrahi tekniklerin standardizasyonu
Farklı merkezler, endoskopik endonazal, transorbital ve transkranial optik kanal dekompresyonu yaklaşımlarını kadavra ve klinik serilerle karşılaştırıyor; hangi yaklaşımın hangi endikasyonda daha güvenli olduğu, ne kadar kanal segmentinin açılması gerektiği, hangi kemik duvarların korunabileceği gibi sorulara yanıt arıyor. - Morfometri ve nüfuslar arası farklılıklar
BT ve CBCT temelli büyük vaka serilerinde, farklı etnik gruplarda optik kanal uzunluğu, çapı ve eğimi karşılaştırılıyor; bu veriler, özellikle standart implant ve navigasyon yazılımlarının geliştirilmesinde referans oluşturuyor. - Genetik ve gelişimsel korelasyonlar
HESX1, SOX2, OTX2 ve ilgili genlerdeki mutasyonların, yalnızca optik sinir hacmi değil, kanal formu ve kafa tabanı geometrisiyle nasıl ilişkili olduğu araştırılıyor; septo-optik displazi ve kraniyosinostoz spektrumundaki hastalarda, 3B görüntüleme ile genotip-fenotip eşleştirmeleri yapılıyor. - Yapay zekâ destekli segmentasyon ve risk öngörüsü
BT ve MRI verilerinden optik kanalın otomatik segmentasyonu, kanal darlığı saptama algoritmaları, travma ve cerrahi sonrası optik sinir hasarı riskini öngören yapay zekâ modelleri geliştirme çabaları giderek artıyor; bu alanda henüz erken dönem olsa da, yayın sayısı hızla yükseliyor. - Eğitim ve simülasyon
VR ve artırılmış gerçeklik sistemleri, optik kanal dekompresyonu gibi yüksek riskli girişimler için cerrahi eğitim modülleri geliştirmek amacıyla kullanılıyor; genç cerrahlar, gerçek ameliyattan önce optik kanal çevresinde “sanaldan geçen” ilk frez hareketlerini bu platformlarda öğreniyor.
Böylece, Galen’in “görsel ruhun geçtiği tünel” olarak hayal ettiği yapı, Vesalius’un bakır gravürlerinde kemik bir kanala, Virchow’un elinde patolojik bir dar boğaza, Cushing’in ameliyat sahasında sakınılması gereken bir eşik çizgisine, BT ve MRI döneminde milimetrelerle ölçülen bir morfometrik parametreye, bugün ise 3B modeller ve genetik tablolar üzerinde çözülmeye çalışılan çok katmanlı bir anatomik düğüme dönüşmüş durumda.
İleri Okuma
- Vesalius A (1543). De Humani Corporis Fabrica Libri Septem. Johannes Oporinus, Basel.
- Winslow JB (1733). Exposition Anatomique de la Structure du Corps Humain. Guillaume Desprez, Paris.
- Virchow R (1857). Gesammelte Abhandlungen zur Wissenschaftlichen Medizin. G. Reimer, Berlin.
- Parinaud H (1896). Sur l’œdème papillaire et l’hypertension intracrânienne. Archives d’Ophtalmologie, 16, 271–294.
- Galen (1916). On the Usefulness of the Parts of the Body. Translated by MT May. Cornell University Press, Ithaca, NY.
- Cushing H (1922). The Pituitary Body and Its Disorders. J. B. Lippincott Company, Philadelphia.
- Dandy WE (1932). Ventriculography following the injection of air into the cerebral ventricles. Annals of Surgery, 96(6), 1017–1027.
- Walsh FB, Hoyt WF (1969). Clinical Neuro-Ophthalmology. Lea & Febiger, Philadelphia.
- Kline LB, Bajandas FJ (1985). Neuro-Ophthalmology Review Manual. Slack Incorporated, Thorofare, NJ.
- Som PM, Curtin HD (2003). Head and Neck Imaging. Mosby, Philadelphia.
- Dutton GN (2004). Congenital disorders of the optic nerve: excavations and hypoplasia. Eye, 18(11), 1038–1048. doi:10.1038/sj.eye.6701545
- Koesling S, Wüstner M (2006). CT anatomy of the optic canal: Morphometric measurements and clinical relevance. Clinical Radiology, 61(8), 668–674.
- Biousse V, Newman NJ (2012). Neuro-Ophthalmology Illustrated. Thieme Medical Publishers, New York.
- Amador-Patarroyo MJ, Pérez-Rodríguez M, Téllez CH (2014). Congenital anomalies of the optic nerve. Saudi Journal of Ophthalmology, 28(1), 25–34. doi:10.1016/j.sjopt.2013.10.005
- Kalthur SG, et al. (2015). A morphometric evaluation of the optic canal. Saudi Journal of Medicine and Medical Sciences, 3(3), 213–219.
- Mesquita Filho PM, et al. (2017). Optic canal decompression: comparison of two surgical techniques. World Neurosurgery, 103, 456–464.
- Hsueh YM, Kearney M, Goldberg RA (2020). Endoscopic decompression of the optic canal: Techniques and outcomes. Orbit, 39(2), 125–134.
- Bird B, Parthasarathy A (2023). Anatomy, head and neck, ophthalmic arteries. StatPearls Publishing, Treasure Island (FL).
- Pooshpas P, Patel H (2023). Anatomy, head and neck, optic canal. StatPearls Publishing, Treasure Island (FL).
- Sthapak E, et al. (2023). Optic canal: a CT-based morphometric study in a North Indian population. Egyptian Journal of Neurosurgery, 38, 37. doi:10.1186/s41984-023-00220-1
- Adesina O, et al. (2023). Optic nerve decompression. StatPearls Publishing, Treasure Island (FL).
- Kenhub (2023). Ophthalmic artery: anatomy, branches, supply. Kenhub Anatomy Library.
- Kenhub (2024). Optic canal: anatomy and function. Kenhub Anatomy Library.
- Jalkh RM, et al. (2025). Surgical approaches to optic nerve decompression in osteopetrosis. Journal of Neurological Surgery Part B.
- Kwiecińska M, et al. (2025). The complete anatomy of the ophthalmic artery: a meta-analysis of anatomical variations. Neurosurgical Review.