Hepar — Anatomisi, Fizyolojisi, Patolojisi ve Klinik Önemi Üzerine Ansiklopedik Bir İnceleme
İçindekiler
I. ETİMOLOJİ VE TERMİNOLOJİ
Karaciğer kavramının dil tarihi, birbirinden bağımsız kültürlerin bu organa verdikleri önemi açıkça yansıtır. Türkçedeki ‘karaciğer’ sözcüğü, Farsça kökenli ‘ciğer’ ya da ‘cīgar’ biçimlerinden türemiştir; bu kök Hint-Avrupa dil ailesinin ortak atası sayılan Proto-Hint-Avrupa dilindeki *yekwr- köküne dayanmaktadır. Sözcüğün ‘kara’ öneki ise organın dokusunun koyu rengine —özellikle akciğer dokusunun açık pembemsi tonuyla karşılaştırıldığında belirginleşen bu renk farkına— yapılan görsel bir göndermedir. Latince ‘iecur’, Yunanca ‘hêpar’ (ἧπαρ) ve onun türevi ‘hepat-/hepato-‘ kökü aynı Proto-Hint-Avrupa kökeninden beslenmekte; ‘hepatitis’, ‘hepatosellüler’, ‘hepatomegali’ gibi modern tıp terimlerinin altyapısını oluşturmaktadır. Yunan geleneğinde karaciğer, korku ve öfke gibi güçlü duyguların yurdu sayılmış, hatta antik kehanet ritüellerinde hayvan karaciğerlerinin yorumlanması (haruspisy) siyasi kararların ve savaş stratejilerinin belirlenmesinde belirleyici rol üstlenmiştir. Bu etimolojik arka plan, karaciğerin salt biyolojik değil, kültürel ve sembolik bir öneme de sahip olduğunu ortaya koymaktadır.
II. EVRİMSEL BİYOLOJİK BAĞLAM
Karaciğer işlevi gören organlara omurgalı soylarının tamamında rastlanır; ancak gerçek anlamda bir karaciğerin ilkel formları, yaklaşık 500 milyon yıl önce ortaya çıkan ilk çeneli balıklara kadar izlenebilmektedir. Bunun yanı sıra omurgasız birçok hayvan türünde de benzer metabolik işlevleri üstlenen ‘hepatopankreas’ adı verilen yapılar bulunmaktadır. Bu geniş filogenetik dağılım, merkezi bir metabolik organın evrimsel açıdan ne denli derin köklere sahip olduğunu ve ne ölçüde seçici avantaj sağladığını açıkça ortaya koyar.
Omurgalı evriminde karaciğer, organizma büyüdükçe ve metabolik gereksinimleri çeşitlendikçe, bağırsak duvarının ötesinde ikinci bir metabolik kontrol katmanına duyulan ihtiyacı karşılayacak biçimde gelişmiştir. Portal dolaşım sistemi —sindirim kanalından karaciğere zengin besin içeriğiyle akan kan— bu evrimsel çözümün en somut anatomik ifadesidir. Sistemi olağanüstü kılan, bağırsak tarafından emilen besin maddelerinin genel dolaşıma geçmeden önce enzimatik süreçler, depolama mekanizmaları ve detoksifikasyon basamakları aracılığıyla titizlikle işlenip denetlenmesidir.
Memelilerde karaciğer, pıhtılaşma faktörlerinin sentezlenmesiyle ve glikojen depolaması yoluyla kan glukoz homeostazısının düzenlenmesiyle birlikte daha da karmaşık bir işlev repertuvarı kazanmıştır. Karaciğerin bu olağanüstü rejenerasyon kapasitesi —yani rezeksiyonun ardından kayıp doku kütlesinin büyük bölümünü yeniden üretebilme yeteneği— hepatositlerin, yani karaciğer hücrelerinin mitoz yoluyla yüksek çoğalma potansiyeline sahip olduğunu gösterir. Bu özellik, fizyolojik bütünlük korunurken cerrahi girişimlerin yapılabilmesine olanak tanıması bakımından klinik açıdan son derece büyük bir önem taşımaktadır.
III. EMBRİYOLOJİ VE GELİŞİMSEL BİYOLOJİ
Karaciğer, embriyonik gelişimin erken dönemlerinde ön bağırsağın (foregut) endoderminden köken alır. Yaklaşık dördüncü embriyonik haftada, endodermal epitel hücreleri, hepatik divertikül adıyla bilinen bir tomurcuk yapısı oluşturarak prolifere olmaya ve gelişmekte olan septum transversum mezenşimine doğru göç etmeye başlar. Bu hücre göçü, hepatoblastlar adı verilen öncü hücrelerin ortaya çıkmasını beraberinde getirir; hepatoblastlar zamanla hem hepatositlere hem de intrahepatik safra yolu epitel hücrelerine, yani kolanjiositlara farklılaşır. Böylece karaciğer, tam anlamıyla endodermden türeyen bir organdır.
Embriyonik karaciğer, hematopoietik bir merkez olarak da işlev görerek fetal dönemde kan hücrelerinin üretildiği başlıca doku konumuna gelir. Bu işlev doğumun ardından büyük ölçüde kemik iliğine devredilmekle birlikte, patolojik koşullar altında —özellikle miyelofibrozis gibi durumlarda— karaciğerde ekstramedüller hematopoiez yeniden etkinleşebilir.
Fetal dolaşımda karaciğer, plasentadan gelen oksijenli kanın yüksek basınçlı portal akımı devre dışı bırakarak sisteme girdiği ductus venosus aracılığıyla özel bir şant mekanizmasına sahiptir. Doğumla birlikte bu kanal kapanarak ligamentum venosum adını alır; ductus venosusun kapanmaması ise ciddi portosistemik şantlara yol açabilir. Karaciğerin morfolojik gelişimi, anatomik yapısını kısaca tanımlayan bir ifadeyle nitelendirilebilir: Portal ven, hepatik arter ve safra kanalı dallarının üçlü organizasyonuna dayanan portal triad mimarisi bu yapının temel taşını oluşturmaktadır.
IV. ANATOMİ
A. Makroskopik Anatomi ve Lob Yapısı
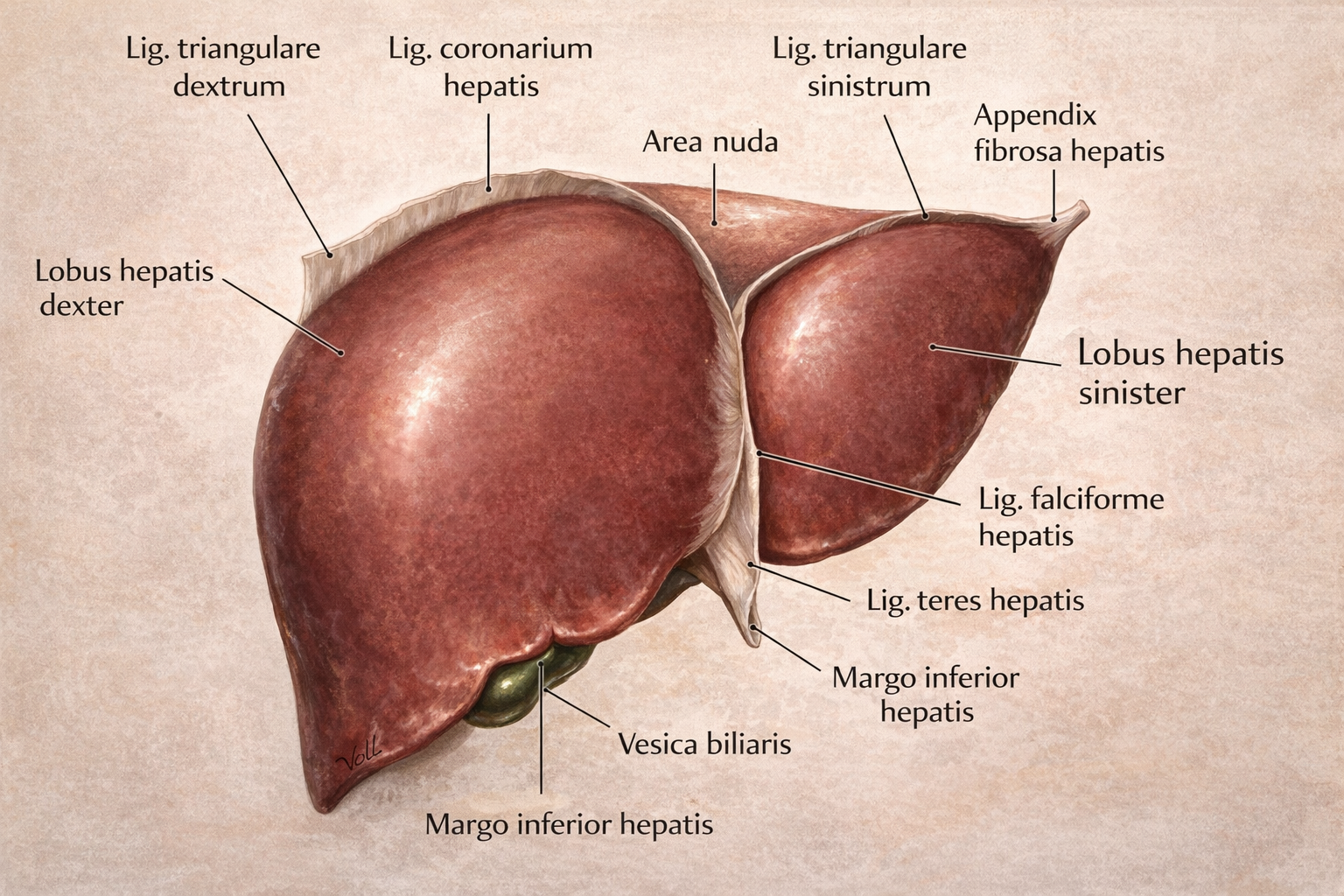
Karaciğer, erişkin insan vücudunun en büyük iç organı olup ağırlığı genellikle 1.400 ile 1.800 gram arasında değişmektedir. Karın boşluğunun sağ üst kadranında, diyaframın hemen altında yer alan bu organa periton zarı büyük ölçüde örtmektedir; yalnızca diyaframla doğrudan temas halinde olan ‘area nuda’ bölgesi bu örtüden yoksundur. Karaciğer, çıplak gözle dört anatomik loba ayrılır: sağ lob (lobus hepatis dexter), sol lob (lobus hepatis sinister), kare lob (lobus quadratus) ve kuyruk lobu (lobus caudatus). Sağ ve sol lobları makroskopik düzeyde birbirinden ayıran yapı, karaciğerin diyaframatik yüzeyinde seyreden ve falciform bağı barındıran interlober yarıktır.
Bu makroskopik lob ayrımı, derin ve görkemli bir anatomi geleneğini yansıtmakla birlikte, işlevsel açıdan kısmen yanıltıcı olabilir. Nitekim gerçek fonksiyonel bölünme, makroskopik değil vasküler anatomiye dayanır ve bu bölünme, ortaya çıkardığı klinik önemi bakımından çok daha anlamlıdır.
B. Couinaud Segmentasyonu
1957 yılında Fransız cerrah Claude Couinaud tarafından geliştirilen ve giderek uluslararası bir standart haline gelen Couinaud segmentasyon sistemi, karaciğeri sekiz bağımsız fonksiyonel segmente ayırır. Bu sistemin anatomik temeli, portal ven, hepatik arter ve safra kanalı dallarının karaciğer parankimi içindeki üçlü dağılım örüntüsüdür. Her segment, tabanı karaciğerin ön yüzeyine, tepesi ise hilus bölgesine yani portal triadın girişine doğru uzanan piramidal bir yapı sergiler. Her segmentin bağımsız bir vasküler ve biliyer beslenme-drene ağına sahip olması, komşu segmentlerin fonksiyonelliğini önemli ölçüde etkilemeksizin cerrahi rezeksiyona —segmentektomiye ya da daha geniş kapsamlı hepatektomiye— olanak tanır.
Segment I kuyruk lobuna karşılık gelir ve diğer segmentlerden belirgin biçimde ayrışır; zira hepatik venlerden bağımsız olarak inferior vena kavaya direkt venöz drenaj sağlar. Segment II ve III, sol lobun lateral kesimlerini; Segment IV ise sol lobun medial bölümünü, yani kare lobu oluşturur. Segmentler V ile VIII, birbirleriyle belirli bir düzenlilik içinde sağ lobu meydana getirir. Bu numaralandırma sistemi yalnızca anatomik değil, her şeyden önce kliniktir: Radyolojik görüntülemelerde saptanan lezyonların —tümörlerin, kistlerin ya da vasküler anomalilerin— karaciğer içindeki kesin konumunu tanımlamaya; rezeksiyon planlamalarına ve girişimsel radyolojik işlemlere rehberlik etmeye; ayrıca karaciğer hastalığının yaygınlığını ve evresini değerlendirmeye hizmet eder.
C. Bağlar ve Topografik İlişkiler
Karaciğer, karın boşluğu içinde çok sayıda peritoneal bağ aracılığıyla hem diyaframa hem de karın duvarına sabitlenir. Ligamentum falciforme hepatis, peritonun iki yapraklı bir katlanması olup karaciğerin sağ ve sol loblarını ön yüzeyde makroskopik düzeyde birbirinden ayırır ve organu karın ön duvarına bağlar. Bu bağın serbest kenarında ligamentum teres hepatis yer alır; bu yapı, fetal dönemde aktif işlev gören umbilikal venin fibröz kalıntısıdır. Koroner bağlar ve üçgen bağlar (ligg. triangularia) karaciğeri diyaframa bağlayan yapılar olup area nuda’nın sınırlarını belirler.
Klinik açıdan son derece önemli olan omentum minus, birbirinin devamı niteliğinde iki bağdan oluşur: mide ile karaciğer arasında uzanan ligamentum hepatogastricum ve duodenum ile karaciğer arasında yer alan ligamentum hepatoduodenale. Bu sonuncusu büyük pratik önem taşır; zira içinden portal ven, hepatik arter ve ana safra kanalından oluşan yapılar geçer. Portal triad oluşturan bu üç anatomik yapı, Pringle manevrası sırasında karaciğere giden kan akımının geçici olarak durduracak biçimde —karaciğer cerrahisinde sık başvurulan bir teknik olarak— burada sıkıştırılabilir.
Karaciğerin topografik ilişkileri, organın çevresindeki yapılarla sıkı bir komşuluk ilişkisi içinde olduğunu gözler önüne serer. Sağ lob; sağ kolik fleksura, duodenumun üst parçası ve sağ böbreğin üst kutbuyla temas halindedir; bu temaslara bağlı olarak söz konusu yapıların karaciğer yüzeyinde oluşturduğu baskı izleri —impresyon bölgeleri— kolayca seçilebilir. Sol lob ise özofagusun kardiasına yakın bölümü, mide tabanı ve pilor bölgesiyle komşuluk kurar.
D. Vasküler Anatomi
Karaciğerin vasküler mimarisi, diğer organ sistemlerinden işlevsel açıdan belirgin biçimde ayrılır. Karaciğer, çift bir kan beslemesi alır: Vasa privata adıyla anılan ve organın kendi oksijenasyonunu sağlayan hepatik arteryal sistem ile Vasa publica olarak nitelendirilen ve tüm vücuda yönelik metabolik işlevleri destekleyen portal venöz sistem.
Hepatik arterin özgün kaynağı olan çölyak trunkustan ayrılan arteria hepatica communis, arteria gastroduodenalis’i verdikten sonra arteria hepatica propria adını alır ve karaciğer hilusunda sağ (arteria hepatica dextra) ve sol (arteria hepatica sinistra) dallara ayrılarak parankime girer. Hepatik arterin anatomik varyasyonları son derece yaygındır; yaklaşık üçte bir olguda anormal bir sağ hepatik arter süperiyor mezenterik arterden, yaklaşık beşte bir olguda ise anormal bir sol hepatik arter sol gastrik arterden köken alır. Bu varyasyonların bilinmesi, hem hepatik cerrahi hem de transplantasyon ameliyatları açısından kritik önem taşır.
Portal venöz sistem, süperiyor mezenterik ven, inferior mezenterik ven ve splenik venin birleşimiyle oluşur. Portal ven, çoğunlukla pankreas boynunun arkasında şekillenir ve karaciğer hilusuna ulaşmadan önce hepatoduodenal ligament içinde seyreder. Midenin kardiasından rektumun üst yarısına kadar uzanan gastrointestinal kanaldan, pankreastan ve dalaktan gelen kanı toplar; bu kan besin maddeleri ve metabolik ara ürünler açısından zengindir. Portal vende normal basınç 3 ila 6 mmHg arasında seyreder.
Hepatik venler üç ana kol halinde organize olur: sağ (vena hepatica dextra), sol (vena hepatica sinistra) ve orta (vena hepatica intermedia). Bu damarlar genellikle inferior vena kavaya dökülmeden hemen önce birleşir. Kuyruk lobu, diğer segmentlerden bağımsız olarak inferior vena kavaya ayrı venler aracılığıyla drene olur; bu özellik, Budd-Chiari sendromu gibi hepatik ven trombozlarında önem taşır; zira bu sendromda kuyruk lobu kendi venöz drenajı nedeniyle diğer bölgelere kıyasla büyük ölçüde korunabilir.
E. Portocaval Anastomozlar
Portocaval anastomozlar, portal venöz sistem ile sistemik venöz dolaşım arasında birden fazla kritik bağlantı noktası oluşturur. Kliniğin derinliklerine işleyen bu bağlantılar, portal hipertansiyon koşullarında varislerin ortaya çıkmasına zemin hazırladıkları için ayrı bir öneme sahiptir.
En önemli portocaval anastomozlar şu anatomik bölgelerde toplanır: Birinci grupta, özofagus alt ucunda sol gastrik venin özofageal venlerle birleştiği bölgede, azigos sistemi aracılığıyla superiyor vena kavaya uzanan anastomozlar yer alır. İkinci grupta, rektal pleksus seviyesinde üst rektal venin middle ve inferior rektal venlerle birleşerek inferiyor vena kavaya döküldüğü bağlantılar bulunur. Üçüncü grupta, umbilikal ven rekanalizasyonu yoluyla para-umbilikal venlerin karın ön duvarının yüzeyel venlerine bağlandığı bölge gelir. Dördüncü grupta ise retroperitoneal bölgede Retzius venleri aracılığıyla oluşan anastomozlar yer alır. Bu anastomozlar ciddi portal hipertansiyon durumunda kollateral dolaşımın ana yollarına dönüşerek hayati öneme sahip klinik komplikasyonlara neden olabilir.
F. İnnervasyon ve Lenfatik Drenaj
Karaciğer hem sempatik hem de parasempatik innervasyona sahiptir. Sempatik lifler çölyak pleksus aracılığıyla T5-T12 segmentlerinden köken alır ve hepatik arterin adventisyası boyunca karaciğere ulaşır. Parasempatik lifler ise ön ve arka vagal gövdeden ayrılan rami hepatici aracılığıyla omentum minusun portal parçasından geçerek hilusa erişir. Bu otonom innervasyonun fonksiyonel önemi tam olarak aydınlatılamamış olmakla birlikte, vasküler tonusu düzenlediği ve safra sekresyonunu etkilediği kabul görmektedir. Frenik sinirden köken alan duyusal lifler karaciğer kapsülünü innerve eder; bu nedenle karaciğer kapsülünü geren ya da irrite eden patolojik durumlar —apse, tümör baskısı veya hepatomegali— sağ omza yansıyan ağrıya yol açabilir; bu durum İngilizce literatürde ‘referred pain’ olarak tanımlanmaktadır.
Karaciğerin lenfatik drenajı porta hepatis çevresindeki hepatik lenf düğümlerine akar; oradan çölyak lenf düğümlerine geçer ve nihayetinde sisterna chyli aracılığıyla torasik kanala boşalır. Karaciğer, başta hepatositler olmak üzere lenf sıvısı üreten başlıca organlardan biridir; kronik karaciğer hastalığında bu lenf üretimi ve drenajının bozulması assit oluşumuna katkıda bulunur.
V. MİKROSKOPİK ANATOMİ VE HİSTOLOJİ
A. Klasik Lobül
Karaciğerin işlevsel mikromimari birimi olan klasik lobül, altı köşeli bir prizma şeklinde tasarlanmış olup merkezinde santral ven (vena centralis), köşelerinde ise portal triadlar yer alır. Her portal triad; bir portal ven dalı, bir hepatik arter dalı ve bir intrahepatik safra kanalından oluşur. Hepatositler, bu portal triadlar ile santral ven arasında radyal plakalar halinde düzenlenerek karaciğer sinüzoidlerini döşer. Sinüzoidler ise hepatositlerle doğrudan temas eden özelleşmiş kapillerlerdir.
Sinüzoidlerin duvarları; endotel hücreleri, Kupffer hücreleri ve ito hücrelerinden oluşur. Kupffer hücreleri, retiküloendotelyal sistemin karaciğerdeki önemli temsilcileri olan makrofajlardır ve portal sistemden gelen bakteri, endotoksin ile debris partiküllerin fagosite edilmesinde kritik bir rol oynarlar. İto hücreleri ise (hepatik stellat hücreler) yağda çözünen vitaminleri —özellikle A vitamini ve D vitamini— depolar; karaciğer yaralanmalarında aktive olarak myofibroblast benzeri bir fenotip kazanır ve fibrozis gelişimine katkıda bulunur. Hepatositler ile sinüzoid endoteli arasındaki dar aralık olan Disse aralığı, plazmanın filtrasyonunun gerçekleştiği bölgedir ve bu aralık karaciğer fibrozisinde kollajen birikiminin başlıca yeri olduğundan patolojik açıdan son derece önemlidir.
B. Alternatif İşlevsel Birimler
Klasik lobül modeli dışında karaciğerin iki alternatif işlevsel organizasyon modeli daha tanımlanmıştır. Portal lobül modeli, santral safra kanalını merkeze alarak çevresindeki hepatositleri organize eder. Rappaport asini modeli ise karaciğeri terminal portal venülden santral vene uzanan elips biçimli birimler olarak tanımlar. Bu modelde portalden merkeze doğru üç zon belirlenir: oksijen ve besin açısından en zengin alan olan Zon 1 periportal bölgeyi; hem aerobik hem anaerobik metabolizmanın dengeli yürütüldüğü Zon 2 orta kesimi; en az oksijen alan ve bu nedenle iskemik koşullara ve zehirlere karşı en hassas olan Zon 3 ise sentrilobuler bölgeyi temsil eder. Bu zonlara dayalı metabolik ve patolojik farklılıklar —örneğin alkol kaynaklı karaciğer hasarının veya asetaminofen toksisitesinin sentrilobuler bölgede daha şiddetli görülmesi— önemli klinik çıkarımlar doğurur.
C. Safra Kanalı Sistemi
Safra kanalı sistemi, canaliculi biliferiden —yani birbirine komşu hepatosit zarlarının oluşturduğu ince yarık benzeri yapılardan— başlar ve giderek büyüyen intrahepatik safra kanallarına doğru mertebelenir. Hering kanalları, hepatositlerden kaynaklanan hepatosellüler bileşen ile kanalıkül epitelinden oluşan duktal bileşen arasındaki geçiş bölgelerini oluşturur ve karaciğer kök hücrelerinin yerleşim alanı olduğu kabul görmektedir. İnterlobüler safra kanalları portal triadın bir parçasını oluşturur ve prizma şeklindeki izoprizmik epitelle döşelidir. Bu kanallar giderek büyüyen segmental kanallara, ardından sağ ve sol hepatik kanallara birleşerek porta hepatiste karaciğeri terk eder.
VI. FİZYOLOJİ VE METABOLİK FONKSİYONLAR
A. Karbonhidrat Metabolizması
Karaciğer, kan glikoz homeostazısının korunmasında merkezi bir düzenleyici organ olarak işlev görür. Postprandiyal dönemde, bağırsak kaynaklı zengin glikoz yüküne yanıt olarak karaciğer insülin sinyalleri eşliğinde glikojen sentezini hızlandırır; erişkin karaciğeri yaklaşık 100 gram glikojen depolama kapasitesine sahiptir. Açlık durumunda ise glikojenoliz —glikojenin glikoza dönüştürülmesi— ve glukoneogenez —amino asitler, laktat ve gliserol gibi glikoz dışı öncü maddelerden glikoz sentezi— devreye girerek kan şekerinin fizyolojik sınırlar içinde tutulması sağlanır. Fruktoz ve galaktoz gibi diğer şekerler de portal dolaşım aracılığıyla karaciğere ulaşarak burada metabolize edilir; karaciğer bu şekilde glikoz homeostazısının hassas bir bekçisi konumuna gelir.
B. Protein Metabolizması
Karaciğer, plazma proteinlerinin büyük çoğunluğunu sentezler; bu proteinler arasında serumun en bol proteini olan albumin, onkotik basıncın korunmasında yaşamsal önem taşır. Albumin dışında, tüm pıhtılaşma faktörleri —K vitaminine bağımlı Faktörler II, VII, IX ve X dahil— fibrinogen, çeşitli kompleman proteinleri, akut faz reaktanları ve taşıyıcı proteinler de karaciğerde üretilir. Karaciğer fonksiyon bozukluğu; pıhtılaşma faktörlerinin sentezinin azalmasına bağlı koagülopatiye ve albumin düzeylerinin düşmesine bağlı ödem ile assit oluşumuna yol açar. Amino asit metabolizması kapsamında karaciğer, üre döngüsünü gerçekleştirerek azotlu metabolizmanın son ürünü olan amonyağı —nörotoksik potansiyeli yüksek bu bileşiği— üreye dönüştürüp idrar aracılığıyla vücuttan atar; bu mekanizmanın işleyememesi hepatik ansefalopatiye zemin hazırlar.
C. Lipid Metabolizması
Karaciğer, lipid metabolizmasının her aşamasında etkin bir rol üstlenir. Kolesterol sentezini gerçekleştirir ve bu sürecin hız sınırlayıcı enzimi olan HMG-CoA redüktaz, statin grubunun farmakolojik hedefi olması nedeniyle klinik tıpta merkezi bir öneme sahiptir. Safra asitlerini kolesterolden sentezler; trigliseritleri yeniden paketleyerek çok düşük yoğunluklu lipoprotein olan VLDL biçiminde plazmaya salarlar ve yağ asidinin beta-oksidasyonunu keton cisimciklerinin sentezine dönüştürür. Karaciğerin lipid metabolizmasındaki bozuklukları, non-alkolik yağlı karaciğer hastalığının (NAFLD) patofizyolojisinde temel bir rol oynamaktadır.
D. Safra Sentezi ve Salgılanması
Karaciğer, günde yaklaşık 600 ila 1000 mililitre safra üretir. Safranın temel bileşenleri; safra asitleri, kolesterol, fosfolipidler, safra pigmentleri —özellikle bilirubin— ve çeşitli elektrolitlerdır. Safra asitleri, lipidlerin misel formasyonu aracılığıyla emülsifiye edilmesi ve sindirilmesinde işlev görür; safra bu işleve katkısı nedeniyle sindirim sisteminin vazgeçilmez bir salgısı konumundadır. Bilirubin, hemoglobin ile diğer hem içeren proteinlerin yıkım ürünü olan hem grubunun dönüşümünden elde edilir; karaciğer bu yolla hem konjuge hem de konjuge olmayan bilirubini işleyerek safra aracılığıyla dışkıya atar. Safranın karaciğerden duodenuma ulaşması intraheptik safra kanalları, ana hepatik kanal, sistik kanal ve safra kesesi, ardından da ortak safra kanalı aracılığıyla gerçekleşir.
E. Detoksifikasyon ve İlaç Metabolizması
Karaciğer, vücudun ana detoksifikasyon organı olarak bağırsak kaynaklı zararlı maddeleri etkisizleştirme misyonunu omuzlar. Yabancı maddelerin (ksenobiyotiklerin) biyotransformasyonu iki aşamadan oluşur: Faz I reaksiyonları, sitokrom P450 (CYP) enzim ailesi tarafından yürütülen oksidasyon, redüksiyon ve hidroliz işlemlerini kapsar; bu süreçte üretilen metabolitler, bazen ana maddeden daha reaktif yapılardır. Faz II reaksiyonları ise konjugasyon işlemlerini içerir; glukuronidasyon, sülfonasyon ve glutatyon konjugasyonu gibi basamaklarla metabolitler suya daha kolay çözünen, daha az toksik ya da biyolojik olarak inaktif hale getirilir.
CYP sistemi, birbirleriyle ve birbiriyle rekabet eden çok sayıda ilaç arasındaki etkileşimlerin —ilaç-ilaç etkileşimlerinin— merkezinde yer alır. Örneğin CYP3A4, tüm klinik ilaçların yaklaşık yüzde ellisini metabolize eden en önemli karaciğer enzimidir ve bu enzimin aktivitesini baskılayan veya hızlandıran ilaçlar ciddi farmakokinetik etkileşimlere yol açabilir. Asetaminofenin (parasetamol) hepatotoksisitesi, bu mekanizmanın çarpıcı bir örneğidir: Normalde toksik olmayan bu ilaç, yüksek dozlarda CYP2E1 tarafından son derece reaktif bir toksin olan NAPQI’ye dönüştürülür ve glutatyon depolarını tüketerek hepatosit ölümüne neden olur.
F. Vitamin ve Mineral Metabolizması
Karaciğer, A, D, E, K vitamini ile B12 vitamini depolarının tutulduğu başlıca organdır; bunların yanı sıra demir ve bakır gibi esansiyel minerallerin de başlıca depo merkezi konumundadır. D vitamini, güneş ışığı etkisiyle deride sentezlendikten sonra karaciğerde 25-hidroksivitamin D3 biçimine dönüştürülür; bu, D vitamini aktivasyonunun ilk ve kritik adımını oluşturur. A vitamini ise karaciğer ito hücrelerinde retinol esterleri halinde depolanır. Demir metabolizması açısından karaciğer; ferritin ve hemosiderin aracılığıyla demir depolar, transferrin sentezini gerçekleştirir ve demirin sistemik düzeyini etkileyen bir hormon olan hepsidini üretir. Hepsidin eksikliği hemokromatozda demir birikim bozukluğunun merkezi nedeni olduğundan, bu hormonun karaciğerdeki sentezinin bozulması doğrudan hastalığın patofizyolojisiyle örtüşür.
G. Hormonal Metabolizma
Karaciğer, çeşitli hormonların hem sentezlenmesinde hem de yıkımında aktif rol alır. İnsülin büyüme faktörü 1 (IGF-1) büyük ölçüde karaciğerde üretilir ve büyüme hormonu sinyallerinin doku düzeyine taşınmasında aracı görevini üstlenir. Anjiyotensin I ise karaciğer kökenli bir protein olan anjiyotensinojenin renin tarafından enzimatik olarak parçalanmasıyla oluşur; bu süreç tansiyonun düzenlenmesinde kritik bir öneme sahiptir. Karaciğerin hormon yıkımı işlevi de en az sentezi kadar önem taşır: insülin, glukagon, steroid hormonlar ve tiroid hormonları karaciğerde metabolize edilir; bu nedenle karaciğer yetmezliği, hormon birikiminin tetiklediği değişik ve karmaşık endokrin bozukluklara zemin hazırlayabilir.
VII. SAFRA YOLLARI: EKSTRAHEPATIK ANATOMİ
Karaciğeri terk eden sağ ve sol hepatik kanallar porta hepatis düzeyinde birleşerek ana hepatik kanalı (ductus hepaticus communis) oluşturur. Bu kanal, sistik kanal (ductus cysticus) ile birleşerek ortak safra kanalını (ductus choledochus) meydana getirir. Ortak safra kanalı, uzunluğu 4 ila 8 santimetre ve çapı normalde 5 milimetrenin altında olup hepatoduodenal ligamentin serbest kenarında portal ven ile hepatik arterin yanı sıra seyreder. Pankreas başının arkasından geçtikten sonra genellikle pankreas kanalıyla birleşerek hepatopankreatik ampullada (Vater ampullası) sonlanır ve duodenumun inen parçasındaki papilla duodeni majordan (Vater papillası) duodenuma açılır.
Papilla duodeni majörün hemen etrafında konumlanan Oddi sfinkteri, birkaç kas tabakasından oluşan karmaşık bir düzenleyici kapak mekanizmasıdır: sfinkter ampullae, sfinkter ductus choledochi ve sfinkter ductus pankreatici olarak üç ayrı bileşenden meydana gelir. Oddi sfinkterinin koordineli kasılıp gevşemesi, safra ve pankreas sıvısının duodenuma akışını düzenleyerek sindirim sürecini ince bir denge içinde kontrol eder. Sfinkter Oddi disfonksiyonu, safranın anormal birikimi nedeniyle tekrarlayan biliyer veya pankreatik ağrı ataklarına yol açabilir.
Safra kesesinin cysticus kanalının anatomik varyasyonları son derece sık görülür. Kistik kanal ile ana hepatik kanal birleşme açısı, hepsinin klinisyen tarafından bilinmesi gereken geniş bir anatomik yelpaze içinde değişkenlik gösterir: olguların üçte ikisinde kistik kanal ana hepatik kanala sağdan dik açıyla bağlanırken, dörtte birinde uzun ve paralel bir seyir izler, kalan olgularda ise çok kısa olabilir ya da safra kesesi boynu doğrudan ana kanala açılabilir. Bu değişkenlikler, laparoskopik kolesistektomi sırasında safra yollarının yanlışlıkla kesilmesi ya da bağlanması riskini artırdığından safra yolu yaralanmaları açısından önemli bir tehlike faktörü oluşturur.
VIII. KLİNİK BÖLÜM: PORTAL HİPERTANSİYON
Portal hipertansiyon, portal ven basıncının 10 mmHg’nin üzerine çıkmasıyla tanımlanır; klinik komplikasyonlar açısından anlamlı eşik değer ise genellikle 12 mmHg olarak kabul edilmektedir. Patolojik basınç yükselmesine neden olan nedenler anatomik konumlarına göre prehepatik (portal ven trombozu gibi), intrahepatik (özellikle karaciğer sirozu) ve posthepatik (Budd-Chiari sendromu veya sağ kalp yetmezliği gibi) olarak üç grupta incelenir. Tüm etyolojik faktörler içinde siroz en yaygın neden olmayı sürdürmektedir.
Portal basıncın yükselmesi, zaten var olan portosistemik anastomoz kanalları aracılığıyla kollateral dolaşımın gelişmesini zorlar. Özofagus varisleri, bu süreçte en dread komplikasyon kaynağı olmaya devam eder; varislerin rüptürü, ilk kanama atamasında mortalitesi yüzde yirmi ile yirmi beş arasında seyreden bir tıbbi acil durum oluşturur. Umbilikal venin yeniden açılması ve karın ön duvarı venlerinin belirginleşmesi ‘caput Medusae’ görünümünü ortaya çıkarır. Rektal varisler anorektal varislere yol açabilir; bu yapılar anatomik konumları nedeniyle hemoroidlerle karıştırılmamalıdır. Asit, portal hipertansiyon varlığında hipoalbümineminin ve böbrek sodyum tutulumunun eşzamanlı etkisiyle ortaya çıkan birden fazla patofizyolojik mekanizmanın birleşimi sonucu gelişir.
IX. KARACİĞER SİROZU
Siroz, herhangi bir kronik karaciğer hasarına karşı gelişen ortak son yanıtı temsil eder ve yaygın fibrozis, mimarinin bozulması ve rejeneratif nodüllerin oluşumuyla karakterizedir. Sirozu farklı hastalıklardan ayıran bu histolojik tablo; karaciğerin işlevsel kapasitesini ilerleyici biçimde azaltır ve portal hipertansiyonun başlıca nedenleri arasında yer alır.
Histopatolojik olarak sirozda portal alanlar arasında ve santral venlerle portal alanlar arasında fibröz köprüler gelişir; bu köprüler normal lobüler mimariyi bozarak parankimi fonksiyonel olarak birbirinden izole eder. Rejeneratif nodüller, fibröz dokularla çevrilmiş hepatosit adacıklarından oluşur. Mikroskopik incelemede merkezi toplardamarın ortadan kaybolduğu, kronik inflamatuar hücre infiltrasyonunun bulunduğu, safra kanalı proliferasyonunun eşlik ettiği ve hepatositlerde yağlanmanın (steatoz) olduğu gözlemlenir.
Alkole bağlı karaciğer hastalığı için özgün bir histolojik bulgu olan Mallory-Denk cisimcikleri (alkolik hyalin), hasar görmüş hepatositlerin sitoplazması içinde biriken sitokeratin ara filamentlerinin anormal agregatlarından oluşur. Kolestaz ise hepatosit ve safra kanalcıklarında safra pigmentinin birikmesiyle belgelenebilir. Tüm bu patolojik değişiklikler, karaciğerin hem metabolik hem de ekskretuar işlevlerinin derin bir şekilde bozulduğunun morfolgojik kanıtlarıdır.
X. KARACİĞER KANSERLERI
A. Hepatoselüler Karsinom
Hepatoselüler karsinom (HCC), birincil karaciğer kanserlerinin en yaygın türü olup dünya genelinde en sık görülen kanserler arasında beşinci, kansere bağlı ölümler arasında ise üçüncü sıraya yerleşmiştir. Olguların büyük çoğunluğu siroz zemininde gelişmektedir; ancak kronik Hepatit B enfeksiyonuyla ilişkili vakalarda altta yatan siroz olmadan da HCC ortaya çıkabilmektedir. Kronik Hepatit B veya Hepatit C enfeksiyonu, non-alkolik steatohepatit (NASH) ve alkolün yol açtığı siroz, HCC için en önemli risk faktörleri arasındadır.
Histopatolojik açıdan HCC; geniş trabeküler yapılar, psödoglandüler ya da asiner paternler, hücreler içinde safra pigmenti varlığı, sinüzoid benzeri yapılar, psödokapsül oluşumu ve mitotik aktivitenin belirgin artışı gibi özgün morfolojik özellikler sergiler. Tümörü besleyen sinüzoidlerde eritrosit ve lökosit varlığı, tümörün neovaskülarizasyon sürecini yansıtır. Atipik hepatositler, çekirdek-sitoplazma oranındaki artış ve anormal nükleer morfoloji ile kolayca ayırt edilir.
Klinik tanı; serum alfafetoprotein (AFP) düzeyi ölçümü, bilgisayarlı tomografi ve manyetik rezonans görüntüleme gibi dinamik görüntüleme yöntemleri ve gerektiğinde karaciğer biyopsisine dayanır. Tedavi seçenekleri tümörün evresine göre değişmekte olup cerrahi rezeksiyon, karaciğer transplantasyonu, lokorejyonel yöntemler —radyofrekans ablasyonu, transarteriyel kemoembolizasyon (TACE)— ve sorafenib ile lenvatinib gibi sistemik tedaviler bu seçenekler arasında yer almaktadır.
B. Kolanjiyokarsinom
Kolanjiyokarsinom, intrahepatik veya ekstrahepatik safra kanalı epitelinden kaynaklanan bir tümördür. Primer sklerozan kolanjit, karaciğer kist enfeksiyonları, safra taşı hastalığı ve bölgesel paraziter infestasyonlar risk faktörleri arasında sayılmaktadır. Histopatolojik olarak tübüler ya da papiller yapılar sergileyen mukus üreten adenokarsinom görünümündedir. Kötü prognozuyla bilinen bu tümörde rezektabilite, tanı anındaki evreye bağlı olarak büyük ölçüde değişkenlik gösterir.
XI. TANI YÖNTEMLERİ
A. Biyokimyasal Belirteçler
Serum karaciğer enzimleri karaciğer hasarının ve fonksiyon bozukluğunun değerlendirilmesinde temel tanı araçlarıdır. Alanin aminotransferaz (ALT) ve aspartat aminotransferaz (AST) hepatoselüler hasarın göstergesi olup hücre ölümüyle birlikte seruma salınır; bu nedenle hepatit ve iskemi gibi durumların tanısında kullanılır. ALT karaciğere daha özgül iken AST kalp, iskelet kası ve diğer organlarda da yükselebilir. Alkalen fosfataz (ALP) ve gama-glutamil transferaz (GGT), safra yolu hastalığının ve kolestazın özgün belirteçleri olarak bilinir. Serum bilirubini, albumin düzeyi ve protrombin zamanı ise sentetik karaciğer fonksiyonunu yansıtır; bu üç parametre karaciğer hastalığının ağırlığını ve prognozunu değerlendirmede kullanılan Child-Pugh ve MELD skorlama sistemlerinin temel bileşenlerini oluşturur.
B. Görüntüleme Yöntemleri
Ultrasonografi, karaciğer görüntülemesinde ilk basamak yöntem olma özelliğini korumaktadır; ekipman gereksiniminin mütevazı olması, iyonizan radyasyon içermemesi ve ucuz maliyeti bu tercih için başlıca nedenlerdir. Ultrasonografi ile karaciğer boyutu, parankim ekojenitesi, fokal lezyonlar ve safra yolu patolojileri değerlendirilebilir. Duplex Doppler ultrasonografisi ile portal ve hepatik ven akımı incelenerek vasküler patolojiler —portal ven trombozu, Budd-Chiari sendromu— saptanabilir. Elastografi, karaciğer fibrozis derecesini biyopsi gerektirmeksizin değerlendirmeye olanak tanıyan, giderek yaygınlaşan bir ultrasonografi tekniğidir.
Dinamik kontrastlı bilgisayarlı tomografi ve manyetik rezonans görüntüleme, fokal karaciğer lezyonlarının karakterizasyonu, tümör evrelemesi ve vasküler anatomi değerlendirmesi için daha üstün tanısal özellikler sunmaktadır. MRG’nin özel teknikleri olan manyetik rezonans kolanjiyopankreatikografi (MRCP) safra yolu anatomisini invaziv olmayan bir yöntemle görüntülerken, demir ve yağ içeriğini ölçmeye yönelik özel MRG sekansları non-alkolik yağlı karaciğer hastalığının ve hemokromatozun değerlendirilmesinde giderek artan bir kullanım alanı bulmaktadır.
C. Karaciğer Biyopsisi
Karaciğer biyopsisi, diffüz parankimal karaciğer hastalığının tanısında altın standart olmayı sürdürmektedir; kronik hepatitin etiyolojisi ve evresi ile özellikle tedavi kararını doğrudan etkileyen fibrozis derecesinin belirlenmesi bu standart gereksinimin başlıca nedenleridir. Perkutan ultrasonografi rehberliğinde yapılan biyopsi en yaygın kullanılan yöntemdir; koagülopati ya da assit varlığında ise transjugüler yol tercih edilir. Doku örneği Metavir ya da Ishak fibrozis skorlama sistemlerine göre değerlendirilerek fibrozis ve enflamasyon derecelendirilir. Biyopsinin bu katkılarına karşın, intrahepatik örnekleme hatasına olan duyarlılığı ve komplikasyon olasılığı nedeniyle kullanımına yönelik endikasyonlar son yıllarda giderek daralmaktadır.
XII. KARACIĞER TRANSPLANTASYONU
Karaciğer transplantasyonu, son dönem kronik karaciğer hastalığı ve fulminan hepatik yetmezlik olgularında son çare tedavi seçeneği olarak yerini almıştır. Kadavradan organ nakline ek olarak, yaşayan vericiden sağ lob veya sol lateral segment alınarak gerçekleştirilen canlı vericiden karaciğer nakli; organ yetersizliği nedeniyle nakil bekleyen hastalarda kadavra organ bekleme sürelerini belirgin biçimde kısaltan önemli bir alternatif olarak günümüzde geniş uygulama alanı bulmaktadır.
Transplantasyon endikasyonları, karaciğer hastalığının klinik ağırlığını ve mortalite riskini tahminen değerlendiren MELD skoru temel alınarak belirlenir. Cerrahiyi takiben uygulanan immünosüpresif tedavi rejimi; kalsinörin inhibitörleri (siklosporin, takrolimus), kortikosteroidler ve antiproliferatif ajanlardan (mikofenolat mofetil, azatiyoprin) oluşur. Allograft reddi, enfeksiyon ve immünosüpresyona bağlı uzun dönem komplikasyonlar —özellikle böbrek yetmezliği ve kardiyovasküler hastalık— transplantasyonun başlıca klinik sorunları olmaya devam etmektedir. Karaciğerin tam iyileşmesi mümkün olmakla birlikte, HCC nedeniyle gerçekleştirilen transplantasyon olgularında tümörün yeniden ortaya çıkma riski titiz bir takip gerektirmektedir.
XIII. KARACIĞER VE FARMAKOLOMOJININ KESIŞIMI
Karaciğer, ilaç metabolizmasının merkezi organı olarak farmakoloji alanında ayrı bir önem taşımaktadır. İlaçların oral yoldan alınması ve emiliminin ardından portal dolaşım aracılığıyla karaciğere ulaşması, ‘ilk geçiş etkisi’ adı verilen fenomene yol açar; bu süreçte bazı ilaçlar sistemik dolaşıma geçmeden önce büyük ölçüde metabolize edilir. İlk geçiş etkisi, nitratlar ve propranolol gibi ilaçların biyoyararlanımını belirgin biçimde azaltır; bu durum, söz konusu ilaçların oral dozlarının hesaplanmasında doğrudan göz önünde bulundurulmasını zorunlu kılar.
Karaciğer yetmezliğinde, normalde karaciğerde geniş ölçüde metabolize edilen ilaçların plazmada birikmesi ve toksisite eşiğinin aşılması kaçınılmaz olur. Dolayısıyla Child-Pugh ya da MELD skoru yüksek olan hastalarda ilaç dozlarının dikkatli biçimde yeniden ayarlanması gerekmektedir. Tersine, biyoaktivasyona —yani aktif olmayan bir proilacın karaciğerde aktif formuna dönüştürülmesine— ihtiyaç duyan ilaçlar karaciğer yetmezliğinde yeterli terapötik etkiyi gösteremeyebilir; kodein ve klopidogrel bu mekanizmanın tipik örnekleri arasında sayılabilir.
İlaç ilişkili karaciğer hasarı (DILI), ilaç sınıfları arasında en sık görülen yan etki profillerinden biri olmaya devam etmektedir. Asetaminofen yüksek doz kullanımında öngörülebilir doz bağımlı hepatotoksisite gösterirken, diğer pek çok ilaçta görülen karaciğer hasarı idiyosinkratik niteliktedir ve tahmin edilemez biçimde ortaya çıkmaktadır. DILI, ilaç geliştirme süreçlerinde onay sonrası ilaç geri çekilmelerinin başlıca nedeni olması bakımından hem klinik hem de farmakovijilans alanında kritik bir sorun olma niteliğini korumaktadır.
XIV. REJENERASYONİN BİYOLOJİSİ
Karaciğerin rejenerasyon kapasitesi, tüm organ sistemleri içinde en dikkat çekici olanlardan biridir. Parsiyel hepatektomi modellerinde karaciğer kütlesinin yaklaşık yüzde yetmişinin alınmasının ardından kalan dokudaki hepatositler hızla çoğalarak operasyon öncesi karaciğer kütlesini 4 ila 6 hafta içinde büyük ölçüde yeniden oluşturur. Bu süreç yeni bir organ oluşumundan ziyade kompansatör hipertrofi ve hiperplazi olarak nitelendirilmelidir.
Karaciğer rejenerasyonunun moleküler mekanizmaları; hepatosit büyüme faktörü (HGF), epidermal büyüme faktörü (EGF) ve tümör nekroz faktörü-alfa (TNF-α) ile interlökin-6 (IL-6) gibi proinflamatuvar sitokinlerin oluşturduğu karmaşık sinyal ağlarını kapsamaktadır. Metabolik kapasiteyi büyük ölçüde koruyan olgun hepatositlerin hızlı proliferasyonu rejenerasyonun birincil mekanizmasını oluşturur; daha ağır ya da kronik karaciğer hasarı koşullarında ise Hering kanallarından köken alan progenitör —kök hücre benzeri— hücreler devreye girerek onarım sürecine katılır.
Karaciğer rejenerasyonunun sınırlılıkları da klinik uygulamada belirleyici bir öneme sahiptir. Altta yatan siroz, rejenerasyonu ciddi ölçüde kısıtlar; bu nedenle sirotik bir karaciğerde parsiyel rezeksiyonun sınırları sağlıklı bir karaciğere kıyasla çok daha dar tutulmak zorundadır. Yeterli fonksiyonel karaciğer parankiminin muhafaza edilmesi —bu oran cerrahi literatürde ‘future liver remnant’ (FLR) olarak tanımlanmaktadır— post-hepatektomik karaciğer yetmezliğini önlemenin temel koşulunu oluşturur.
XV. SONUÇ
Karaciğer, insan fizyolojisinde olağanüstü ve eşsiz bir konuma sahiptir. Evrimsel kökleri omurgalı tarihinin derinliklerine uzanan bu organ, yüzyıllar boyunca anatomistlerin, fizyologların ve klinisyenlerin odak noktası olmuştur. Tarihin ilk dönemlerinde kehanet ritüellerinde kullanılan bu organa duyulan ilgi, modern tıbbın sunduğu derin anlayışla şekillenerek bugünkü bilimsel formuna kavuşmuştur.
Metabolizmanın tüm temel süreçlerini kapsaması, çift vasküler beslenme mimarisi, portal venöz dolaşımdaki stratejik konumu ve olağanüstü rejenerasyon kapasitesi bir arada değerlendirildiğinde karaciğerin fizyolojik açıdan ne denli merkezi bir organ olduğu açıkça ortaya çıkar. Hepatoloji, cerrahisi, radyoloji ve biyomedikal araştırmalar alanında süregelen hızlı gelişmeler, karaciğer biyolojisine ve patolojisine ilişkin anlayışımızı her geçen yıl daha da derinleştirmektedir. Non-alkolik yağlı karaciğer hastalığının küresel ölçekte artışı, doğrudan etkili antiviral ajanların kronik viral hepatiti büyük ölçüde tedavi edilebilir bir hastalığa dönüştürmesi ve karaciğer transplantasyonu tekniklerindeki süregelen ilerlemeler, bu dinamizmin en somut göstergeleridir.
Karaciğerin bütüncül bir perspektiften anlaşılması —yani etimolojik köklerden evrimsel biyolojiye, ince hücresel düzenekten klinik patolojiye uzanan geniş bir bakış açısıyla kavranması— hem eğitimsel hem klinik hem de araştırma açısından vazgeçilmez bir gereklilik olmayı sürdürmektedir.
Tarih
Karaciğer yüzyıllardır insan anatomisi ve fizyolojisinde önemli bir organ olmuştur. Dünyadaki eski uygarlıklar tarafından incelenmiş ve tanımlanmıştır ve insan sağlığına olan önemi binlerce yıldır kabul edilmektedir.
- Eski Mısır: Karaciğer, eski Mısırlılar tarafından vücuttaki en önemli organlardan biri olarak kabul edildi. Karaciğerin ruhun ve duyguların yeri olduğuna ve sindirimi, kan üretimini ve diğer bedensel işlevleri düzenlemekten sorumlu olduğuna inanıyorlardı.
- Antik Yunanistan: Yunan hekimi Hipokrat (MÖ 460-370), karaciğerin anatomisini ve fizyolojisini ayrıntılı olarak tanımlayan ilk kişilerden biriydi. Karaciğerin kan üretiminden sorumlu olduğuna ve ayrıca yiyeceklerin sindirilmesinde ve toksinlerin atılmasında rol oynadığına inanıyordu.
- Antik Roma: Romalı doktor Galen (MS 130-200), karaciğer anatomisi ve fizyolojisi anlayışını daha da geliştirdi. Sindirim için gerekli olan safranın üretilmesinden karaciğerin sorumlu olduğuna inanıyordu. Ayrıca karaciğerin kan üretiminde ve toksinlerin yok edilmesinde rol oynadığına inanıyordu.
- Orta Çağlar: Orta Çağ boyunca karaciğer, tıbbi araştırmaların odak noktası olmaya devam etti. Arap hekim Avicenna (MS 980-1037) karaciğer hakkında kapsamlı yazılar yazdı ve çalışmaları yüzyıllar boyunca Avrupa’da etkili oldu.
- Rönesans: Rönesans’ta anatomi ve fizyolojiye yeniden bir ilgi vardı. İtalyan hekim Andreas Vesalius (1514-1564), karaciğerin ayrıntılı resimlerini içeren anatomi üzerine dönüm noktası niteliğinde bir kitap yayınladı.
- Modern çağ: Modern çağda karaciğer hakkında çok sayıda araştırma yapılmıştır. Bilim adamları karaciğerin anatomisi, fizyolojisi ve biyokimyası hakkında daha fazla şey öğrendiler. Ayrıca hepatit, siroz ve karaciğer kanseri gibi karaciğeri etkileyebilen hastalıklar hakkında daha fazla şey öğrendiler.
Karaciğer, insan sağlığında bir dizi önemli rol oynayan hayati bir organdır. Sindirim için gerekli olan safranın üretilmesinden sorumludur; toksinleri parçalamak; enerji depolamak; ve kan şekeri seviyelerinin düzenlenmesi. Karaciğer ayrıca kan hücrelerinin üretiminde ve atık ürünlerin vücuttan uzaklaştırılmasında rol oynar.
Karaciğer karmaşık bir organdır ve işlevi tam olarak anlaşılamamıştır. Bununla birlikte, bilim adamları karaciğer hakkında daha fazla şey öğrenmeye devam ediyor ve bu araştırma, karaciğer hastalıklarının teşhis ve tedavisinin iyileştirilmesine yardımcı oluyor.
Kaynak:
- Joseph Ahn, Michael E. Breen, “Biliary Ultrasound.” StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2022.
- Grant EG, Benson CB, Moneta GL, et al. “Carotid artery stenosis: grayscale and Doppler ultrasound diagnosis – Society of Radiologists in Ultrasound Consensus Conference.” Ultrasound Q. 2003;19(4):190–198.
- Caddy, G. R., Tham, T. C., & Craig, D. A. (2004). “The role of ultrasound in the diagnosis and management of gallstones.” British journal of nursing (Mark Allen Publishing), 13(12), 710–714.
- Paul K. Newton, Lawrence A. Frizzell, “Ultrasonic methods in solid state physics.” Elsevier; 2012.