- Meme hücrelerinde başlayan kanser türüdür.(bkz; mamma)
İçindekiler
Epidemiyoloji
Risk faktörleri
- İnsan yaşlanması,
- Jinekolojik;
- Hastanın bilinen hastalıkları,
- Aileden kalıtım
- Genetik mutasyonlar;
- BRCA1- veya BRCA2-Mutasyonu
- Li Fraumeni-Sendromu
- Peutz-Jegher-Sendromu
- Cowden-Sendromu
- Ataksi
- Telenjiektazi
- Torakal ışın tedavisi
- Alkol kullanımı
Sınıflandırma
- Duktal Karsinom: Süt kanallarından kaynaklanan en yaygın meme kanseri türüdür. İn situ (DCIS) veya invaziv olabilir.
- Özel Tip Yok (NST): Daha önce invaziv duktal karsinom olarak bilinen bu terim, spesifik histolojik özelliklere sahip olmayan invaziv meme kanserlerinin çoğunu kapsar.
Meme kanserlerinin %99’u adenokarsinomdur.
Duktal invaziv meme kanseri:
En sık karşılaşılan meme kanseri tipidir; (40-75%) infiltrasyona yola açan, kötü huylu ve neoplaztik hücreleri anormal çoğaltır.
Duktal karsinoma in situ (DCIS, ductal carcinoma in situ)
Keşfedilmiş meme kanserlerinin 15-20%’unu oluşturur. İnvaziv olmayan, süt yollarından meydana gelmiş bir kanserdir. Bazal zarı yırtmaz.
Lobüler karsinoma in situ (LCIS, lobular carcinoma in situ)
- Meme kanserlerinin 5-10%’unu oluşturur.
- Süt bezi lopcuklarından oluşur.
- Epitel proliferasyon sayesinde meydana gelir.
- Terminal süt yollarını (Duktolobuler birimleri) sınırlar.
- Bazal zarı yırtmaz.

Epitel olmayan kötü kanser tipleri ise;
Hastaların% 4’ünde tanı konulduğunda her iki meme de etkilenir.
Meme kanserlerinin% 50’si, meme bezinin dış üst kadranda bulunur. % 20’si meme başı üzerinde ve çevresinde lokalizedir. Her birinin% 10’u kalan üç çeyreği etkiler. Bir çeyrekte birkaç odak varsa, biri multifokal istiladan bahseder; aynı memenin birkaç çeyreği varsa, buna çok merkezli istila denir.
Meme kanserleri lenfojen ve hematojen metastazlara neden olur. Metastaz olasılığı, tümörün hacmi ile artar. Dışarıda ve meme bölgesinde bulunan karsinomlar tercihen aksiller lenf nodlarına metastaz yapar. İç kadranlarda bulunan meme karsinomları, iç torasik arter boyunca lenf nodu istasyonlarına daha sık metastaz yapar.
Prensip olarak, herhangi bir organ hematojen yayılmadan dolayı metastazdan etkilenebilir. Kemik metastazları en sık görülür, bunu karaciğer ve akciğer metastazları takip eder. Beyin metastazları daha az görülür.
Evreleme TNM sınıflandırmasına göre yapılır.
- BT-Toraks ve Abdomen
- İskelet sintigrafisi
- Belli olmayan bulgularda PET veya PET-CT
- Santral sinist sistemi metastazında MR
Teşhis
- İnspeksiyon sırasında, deri gamzeleri(skin dimpling) ile farkedilebilir.
- Mamografi, Meme kanserinin teşhisindeki en etkin görüntüleme yöntemlerinden biridir.
- Palpasyon ile sertlik oluşumuna dikkat edilmelidir.
- Jackson testi; Sertlik merkez alınırken iki el yardımıyla meme sıkıştırılır.
- İyi huyluya işaret, deri katlanır.
- Kötü huylu (malign) işareti ise deri içeriye doğru çekilir.
- Aksilar ve Supra-, infraklavikular lenf düğümü hattı kontrol edilmelidir.
- Sertlik hissediliyorsa TNM Sınıflandırmasına göre en az T2 seviyesinde olmalıdır.
- Jackson testi; Sertlik merkez alınırken iki el yardımıyla meme sıkıştırılır.
Fizik muayeneye ve anamnezin yanı sıra, meme kanseri teşhisi ayrıca cihaz ve laboratuvar testlerini de içerir. Fizik muayene her zamaniki yanı karşılaştırmalı yapılmalıdır ve şunları içerir:
- Muayene (cilt retraksiyonu, ülserasyon veya egzama)
- Memenin palpasyonu ve lenf nodu istasyonları (hareketlilik, lenfadenopatiler)
- Kolların nörolojik muayenesi (brakiyal pleksusun infiltrasyonu)
- Teşhis aşağıdakilerle desteklenir:
- Mamografi
- Meme sonografisi, muhtemelen elastosonografi
- Galaktografi
- Meme MRG
Labor
- CEA (Carcinoembryonales Antigen)
- CA15-3 (Cancer-Antigen 15-3)
Endokrin Tedavi:
Östrojen Reseptörü (ER) Pozitif ise: Tümör hücreleri östrojen reseptörlerini ifade ediyorsa, hormon etkilerini engellemek ve kanser büyümesini yavaşlatmak için endokrin tedavisi (örn. tamoksifen, aromataz inhibitörleri) kullanılabilir.
HER2 Pozitifi ise: HER2 (insan epidermal büyüme faktörü reseptörü 2) aşırı ekspresyonu daha agresif meme kanseri ile ilişkilidir. HER2-pozitif kanserler trastuzumab (Herceptin) gibi hedefe yönelik tedavilerle tedavi edilebilir.
İmmünoreseptör Testi: Tedavi kararlarını yönlendirmek için hormon reseptörlerinin (ER ve progesteron reseptörü [PR]) varlığını ve HER2 durumunu belirler.
Derecelendirme ve İndeksleme
Ki-67 Proliferasyon İndeksi: Kanser hücrelerinin çoğalma oranını belirlemek için kullanılan bir belirteçtir. 14’ün üzerinde bir Ki-67 indeksi, daha agresif bir tümöre işaret eden daha yüksek bir büyüme fraksiyonunu gösterir.
Polidifferans İndeksi: Tümör içindeki heterojenliği değerlendirmek için kullanılır ve ek prognostik bilgi sağlar.
Görüntüleme
Görüntüleme ve Evreleme:
- Tümörler < 2 cm:
- Başlangıç Çalışması: Primer tümörü ve bölgesel lenf düğümlerini değerlendirmek için göğüs röntgeni ve sonografiyi içerir.
- Kemik Sintigrafisi: Kemik metastazlarını tespit etmek için kullanılır.
- Tümörler ≥ 2 cm:
- Kapsamlı Evreleme: Uzak metastazları değerlendirmek için göğüs BT’si ve kemik sintigrafisini içerir.
Sonografi
Meme sonografisi (ultrason) meme anormalliklerini değerlendirmek için kullanılan önemli bir tanı aracıdır. Özellikle mamografi ile tespit edilen şüpheli bulguların ileri tetkikinde ve ele gelen yumruların değerlendirilmesinde faydalıdır.
Hissedilebilir kitle olduğu vakitte başvurulması gereken ilk teşhis aracıdır. 40 yaş altı kadınlarda meme kanseri teşhisi için standart yöntemdir.
Meme Sonografisinde Temel Özellikler:
- Yıldız Deseni: Meme dokusundaki yıldız şeklindeki bir desen genellikle maligniteyi düşündürür. Bu patern tipik olarak, lezyonun çevre dokuya yayılan spiküle kenarlara sahip olduğu invaziv kanserlerde görülür.
- Fibrozis ve Yoğunluklar: Artmış fibröz doku ve yüksek yoğunluklu alanlar, iyi huylu fibrokistik değişiklikler ve maligniteler dahil olmak üzere çeşitli meme durumlarının göstergesi olabilir. Bu özellikler daha fazla araştırma yapılmasını gerektirebilir.
Maligniteyi Gösteren İşaretler
Sonografide belirli özellikler görüldüğünde, meme kanseri şüphesi uyandırır ve genellikle daha ileri tanı prosedürleri gerektirir:
- Düzensiz Kenarlar: Düzensiz veya spiküle sınırlara sahip lezyonlar.
- Hipoekoik Kitleler: Ultrasonda çevre dokuya kıyasla daha koyu görünen katı kitleler.
- Posterior Akustik Gölgelenme: Bu, ultrason dalgaları yoğun bir kitle tarafından bloke edildiğinde ortaya çıkar ve genellikle malignitelerde görülür.
- Artmış Vaskülarite: Bir lezyonun etrafında Doppler ultrason ile tespit edilebilen artmış kan akışı maligniteye işaret edebilir.
Mamografi
- Memede hissedilebilir kitle veya önlem amaçlı 50. yaşını doldurmuş kadınlarda endikasyonu vardır.
- Kraniyo-kaudal ve medio-lateral obliklere ışın gönderilerek üç boyutlu olarak incelenir.

Biyopsi
Meme biyopsisi
- Meme kanseri tanısını doğrulamak için biyopsi yapılması şarttır. Teknikler arasında çekirdek iğne biyopsisi, ince iğne aspirasyonu ve eksizyonel biyopsi yer alır.
- Klips Sistemi: Biyopsiden sonra, ileride başvurmak üzere lezyonun yerini işaretlemek için memeye küçük bir işaretleyici (klips) yerleştirilebilir.
- Gözcü Sistemi: Bu sistem ameliyat sırasında klipsin veya biyopsi bölgesinin yerini belirlemek için kullanılır ve lezyonun kesin olarak çıkarılmasını sağlar.
Lenf düğümü biyopsisi

Son tanı, sonraki histolojik değerlendirmeyle biyopsi (punch biyopsi veya açık örnek eksizyonu) ile doğrulanır. Sınıflandırmaya ek olarak, progesteron (PR) ve östrojen reseptörleri (ER) ve HER2 / neu (c-erb-B2) ifadesi burada belirlenebilir.
- Östrojen, prolaktin, FSH ve FH ile hormon durumu esas olarak laboratuarda incelenir. Tümör belirteçleri, ör. B. CEA, CA 15-3 ve CA 19-9 belirlenebilir.
- Olumlu sonuçların ortaya çıkması durumunda aşamayı tamamlamak için forma bağlı olarak ek incelemeler gereklidir:
- Göğüs, karın ve başın BT’si
- PET-BT
İleri Teknikler:
- Meme Baskısı: Cerrahi öncesi planlama ve kişiselleştirilmiş tedavi yaklaşımları için doğru modeller oluşturmak üzere gelişmiş görüntüleme ve 3D baskı teknolojilerinin kullanımını içerir.
- Genetik Test: BRCA1/BRCA2 gibi genlerde tedavi seçeneklerini ve profilaktik cerrahi hususlarını etkileyebilecek mutasyonları değerlendirir.
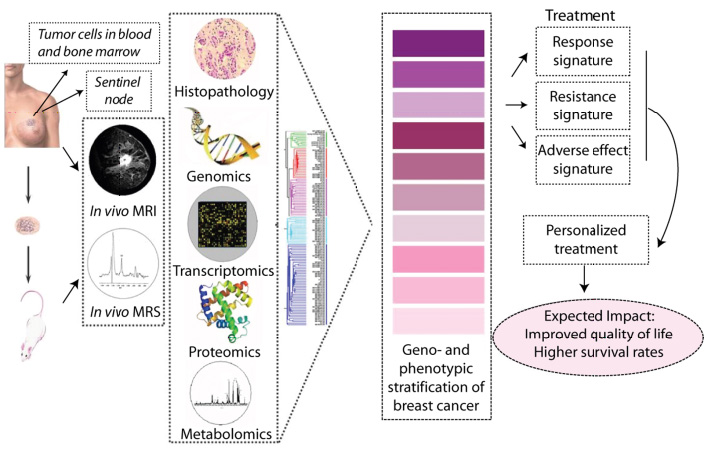
Genomik tümör
Bu muayene yöntemlerine ek olarak, ileri tümör genomikleri de giderek daha önemli bir teşhis rolü oynamaktadır. Tümör hücrelerinin farklı genlerinin ekspresyon seviyesi belirlenir, bu da büyüme davranışı ve metastaz hakkında açıklamalar yapılmasını sağlar. Onkogenleri belirleyerek, yani. Hangi hastaların kemoterapiden yarar gördükleri ve hangilerinin yararlanmadığı hakkında da açıklamalar yapılmaktadır.
TNM evrelemesi
| T-Kategori | Anlamı |
|---|---|
| Tis | Saptanabilir tümör olmayan duktal veya lobüler karsinom veya memenin Paget hastalığı, |
| T1 | En büyük ölçüde 2 cm veya daha az tümör T1a – > 0,1 – 0,5 cm T1b – > 0.5 – 1 cm T1c – > 1 – 2 cm |
| T2 | 2 cm < Tümör ≤ 5 cm |
| T3 | Tümör> 5 cm |
| T4 | T4a’dan T4d’ye kadar tarif edildiği gibi göğüs duvarına veya cilde doğrudan genişleyen herhangi bir boyuttaki tümör T4a – göğüs duvarı T4b – cilt ülseri ve ödem T4c – 4a ve 4b kombinasyonu T4d – Enflamatuar meme kanseri (özel form) |
| TX | Primer tümör değerlendirilemez |
Lenf düğümleri
| N-Kategori | Anlamı |
|---|---|
| N0 | Bölgesel lenf nodu metastazı yok |
| N1 | Seviye I ve II’nin hareketli ipsilateral aksiller lenf nodlarında metastaz (lar) |
| N2 | Seviye I ve II düzeyindeki hareketli ipsilateral aksiller lenf nodlarında, kendi aralarında veya diğer yapılarda veya klinik olarak tanınabilir aksiller lenf nodlarının yokluğunda dahili arter boyunca ipsilateral lenf nodlarında metastaz (lar) klinik olarak tanınabilir N2a – Aksiller lenf nodu tutulumu, taşınmaz N2b – İnternal torasik arterde lenf nodu tutulumu |
| N3 | Ipsilateral infraklaviküler lenf nodlarında (seviye III) seviye I ve II’nin aksiller lenf nodları ile veya klinik olarak tanınabilir aksiller lenf nodu metastazları ve metastazları veya metastaz varlığında klinik olarak tanınabilir ipsilateral lenf nodlarında (seviye III) metastaz (lar) ) iç meme arteri boyunca aksiller lenf nodları veya lenf nodlarının tutulumu olan veya olmayan ipsilateral supraklaviküler lenf nodlarında |
| NX | Bölgesel lenf düğümleri değerlendirilemez |
Uzak metastazlar
| M-Kategori | Anlamı |
|---|---|
| M0 | Uzak metastaz yok |
| M1 | Uzak metastaz var |
Tümör büyümesi, etkilenen memede karakteristik değişikliklere yol açar ve bu da muayeneyi duyarlı hale getirmelidir. Ele gelen, sınırları belli olmayan göğüs yumrusu, meme kanserinin en iyi bilinen işaretidir. İyi huylu değişikliklerin (fibroadenom, kistler) aksine, meme karsinomlarının destekle birlikte büyüme eğilimi vardır, böylece nodül taşınmaz olarak sabit gibi görünür.
Retromamiller formlar, meme ucunun geri çekilmesi ve cildin etkilenen bölge üzerinde geri çekilmesi ile sonuçlanır. Meme başı çevresinde dairesel bir karık adı verilen ve tümör bölgesinin üzerindeki cildin portakal kabuğu benzeri bir dokusu da düzenli olarak gözlenir. Enflamatuar meme kanseri olarak adlandırılan özel bir meme kanseri formunu mastitten tamamen morfolojik olarak ayırt etmek zordur.
Meme kanserinin ileri evreleri cilt ülseri oluşumuna yol açar. Böyle bir durumda, ülserli bir meme kanserinden bahsedilir.
Meme kanserinden şüpheleniliyorsa, ayırıcı tanı için bir grup iyi huylu hastalık kullanılabilir:
- Meme iltihabı
- Memenin fibroadenomu
- Mastopatileri
- Süt kanalı papilloma
Meme kanserinin patolojik tanısı
- Biyopsi ile teşhis edilen meme kanseri durumunda biyopsi materyali üzerinde aşağıdaki patolojik parametreler belirlenir:
- Invaziv veya in situ meme kanseri olup olmadığı
- Invaziv karsinomlar: histolojik tip (WHO’ya göre); En yaygın alt tipleri invaziv (duktal) karsinom NST (özel tip yok) ve invaziv lobüler meme kanseridir.
- Derecelendirme: farklılaşma derecesi; In situ ve invaziv tümör parçaları için ayrı ayrı İmmünohistokimya kullanılarak tedavi önerisi için
- Prognostik ve prediktif belirteçler: Östrojen reseptörü (ER), progesteron reseptörü (PR), HER2, proliferasyon belirteci Ki67
- Hâlihazırda geçerli olan kılavuzlara göre HER2 pozitif ve üçlü negatif (ER-, PR-, HER2-) meme kanserleri ameliyattan önce kemoterapi ile tedavi edilmelidir. Bu nedenle tanı koyarken yukarıdaki faktörlerin belirlenmesi önemlidir. Meme kanseri tanısı biyopsi ile doğrulandıktan sonra optimal cerrahi tedavi belirlenebilir. İnvaziv meme kanseri durumunda, bu sadece tümör dokusunun tamamen çıkarılmasını değil, aynı zamanda tümörün drenaj alanındaki ilk aksiller lenf düğümü olan sentinel lenf düğümünün cerrahi olarak çıkarılmasını da içerir. Tümör dokusunun rezeksiyon sınırları ve sentinel lenf nodunun herhangi bir tümör tutulumu intraoperatif olarak donmuş kesit incelemesi ile belirlenebilir. Geçmişte, sentinel lenf nodu enfekte olduğunda ek bir aksiller lenf nodu diseksiyonu yapılırdı. Mevcut çalışmalar, 1-3 sentinel lenf nodu enfekte ise, ilave aksiller lenf nodlarının çıkarılmasının hayatta kalmada herhangi bir iyileşmeye yol açmadığını göstermektedir.
Tedavi
Terapötik yaklaşım öncelikle tümör evrelemesi ve derecelendirmesinden oluşur, böylece tümör genomiklerinin sonuçları giderek daha fazla dahil edilir.
Cerrahi tedavi
Meme kanseri, bulgulara bağlı olarak, etkilenen memenin bakımı veya amputasyonu veya ablasyonuyla cerrahi olarak tedavi edilir. Genellikle bölgesel lenf düğümlerinin (aksiller lenf nodu diseksiyonu) çıkarılması eşlik eder. Cerrahi teknikler:
| Çeyrek rezeksiyon (Veronesi’ye göre) | Tis, T1 veya 2.5-3 cm çapında tümörler için 2 cm güvenlik mesafeli tümör çıkarma Sentinel lenf nodunun çıkarılması |
| Sınırlı radikal mastektomi | 3 cm’lik tümörler için, meme ucunun istilası, çok merkezli tümörler veya cilt infiltrasyonları için |
Bulgulara bağlı olarak operasyondan sonra polikemoterapi, hormon ve ışın tedavisi uygulanmaktadır.
| Tahlil | Tedavi |
|---|---|
| LN negatif ve negatif hormon reseptörleri | Poli kemoterapi |
| LN negatif ve hormon reseptörü pozitif | Hormon tedavisi |
| LN pozitif ve hormon reseptörü pozitif | Polikemoterapi ve hormon tedavisi (sadece orta riskli meme kanseri ile) |
| LN pozitif ve hormon reseptörü negatif | Polikemoterapi |
| Metastatik veya palyatif | Ameliyatsız polikemoterapi (hormona bağımlı tümörler için endokrin tedavisi) |
Sistemik Terapi:
Anti-Hormonal Terapi: Rekürrens riskini azaltmak için hormon reseptörü pozitif tümörler için önerilir. Seçenekler arasında seçici östrojen reseptör modülatörleri (SERM’ler), aromataz inhibitörleri ve yumurtalık baskılama yer alır.
Ameliyat Sonrası Sistemik Tedavi: Tümörün özelliklerine bağlı olarak, sistemik tedavi kemoterapi, endokrin tedavisi ve immünoterapiyi içerebilir.
- Neoadjuvan Sistemik Terapi: Hormon reseptörü pozitif, HER2-negatif meme kanseri için neoadjuvan tedavi tipik olarak ameliyattan önce tümörü küçültmek için endokrin (anti-hormonal) tedaviyi içerir. Tümör boyutu, derecesi ve diğer risk faktörlerine bağlı olarak kemoterapi de düşünülebilir.
- Üçlü-Negatif Meme Kanseri: Bu alt tipte östrojen reseptörleri, progesteron reseptörleri ve HER2 ekspresyonu yoktur ve agresif doğası nedeniyle tipik olarak neoadjuvan kemoterapi gerektirir.
Kemoterapi
Kemoterapi genellikle 5-florourasil + epirubisin veya Adriamisin + siklofosfamid kombinasyonu ile 6 döngüden oluşur. Hormon reseptörü negatif tümörleri için, 5-FU yerine paklitaksel veya dosetaksel kullanılır. HER2 / neu aşırı ekspresyonu durumunda, hastalara ayrıca 1 yıl boyunca trastuzumab verilir. Metastazlar için bevacizumab (VEGF bloker) ve paklitakselin bir kombinasyonu da kullanılır.
Kemoterapiye karar vermeden önce, erken ve hormon reseptörü pozitif meme kanseri olan hastalarda tanısal bir genetik test (örn. Oncotype DX) yapılmalıdır. Genetik test, doku örneklerinde 20’den fazla onkogen belirler ve hangi hastaların adjuvan kemoterapiyi faydalı veya gerekli hale getirdiğini ve hangilerinin yapmadığını ayırt etmeye yardımcı olur.
Ek hormon terapisi
- Tamoksifen (östrojen kısmi etkisi olan anti-östrojen): LN pozitif, hormon reseptör durumu olan postmenopozal kadınlar için tercih edilen ajan
- Toremifen: tamoksifen gibi, endometriyum üzerinde daha az yan etki
- Anastrozol / Letrozol: testosteronun östradiole dönüşümünü engelleyen aromataz inhibitörleri. Bazen tamoksifen’den daha etkilidirler ve daha az yan etki üretir (osteoporoz ve artralji dışında)
- Goserelin (GnRH analogu): Hipofiz bezinde uyarıcı fonksiyon. Sürekli azalmış gonadotropin salınımı (LH ve FSH) ile aşırı stimülasyona ve böylece fonksiyonel bir ovariektomi – premenopozal kadınlarda kullanım
- Fulvestrant (östrojen reseptörü aşağı regülasyonu): diğer ilaçlar başarısız olursa ve metastaz oluşursa bir seçenek olarak
Cilt Metastazı Yönetimi:
- Aksillada Kırmızı Noktalar: Aksiller bölgede kırmızı veya mor nodüller veya plaklar şeklinde ortaya çıkabilen cilt metastazının göstergesidir.
- Tedavi: Metastazın boyutuna bağlı olarak lokal tedavileri (radyasyon veya cerrahi) ve sistemik tedavileri (kemoterapi, hedefe yönelik tedavi veya immünoterapi) içerir.
Cerrahi Sonrası Yönetim:
- Ablasyon Sonrası Protokol: Mastektomi veya meme koruyucu cerrahiden sonra, tam iyileşmeye izin vermek ve hemen nüks olmamasını sağlamak için rekonstrüksiyon genellikle en az 6 ay ertelenir.
- Onkoplastik Meme Cerrahisi: Grisotti flebi gibi teknikler meme başı-areola kompleksinin korunmasına yardımcı olur ve yerel dokuyu yeniden düzenleyerek daha iyi kozmetik sonuçlar elde eder.
- Tümör Kurulu Değerlendirmesi: Multidisipliner bir ekip, ameliyat sonrası sistemik tedavi (bağışıklık tedavisi veya kemoterapi) ihtiyacı da dahil olmak üzere en iyi tedavi sürecini belirlemek için vakayı değerlendirir.
Profilaksi
Her kadın ayda bir kez göğsünü kendisi için kontrol etmelidir. Optimal zaman menstrüasyondan kısa bir süre sonradır. 30 yaşından itibaren, doktor tarafından yıllık dokunsal muayene yapılmalıdır.
Bir kerelik mamografi, ‘temel mamografi’ olarak adlandırılan, daha sonraki görüntüler için karşılaştırmalı bir görüntü görevi gören 35 ve 40 yaşları arasında önerilir. 50 ila 69 yaşları arasında, mamografi her 2 yılda bir yapılmalıdır. Yüksek riskli hastalar için yıllık olarak önerilir.
Primer tümörün tedavisinden sonraki ilk 3 yıl içinde üç ayda bir kontrol
Her 6 ayda bir 4. yıl postoperatif kontrollerden
6. yıldan itibaren yıllık kontroller
Tarih
Antik Mısır (MÖ 3000-1500):
En Eski Kayıtlar: Eski bir Mısır tıbbi metni olan Edwin Smith Papirüsü, meme kanserinin bilinen en eski tanımını içermekte ve tedavisi olmadığını belirtmektedir.
Antik Yunan (MÖ 460-370):
Hipokrat: Meme kanserini aşırı kara safranın neden olduğu sistemik bir hastalık olarak tanımlamıştır (humoral teori).
MS 2. Yüzyıl:
Galen: Meme kanserinin vücut sıvılarının dengesizliğinden kaynaklandığına inanmış ve yalnızca tümör küçükse ve ülserleşmemişse ameliyat önermiştir.
19. Yüzyıl
Cerrahideki Gelişmeler: Memenin, altta yatan göğüs kasının ve lenf düğümlerinin alınmasını içeren radikal mastektomi, 1800’lerin sonlarında William Halsted tarafından popüler hale getirildi.
Anestezinin Kullanılmaya Başlanması (1846): Daha karmaşık ve kapsamlı cerrahi prosedürlere izin verdi.
1895, Wilhelm Roentgen tarafından X-ışınlarının keşfi: Tıbbi görüntülemede devrim yarattı ve meme tümörlerinin erken teşhis edilmesini sağladı.
20. Yüzyılın Başları
1920’ler-1930’lar:
Radyoterapi: Başlangıçta cerrahiye ek olarak meme kanseri tedavisi için kullanılmaya başlandı.
Mamografi: İlk olarak 1930’larda tanıtıldı, ancak 1970’lere kadar yaygın olarak kullanılmadı.
1940’lar:
Kemoterapi Gelişimi: Başlangıçta savaş için geliştirilen azot hardalları, modern kemoterapinin başlangıcını işaret ederek kanser tedavisi için yeniden tasarlandı.
1950’ler-1960’lar:
Hormonal Terapi: Hormon reseptörü pozitif meme kanserini tedavi etmek için ooferektomi ve tamoksifen gibi anti-östrojen ilaçların kullanımı gibi hormon tedavisinin tanıtılması.
1970’lar:
Meme Koruyucu Cerrahi (Lumpektomi): Radikal mastektomiye alternatif olarak ortaya çıktı ve genellikle radyasyon tedavisi ile birleştirildi.
Tarama Mamografisi: Meme kanserinin daha erken tespit edilmesine yol açarak daha yaygın bir şekilde benimsendi.
1980’lar:
Monoklonal Antikorlar: Kanser tedavisi için monoklonal antikorların geliştirilmesi, 1998 yılında HER2-pozitif meme kanseri için trastuzumabın (Herceptin) onaylanmasına yol açtı.
Onkogenler ve Tümör Baskılayıcılar: BRCA1 ve BRCA2 gibi meme kanserinde rol oynayan anahtar genlerin tanımlanması.
1990’lar:
- Genetik Testler: BRCA mutasyonları için genetik testler kullanıma sunuldu ve kişiselleştirilmiş risk değerlendirmesi ve yönetimine olanak sağladı.
- Adjuvan Tedavi: Ameliyat sonrası nüks riskini azaltmak için adjuvan kemoterapi ve hormonal terapi kullanımının artması.
21. Yüzyıl
2000’ler:
- Hedefe Yönelik Tedaviler: Aromataz inhibitörleri ve lapatinib gibi yeni HER2-hedefli ilaçlar gibi hedefe yönelik tedavilerin tanıtımı.
- Genomik Profilleme: Genomik profillemedeki gelişmeler, tümörün moleküler özelliklerine dayalı olarak daha kişiselleştirilmiş tedavi planlarına olanak tanır.
2010’lar:
- İmmünoterapi: Meme kanserinin belirli alt tiplerinin tedavisi için kontrol noktası inhibitörleri de dahil olmak üzere immünoterapinin ortaya çıkışı.
- PARP İnhibitörleri: BRCA mutasyonlu meme kanseri için PARP inhibitörlerinin onaylanması ve bu yüksek riskli grup için yeni bir tedavi seçeneği sunulması.
2020’ler:
- Sıvı Biyopsiler: Kandaki kanser DNA’sını tespit etmek için sıvı biyopsilerin geliştirilmesi, kanser ilerlemesinin ve tedavi yanıtının invazif olmayan bir şekilde izlenmesine olanak sağlar.
- Görüntülemede Gelişmeler: 3D mamografi (tomosentez) gibi gelişmiş görüntüleme teknikleri, meme kanseri taraması ve teşhisinin doğruluğunu artırır.
- Kişiselleştirilmiş Tıp: Tedavileri bireysel hastalara göre uyarlamak için kapsamlı genomik ve proteomik verileri kullanarak kişiselleştirilmiş tıbba odaklanmaya devam edilmesi.
İleri Okuma
- National Comprehensive Cancer Network (NCCN). “Clinical Practice Guidelines in Oncology: Breast Cancer.”
- Saslow, D., et al. (2007). “American Cancer Society Guidelines for Breast Screening with MRI as an Adjunct to Mammography.” CA: A Cancer Journal for Clinicians, 57(2), 75-89.
- Jung, S. Y., et al. (2010). “The Ki-67 Labeling Index is a Significant Prognostic Factor in Triple-Negative Breast Cancer.” Oncology, 79(3-4), 312-319.
- Schnitt, S. J. (2010). “Classification and Prognosis of Invasive Breast Cancer: From Morphology to Molecular Taxonomy.” Modern Pathology, 23(S2), S60-S64.
- American Cancer Society. “Breast Cancer Facts & Figures 2020-2021.”
- Burstein, H. J., et al. (2016). “Adjuvant Endocrine Therapy for Women With Hormone Receptor-Positive Breast Cancer: ASCO Clinical Practice Guideline Focused Update.” Journal of Clinical Oncology, 34(33), 3881-3885.
- Denton, E., & Maddox, P. (2017). “3D Printing in the Service of Medicine.” Medical Image Analysis, 39, 92-102.