Etimolojik ve Terminolojik Çerçeve
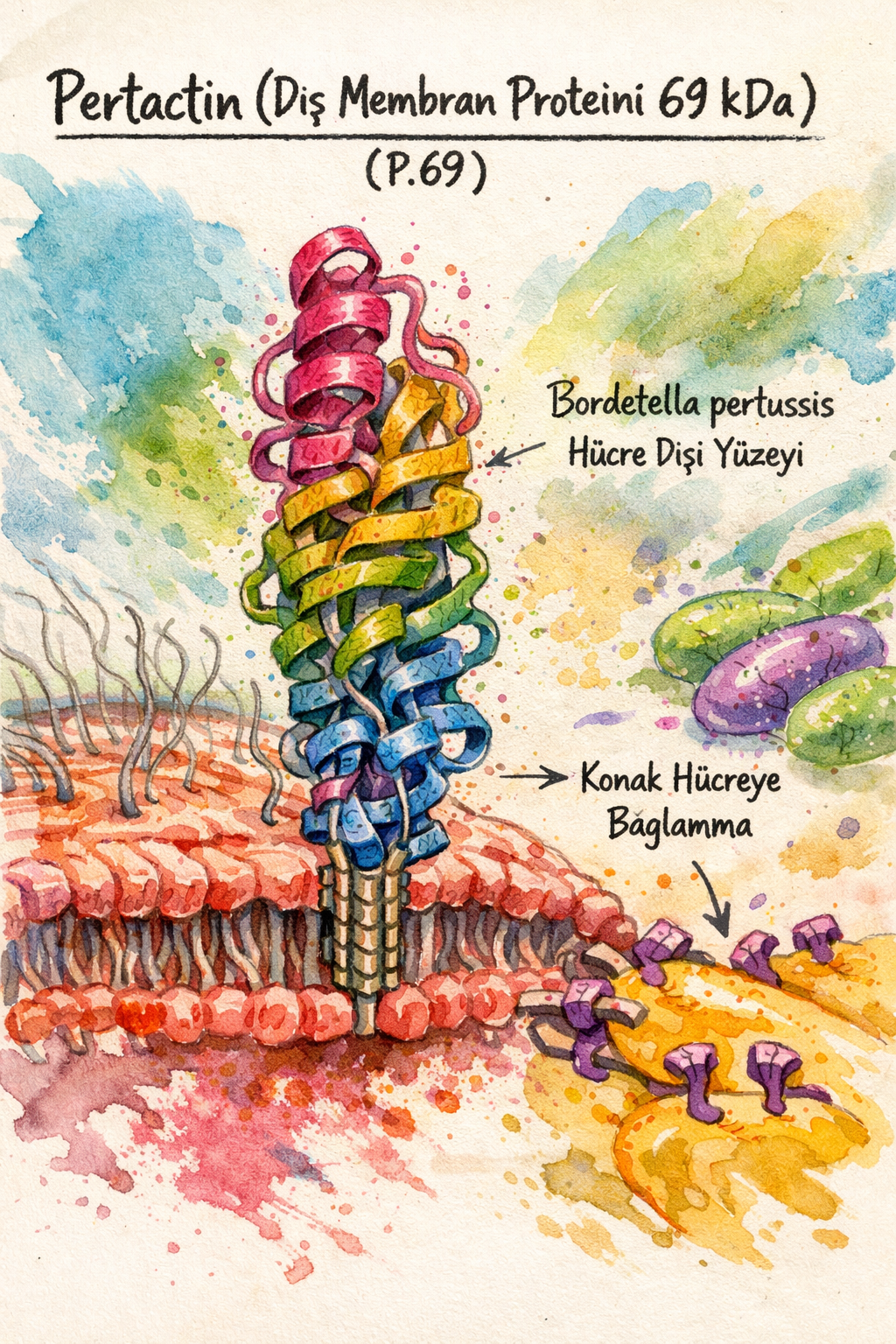
“Pertaktin” terimi, etimolojik olarak etken maddenin ilişkili olduğu hastalık olan pertussis (Latince: per-, “şiddetli” ve tussis, “öksürük”) ile İngilizce “attachment” (tutunma) sözcüklerinin birleşiminden türetilmiştir. Molekül, bilimsel literatürde aynı zamanda “P.69” veya “dış membran proteini 69 kDa” (P.69) olarak da anılmakta olup, Bordetella pertussis’in hücre dışı yüzeyinde konumlanan ve patogenezin ilk basamağı olan kolonizasyonda kritik rol oynayan bir adhezindir.
Evrimsel Biyoloji ve Mikrobiyal Patogenezdeki Yeri
Evrimsel bakıldığında, Bordetella pertussis, insan konakçısına mükemmel düzeyde adapte olmuş bir patojendir. Pertaktin, bu adaptasyonun moleküler vitrini niteliğindedir. Mikroorganizmanın genetik arka planı incelendiğinde, pertaktin genini (prn) kodlayan bölgenin, aşılama programlarının yoğun baskısı altında yüksek oranda seçilime maruz kaldığı görülmektedir. Bu durum, patojenin konak immün sistemi ve tıbbi müdahaleler karşısında gösterdiği dinamik evrimsel yanıtın en somut örneklerinden birini teşkil eder. Özellikle aselüler aşıların (asetüler boğmaca aşıları) yaygın kullanımıyla birlikte, pertaktin eksprese etmeyen (Prn-negatif) suşların popülasyonlarda hâkim hale gelmesi, mikrobiyal evrimin “aşı baskısı” karşısında ne denli hızlı bir adaptasyon sergileyebileceğini gözler önüne sermektedir.
Moleküler Yapı ve Biyolojik Fonksiyon
Pertaktin, Bordetella pertussis’in dış zarında lokalize olan, ototransporter sistemine ait bir protein yapısındadır. Yaklaşık 69 kilodaltonluk moleküler ağırlığı, arginin-glisin-aspartik asit (RGD) motifi içeren yapısal bölgesi sayesinde hücre adezyonunda görev alır. Molekül, bakterinin hücre yüzeyinden dışarıya doğru uzanarak, konak epitel hücrelerinin yüzeyinde bulunan integrin benzeri reseptörlerle etkileşime girer.
Bu etkileşim, patojenin solunum epitelinde, özellikle trakea (soluk borusu) mukozasında kalıcı kolonizasyonunu sağlayan ilk mekanik adımdır. Pertaktin, tek başına hareket etmekle kalmaz; filamentöz hemaglutinin (FHA) ve trakeal kolonizasyon faktörü (Tcf) gibi diğer adezinlerle sinerjik bir ağ oluşturarak bakterinin konak dokuya çok noktalı ve sağlam bir şekilde tutunmasına olanak tanır. Bu çoklu adezyon mekanizması, mukosilier klirens gibi konak savunma mekanizmalarının bakteriyi elimine etmesini engelleyen kritik bir evrimsel kazanımdır.
Güncel Bilimsel Anlayış: İmmünojenisite ve Varyasyon
Pertaktin, yüksek immünojenik kapasitesi nedeniyle aselüler boğmaca aşılarının temel bileşenlerinden biri olarak kullanılagelmiştir. Bu protein, doğal enfeksiyon sırasında da güçlü bir humoral immün yanıtı tetikler; bireyde oluşan anti-pertaktin antikorları, bakterinin solunum epiteline tutunmasını bloke ederek nötralizasyon sağlar.
Ancak güncel bilimsel anlayış, bu etkileşimin karmaşık bir silahlanma yarışına dönüştüğünü ortaya koymaktadır. Son yirmi yılda, özellikle yüksek aşılama oranlarına sahip ülkelerde, Bordetella pertussis popülasyonlarında pertaktin ekspresyonunun kaybına yönelik belirgin bir evrimsel eğilim gözlemlenmiştir. Prn-negatif suşlar olarak adlandırılan bu varyantlar, aşı kaynaklı immün seçilim baskısı altında ortaya çıkmış ve birçok coğrafyada endemik suşlar haline gelmiştir. Bu olgu, klasik anlamda “aşıdan kaçış” (vaccine escape) mekanizmasından farklı olarak, patojenin virülans faktörlerini düzenleyerek aşının etkinliğini azaltma stratejisi olarak yorumlanmaktadır. Pertaktin kaybına rağmen bakterinin kolonizasyon yeteneğini sürdürebilmesi, diğer adezinlerin (özellikle FHA) devreye girmesiyle açıklanmakta olup, bu durum B. pertussis’in genetik redündan sistemi ve metabolik esnekliği hakkında yeni araştırma alanları açmıştır.
Klinik Uygulamalar ve Farmakolojik Boyut
Klinik pratikte pertaktin, hem tanısal hem de aşı temelli stratejilerde merkezi bir öneme sahiptir. Tanısal açıdan, pertaktin gen bölgesine özgü polimeraz zincir reaksiyonu (PZR) yöntemleri, günümüzde boğmaca tanısında altın standart moleküler testlerin hedef bölgelerinden birini oluşturur. Pertaktin varyasyonlarının moleküler epidemiyolojik izlenmesi, dolaşımdaki suş tiplerinin belirlenmesi ve aşı uyumsuzluğunun takibi açısından kritik bir sürveyans aracıdır.
Farmakolojik ve immünolojik boyutta ise pertaktinin durumu, modern aşı biliminde önemli bir paradigma değişimini tetiklemiştir. Aselüler aşıların yaygın kullanımına rağmen son yıllarda boğmaca vakalarında görülen artış (resurgans), pertaktin içeren mevcut aşıların sınırlılıklarını gündeme taşımıştır. Bu durum, aşı formülasyonlarının yeniden değerlendirilmesine yol açmıştır. Bilim camiası, güncel yaklaşım olarak yalnızca antijenik bileşenlerin (pertaktin, toksin, FHA gibi) sayısını artırmaya değil, aynı zamanda canlı atenüe aşılar veya bütün hücre aşılarının geliştirilmiş versiyonları gibi, patojenin evrimsel esnekliğine karşı daha geniş ve çeşitli bir immün yanıt oluşturacak stratejilere yönelmektedir.
Bütüncül Değerlendirme ve Sonuç
Pertaktin, Bordetella pertussis’in patogenezinde bir adezin olarak başlayan biyolojik rolünün çok ötesinde, konak-patojen etkileşimlerinin evrimsel dinamiklerini ve modern tıbbın karşılaştığı zorlukları anlamak için bir model sistem niteliği taşımaktadır. Bu molekül, bir yandan etkili immünojenik yapısıyla aşı geliştirme için ideal bir hedef sunarken, diğer yandan aşı baskısı altında ekspresyonunu kaybederek klinik epidemiyolojide beklenmedik bir kırılma yaratmıştır.
Akademik perspektiften bakıldığında, pertaktin üzerine yapılan çalışmalar, moleküler mikrobiyoloji, immünoloji, evrimsel biyoloji ve halk sağlığı disiplinlerinin kesişim noktasında bulunmaktadır. Güncel bilimsel anlayış, tek bir virülans faktörüne odaklanan müdahalelerin, mikrobiyal adaptasyon karşısında sürdürülebilirliğinin sınırlı olabileceğini; başarılı kontrol stratejilerinin, patojenin biyolojik esnekliğini gözeten çok bileşenli ve bütüncül yaklaşımları gerektirdiğini ortaya koymaktadır. Pertaktinin keşfinden günümüze uzanan süreç, enfeksiyon hastalıklarıyla mücadelede statik bir hedef belirlemenin ötesine geçerek, patojenin evrimsel yörüngesini sürekli izleyen dinamik bir strateji geliştirmenin zorunluluğunu vurgulamaktadır.
Keşif
Erken Dönem: Mikroskobun Altındaki Düşman
1900 yılının hemen öncesinde, Belçikalı bakteriyolog Jules Bordet, Fransa’nın Pasteur Enstitüsü’nde çalışırken difteri ve boğmaca gibi hastalıkların mikrobiyal temelini aydınlatmaya girişti. 1906 yılında, eşi Octave Gengou ile birlikte, bugün Bordetella pertussis olarak bildiğimiz bakteriyi ilk kez saf kültürde izole etmeyi başardılar. Bu, yalnızca bir mikroorganizmanın keşfi değil, aynı zamanda bir patojenite mekanizmaları çağının da habercisiydi. Ancak o dönemde dikkatler, bakterinin bir toksin ürettiği ve bu toksinin hastalığın sistemik etkilerinden sorumlu olduğu yönündeydi. Bakterinin solunum yolu epiteline nasıl tutunduğu sorusu, henüz sorulmamıştı bile.
1930’larda ve 1940’larda, bütün hücre boğmaca aşılarının geliştirilmesiyle birlikte bilim insanları, bakterinin hücre yüzeyinin immünolojik olarak ne denli karmaşık olduğunu fark etmeye başladılar. Aşılar, hastalığı kontrol altına almakta büyük başarı sağlıyordu, ancak içerdikleri yüzlerce antijenik bileşenin hangilerinin gerçekten koruyuculukta anahtar rol oynadığı karanlıkta kalıyordu. Bu belirsizlik, bir sonraki kuşağın bilim insanlarını daha hassas bir arayışa yönlendirecekti.
1970’ler: Yüzeyde Bir İpucu
Moleküler biyolojinin altın çağına adım atılan 1970’lerde, araştırmacılar Bordetella pertussis’in dış zarını sistematik olarak taramaya başladılar. Elektroforez tekniklerindeki ilerlemeler sayesinde, bakteri hücresinin dış yüzeyinde farklı moleküler ağırlıklarda protein kümeleri tanımlandı. Bu dönemde, P.68 veya P.69 gibi geçici adlarla anılan, yaklaşık 69 kilodalton büyüklüğünde bir dış membran proteininin dikkat çekici ölçüde immünojenik olduğu gözlemlendi. Ancak bu proteinin ne işe yaradığı henüz bilinmiyordu; yalnızca doğal enfeksiyon geçiren bireylerin serumlarında bu proteine karşı güçlü antikor yanıtları geliştiği fark edilmişti.
Bu gözlem, bilimsel merakın bir sonraki adımını ateşledi: Eğer bu protein enfeksiyon sırasında güçlü bir hedefse, patogenezde de bir işlevi olmalıydı.
1980’ler: Bir Protein Kimliğine Kavuşuyor
1980’lerin başında, Alison Weiss ve Charles Weiss öncülüğündeki araştırma grupları, Bordetella pertussis’in virülans genlerini klonlamaya giriştiler. Bu dönemde, pertaktinin genini (prn) kodlayan bölge başarıyla izole edildi ve genetik düzeyde analiz edildi. 1983 yılında yapılan bu klonlama çalışmaları, proteinin yapısına dair ilk moleküler ipuçlarını sundu. Ancak asıl sıçrama, İtalyan bilim insanı Rino Rappuoli ve ekibinin bu proteinin dizisinde bir arginin-glisin-aspartik asit (RGD) motifi keşfetmesiyle geldi. RGD motifi, o dönemde hücre adezyonuyla ilişkili proteinlerde bilinen kritik bir yapıydı; hücrelerin integrin reseptörlerine tutunmasını sağlayan anahtar bir diziydi.
Bu keşif, proteinin biyolojik rolünün anlaşılmasında bir dönüm noktası oldu. Bilim insanları artık şu soruyu sorabiliyordu: Bordetella pertussis, bu motif aracılığıyla doğrudan konak epitel hücrelerine mi tutunuyordu? Kısa süre içinde, yapılan adezyon inhibisyon deneyleri bu hipotezi doğruladı. Anti-P.69 antikorları, bakterinin soluk borusu epitel hücrelerine tutunmasını engelliyordu. Proteinin adı, artık bu işlevine atıfla “pertaktin” (pertussis + attachment) olarak değiştirildi. Artık biliniyordu: pertaktin, patojenin kolonizasyondaki ilk elçisiydi.
1990’lar: Aşıların Kalbine Yolculuk
Pertaktinin yüksek immünojenik kapasitesi ve patogenezdeki merkezi rolü, onu aselüler boğmaca aşılarının vazgeçilmez bir bileşeni haline getirdi. 1980’lerin sonunda Japonya’da başlayan aselüler aşı denemeleri, pertaktin, filamentöz hemaglutinin (FHA) ve toksin gibi saflaştırılmış antijenleri içeriyordu. Bu aşılar, bütün hücre aşılarının neden olduğu lokal ve sistemik reaktijeniteyi azaltırken, koruyucu immün yanıtı hedefe yönlendiriyordu.
1990’lı yılların ortalarında, ABD ve Avrupa’da yapılan büyük ölçekli klinik çalışmalar, pertaktin içeren aselüler aşıların etkinliğini onayladı. 1996 yılında ABD’de ilk aselüler aşı lisanslandığında, pertaktin artık modern aşı biliminin en parlak bileşenlerinden biri olarak kabul ediliyordu. Bu dönemde, aşıların içerdiği pertaktin miktarının standardizasyonu, biyolojik ve immünolojik açıdan titizlikle yürütülen bir süreçti. Her şey yolunda görünüyordu; patojenin en önemli adezinlerinden birine karşı kazanılmış bir immün zafer söz konusuydu.
2000’ler: Sessiz Gelen Evrimsel Cevap
Ancak biyoloji, statik bir hedefi asla affetmez. 2000’li yılların başında, özellikle yüksek aşılama oranlarına sahip ülkelerde, Bordetella pertussis suşları arasında beklenmedik bir değişim gözlemlenmeye başlandı. Fransa, Japonya, Avustralya ve ABD gibi ülkelerde yapılan moleküler epidemiyoloji çalışmaları, pertaktin genini (prn) fonksiyonel olarak eksprese etmeyen suşların (prn-negatif) giderek yaygınlaştığını ortaya koydu. 2008 yılında ABD’de yapılan bir sürveyans çalışmasında, dolaşımdaki suşların neredeyse yarısının pertaktin üretmediği görüldüğünde, bilim camiasında bir şok dalgası yayıldı.
Bu, klasik anlamda bir antibiyotik direnci değildi; bu, bir patojenin aşı baskısı altında virülans faktörlerini silah olarak kullanmayı bırakarak hayatta kalma stratejisiydi. Araştırmacılar, bu değişimin genetik mekanizmasını çözmek için kolları sıvadılar. İnsan genom projesinin ardından gelen yeni nesil dizileme teknolojileri sayesinde, prn-negatif suşlarda genin okuma çerçevesinde kaymalar, delesyonlar veya promotör bölgelerinde mutasyonlar olduğu keşfedildi. Bu bulgu, mikrobiyal evrimin hızı ve modern tıbbın uyguladığı seçilim baskısının yönlendirici gücü hakkında çarpıcı bir ders niteliğindeydi.
2010’lar ve Günümüz: Genomik Çağda Pertaktin
2010’lardan itibaren pertaktin, yalnızca bir adezin olmanın ötesinde, konak-patojen evrimsel silahlanma yarışının model bir sistemi haline geldi. Küresel sürveyans ağları, pertaktin varyantlarının coğrafi dağılımını gerçek zamanlı olarak izlemeye başladı. Genomik epidemiyoloji, prn-negatif suşların aslında bağımsız evrimsel olaylar sonucu farklı coğrafyalarda birden fazla kez ortaya çıktığını gösterdi. Bu, doğal seçilimin aynı moleküler hedefe yönelik aynı çözümü bağımsız olarak keşfetmesinin çarpıcı bir örneğiydi.
Aynı dönemde, bilim insanları pertaktin kaybının bakterinin virülansında ne gibi değişikliklere yol açtığını anlamaya çalıştı. İlginçtir ki, hayvan modellerinde prn-negatif suşlar, kolonizasyon yeteneklerini büyük ölçüde koruyor; hatta bazı çalışmalarda, bu suşların daha uzun süre kolonize olduğu gözleniyordu. Bu durum, Bordetella pertussis’in yedekli adezin sistemlerine sahip olduğunu (özellikle FHA gibi) ve bu sayede pertaktin kaybını kompanse edebildiğini ortaya koydu. Bu keşif, aşı tasarımı felsefesinde bir paradigma değişimine yol açtı: artık tek bir antijene odaklanmak yerine, patojenin evrimsel esnekliğini kıracak çok bileşenli veya tüm genomu hedef alan stratejiler ön plana çıktı.
Günümüzdeki Ufuklar: Dersler ve Yeni Yönelimler
Bugün pertaktin, hem bir başarı hem de bir uyarı hikâyesi olarak tıbbi literatürdeki yerini koruyor. Bir yandan, moleküler biyolojinin ve aşı biliminin bir antijeni keşfetmekten, onu saflaştırmaya, geniş popülasyonlarda uygulamaya kadar uzanan muazzam kapasitesini simgeliyor. Diğer yandan, patojenlerin statik hedefler olmadığını; evrimsel baskı altında şaşırtıcı hızla adapte olabildiklerini gösteren bir ders niteliği taşıyor.
Günümüzdeki en güncel araştırmalar, pertaktin deneyiminden çıkarılan derslerle şekilleniyor. Canlı atenüe aşı adayları (örneğin BPZE1 suşu) gibi, tüm virülans faktörlerini çok yönlü olarak hedef alan aşı stratejileri klinik denemelerde ilerliyor. Aynı zamanda, tersine aşı bilimi (reverse vaccinology) yaklaşımlarıyla, Bordetella pertussis’in genomu yeniden taranarak, pertaktin gibi tek bir moleküle bağımlı olmayan, daha geniş ve dayanıklı immün yanıtlar hedefleniyor.
Pertaktinin keşif süreci, bilimsel merakın bir molekülden yola çıkarak nasıl bütün bir patogenez anlayışını, aşı teknolojisini ve evrimsel biyolojiyi yeniden şekillendirebileceğinin en somut örneklerinden biridir. Bu yolculuk, 1906’da bir bakterinin saf kültürde izole edilmesiyle başlayıp, 21. yüzyılda genomik verilerin ışığında bir mikroorganizmanın hayatta kalma stratejilerini haritalandırmaya uzanan, bilimin doğasına içkin dinamik ilerlemenin canlı bir portresidir. Her yeni keşif, ardında yeni sorular bırakmış; her dönüm noktası, bir sonraki entelektüel atılımın zeminini hazırlamıştır. Pertaktin, artık yalnızca bir bakteri proteininin adı değil; modern tıbbın enfeksiyonlarla mücadelede öğrendiği en önemli derslerden birinin—patojenlerle savaşta sürekli öğrenen, uyum sağlayan ve evrilen bir yaklaşımın zorunluluğunun—simgesidir.
İleri Okuma
- Bordet J, Gengou O. Le microbe de la coqueluche. Annales de l’Institut Pasteur. 1906;20:731-741.
- Weiss AA, Hewlett EL, Myers GA, Falkow S. Tn5-induced mutations affecting virulence factors of Bordetella pertussis. Infection and Immunity. 1983;42(1):33-41.
- Emschermann C, et al. A 69-kilodalton outer membrane protein of Bordetella pertussis: isolation, characterization and role in adherence. Journal of General Microbiology. 1985;131(8):2029-2038.
- Charles IG, Dougan G, Pickard D, Chatfield S, Smith M, Novotny P, Morrissey P, Fairweather NF. Molecular cloning and characterization of protective outer membrane protein P.69 from Bordetella pertussis. Proceedings of the National Academy of Sciences USA. 1988;85(16):5879-5883.
- Rappuoli R. Pertussis toxin and pertactin: two proteins that play a role in the pathogenesis of whooping cough and are components of new vaccines. Research in Microbiology. 1990;141(7-8):799-803.
- Gustafsson L, Hallander HO, Olin P, Reizenstein E, Storsaeter J. A controlled trial of a two-component acellular, a five-component acellular, and a whole-cell pertussis vaccine. New England Journal of Medicine. 1996;334(6):349-355.
- Mooi FR, van Loo IH, King AJ. Adaptation of Bordetella pertussis to vaccination: a cause for its reemergence? Emerging Infectious Diseases. 2001;7(3 Suppl):526-528.
- Heikkinen E, Xing D, Olander RM, Hviid A, Viljanen MK, Mertsola J. Bordetella pertussis isolates in Finland: serotype and fimbrial expression. BMC Infectious Diseases. 2009;9:169.
- Bouchez V, Brun D, Cantinelli T, Dore G, Njamkepo E, Guiso N. First report of a Bordetella pertussis isolate not expressing pertactin in France. Journal of Clinical Microbiology. 2010;48(8):3045-3047.
- Pawloski LC, Queenan AM, Cassiday PK, Lynch AS, Harrison MJ, Shang W, et al. Prevalence and molecular characterization of pertactin-deficient Bordetella pertussis in the United States. Clinical and Vaccine Immunology. 2012;19(8):1195-1202.
- Lam C, Octavia S, Ricafort L, Sintchenko V, Gilbert GL, Wood N, McIntyre P, Marshall H, Guiso N, Keil AD, et al. Rapid increase in pertactin-deficient Bordetella pertussis isolates, Australia. Emerging Infectious Diseases. 2014;20(4):626-633.
- Safarchi A, Octavia S, Luu LD, Tay CY, Sintchenko V, Wood N, Marshall H, McIntyre P, Lan R. Pertactin negative Bordetella pertussis demonstrates higher fitness under vaccine selection pressure in a murine model. Clinical Microbiology and Infection. 2015;21(5):467.e1-7.
- Breakwell L, Kelso P, McIntyre P, Chiu C, Quinn HE. Pertactin-negative Bordetella pertussis in Australia: 2008–2012. Communicable Diseases Intelligence Quarterly Report. 2016;40(1):E20-24.
- Weigand MR, Peng Y, Loparev V, Batra D, Bowden KE, Burroughs M, Cassiday PK, Davis JK, Johnson T, Juieng P, et al. The history of Bordetella pertussis genome evolution includes structural rearrangement and extensive loss of genetic information. Microbial Genomics. 2019;5(10):e000311.
- Dewan KK, Linz B, DeRocco SE, Harvill ET. Acellular pertussis vaccine components: today and tomorrow. Infection and Immunity. 2021;89(9):e00108-21.
- Maugeri A, Basta NE, Guiso N. Pertactin-deficient Bordetella pertussis: a global perspective. Clinical Microbiology Reviews. 2023;36(2):e00141-22.