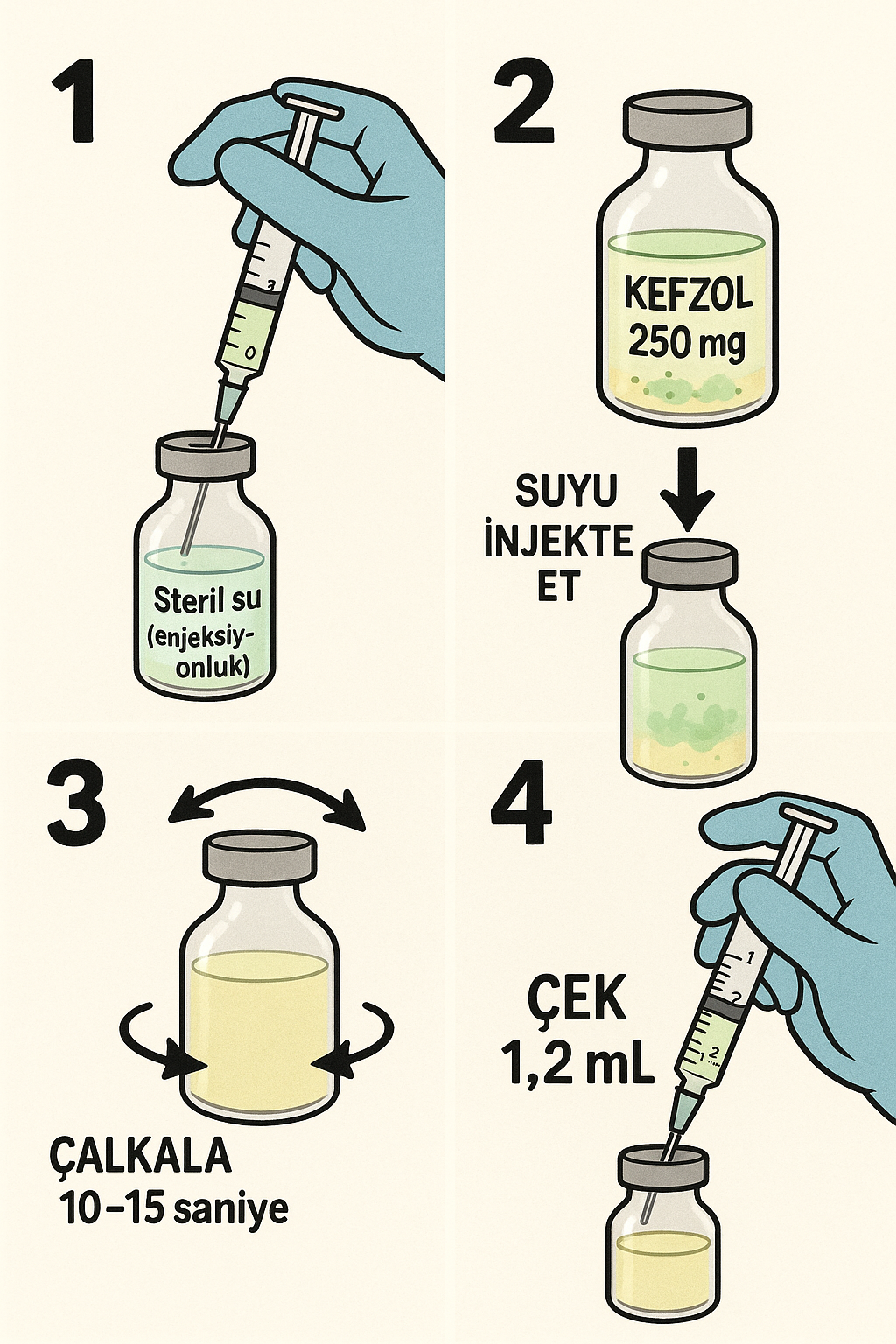
Latince kökenli reconstitute terimi, “re–” (yeniden, tekrar) ön eki ile “constitute” (oluşturmak, meydana getirmek) fiilinden türetilmiştir. Farmasötik bağlamda “reconstitution”, bir farmasötik formülasyonun, özellikle stabilite amacıyla kurutulmuş ya da liyofilize edilmiş bir ürünün, uygun bir çözücü eklenerek tekrar kullanıma hazır hale getirilmesi sürecini tanımlar. Bu işlem sonucunda ilaç, orijinal farmasötik formuna—çoğunlukla enjeksiyonluk çözelti, infüzyon çözeltisi ya da oral süspansiyon—geri döndürülmüş olur.
İçindekiler
1. Rekonstitüsyonun Amacı ve Uygulama Alanları
Rekonstitüsyon işlemi, özellikle aşağıdaki durumlarda farmasötik pratikte yaygın olarak uygulanmaktadır:
- Liyofilize (dondurularak kurutulmuş) tozların enjeksiyonluk çözeltilere dönüştürülmesi (örneğin bazı antibiyotikler, biyoteknolojik ürünler).
- Oral süspansiyonların (çoğunlukla pediatrik formülasyonlar) kullanılmadan önce sulandırılarak hazırlanması.
- Konsantre çözeltilerin (örneğin sitotoksik ilaçlar) seyreltilerek infüzyona uygun hale getirilmesi.
Rekonstitüsyon genellikle doğrudan flakon veya vial içinde gerçekleştirilir. Bu süreçte kullanılan çözücüler (örn. steril enjeksiyonluk su, izotonik sodyum klorür çözeltisi) ilaç monografisine uygun olarak seçilmelidir.
2. Hijyen ve Sterilite Koşulları
Rekonstitüsyon işlemi sırasında aseptik tekniklerin titizlikle uygulanması hayati önem taşır. Enjeksiyonluk veya infüzyonluk preparatlar söz konusu olduğunda, kontaminasyon riski taşıyan en ufak ihmal ciddi klinik sonuçlara yol açabilir. Bu nedenle işlem, steril koşullar altında ve tercihen laminar akış kabinlerinde gerçekleştirilmelidir.
3. Farmasötik ve Klinik Avantajlar
Liyofilize formülasyonların tercih edilmesinin başlıca avantajları şunlardır:
- Artırılmış raf ömrü: Sulu çözeltilere kıyasla stabiliteleri daha yüksektir.
- Depolama kolaylığı: Katı formlar hacim ve ağırlık açısından daha avantajlıdır.
- Kimyasal stabilite: Su içeriği azaltıldığından birçok aktif bileşik daha uzun süre bozulmadan saklanabilir.
4. Sulandırma Sonrası Stabilite ve Saklama Koşulları
Rekonstitüsyondan sonra elde edilen preparatlar genellikle sınırlı bir kullanım süresi ile karakterize edilir. Bu süre birkaç saatten birkaç güne kadar değişebilir ve üretici tarafından belirtilen stabilite verilerine bağlıdır. Çoğu preparat sulandırıldıktan sonra 2–8 °C aralığında buzdolabında saklanmalıdır. Ancak bazı preparatlar saklanmadan, yalnızca hemen kullanım için hazırlanmalıdır. Bu durumlar genellikle ürünün prospektüsünde açıkça belirtilmiştir.
5. Kullanım Öncesi Kontrol ve Kalite Güvencesi
Rekonstitüe edilmiş preparat, kullanımdan önce aşağıdaki parametreler açısından görsel olarak incelenmelidir:
- Renk değişikliği
- Bulanıklık veya opaklık
- Yabancı partikül varlığı
Herhangi bir fiziksel bozulma saptanması durumunda ürün kullanılmamalıdır. Ayrıca, özellikle süspansiyon formunda hazırlanan ürünler kullanımdan hemen önce hafifçe çalkalanmalı veya yavaşça ters çevrilerek karıştırılmalıdır. Bu işlem, partiküllerin eşit dağılımını ve dozaj doğruluğunu garanti altına alır.
Keşif
1. Antik ve Ortaçağ Tıbbı Dönemlerinde Ön Belirtiler
- Antik Yunan ve Roma tıbbında kurutulmuş bitki özlerinin kullanımından önce sıvı içerisinde çözündürülmesi sık görülen bir uygulamaydı (örneğin: Theriac gibi preparatlar).
- Bu, doğrudan rekonstitüsyon kavramına eşdeğer olmasa da, “formülasyonu son anda sıvılaştırma” fikrinin kökeni olarak düşünülebilir.
2. 19. Yüzyılda Parenteral İlaçların Ortaya Çıkışı
- İğne ve şırınganın geliştirilmesi (özellikle 1853’te Charles Gabriel Pravaz ve Alexander Wood tarafından) sonrası parenteral uygulamalar artmıştır.
- Ancak birçok etkin madde sulu çözeltide kimyasal olarak kararsız olduğundan, kullanım öncesi çözülecek toz formülleri geliştirilmeye başlanmıştır.
- Bu dönemde ilk defa enjeksiyonluk kuru maddeler, steril çözücülerle çözülerek uygulanmaya başlanmış, rekonstitüsyon fikri şekillenmiştir.
3. 20. Yüzyılda Liyofilizasyonun (Freeze-Drying) Gelişimi
- Liyofilizasyon (dondurarak kurutma) tekniği, 1930’larda geliştirilmiş ve II. Dünya Savaşı sırasında kan plazması gibi hassas biyolojik ürünlerin saklanması için yaygınlaşmıştır.
- Bu teknik sayesinde birçok ilaç stabil, kuru formda üretilip saklanabilir hale gelmiş ve rekonstitüsyon süreci endüstriyel olarak standart hale gelmiştir.
- Özellikle 1940’lı yıllardan itibaren penisilin ve diğer antibiyotiklerin toz formda hazırlanarak sulandırılması, rekonstitüsyonun klinik pratikte temel bir adım haline gelmesini sağlamıştır.
4. Farmasötik Endüstride Modernleşme ve GMP Standartları
- 1960’lardan itibaren, rekonstitüsyon işlemleri farmasötik kalite standartları ile tanımlanmış, USP, Ph. Eur. ve WHO gibi kurumların yönergelerinde sistematik olarak yer almaya başlamıştır.
- Modern anlamda rekonstitüsyon terimi, enjeksiyonluk liyofilizatların ya da oral süspansiyonların sulandırılmasıyla ilişkilendirilir.
- Bugün bu işlem, hazır steril çözücüler, kapalı transfer sistemleri ve aseptik tekniklerle desteklenmekte ve GMP kapsamında detaylı olarak düzenlenmektedir.
İleri Okuma
- United States Pharmacopeia (USP). (2019). General Chapter <797>: Pharmaceutical Compounding – Sterile Preparations. United States Pharmacopeial Convention.
- European Medicines Agency (EMA). (2021). Guideline on stability testing for applications for variations to a marketing authorisation. EMA/CHMP/QWP/441071/2011 Rev.2.
- Aulton, M. E., & Taylor, K. (2021). Aulton’s Pharmaceutics: The Design and Manufacture of Medicines (5th ed.). Churchill Livingstone.
- Allen, L. V. (2022). Remington: The Science and Practice of Pharmacy (23rd ed.). Pharmaceutical Press.
- World Health Organization (WHO). (2023). WHO Good Manufacturing Practices: main principles for pharmaceutical products. WHO Technical Report Series, No. 1025.