20. yüzyılın başında, Berlin’de çalışan genç bir patolog olan Paul Ehrlich, boyalarla deneyler yaparak hücreleri renklendirmeyi seviyordu. Bir yandan da zihninde giderek netleşen bir fikri vardı: Eğer bazı kimyasal maddeler belirli hücre yapılarına seçici olarak bağlanabiliyorsa, neden aynı prensip enfeksiyon etkenleri için de geçerli olmasın? Bu düşünce onu, daha sonra “antikor” ve “sihirli mermi (magic bullet)” kavramlarına götürecek olan yan-zincir teorisine hazırlıyordu.
-
Ehrlich, Metchnikoff ve bağışıklık biliminin doğuşu
Ehrlich, difteri ve tetanoz gibi hastalıklara karşı serum tedavileri üzerinde çalışan Emil von Behring ile aynı dönemde çalışıyordu. Behring’in “antitoksin” serumları klinikte hayat kurtarırken, Ehrlich bu antitoksinlerin hücre düzeyinde nasıl ortaya çıktığını anlamaya odaklandı. 1897 civarında formüle ettiği yan-zincir teorisi, hücre yüzeyinde “yan zincir” dediği reseptörlerin bulunduğunu, toksinlerin (antijenlerin) bu reseptörlere bağlandığını, hücrenin de kendini korumak için bu reseptörlerden fazladan üretip seruma saldığını öne sürüyordu. Bu seruma salınan reseptörler, bugün antikor dediğimiz moleküllerin kavramsal karşılığıydı.
Bu sırada, Rus kökenli zoolog Élie Metchnikoff, bütünüyle başka bir cepheden bağışıklık sorununa yaklaşıyordu. O, vücut savunmasının merkezine hücreleri –özellikle fagositleri– yerleştiren fagositik teoriyi savunuyordu. Deniz canlılarından böceklere kadar pek çok tür üzerinde yaptığı karşılaştırmalı çalışmalarla, fagositozun enfeksiyonla savaşta temel bir olay olduğunu gösteriyordu.
Bu iki bakış açısı –Ehrlich’in “humoral” antikor merkezli yaklaşımı ve Metchnikoff’un “hücresel” fagosit teorisi– o dönemde sert tartışmalara yol açmış olsa da, bugün biliyoruz ki her ikisi de doğrudur ve birbirini tamamlar: Hücreler antikor üretir, antikorlar ise sıvı fazda patojenleri nötralize eder ve fagositozu kolaylaştırır. 1908’de Nobel Fizyoloji veya Tıp Ödülünün Metchnikoff ve Ehrlich’e birlikte verilmesi, bağışıklığın bu iki yüzünün de bilimsel meşruiyet kazandığı anı simgeler.
Antikorun görünmeyen molekülden somut yapıya dönüşmesi
20. yüzyılın ilk yarısında antikorlar hâlâ “serumdaki görünmez koruyucu faktörler” olarak algılanıyordu. Karl Landsteiner, küçük kimyasal haptenlerle yaptığı deneylerle antikor özgüllüğünün inanılmaz inceliğini, neredeyse atom düzeyinde farkları seçebildiğini gösterdi. Michael Heidelberger ve Oswald Avery gibi araştırmacılar, antikorların gerçekten protein olduklarını nicel kimyasal analizlerle ortaya koydular.
-
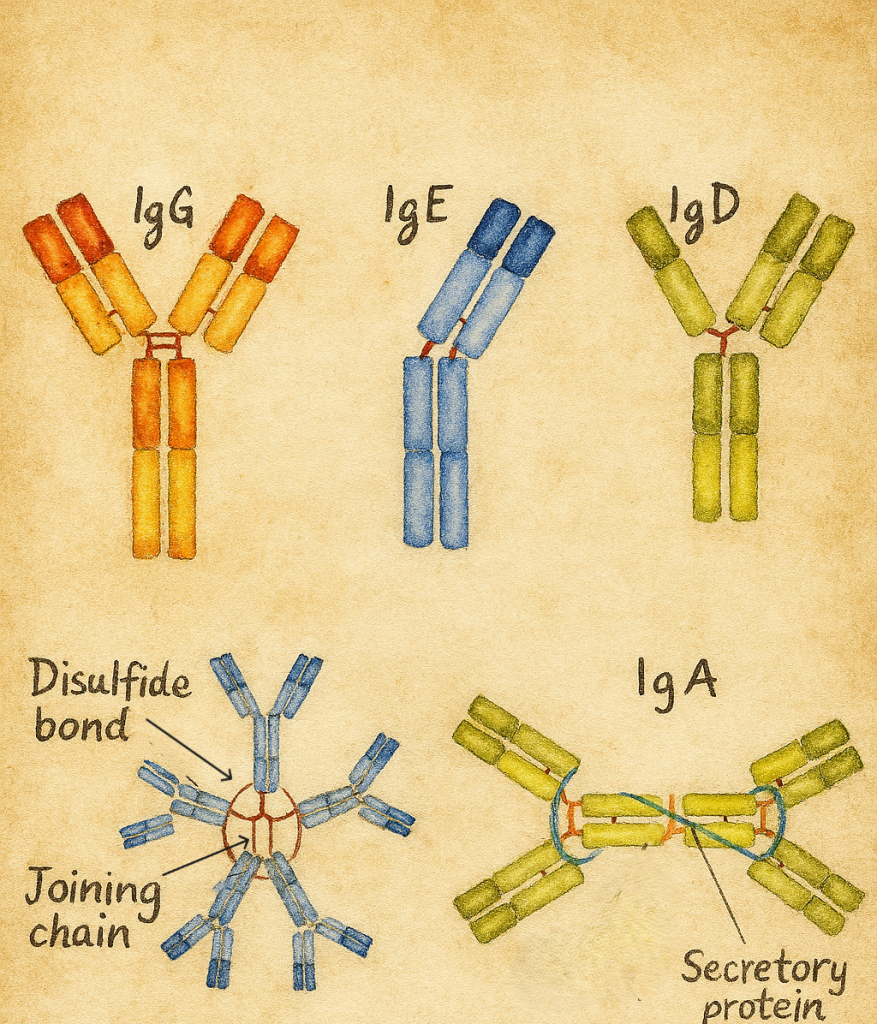
1940’larda Arne Tiselius ve Elvin Kabat, serum proteinlerini elektroforez ile ayırdıklarında, antikorların büyük ölçüde gamma globulin fraksiyonunda yoğunlaştığını gösterdiler; “γ-globulin” ve “immünoglobulin” kavramlarının klinikte yerleşmesinde bu çalışmaların payı büyüktü.
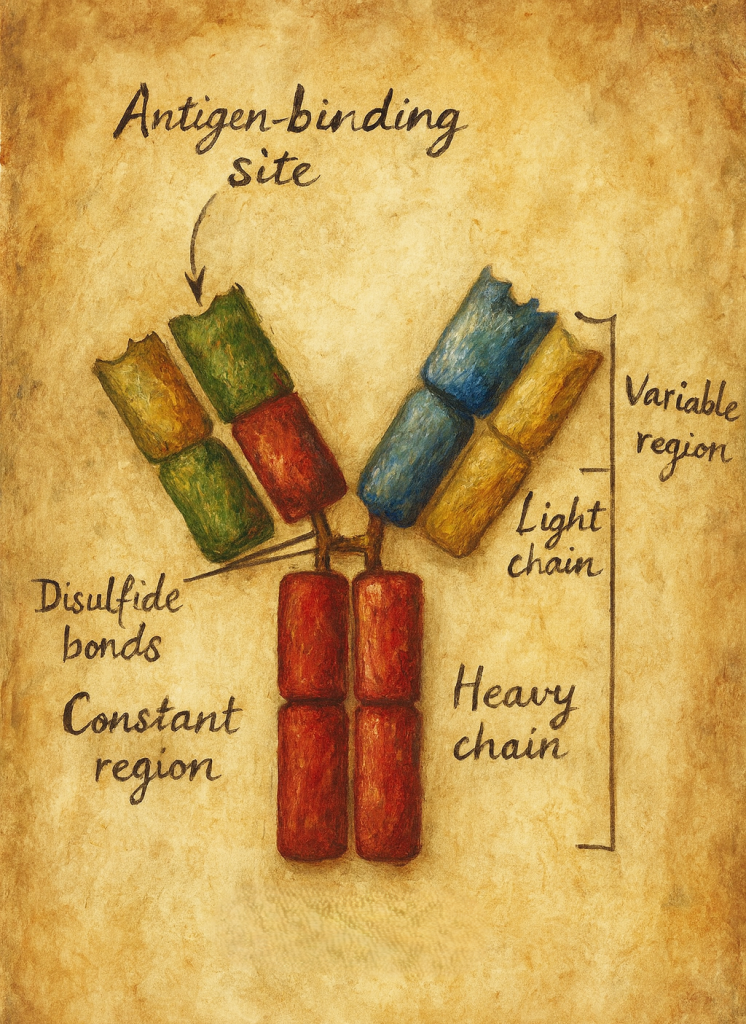
Asıl büyük sıçrama ise 1950–1960’lı yıllarda geldi. Gerald Edelman ve Rodney Porter, farklı proteolitik enzimler ve kimyasal indirgeme yöntemleri kullanarak antikor molekülünü parçalara ayırdılar. Bu parçaların bir kısmı antijene bağlanma özelliğini korurken, bir kısmı kristalleşme eğilimi gösteriyordu. Böylece Fab (antijen bağlayan) ve Fc (kristallenebilir, efektör) fragmanları tanımlandı; disülfit bağlarıyla birbirine bağlanan iki ağır ve iki hafif zincirden oluşan Y-şekilli yapı deneysel olarak doğrulandı. Bu çalışmalar, antikor mimarisinin modern anlamda anlaşılmasının temelini oluşturdu ve 1972’de Edelman ve Porter’a Nobel Ödülü kazandırdı.
Bu dönem aynı zamanda, multipl miyelomlu hastaların serumlarında bulunan tek tip, anormal immünoglobulinlerin –paraproteinlerin– antikor yapısını incelemek için benzersiz bir model olduğunun anlaşıldığı dönemdi. Hastaların serumunda tek bir klona ait homojen antikor bulunduğu için, bu molekülü saflaştırmak ve değişken/sabit bölgeleri, ağır/hafif zincir ilişkilerini çözümlemek çok daha kolaydı. Paraproteinler, antijen bağlama bölgelerinin çeşitliliğini ve özgüllüğünü anlamak için adeta bir “doğal monoklonal antikor kütüphanesi” işlevi gördü.
Kohler, Milstein, Jerne ve hibridoma devrimi
1970’lere gelindiğinde, antikorun yapısı artık iyi tanımlanmıştı; ancak en büyük pratik sorun devam ediyordu: Belirli bir antijene özgü, tek klondan gelen (monoklonal) antikorları, sınırsız ve standartlaştırılmış şekilde üretmek mümkün değildi. Fareleri immunize edip serum toplamak, hep çok sayıda farklı B hücresinin ürünü olan poliklonal karışımlar veriyor; bunlar deneysel olarak kullanışlı olsa da tanısal ve terapötik amaçlar için yeterli homojenlik ve sürdürülebilirlik sağlamıyordu.
İşte bu noktada, 1975 yılında, Cambridge’de çalışan Georges Köhler ve César Milstein, çığır açan bir fikirle ortaya çıktılar. Bir yanda, belirli bir antijene karşı özgül antikor üreten fakat kültürde sınırlı ömürlü olan B lenfositleri vardı. Diğer yanda, sonsuz bölünebilen ama antikor üretmeyen miyelom hücreleri. Eğer bu iki hücre birleştirilirse, ortaya hem ölümsüz hem de tek bir özgüllükte antikor üreten bir hücre hattı çıkabilirdiç
Bu füzyon hücrelerine hibridoma adı verildi; terimi, daha sonra Leonard Herzenberg’in kullandığı bilinir. Hibridomalar:
- Farede belirli bir antijenle immunizasyon sonrası seçilmiş B hücrelerinden türediği için tek bir epitopa özgül,
- Miyelom bileşeni sayesinde kültürde süresiz çoğalabilen,
hücresel “antikor fabrikaları” idi. Böylece ilk kez monoklonal antikorlar endüstriyel ölçekte, standartlaştırılmış, saf ve teorik olarak sınırsız miktarda üretilebilir hale geldi. Bu buluşun bağışıklık bilimi ve tıptaki etkisi o kadar büyüktü ki, Köhler ve Milstein, bu alana teorik katkılar yapan Niels K. Jerne ile birlikte 1984’te Nobel Fizyoloji veya Tıp Ödülü’nü aldılar.
Başlangıçta bu monoklonal antikorlar daha çok:
- Hücre yüzeyi belirteçlerini tanımlamak,
- Lenfosit alt gruplarını ayırt etmek,
- Moleküler hedefleri işaretlemek
gibi temel araştırma amaçları için kullanıldı. Ancak kısa sürede tanı kitleri, görüntüleme ajanları ve terapötik moleküller için de ideal adaylar oldukları anlaşıldı.
Gregory Winter ve antikor mühendisliğinin doğuşu
Hibridoma teknolojisinin ilk nesil ürünleri, çoğunlukla tamamen fare kökenli antikorlardı. Bunlar insan hastalara verildiğinde, insan bağışıklık sistemi bu antikorları “yabancı protein” olarak tanıyıp anti-fare antikorlar geliştirebiliyor, bu da tedavinin etkinliğini azaltıyor ve yan etkilere yol açıyordu.
1980’lerin ortasında, Cambridge’de yine Milstein’in yakın çevresinde çalışan Gregory Winter, bu sorunu çözmek için protein mühendisliğini devreye soktu. Fikir basit, uygulaması son derece sofistikeydi: Fare monoklonal antikorun antijen bağlayan değişken bölgelerini koruyup, geriye kalan sabit bölgeleri insan immünoglobulin dizileriyle değiştirmek. Böylece antikor molekülünün büyük kısmı “insan” olacak, yalnızca antijen özgüllüğünü belirleyen küçük bir fare segmenti kalacaktı.
Bu yaklaşım, önce kimerik, sonra daha da ileri gidilerek humanize antikorların geliştirilmesini sağladı. Humanize antikorlar:
- İmmünojeniteleri belirgin şekilde azalmış,
- Dolaşımda kalış süreleri uzamış,
- Tekrarlayan dozlara daha uygun
hale geldiler. Özellikle enfeksiyon hastalıkları, otoimmün bozukluklar ve kanser için tasarlanan monoklonal antikorların klinik kullanımının önünü açan kritik adım buydu. Gregory Winter, bu alanı daha da ileri götürerek faj display ile tamamen insan antikor kütüphanelerinden özgül antikor seçimi tekniklerini geliştirdi; bu çalışmalar, 2018’de Nobel Kimya Ödülü ile ödüllendirildi.
Bu süreçte ortaya çıkan antikorlardan bazıları –örneğin TNF-α’ya karşı geliştirilen adalimumab gibi– hem romatolojik hastalıkların hem de farmasötik pazarın gidişatını değiştiren “blokbuster” ilaçlar haline geldi.
Antikorlar klinikte: Pasif immünizasyondan hedefe yönelik terapilere
Antikorların klinik kullanımı, aslında çok daha eskiye, Behring’in antitoksin serumlarına kadar gider; bu, modern anlamda pasif immünizasyonun başlangıcıdır. Günümüzde de:
- Tetanoz toksoidine maruziyet,
- Kuduz temas profilaksisi,
- Hepatit B’ye maruziyet,
gibi durumlarda immünoglobulin preparatları, hızlı ama geçici koruma sağlamak için kullanılır. Bu ürünler, çoklu donör serumlarından saflaştırılmış poliklonal antikor karışımlarıdır.
Monoklonal antikor çağıyla beraber, antikorlar artık yalnızca “koruyucu” değil, aynı zamanda hassas cerrah gibi davranan terapötik ajanlara dönüştüler. Romatoid artrit, psöriazis, inflamatuar bağırsak hastalığı, multipl skleroz gibi otoimmün ve inflamatuar hastalıklarda:
- TNF-α, IL-6, IL-17 gibi sitokinlere,
- CD20 gibi B hücre yüzey belirteçlerine,
- Adhezyon moleküllerine
karşı geliştirilen monoklonal antikorlar, hastalığın seyrini kökten değiştirebildi.
Kanserle savaşta antikor devrimi: checkpointler, ADC’ler, bispesifikler
Onkolojide antikor temelli tedaviler birkaç dalga halinde ortaya çıktı:
- Hedefe yönelik klasik antikorlar
HER2-pozitif meme kanserinde trastuzumab gibi antikorlar, tümör hücresi üzerindeki özgül reseptörleri bloke ederek hücre proliferasyonunu durdurur ve immün efektör mekanizmalarını harekete geçirir.
- İmmün kontrol noktası (checkpoint) inhibitörleri
CTLA-4, PD-1, PD-L1 gibi molekülleri hedefleyen antikorlar, T hücrelerinin üzerindeki “frenleri” kaldırarak, tümöre karşı bağışıklık yanıtını yeniden etkinleştirir. Bu grup ajanlar, melanomdan akciğer kanserine, mesane kanserinden pek çok solid tümöre kadar onkoloji pratiğini köklü biçimde değiştirdi; immünoterapinin simgesi haline geldi.
- Antikor–ilaç konjugatları (ADC)
Burada antikor, kemoterapi alanında bir “güdümlü füze” gibi kullanılır: Antikor, yalnızca tümör hücresindeki hedef reseptöre bağlanır; bu antikora kimyasal bağla eklenmiş sitotoksik ilaç içeri girer ve tümör hücresini içeriden öldürür. Trastuzumab emtansine veya trastuzumab derukstekan gibi örnekler, özellikle meme kanseri alanında güçlü klinik sonuçlar göstermiştir. Güncel çalışmalar, bispesifik ADC’ler ile hem tümör seçiciliğini artırmayı hem de direnç mekanizmalarını aşmayı hedeflemektedir.
- Bispesifik antikorlar
Bu antikorlar, bir koluyla tümör hücresindeki antijene, diğer koluyla T hücrelerindeki CD3 gibi moleküllere bağlanarak iki hücreyi fiziksel olarak yakınlaştırır ve T hücresinin tümörü öldürmesini tetikler. Hem hematolojik neoplazilerde hem de solid tümörlerde bispesifik antikorların sayısı hızla artmaktadır.
Antikorlar yalnız başına değil, CAR-T hücreleri gibi ileri hücre tedavilerinin tasarımında da merkezî rol oynar; çünkü CAR reseptörlerinin antijen tanıyan kısmı, antikorların tek zincirli değişken fragmanlarından (scFv) türetilir. Böylece antikor teknolojisi, hücresel immünoterapinin mimarisine de damgasını vurmuş olur.
Güncel ufuklar: tam insan antikor kütüphaneleri, mRNA ve yapay zekâ destekli tasarım
- yüzyılda antikor geliştirme alanındaki yenilikler, hikâyeyi daha da ileri taşıyor:
- Faj display ve buna benzer görüntüleme (display) teknolojileri, geniş insan antikor kütüphanelerinden “en uygun” bağlayıcıların seçilmesine olanak tanıyor.
- Tamamen insanlaştırılmış veya “fully human” antikorlar, immünojeniteyi daha da azaltarak kronik kullanıma daha uygun hale geliyor.
- Kombinasyon tedavileri, monoklonal antikorları kontrol noktası inhibitörleri, küçük moleküller, CAR-T hücreleri veya radyonüklidlerle birleştirerek daha kalıcı yanıtlar elde etmeye çalışıyor.
- Yeni nesil bispesifik antikorlar ve bispesifik ADC’ler, tek seferde birden fazla hedefi vurarak tümör heterojenliğini aşmaya, aynı zamanda toksisiteyi sınırlamaya aday görünüyor.
- Büyük farmasötik ve biyoteknoloji şirketleri, bispesifik ve yeni nesil antikorlar etrafında milyar dolarlık iş birlikleri kurarak, antikorların ilaç geliştirme dünyasındaki merkezî konumunu daha da güçlendiriyor.
Bugün, Ehrlich’in “sihirli mermi” diye hayal ettiği şey, aslında onlarca farklı antikor sınıfı, yüzlerce onaylı ve aday molekül, karmaşık kombinasyon protokolleri ve kişiselleştirilmiş tedavi stratejileri halinde karşımızda duruyor.
Bir yüzyıl önce mikroskop başında düşündüğü “belirli bir kimyasalın belirli bir hücreyi seçerek vurabileceği” fikri, önce yan-zincir teorisiyle kağıda döküldü; sonra Edelman ve Porter’ın deney tüplerinde somut bir Y’ye dönüştü; Milstein ve Köhler’in hücre kültürlerinde ölümsüzleşti; Winter’ın laboratuvarında insanlaştırıldı ve fajların üzerinde yeniden yazıldı. Bugün ise aynı temel prensip, tetanoz immün globulini enjektöründen, checkpoint inhibitörü infüzyon setine, bispesifik ADC taşıyan damardan ve CAR-T hücresinin yüzeyindeki scFv’den, farklı ama akraba dillerle konuşmaya devam ediyor.

 Bir insanın ilk kez yakalandığı influenza (grip) virüsü enfeksiyonu ile daha sonra bu virüsün değişik mevsimsel türlerine karşı tepki vermesini sağlayacak ilk anahtar antikorlar (bağışıklık proteinleri : genellikle bağışıklık sağlayan savunma hücrelerinde bulunan ve zararlı madde, bakteri veya virüsleri tespit ederek tanıyabilen proteinler) üretilir. Cell Reports’da yayımlanan yeni bir makalede Harvard’lı araştırmacılar nezleye maruz kalmanın bağışıklık sistemini nasıl etkilediğine dair bakış açıları geliştiriyorlar ve böylelikle daha etkili ve kalıcı aşılar üretebilmeyi hedefliyorlar.
Bir insanın ilk kez yakalandığı influenza (grip) virüsü enfeksiyonu ile daha sonra bu virüsün değişik mevsimsel türlerine karşı tepki vermesini sağlayacak ilk anahtar antikorlar (bağışıklık proteinleri : genellikle bağışıklık sağlayan savunma hücrelerinde bulunan ve zararlı madde, bakteri veya virüsleri tespit ederek tanıyabilen proteinler) üretilir. Cell Reports’da yayımlanan yeni bir makalede Harvard’lı araştırmacılar nezleye maruz kalmanın bağışıklık sistemini nasıl etkilediğine dair bakış açıları geliştiriyorlar ve böylelikle daha etkili ve kalıcı aşılar üretebilmeyi hedefliyorlar.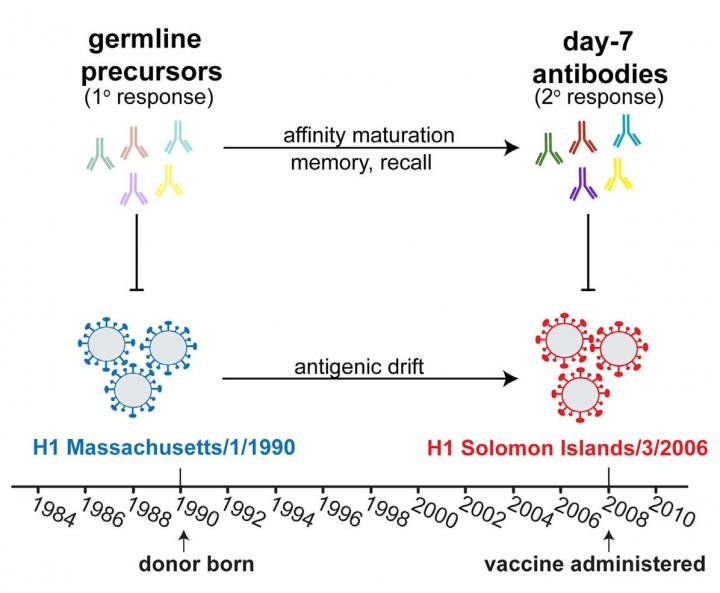
Yorum yazabilmek için oturum açmalısınız.