1. Etimoloji
- “Histoplazmoz” terimi, Antik Yunanca’dan türetilmiştir:
- Bu terim, mantarın doku içinde yapılandırılmış formunu tanımlamak için kullanılır.
2. ICD-10 Sınıflandırması
| Kodu | Tanımı |
|---|---|
| B39.- | Histoplazmoz (genel kod) |
| B39.0 | Akut pulmoner histoplazmoz (Histoplasma capsulatum) |
| B39.1 | Kronik pulmoner histoplazmoz (Histoplasma capsulatum) |
| B39.2 | Tanımlanmamış pulmoner histoplazmoz (Histoplasma capsulatum) |
| B39.3 | Yaygın histoplazmoz (Histoplasma capsulatum) |
| B39.4 | Tanımlanmamış histoplazmoz (Histoplasma capsulatum) |
| B39.5 | Histoplazmoz (Histoplasma duboisii) |
| B39.9 | Tanımlanmamış histoplazmoz |
3. Epidemiyoloji
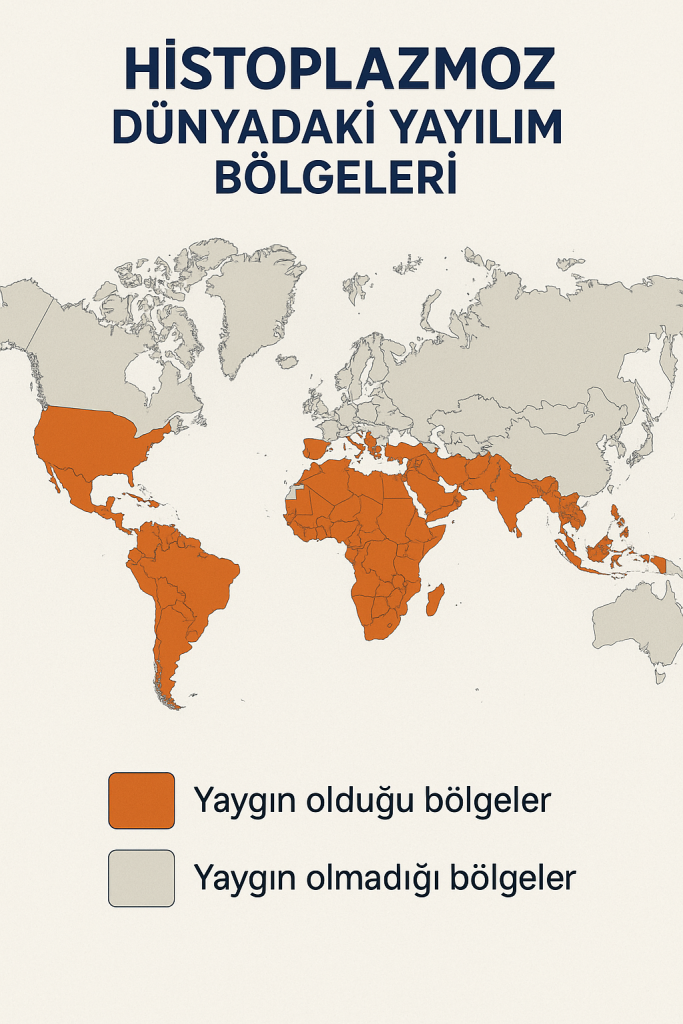
- Coğrafi dağılım:
- ABD’nin Ortabatı ve Ohio-Mississippi Vadisi başta olmak üzere yaygındır.
- Ayrıca Hindistan, Afrika, Karayipler, Avustralya ve Latin Amerika’da endemiktir.
- Reservuar: Toprak ve kuş/yara dışkısıyla kontamine alanlar.
- Mesleki risk: Mağara işçileri, çiftçiler, inşaat işçileri ve kuşlarla temas eden kişiler.
- Görülme sıklığı: Yılda yaklaşık 500.000 vaka (özellikle endemik bölgelerde).
- Türkiye: Vaka bildirimleri nadirdir ve çoğu vakalar ithal edilmiştir.
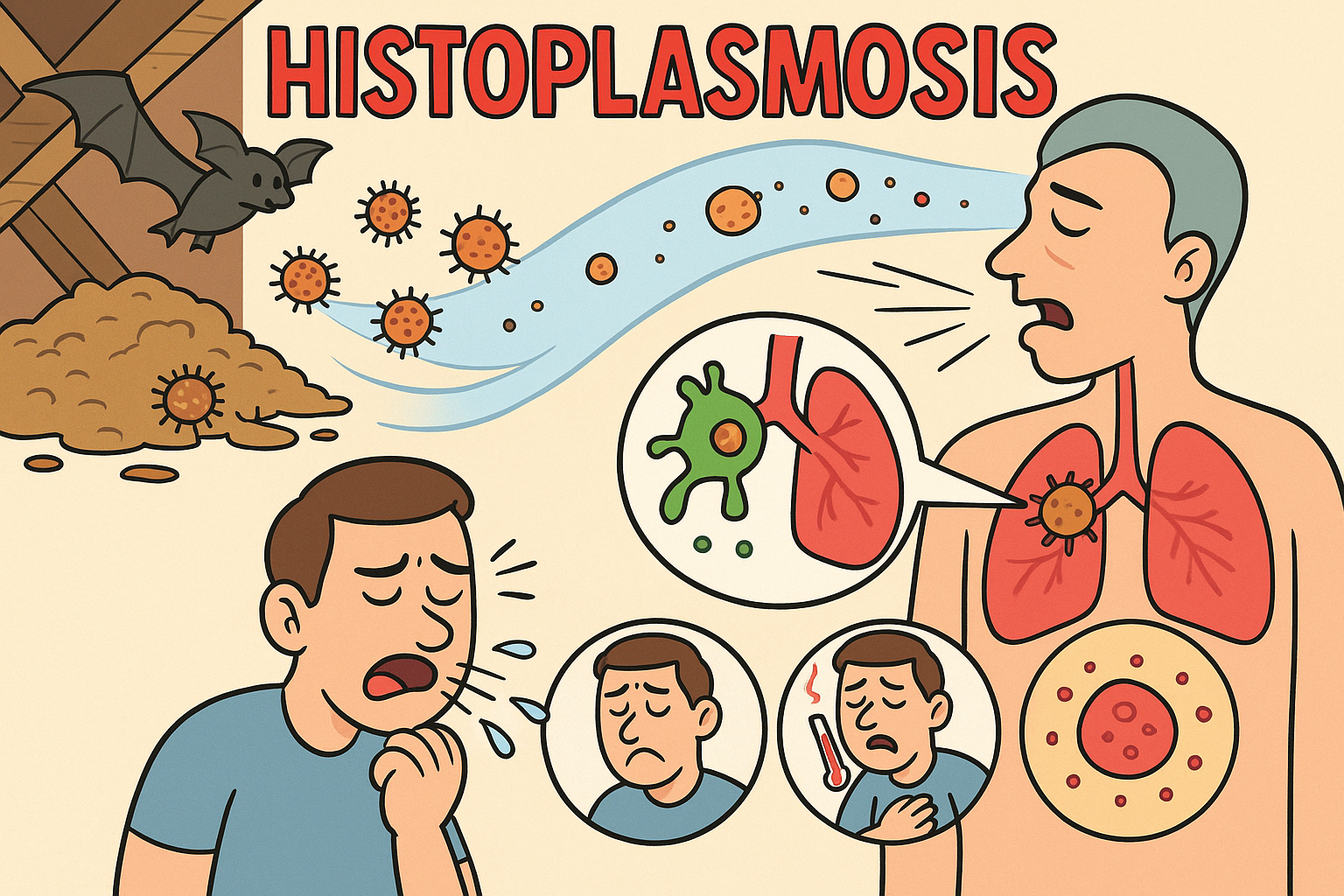
4. Bulaşma Yolu
- Mikrobiyolojik form: Toprakta saprofitik olarak bulunan konidyumlar (sporlar).
- Bulaş mekanizması: Kirlenmiş tozun solunması sonucu sporlar akciğerlere ulaşır.
- İnsandan insana bulaş: Yoktur.
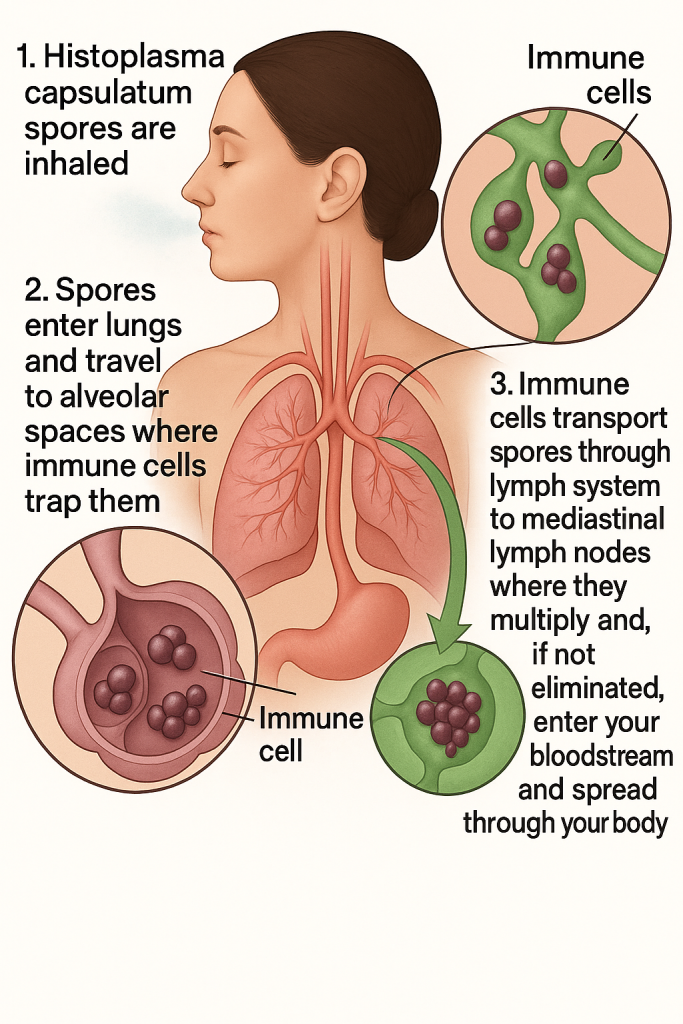
5. Patogenez
- İnkübasyon süresi: 7–21 gün.
- Spor inhalasyonu: Conidia’lar akciğerlere ulaşır.
- Makrofaj fagositozu: Sporlar alveolar makrofajlar tarafından fagosite edilir.
- Transformasyon: Sporlar, hücre içi koşullarda maya formuna dönüşür.
- İntraselüler çoğalma: Mantar hücre içinde bölünerek çoğalır.
- İmmün yanıt: Granülomatöz inflamasyon odakları gelişir.
- Yayılım: Bağışıklığı zayıf kişilerde retiküloendotelyal sisteme yayılır (dalak, karaciğer, kemik iliği).
6. Klinik Seyir ve Semptomlar
6.1. Asemptomatik Histoplazmoz
- En yaygın formdur.
- Radyolojik olarak tesadüfen saptanabilir.
6.2. Akut Pulmoner Histoplazmoz
- Özellikle sigara içenler ve KOAH hastaları risk altındadır.
- Semptomlar:
- Ateş, öksürük, göğüs ağrısı
- Grip benzeri bulgular
- Eritema nodozum veya eritema multiforme
6.3. Kronik Pulmoner Histoplazmoz
- Genellikle yaşlılarda görülür.
- Klinik ve radyolojik olarak tüberküloza benzer.
6.4. Yaygın (Dissemine) Histoplazmoz
- İmmünsüpresif bireylerde gelişir (örneğin HIV/AIDS).
- Belirtiler:
- Ateş, halsizlik, kilo kaybı
- Hepatosplenomegali
- Lenfadenopati
- Ciltte granülomlar
- Menenjit, endokardit
- Kemik iliği baskılanması (pansitopeni)
- Böbreküstü bez tutulumu
7. Tanı Yöntemleri
7.1. Direkt Patojen Tespiti
- Balgam, bronkoalveolar lavaj, kan veya biyopsi örneklerinden kültür.
- Önemli: Yavaş büyüme süresi (haftalar); özel laboratuvar gerekir.
7.2. Moleküler Yöntemler
- PCR ve DNA prob temelli testler: hızlı ve spesifik tanı sağlar.
7.3. Serolojik Testler
- Enfeksiyondan ~5 hafta sonra antikorlar saptanabilir.
- Kullanılan testler:
- Western Blot
- Kompleman fiksasyon testi (CF)
- İmmünodifüzyon
7.4. Histoplazmin Deri Testi
- Artık rutin kullanımda değildir.
- Önceden endemik bölgelerde epidemiyolojik tarama amaçlı kullanılmıştır.
8. Tedavi
8.1. Asemptomatik ve Hafif Olgular
- Genellikle tedavi gerekmez.
8.2. Kronik ve Dissemine Histoplazmoz
- Itrakonazol: Oral antifungal ajan; ilk tercih.
- Amfoterisin B: Şiddetli vakalarda intravenöz kullanım.
- Liposomal formu, toksisiteyi azaltır.
- Vorikonazol: Alternatif olarak kullanılabilir.
- Tedavi süresi:
- Akut vakalar: genellikle 6–12 hafta
- Kronik/dissemine vakalar: 12 ay veya daha uzun
Keşif
1. İlk Keşif: Samuel Taylor Darling (1905)
- Keşif yeri: Panama Kanalı bölgesi, Kolon, Panama.
- Keşfi yapan kişi: Dr. Samuel Taylor Darling (1872–1925), Amerikalı patolog ve mikrobiyolog.
- Yıl: 1905
- Bağlam: Darling, ABD tarafından yürütülen tropikal hastalık araştırmaları kapsamında sıtma ve sarı humma gibi hastalıkların etiyolojisini araştırmak üzere Panama’ya gönderilmişti.
- Gözlem: Otopsi sırasında retiküloendotelyal sistemde (dalak, karaciğer ve kemik iliği) maya benzeri küçük organizmalar saptadı.
- Yanlış tanı: Bu organizmaların bir protozoon olduğunu düşündü ve “Histoplasma capsulatum” adını verdi.
- Histoplasma: Doku içinde oluşan yapılar nedeniyle
- Capsulatum: Hücre çevresinde görülen “halo” yapısından dolayı (gerçekte kapsül değildir; bu halo, preparattaki artefakttır).
2. Mantar Olduğunun Anlaşılması (1912–1930’lar)
- 1912–1920 arası: Organizmanın protozoon değil, mantar olduğu yönünde ilk şüpheler ortaya çıktı.
- 1930’lar:Sabouraud agar gibi mantar kültürlerinin geliştirilmesiyle organizmanın dimorfik bir mantar olduğu anlaşıldı.
- Ortam sıcaklığında küf formunda, vücut ısısında maya formunda bulunur.
- Bu dönemde Histoplasma’nın doğadaki rezervuarı ve bulaş yolları da incelenmeye başlandı.
3. Dimorfizm ve Patogenez (1940–1950’ler)
- 1940’lar: Histoplasma’nın dimorfik doğası (iki farklı morfolojik forma sahip olması) mikroskobik ve kültürel yöntemlerle doğrulandı.
- 1945: Organizmanın toprakta özellikle kuş ve yarasa dışkısı içeren bölgelerde saprofitik olarak bulunduğu gösterildi.
- 1950’ler: Solunum yoluyla bulaşma ve alveolar makrofajlar içindeki çoğalma gibi patogenez süreçleri tanımlandı.
4. Endemik Haritalama ve Epidemiyolojik Çalışmalar (1950–1970’ler)
- 1952: Emmons ve arkadaşları, ABD’nin orta bölgelerinde yaygın olduğunu saptadı.
- Histoplazmin deri testleri ile endemik bölgeler (özellikle Ohio ve Mississippi vadileri) haritalandı.
- Histoplazmin testi, o dönemde hem tanı hem de epidemiyolojik tarama için kullanılmıştır.
5. Moleküler ve Serolojik Gelişmeler (1980–2000’ler)
- 1980’ler: Kompleman fiksasyon ve immünodifüzyon testleriyle serolojik tanı gelişti.
- 1990’lar ve sonrası: PCR ve DNA tabanlı tanı yöntemleri geliştirildi.
- Antijen testleri, özellikle idrar ve serumda hızlı tanı için kullanılmaya başlandı.
- Liposomal Amfoterisin B ve Itrakonazol ile daha etkili tedavi protokolleri geliştirildi.
6. Günümüzde Klinik Önemi
- HIV/AIDS pandemisiyle birlikte, immünsüprese hastalarda yaygın ve ölümcül bir fırsatçı enfeksiyon olarak ön plana çıktı.
- Günümüzde Histoplasma capsulatum enfeksiyonu, endemik bölgelerde pulmoner ve dissemine mikozlar açısından önemli bir sağlık sorunu olarak kabul edilmektedir.
İleri Okuma
- Darling, S. T. (1906). A protozoon general infection producing pseudotuberculosis in man. Journal of the American Medical Association, 46(17), 1283–1285.
- Emmons, C. W. (1949). Histoplasma capsulatum: natural habitat and growth in soil. Science, 109(2825), 219–220.
- Huppert, M. et al. (1967). Histoplasmin skin sensitivity surveys in the United States. American Review of Respiratory Disease, 95(3), 405–415.
- Kauffman, C. A. (2007). Histoplasmosis: a clinical and laboratory update. Clinical Microbiology Reviews, 20(1), 115–132.
- Wheat, J. et al. (2007). Clinical practice guidelines for the management of patients with histoplasmosis. Clinical Infectious Diseases, 45(7), 807–825.
- Hage, C. A. et al. (2010). Pulmonary histoplasmosis. Seminars in Respiratory and Critical Care Medicine, 31(6), 735–742.
- Assi, M. A. et al. (2013). Systemic histoplasmosis: a 15-year retrospective institutional review of 111 patients. Medicine, 92(5), 287–299.
- Bahr, N. C. et al. (2015). Central nervous system histoplasmosis: Multicenter retrospective study on clinical features, diagnostic approach and outcome. Medicine, 94(1), e2017.
- Scheel, C. M. et al. (2018). Development of a Histoplasma urine antigen lateral flow assay. PLoS Neglected Tropical Diseases, 12(1), e0006271.
- Wheat, L. J., & Azar, M. M. (2021). Histoplasmosis. Infectious Disease Clinics of North America, 35(2), 471–491.
Yorum yazabilmek için oturum açmalısınız.