
California Üniversitesi’nden bir grup araştırmacı, sadece bir düğmeye basarak uyuyan farenin rüya görmeye başlamasını sağladı. Araştırmacılar beynin medulla adı verilen ilkel bölgesinde yer alan sinir hücrelerine optogenetik bir düğme yerleştirerek, bu hücrelerin nöronları aktif ve pasif duruma getirmelerini lazerle kontrol etmeyi başardı.
Nöronlar aktifleştirildiklerinde, fareler saniyeler içinde REM uykusuna daldılar. Hızlı göz hareketleriyle karakterize edilen REM uykusu, memelilerde iskelet kaslarının geçici felç durumuna girdiği ve beyin korteksindeki etkinliğin eşlik ettiği uyku evresidir. Deneyde nöronları etkisizleştirmenin, farelerin REM uykusuna dalma yeteneğini azalttığı, hatta ortadan kaldırdığı görüldü. UC Berkeley ekibi bulgularını, Nature dergisinin 15 Ekim tarihli sayısında yayımladı.
UC Berkeley’den Prof. Howard Hughes ve makalenin başyazarı Yang Dan şunları söyledi: “Önceden medullanın bu bölgesinin, REM uykusu sırasında iskelet kaslarının felç durumuna girmesinde rol aldığı düşünülüyordu. Burada gösterdiğimiz şey, bu nöronların REM uykusunu, kasların geçici felci ve beynin NREM uykusuna göre daha uyanık görünmesini sağlayan tipik kabuk aktivasyonun da aralarında olduğu tüm yönleriyle harakete geçirdiğidir.”
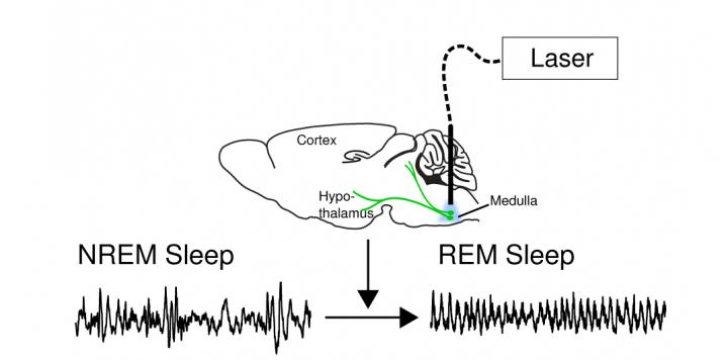 Beyin sapı ve hipotalamusdaki diğer nöronların REM uykusu üzerinde etkisi olduğunun gösterilmesine rağmen, “REM uykusunun yüksek indüksiyonundan dolayı–denemelerimizin yüzde 94’ünde, fareler nöronların etkinleştirilmesiyle saniyeler içinde REM uykusuna girdiler– bunun, uykuya girip girmeyeceğinize karar veren görece küçük bir ağ içerisinde kritik bir düğüm olabileceğini düşünüyoruz.” diye ekliyor Dan.
Beyin sapı ve hipotalamusdaki diğer nöronların REM uykusu üzerinde etkisi olduğunun gösterilmesine rağmen, “REM uykusunun yüksek indüksiyonundan dolayı–denemelerimizin yüzde 94’ünde, fareler nöronların etkinleştirilmesiyle saniyeler içinde REM uykusuna girdiler– bunun, uykuya girip girmeyeceğinize karar veren görece küçük bir ağ içerisinde kritik bir düğüm olabileceğini düşünüyoruz.” diye ekliyor Dan.
Araştırmacılar, bu çalışmanın sadece beyinde rüya görmenin ve uyku üzerindeki karmaşık denetimin daha iyi anlaşılmasını sağlamayacağını, ayrıca bilim insanlarının farelerde rüya görmeyi durdurup başlatmasının neden rüya gördüğümüzü anlamamıza olanak sağlayacağını söylüyor.
UC Berkeley’de doktora sonrası araştırmacısı olan Franz Weber, “Pek çok piskiyatrik hastalık, özellikle duygudurum bozuklukları, REM uykusundaki değişikliklerle ilişkilidir ve bazı yaygın kullanılan ilaçlar REM uykusunu etkileyebilir, bu nedenle zihinsel ve duygusal sağlığın hassas bir belirtisi olarak görünmektedir. Uyku çevirimi üzerine çalışma yapmanın, bu hastalıklara, ayrıca uykuyu etkileyen diğer nörolojik hastalıklara, Parkinson ve Alzheimer hastalıkları gibi, yeni bir bakış kazandıracağını umuyoruz,” diye anlatıyor.
Yemek ve Rüya Görmek
Araştırmacılar ayrıca, farelerde bu beyin hücrelerinin uyanıkken etkinleştirilmesinin, uyanık olma hali üzerinde bir etkisi olmadığını, fakat farelerin daha çok yemelerine neden olduğunu buldu. Normal farelerde, bu nöronlar – nörotransmiter gama-amino bütrik asit (GABA) salınımı yapan bir sinir hücreleri dizisi, bu nedenle sıklıkla GABAerjik nöronlar olarak anılırlar – fareler çok keyifli iki aktivite olan yemek yerken veya taranırken, uyanma süreçlerinde en çok aktif olan nöronlardır.
Dan, medulladaki GABAerjik nöronların, beynin evrimsel süreçte çok eski bir diğer bölümü ponstaki nöradrenerjik nöronlar gibi stres nöronlarının tam tersine etki ettiğini düşünüyor.
“Diğer araştırmacılar, koşarken aktif olan nöradrenerjik nöronların, yemek yerken veya taranırken pasif olduğunu buldular. Görünüşe göre sakinleşmişken ve huzurluyken, bu nöradrenerjik nöronlar kapanıyor ve medulladaki GABAerjik nöronlar açılıyor.” diye aktarıyor Dan.
Bu GABAerjik nöronlar, omurga kanalının tepesinde bulunan medullanın karın kısmından, beyin sapının ve hipotalamusun pek çok bölgesine yansır, böylece pek çok vücut fonksiyonunu etkileyebilirler. Bu bölgeler — düşünce ve mantığın merkezi beyin zarından daha ilkel — nefes almak gibi otomatik işlevler ve kasların kontrol merkezi olduğu kadar, duygular ve doğuştan davranışların da oturduğu bölgelerdir.
Optik Beyin Durumu Değişimi
Dan, Weber ve çalışma arkadaşları, medulladaki REM bağlantılı bu GABAerjik nöronları araştırmak içinoptogenetik denilen güçlü bir teknik kullandılar. Bu teknik, bir virüs sayesinde, özel nöron türlerine ışığa hassas iyon kanalları eklemeyi gerektiriyor. Araştırmacılar bu virüsü GABAerjik nöronlara yönlendirmek için, işaretçi proteinleri bu özel nöronlara taşıyan, genetik olarak düzenlenmiş bir fare hattı kullandılar. Bir kere eklendiğinde, beyne eklenmiş optik fiber üzerinden lazer ışığıyla uyarılan iyon kanalları, nöronların etkinleşmesini sağlayabiliyor. Alternatif olarak, GABAerjik nöronlara iyon pompası eklemek, lazer ışığı uyarımıyla bu nöronların aktivitesini kapatmalarına olanak sağladı.
Farelerin genetik olarak düzenlenmiş bu türünü kullanarak, araştırmacılar medulladaki bu nöronların aktivitesinin haritasını çıkardılar ve kısa periyotlarda nöronları aktifleştirme veya pasifleştirmenin, uyku ve uyanma davranışını nasıl etkilediğini kaydettiler.
Ayrıca aynı nöron grubunu etkisizleştirmek için ilaç kullandılar ve çabuk olmaması ve uzun sürmesine rağmen REM uykusunda azalma tespit ettiler, çünkü ilacın etki etmesi için yaklaşık yarım saat gerekti ve çok yavaş tükendi.
Ayrıca medulladaki bir başka nöron grubuna da ışığa duyarlı iyon kanalları eklediler: glutamat nörotransmiter salınımı yapan glutamaterjik nöronlar. Bu nöronları aktifleştirmek hayvanları kısa sürede uyandırdı, GABAerjik nöronları etkinleştirmenin tam tersi etki ederek.
Dan bu nöronlar üzerindeki çalışmalarını, sadece REM uykusunu etkileyecek şekilde değil, ayrıca NREM uykusunu da etkileyecek şekilde sürdürüyor.
Kaynak:
- Bilimfili,
- University of California – Berkeley. “Dreams turned off and on with a neural switch: Activating small group of neurons in medulla causes rapid transition to REM sleep.” ScienceDaily. ScienceDaily, 15 October 2015. <www.sciencedaily.com/releases/2015/10/151015120128.htm>.
Referans: Franz Weber, Shinjae Chung, Kevin T. Beier, Min Xu, Liqun Luo, Yang Dan. Control of REM sleep by ventral medulla GABAergic neurons.Nature, 2015; 526 (7573): 435 DOI: 10.1038/nature14979


Yorum yazabilmek için oturum açmalısınız.