1. Etken Mikroorganizma
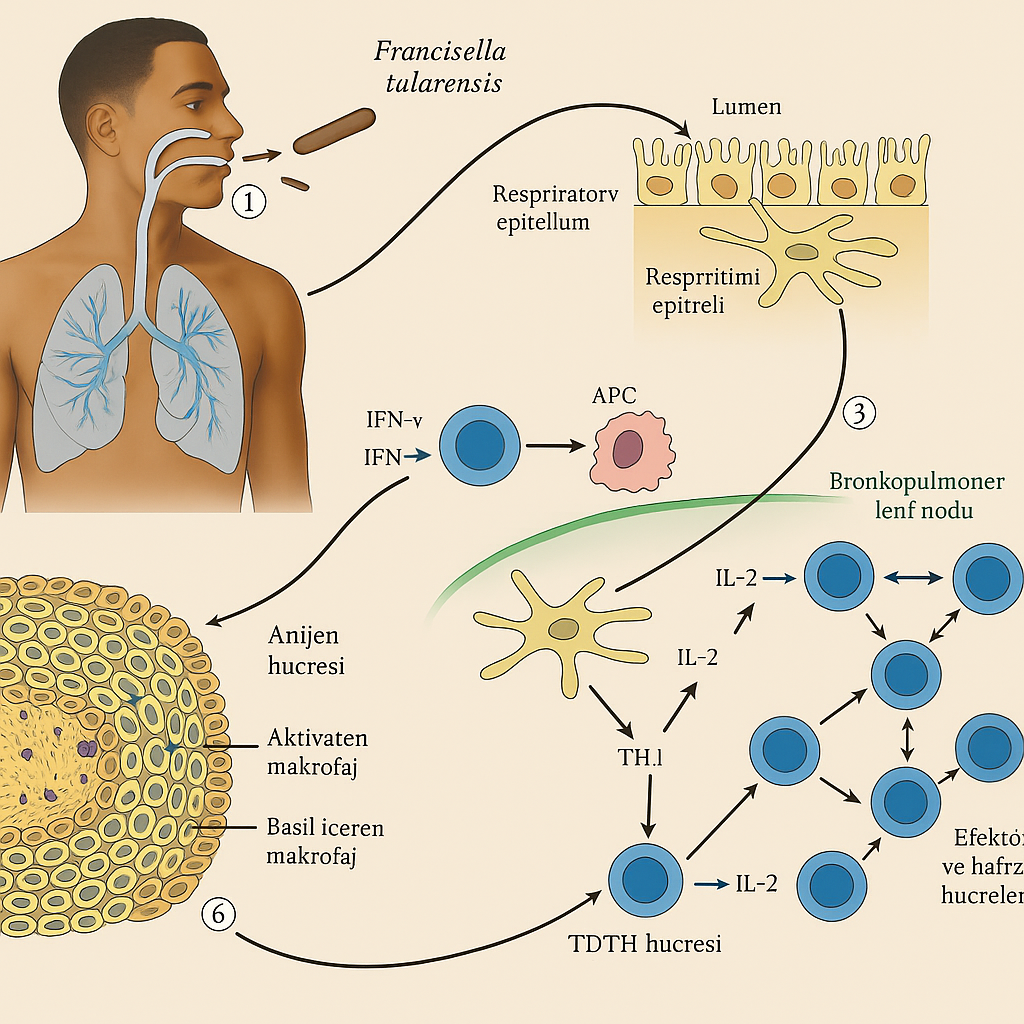
Francisella tularensis, küçük, Gram-negatif, kokobasil şeklinde, zorunlu aerop ve kapsüllü bir bakteridir. Hücre içi paraziti olarak makrofajlar içinde çoğalabilir. Dört alt türü tanımlanmıştır, ancak en fazla patojen olan alt tür Francisella tularensis tularensis (Tip A)’dir. Daha az virülan olan alt tür F. tularensis holarctica (Tip B) ise genellikle Avrupa ve Asya’da, özellikle de Türkiye’de görülmektedir.
Bu bakterinin bulaşıcılığı son derece yüksektir: yalnızca 10-50 bakteri ile enfeksiyon gelişebilir. Bu özelliği nedeniyle biyolojik silah olarak da sınıflandırılmaktadır (Kategori A patojen).
2. Epidemiyoloji
2.1. Coğrafi Dağılım
Tularemia; Kuzey Amerika, Avrupa ve Asya’da endemiktir. Türkiye’de de bazı bölgelerde endemik olarak bulunmaktadır. Özellikle su kaynaklı salgınlar kış aylarında daha fazla bildirilmiştir.
2.2. Türkiye’de Endemik Bölgeler
- Emen-Beyşehir (Konya)
- Yukarçıgil-Ilgın (Konya)
Bu bölgelerde özellikle su kaynaklarına yakın yerleşimlerde salgın riski daha yüksektir.
2.3. Konakçı ve Taşıyıcılar
Tularemia doğada çok çeşitli canlılarda bulunabilir:
- Kemirgenler: Tavşanlar, sincaplar, fareler.
- Haşereler: Keneler (Dermacentor spp., Amblyomma spp.), sivrisinekler, at sinekleri.
- Reservuarlar: Doğal yaşamda su kaynakları ve toprak.
3. Bulaş Yolları
- Deri ve mukozal temas: Enfekte hayvanların dokunulması, derideki çatlaklardan girmesi.
- Vektörle bulaş: Enfekte kene veya sinek ısırığı.
- Sindirim yoluyla bulaş: Pişmemiş veya az pişmiş enfekte et tüketimi; kontamine su içilmesi.
- İnhalasyon: Laboratuvar ortamında aerosolize formun solunması.
İnsandan insana bulaş gösterilmemiştir.
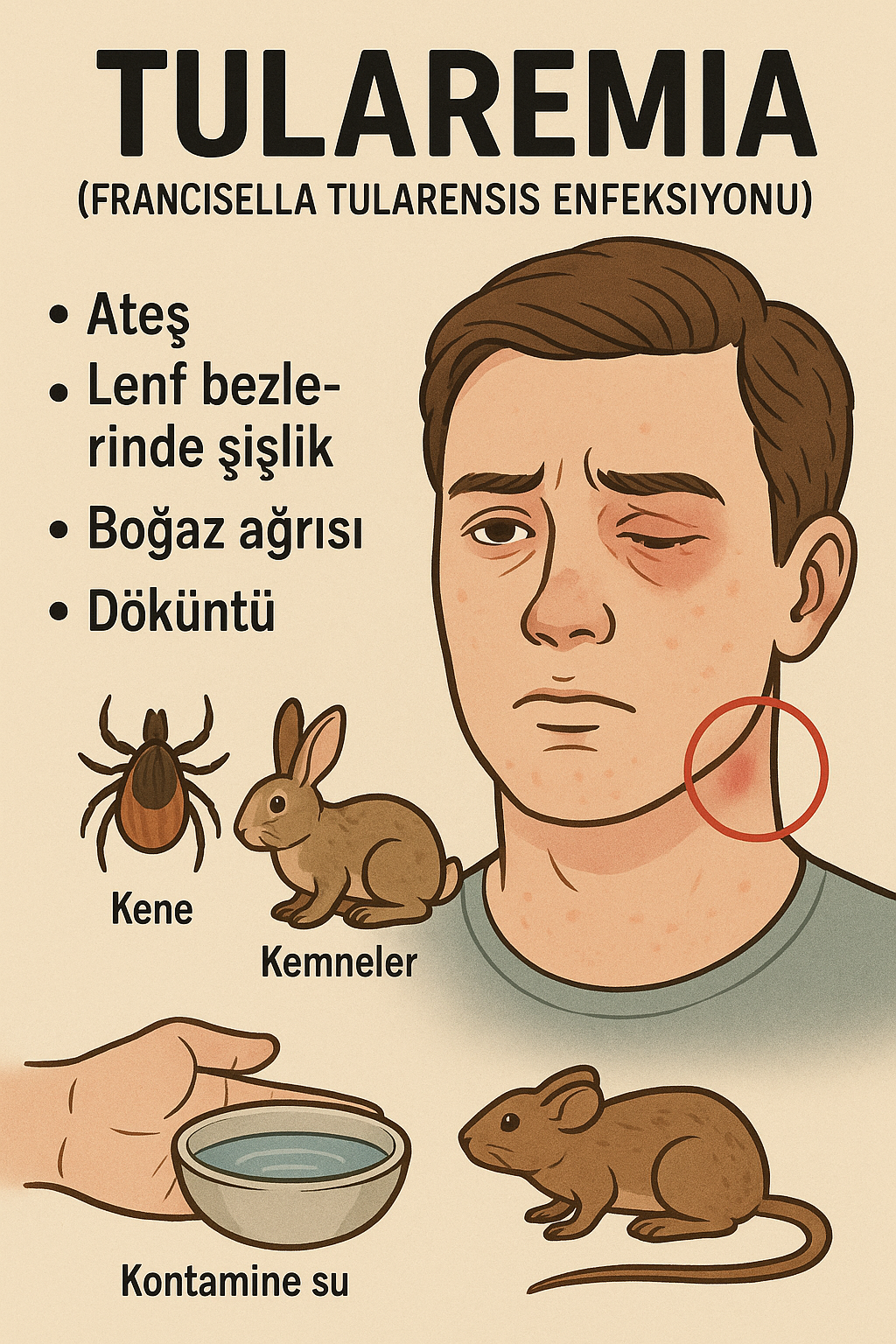
4. Klinik Belirtiler
Tularemia’nın klinik formu bulaş yoluna göre değişir. Başlıca klinik formlar şunlardır:
4.1. Ulseroglandüler Form
- Deride papül ve ardından ülser oluşumu
- Bölgesel lenfadenopati
- En sık rastlanan formdur (kene ısırığı ile bulaşan)
4.2. Glandüler Form
- Deri ülseri olmadan sadece lenf bezi büyümesi
4.3. Orofaringeal Form
- Boğaz ağrısı, disfaji, servikal lenfadenopati
- Patojenin kontamine su ya da gıdayla alınmasına bağlı
4.4. Oculoglandüler Form
- Konjonktivit, gözde ağrı ve kızarıklık
- Preauriküler lenfadenopati
- Gözle temastan sonra gelişir
4.5. Pnömonik Form
- Öksürük, göğüs ağrısı, dispne
- İnhalasyon yoluyla bulaş
- En ciddi ve mortalitesi yüksek form
4.6. Tifoidal Form
- Ateş, halsizlik, hepatosplenomegali, yaygın lenfadenopati
- Belirti olmadan sistemik yayılım
4.7. Yaygın Semptomlar
- Ani başlayan yüksek ateş
- Baş ağrısı
- Kas ağrıları, kırıklık
- Bulantı, kusma, ishal
5. Tanı Yöntemleri
5.1. Klinik Şüphe
- Epidemiyolojik öykü (kemirgen teması, kene ısırığı, endemik bölgede ikamet)
- Yüksek ateş ve bölgesel lenfadenopati
5.2. Serolojik Yöntemler
- Mikroaglütinasyon testi
- ELISA: IgM ve IgG antikorlarının varlığı
- Serokonversiyon en erken 7-10 günde başlar
5.3. Moleküler Yöntemler
- Polimeraz Zincir Reaksiyonu (PCR): En hızlı ve güvenilir tanı yöntemi
5.4. Kültür
- Zor ve tehlikelidir; özel besiyeri (sistein zengin) gerektirir
- Biyogüvenlik seviyesi 3 laboratuvarda yapılmalıdır
6. Tedavi
6.1. Etkili Antibiyotikler
- Streptomisin: İlk tercih, intramüsküler uygulama
- Doksisiklin: Oral tedavi seçeneği (tetrasiklin grubu)
- Gentamisin: Aminoglikozid grubu, intravenöz uygulanabilir
- Kloramfenikol: Alternatif tedavi (göz formunda da kullanılır)
6.2. Tedavi Süresi
- Genellikle 10-14 gün
- Orofaringeal ve tifoidal formlarda tedavi daha uzun sürebilir (21 güne kadar)
6.3. Dirençli Olduğu Antibiyotikler
- Beta-laktam antibiyotikler (Penisilin, sefalosporinler)
- Sulfonamidler
Bu grupların kullanımının etkisiz olduğu bilinmektedir.
7. Korunma ve Kontrol Önlemleri
- Kişisel korunma: Haşere kovucuların kullanılması, eldiven giyilmesi
- Hayvansal ürünlerin iyi pişirilmesi
- Şüpheli su kaynaklarından uzak durulması
- Vaka bildirimi ve epidemiyolojik takip
8. Laboratuvar Güvenliği
Francisella tularensis son derece bulaşıcı olduğu için laboratuvar çalışanlarının aerosol maruziyetine karşı Biyogüvenlik Düzeyi 3 (BSL-3) önlemlerini alması gereklidir.
Keşif
1. İlk Tanımlama ve Bakterinin İzolasyonu
Francisella tularensis‘in keşfi, 20. yüzyılın başlarına dayanmaktadır. Bakteri ilk kez 1911 yılında, Amerika Birleşik Devletleri’nin Kaliforniya eyaletindeki Tulare County bölgesinde, George W. McCoy ve Charles W. Chapin adlı bilim insanları tarafından sıçan vebası araştırmaları sırasında izole edilmiştir. Araştırmacılar bu mikroorganizmayı, ölen kemirgenlerin (özellikle sincapların) dokularında izole etmiş ve yeni bir tür olarak tanımlamışlardır.
Bu ilk izolasyonun ardından mikroorganizma, Bacterium tularense adıyla tanımlanmıştır; burada “tularense” ismi, keşfin yapıldığı Tulare bölgesine ithafen verilmiştir.
2. İnsanlarda İlk Vaka ve Klinik Tanımlama
1914 yılında Amerikalı patolog Edward Francis, bir laboratuvar kazası sonucunda kendisi bu hastalığa yakalanmış ve klinik semptomlarını ayrıntılı biçimde raporlamıştır. Aynı zamanda birkaç yıl boyunca hastalığın bulaşma yolları, konakçıları ve vektörleri üzerine kapsamlı çalışmalar yapmıştır. Bu katkılarından ötürü bakteri daha sonra onun onuruna yeniden adlandırılmış ve Francisella tularensis ismini almıştır.
Francis, bu bakterinin doğada tavşanlar ve kemirgenlerde yaygın olduğunu, insanlara ise çoğunlukla haşere ısırıkları veya doğrudan temas yoluyla bulaştığını göstermiştir. Ayrıca hastalığın farklı klinik formlarını tanımlamış ve özellikle ulseroglandüler formu ilk detaylandıran bilim insanı olmuştur.
3. Epidemiyolojik ve Biyolojik Silah Potansiyeli Araştırmaları
II. Dünya Savaşı sırasında ve sonrasında, Francisella tularensis, Amerika Birleşik Devletleri ve Sovyetler Birliği başta olmak üzere bazı ülkelerin biyolojik silah programlarında incelenmiştir. Çünkü son derece düşük dozlarla enfeksiyon oluşturabilen, solunum yoluyla da bulaşabilen ve yüksek mortaliteye yol açabilen bu bakteri, potansiyel bir biyoterör ajanı olarak değerlendirilmiştir.
Bu çerçevede 1950’li yıllardan itibaren, ABD’de canlı atenüe edilmiş bir tularemi aşısı (LVS – Live Vaccine Strain) geliştirilmiştir. Ancak bu aşı yaygın kullanım görmemiş, sadece risk gruplarında (örneğin laboratuvar personeli) sınırlı olarak uygulanmıştır.
4. Türkiye’de İlk Vaka ve Epidemiyolojik Farkındalık
Türkiye’de tularemiye dair ilk vaka bildirimi 1936 yılında yapılmıştır. Ancak hastalık uzun yıllar boyunca tanınmamış, çoğu zaman yanlış teşhis edilmiştir (örneğin tüberküloz, bruselloz veya basit adenit vakaları olarak değerlendirilmiştir). 1988 yılından itibaren ise Sağlık Bakanlığı tarafından bildirimi zorunlu hastalıklar listesine dahil edilmiştir.
2000’li yıllarda moleküler tanı yöntemlerinin yaygınlaşmasıyla birlikte, Türkiye’de özellikle İç Anadolu, Karadeniz ve Marmara bölgelerinde tulareminin sanılandan daha yaygın olduğu anlaşılmıştır. Bu dönemde çevresel kaynaklar, su örnekleri ve kemirgen rezervuarları üzerine geniş çaplı epidemiyolojik araştırmalar yapılmıştır.
5. Taksonomik Gelişmeler ve Genomik Dönem
Bakterinin genomu ilk kez 2005 yılında tam olarak dizilenmiştir. Bu gelişme sayesinde bakterinin virülans faktörleri, hücre içi yaşam mekanizmaları ve evrimsel ilişkileri daha ayrıntılı biçimde analiz edilmiştir. Ayrıca moleküler filogenetik analizler sonucunda, F. tularensis’in farklı alt türleri (tularensis, holarctica, mediasiatica, novicida) tanımlanmıştır.
Tarihsel Gelişim Kronolojisi
| Yıl | Olay | Bilim İnsanları / Kurum |
|---|---|---|
| 1911 | İlk izolasyon – Tulare County | George W. McCoy & Charles W. Chapin |
| 1914 | İnsan vakası ve tanımı | Edward Francis |
| 1928 | Hastalığın adı “tularemia” olarak netleşti | ABD Sağlık Hizmetleri |
| 1950’ler | Biyolojik silah araştırmaları ve canlı aşı geliştirme | ABD Ordusu |
| 1936 | Türkiye’de ilk vaka bildirimi | Yerli sağlık otoriteleri |
| 1988 | Türkiye’de bildirimi zorunlu hastalık olarak tanımlandı | Türkiye Sağlık Bakanlığı |
| 2005 | Genom dizilimi ve moleküler sınıflama | Genomics konsorsiyumu |
İleri Okuma
- McCoy, G. W., Chapin, C. W. (1912). Bacterium tularense, a new pathogenic organism from ground squirrels. Journal of Infectious Diseases, 10(1), 61–72.
- Francis, E. (1921). Tularemia. Journal of the American Medical Association, 76(10), 706–714.
- Jellison, W. L. (1959). Tularemia in North America: A Summary. Annals of the New York Academy of Sciences, 70(3), 19–24.
- Saslaw, S., Eigelsbach, H. T. (1963). Prophylactic effect of live tularemia vaccine in volunteers. New England Journal of Medicine, 270(15), 747-750.
- Dennis, D. T., Inglesby, T. V., Henderson, D. A. (2001). Tularemia as a biological weapon: medical and public health management. JAMA, 285(21), 2763-2773.
- Keim, P. et al. (2005). Whole-genome analysis of Francisella tularensis reveals insights into pathogenesis and evolution. Nature Genetics, 37(2), 153–160.
- Sjöstedt, A. (2007). Tularemia: history, epidemiology, pathogen physiology, and clinical manifestations. Annals of the New York Academy of Sciences, 1105(1), 1-29.
- Maurin, M., Gyuranecz, M. (2016). Tularaemia: clinical aspects in Europe. The Lancet Infectious Diseases, 16(1), 113-124.
- Hestvik, G., Warns-Petit, E., Smith, L. A. et al. (2017). The status of tularemia in Europe in a one-health context: a review. Epidemiology & Infection, 145(3), 456–466.
- Karadenizli, A., Akyar, I. (2020). Türkiye’de Tularaemi: Epidemiyoloji, Klinik ve Laboratuvar Tanı. Klimik Dergisi, 33(1), 3–10.