Vonoprazan ismi, farmasötik terminolojide yapısal kimya ve işlevsel sınıflandırmayı birleştiren tipik bir sentetik adlandırma biçimidir. Etimolojik olarak bileşenlerine ayrıldığında:
- “Vono-“ öneki, doğrudan belirgin bir klasik Latince ya da Yunanca kökten türetilmemiştir. Muhtemelen firmanın geliştirme sürecindeki kod adı (örneğin TAK-438) üzerinden oluşturulmuş, benzersiz ve ticari olarak ayırt edilebilir bir kök kelime görevi görmektedir.
- “-pra-“ hecesi, çoğu proton pompası inhibitörü (PPI) ve benzeri moleküllerde de görüldüğü gibi, genellikle proton pompası veya “PRAzole” kökenli farmakolojik grubu çağrıştırır.
- “-zan” son eki ise, “azan” türevli kimyasal yapı bileşenlerine (özellikle azot içeren heterosiklik halkalara) işaret edebilir. Aynı zamanda ticari isimlendirme geleneklerine uyan eufonik bir bitiş sağlayarak molekülün benzerlerinden ayırt edilmesini sağlar.
Dolayısıyla vonoprazan adı, doğrudan anlamdan çok, kimyasal sınıf, farmakolojik işlev ve ticari benzersizlik esas alınarak oluşturulmuş yarı-sentetik ve işlevsel bir terimdir.
İçindekiler
1. Farmakolojik Sınıflandırma ve Etki Mekanizması
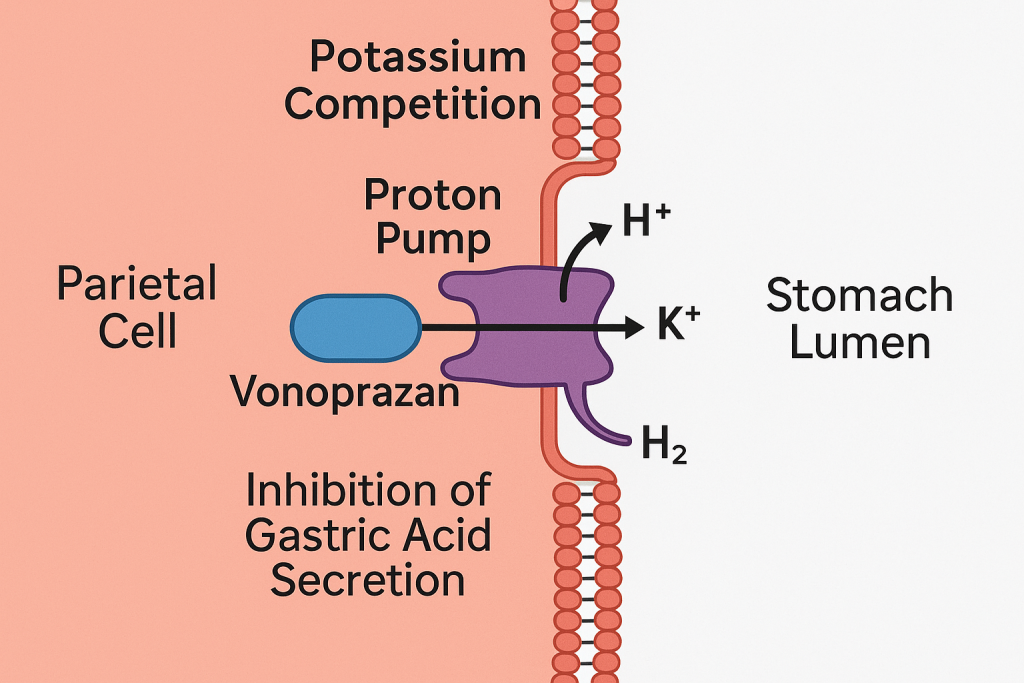
- Vonoprazan, P-CAB (Potassium-Competitive Acid Blockers) olarak bilinen yeni nesil antisekretuar ilaç sınıfına aittir.
- Etki yeri: Parietal hücrelerin apikal yüzeyinde bulunan H⁺/K⁺-ATPaz (proton pompası) enzimidir.
- Etki mekanizması: Potasyum iyonları ile rekabete girerek bu pompayı geri dönüşümlü şekilde inhibe eder.
- Geleneksel proton pompası inhibitörlerinden (örn. omeprazol, pantoprazol) farklı olarak asit aktivasyonu gerektirmez.
- Vonoprazan, kovalent bağlanma yerine iyonik ve geri dönüşümlü bağlarla pompa inhibisyonu gerçekleştirir.
2. Farmakokinetik Özellikler
- Biyoyararlanım: Asitten etkilenmez, bu nedenle enterik kaplama gerekmez.
- Yarı ömür (t½): Yaklaşık 7 saat.
- Metabolizma: Vonoprazan, karaciğerde CYP450 enzimleri tarafından metabolize edilir. Bu enzimler arasında CYP3A4/5, CYP2B6, CYP2C19, CYP2C9 ve CYP2D6 yer alır.
- Dozaj: Endikasyona göre günde bir veya iki defa; yemeklerden bağımsız olarak alınabilir.
3. Kimyasal Özellikler
- Kimyasal formül: C₁₇H₁₆FN₃O₂S
- Molekül ağırlığı: 345.4 g/mol
- Farmasötik form: Tıbbi ürünlerde vonoprazan fumarat olarak, beyaz kristal toz halinde bulunur.
- Suda çözünürlük: Az çözünür.
4. Klinik Endikasyonlar
- Helicobacter pylori eradikasyonu: Amoksisilin ve/veya klaritromisin ile kombinasyon tedavisinde.
- Gastroözofageal reflü hastalığı (GERD).
- Gastrik ve duodenal ülserler.
- NSAİİ ile ilişkili gastrointestinal komplikasyonlara karşı mide koruyucu olarak.
- Fonksiyonel dispepsi ve mide bulantısı.
5. İlaç Formülasyonları ve Onay Durumu
- ABD’de 2022 yılında Voquenzna® (vonoprazan) film kaplı tablet olarak onaylanmıştır.
- Voquenzna Triple Pak®: Vonoprazan + Amoksisilin + Klaritromisin kombinasyonu.
- Japonya’da 2015’ten itibaren Takecab® adı altında monoterapi olarak da mevcuttur.
6. Kontrendikasyonlar
- Vonoprazana veya yardımcı maddelere karşı aşırı duyarlılık.
- Rilpivirin (HIV ilacı) ile birlikte kullanımı kontrendikedir.
- Tüm diğer önlemler uzmanlar için hazırlanan teknik dökümanlarda detaylı olarak verilmiştir.
7. İlaç Etkileşimleri
- CYP450 izoenzimlerinin substratıdır; bu nedenle bu enzimleri indükleyen veya inhibe eden ilaçlarla birlikte dikkatle kullanılmalıdır.
- Potansiyel etkileşimler özellikle CYP3A4 inhibitörleri/indükleyicileri ile önem arz eder.
8. Olası Yan Etkiler
- Monoterapi ve antibiyotik kombinasyonları ile bildirilen en yaygın advers etkiler:
- Tat bozuklukları
- İshal
- Vajinal kandidiyazis
- Baş ağrısı
- Karın ağrısı
- Nazofarenjit
- Arteriyel hipertansiyon
9. Klinik Avantajları
- Asit stabilitesi sayesinde yemek saatlerine bağımlılık yoktur.
- Enterik kaplamaya ihtiyaç duymaz.
- Hızlı ve uzun süreli asit baskılama sağlar.
- GERD ve H. pylori tedavisinde klasik PPI’lara alternatif olarak daha etkili olabilir.
Keşif
1. Bilimsel ve Klinik İhtiyaç Temelli Arka Plan
Proton pompası inhibitörleri (PPI’lar), 1980’lerden bu yana gastroözofageal reflü, peptik ülser hastalıkları ve Helicobacter pylori eradikasyonunda altın standart tedaviler arasında yer almıştır. Ancak PPI’ların önemli farmakolojik sınırlılıkları, yeni nesil asit baskılayıcı ilaç arayışına neden olmuştur:
- Geç etki başlangıcı: PPI’lar asitle aktive olur ve bu aktivasyon gecikmelidir.
- Kısa biyolojik yarı ömür ve kısa süreli proton pompası inhibisyonu.
- Asit stabilitesi düşük olduğundan enterik kaplama zorunluluğu.
- Yemek zamanlamasına bağlılık (genellikle yemekten 30–60 dakika önce alınması gerekir).
- Farmakogenetik varyasyonlara duyarlılık (özellikle CYP2C19 metabolizması yoluyla).
Bu nedenlerle, asit stabilitesi yüksek, daha hızlı ve güçlü asit baskılayıcı etki gösteren ve yemek zamanlamasından bağımsız kullanılabilecek bir ilaç sınıfına gereksinim duyulmuştur. Bu ihtiyaca yanıt olarak Japon ilaç şirketi Takeda Pharmaceutical Company, PPI’lara alternatif olacak yeni bir bileşik ailesi üzerinde çalışmalar başlatmıştır.
2. Keşif Aşaması (2006–2010)
Takeda, 2006 yılında proton pompasını potasyum rekabetiyle inhibe eden moleküler adaylar üzerine odaklanan ilaç tarama programlarını başlattı. Bu programlar kapsamında:
- Benzimidazol yapısından uzaklaşılarak, yeni bir kimyasal iskelet araştırıldı.
- Sülfonil-pirol türevleri üzerinde yapılan çalışmalar sonucunda, TAK-438 kod numarası verilen molekül, asit stabilitesi, yüksek biyoyararlanım, güçlü asit baskılayıcı etki ve CYP2C19 polimorfizminden minimal etkilenen farmakokinetik profil ile dikkat çekmiştir.
3. Preklinik Çalışmalar ve Farmakolojik Özelliklerin Tanımlanması (2008–2011)
- Hayvan modellerinde, TAK-438’ün bazal ve uyarılmış mide asidi sekresyonunu inhibe ettiği gösterildi.
- Preklinik veriler, klasik PPI’lara göre daha hızlı etki başlangıcı ve uzun süreli asit baskılanması sağladığını ortaya koydu.
- TAK-438’ün asit ortamda stabil olduğu ve enterik kaplama gerektirmediği belirlendi.
Referans çalışma:
Hori et al. (2011) tarafından yayımlanan kapsamlı bir preklinik farmakodinamik çalışmada, vonoprazan’ın proton pompasını potasyum rekabeti yoluyla geri dönüşümlü şekilde inhibe ettiği, pantoprazolden anlamlı derecede daha etkili olduğu bildirildi.
4. Klinik Geliştirme Süreci (2012–2015)
Faz I çalışmaları:
- 2012–2013 yıllarında Japonya’da ve Avrupa’da sağlıklı erkek gönüllülerde gerçekleştirildi.
- Vonoprazan’ın doza bağlı mide pH yükseltici etkisi, hızlı etki başlangıcı ve iyi tolere edilme profili gösterildi.
Faz II–III çalışmaları:
- Gastroözofageal reflü, peptik ülser ve H. pylori eradikasyonu endikasyonlarında randomize kontrollü çalışmalarda test edildi.
- Helicobacter pylori eradikasyonunda, klasik PPI bazlı üçlü tedaviden daha yüksek başarı oranları gösterildi (özellikle klaritromisine dirençli suşlarda).
- GERD tedavisinde ise pH>4 süresini anlamlı olarak uzattığı ve semptom kontrolünde PPI’lardan daha hızlı etkili olduğu ortaya kondu.
5. Pazara Giriş ve Ruhsatlandırma Süreci
Japonya’da Onay (2015):
- Şubat 2015: Japonya Sağlık Bakanlığı (PMDA), vonoprazan’ı Takecab® adıyla onayladı.
- Bu onay; GERD, gastrik ve duodenal ülserler, NSAID kaynaklı ülser profilaksisi ve H. pylori eradikasyonu gibi çoklu endikasyonları kapsıyordu.
ABD Onayı (2022):
- Ocak 2022: ABD Gıda ve İlaç Dairesi (FDA), vonoprazanı Voquenzna® adıyla üçlü kombinasyon tedavisinde H. pylori eradikasyonu için onayladı:
- Voquenzna Triple Pak®: Vonoprazan + Amoksisilin + Klaritromisin
- Voquenzna Dual Pak®: Vonoprazan + Amoksisilin
- Bu onay, PPI içermeyen ilk H. pylori eradikasyon protokolü olma özelliğini taşımaktadır.
6. Sonuç ve Klinik Değerlendirme
Vonoprazan, farmakolojik olarak klasik PPI’lardan birçok yönüyle ayrılmaktadır:
- Etki başlangıcı daha hızlıdır.
- Yemek zamanlamasına bağlı değildir.
- CYP2C19 polimorfizminden daha az etkilenir.
- pH kontrolü daha kararlıdır ve gece asit baskılanmasında daha başarılıdır.
Bu özellikleriyle potasyum-rekabetçi asit blokerleri (P-CAB) sınıfının ilk klinik başarı örneği olmuştur ve gastroenterolojik tedavi paradigmasında önemli bir yeniliği temsil etmektedir.
İleri Okuma
- Hori, Y., Imanishi, A., Matsukawa, J., Yasuda, S., & Nishida, H. (2011). TAK-438: A novel potassium-competitive acid blocker for the treatment of acid-related diseases. Journal of Pharmacology and Experimental Therapeutics, 339(2), 412–420.
- Sakurai, Y., Nishimura, A., Kennedy, G., Hibberd, M. L., & Okabe, H. (2015). The pharmacokinetics, pharmacodynamics and safety of repeated doses of vonoprazan (TAK-438), a novel potassium-competitive acid blocker, in healthy male subjects. European Journal of Clinical Pharmacology, 71, 1381–1389.
- Jenkins, H., Sakurai, Y., Nishimura, A., Okamoto, H., Hibberd, M. L., & Ashida, K. (2015). Randomised clinical trial: safety, tolerability, pharmacokinetics and pharmacodynamics of vonoprazan, a novel potassium-competitive acid blocker, in healthy male subjects. Alimentary Pharmacology & Therapeutics, 41(7), 636–648.
- Sakurai, Y., Shiino, M., Nii, T., Funao, N., Nishimura, A., & Ashida, K. (2015). Comparison of vonoprazan with lansoprazole for healing of erosive esophagitis: A randomized double-blind controlled trial. Gut, 64(10), 1432–1441.
- Murakami, K., Sakurai, Y., Shiino, M., Funao, N., Nishimura, A., Asaka, M. (2016). Vonoprazan, a novel potassium-competitive acid blocker, as a component of first-line and second-line triple therapy for Helicobacter pylori eradication: A phase III, randomised, double-blind study. Gut, 65(9), 1439–1446.
- Murakami, K., Sakurai, Y., Shiino, M., Funao, N., Nishimura, A., & Asaka, M. (2016). Vonoprazan as a component of first-line and second-line triple therapy for Helicobacter pylori eradication: A phase III, randomized, double-blind study. Gut, 65(9), 1439–1446.
- Graham, D. Y., Asaka, M. (2022). Update on the use of vonoprazan as a novel acid suppressant for the treatment of acid-related diseases. Digestive Diseases and Sciences, 67(1), 1–10.
- Laine, L., Sugano, K., & Dubois, R. W. (2022). Vonoprazan: A clinical review of a first-in-class potassium-competitive acid blocker for treatment of acid-related diseases. Therapeutic Advances in Gastroenterology, 15, 17562848221108636.

Yorum yazabilmek için oturum açmalısınız.