Tanım ve Taksonomi
Ixodes cinsi, Ixodidae (sert kene) ailesine ait, medikal ve veteriner önemi yüksek ektoparazitlerden oluşur. Bu cins, dorsalinde kitinleşmiş scutum bulunduran, gelişim evrelerinde konak kanı ile beslenen ve trans-stadial patojen aktarımı yapabilen türleri kapsar. Avrupa’da Ixodes ricinus, Kuzey Amerika’da Ixodes scapularis ve Ixodes pacificus, Asya’da ise Ixodes persulcatus en bilinen türlerdir. “Yaz keneleri” olarak anılan populasyonlar, özellikle geç ilkbahar–yaz aylarında (ılıman iklim kuşaklarında çoğunlukla Mayıs–Eylül) saptanan belirgin aktivite piki ile karakterizedir.
Morfoloji ve Ayırt Edici Özellikler
- Vücut planı: Önden geriye daralan oval gövde; gnathosoma (ağız parçası) belirgin; dorsalde sert scutum.
- Cinsiyet farkı: Erkekte scutum tüm dorsumu örter; dişide kısmi, kan emdikçe abdomende belirgin genişleme.
- Ağız parçaları: Uzun hypostom (ters kancalı dentiküller), palpler ve chelicerae; bu yapı dermal ankraj ve kan gölü (hematozöm) oluşturmayı kolaylaştırır.
- Spiraküler plak ve anal oluk: Ixodes cinsinde anal oluğun anüsün önünden geçmesi ve dış kenar anatomisi ayırıcı tanı için kritiktir.
- Larva–Nimf–Erişkin: Larva 6 bacaklı, nimf ve erişkin 8 bacaklıdır; nimf evresi sahada insan ısırıklarının en sık kaynağıdır.
Yaşam Döngüsü ve Fenoloji
Üç konaklı yaşam döngüsü tipiktir: larva → nimf → erişkin. Her evrede farklı konaklardan beslenme görülür.
- Larva: Küçük kemirgenler, kuşlar.
- Nimf: Kemirgenler, kuşlar, küçük–orta memeliler; insana geçişin en kritik basamağı.
- Erişkin: Orta–büyük memeliler (ör. geyik, sığır, köpek) ve fırsatçı olarak insan.
Fenoloji: Ilıman bölgelerde toprak ve çöp katmanının ısınması, bağıl nemin %80+ değerleri ve gün uzunluğunun artışı ile kuyruklanma davranışı (questing) hızlanır. Bu nedenle yaz ayları, özellikle nimf ve erişkinler için en yoğun aktivite dönemidir. Kışın aktivite azalır; okyanus etkili ılıman mikroiklimlerde kısa süreli kış aktivitesi görülebilir.
Ekoloji ve Habitat
- Vejetasyon: Nemli orman altı, çalılık, yaprak döküntüsü zengin taban; ayrıca kıyı şeritleri, parklar, bahçeler, kırsal–kentsel sınır ekotonları.
- Mikroklima: Yüzey nemi ve gölgeleme, desikasyondan korunma için esastır; bu nedenle sabah–akşam serin saatler aktif arama için optimumdur.
- Konak ağları: Biyoçeşitlilik ve ana konak (örn. geyikler) yoğunluğu populasyon büyüklüğünü belirler; ancak bazı patojenlerin rezervuar konakları (örn. Peromyscus veya Apodemus türleri) enfeksiyon döngüsünde belirleyicidir.
Patojen Taşıyıcılığı (Vektörlük)
Ixodes türleri çok sayıda zoonotik patojen için vektör görevi görür:
- Spiroketler: Borrelia burgdorferi sensu lato kompleksi (Lyme borreliyozu), Borrelia miyamotoi (rekürren tip ateş benzeri).
- Flavivirüsler: Kene kaynaklı ensefalit virüsü (TBEV; özellikle I. ricinus / I. persulcatus).
- Anaplasmataceae: Anaplasma phagocytophilum (İnsan granülositik anaplazmozu).
- Rickettsiales: Candidatus Neoehrlichia mikurensis.
- Protozoonlar: Babesia microti, Babesia divergens (insan babesiyozu; aspleni ve immünsüpresyonda ağır seyir).
- Diğerleri: Borrelia mayonii (Kuzey Amerika), bazı riketsiyal etkenler.
Trans-stadial aktarım yaygındır; TBEV gibi bazı virüslerde transovaryen geçiş de bildirilmiştir.
Klinik ve Halk Sağlığı Boyutu
1) Lyme Borreliyozu
- Erken lokalize: Erythema migrans (santral solukluklu genişleyen eritem), ateş, miyalji, artralji.
- Erken yaygın: Multipl lezyonlar, kardit (AV blok), nörolojik tutulum (kraniyal nöropati, aseptik menenjit).
- Geç dönem: Artrit (özellikle diz), nöroborelyoz (radikülit, periferik nöropatiler).
- Tanı: Klinik (EM varlığında serolojiye gerek olmadan tedavi), aksi halde seroloji (iki basamaklı algoritma) ve gerektiğinde BOS incelemesi.
- Tedavi: Doksisiklin, amoksisilin veya sefalosporinler; nörolojik/kardiyak tutulumda parenteral seçenekler.
2) Kene Kaynaklı Ensefalit (TBE)
- Bifazik seyir: İlk fazda grip-benzeri tablo; kısa iyileşme aralığı ardından menenjit/ensefalit.
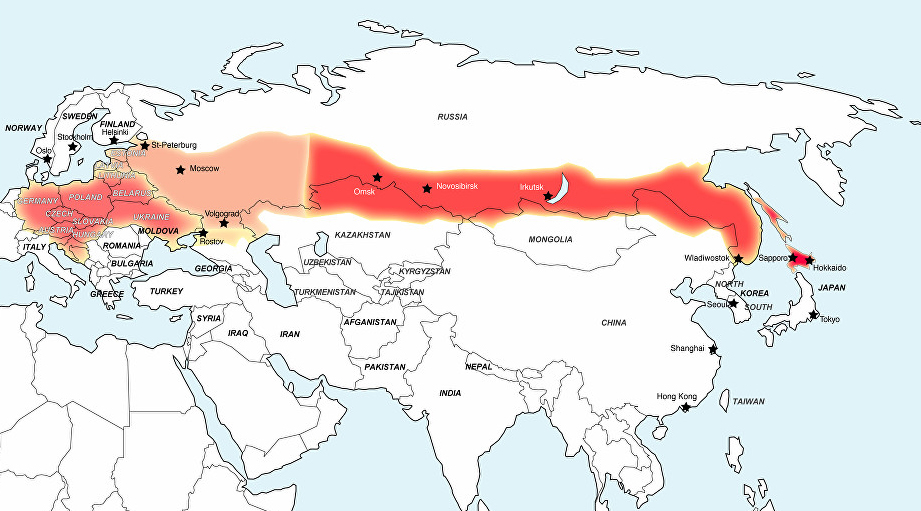
- Korunma: Etkili aşı mevcuttur; endemik bölgelerde (Orta–Doğu Avrupa, Sibirya alt kuşağı) önerilir.
- Destek tedavi: Spesifik antiviral standart tedavi yoktur; yoğun bakım gerektirebilir.
3) Diğer Enfeksiyonlar
- Anaplazmoz: Ateş, lökopeni, trombositopeni, transaminaz yüksekliği; tedavide doksisiklin.
- Babesiyoz: Hemolitik tablo; asplenik ve immünsüprese hastada ağır; azitromisin–atovakvon veya klindamisin–kinin rejimleri.
- Ko-enfeksiyonlar: Aynı ısırıkla iki veya daha fazla patojen bulaşı olabilir; atipik klinik durumlarda düşünülmelidir.
Mevsimsellik ve “Yaz Keneleri” Fenomeni
Yaz aylarında aktivite artışı fizyolojik, çevresel ve davranışsal faktörlerin kesişimidir:
- Isı–Nem Penceresi: Orta düzey sıcaklıklar (yaklaşık 10–25 °C) ve yüksek bağıl nem, su kaybını azaltır ve kuyruklanma süresini uzatır.
- Fotoperiyot: Gün ışığının uzaması, diyapoz düzenleyen nöroendokrin yolları etkiler; nimf ve erişkinlerin dış ortamda aktif kalma süreleri artar.
- Konak Erişilebilirliği: Yazın artan insan açık alan etkinlikleri (yürüyüş, piknik, kamp) ile konak–kene karşılaşmaları yükselir.
- Mikrohabitat Dinamikleri: Yaz fırtınaları ve ara yağışlar, yaprak altı nemini tazeleyerek arama davranışını destekler.
Tanı ve Laboratuvar Yaklaşımları
- Doğrudan saptama: Kene örneğinin tür tayini (morfoloji veya moleküler yöntemler), ancak klinik karar kene testine endekslenmemelidir.
- Seroloji: Lyme için iki aşamalı algoritma (ELISA/EIA + doğrulama testi).
- Moleküler: PCR, BOS veya tam kan/kan yayması (babesiyoz) gibi uygun materyallerde.
- Görüntüleme ve BOS: Nörolojik tutulum şüphesinde endikasyon bazlı.
Korunma ve Kontrol
Bireysel Önlemler
- Giysi ve bariyer: Açık arazide uzun kollu/paçalı giysi, açık renk tekstil; paçaları çorap içine alma.
- Repellent: DEET, pikaridin veya IR3535 içeren ürünler; permethrin ile kıyafet impregnasyonu.
- Vücut kontrolü: Dönüşte tam vücut muayenesi; çocuklarda saçlı deri ve kulak arkası, yetişkinlerde kasık–aksilla odaklı inceleme.
- Kene çıkarma: İnce uçlu pens ile deriye mümkün olduğunca yakın bölgeden yavaş ve dik çekiş; ezme, yakma, yağ–alkol dökme yasak.
- Profilaksi: Endemik bölgelerde TBE aşılaması; Lyme için rutin post-ısırık antibiyotik profilaksisi özel endikasyonlarda (ör. I. scapularis, >36 saat tutulum, bölgesel yüksek enfeksiyon prevalansı) değerlendirilir.
Çevresel ve Toplumsal Önlemler
- Mikrohabitat yönetimi: Park ve bahçelerde düşük çim, yaprak döküntüsünün azaltılması, kenar şeritlerinin bakımı.
- Vektör–konak yönetimi: Yaban hayatı ve evcil hayvanlarda ektoparazit kontrol programları.
- Gözetim: İnsan olgularının bildirim sistemleri, kene bolluk–enfeksiyon izlem çalışmaları; okul/izci programlarında eğitim.
İklim Değişikliği ve Yayılım
Artan ortalama sıcaklıklar ve daha uzun vejetasyon sezonları, Ixodes türlerinin yüksek enlemlere ve rakımlara doğru areal genişlemesine yol açmaktadır. Kışların ılımanlaşması, diyapoz süresini kısaltarak ilkbahar aktivitesini erkene çekebilir; bu durum yaz piki ile birlikte toplam maruziyeti artırır.
Veterinerlik Boyutu
Sığır ve küçükbaşlarda piroplazmozis/babesiyoz, köpeklerde Lyme benzeri klinikler ve anaplazmoz ekonomik ve refah açısından önemlidir. Evcil hayvanların düzenli akarisit uygulaması ve kenelik alanlara girişte koruyucu önlemler zoonotik riskin azaltılmasına katkı sağlar.
Özet Biyogüvenlik Mesajları
- Ixodes cinsi, çok konaklı döngüsü ve yaz aylarında pik yapan aktivitesi ile insan–hayvan sağlığında merkezî role sahiptir.
- Nimf evresi epidemiyolojik olarak başat olup, tanı ve korunma stratejilerinde özel dikkat gerektirir.
- Erken fark etme ve doğru çıkarma komplikasyonları azaltır; TBE için aşı, Lyme için erken tedavi esastır.
Keşif
Kenenin insanla ilişkisi, yazının icadı kadar eski bir rahatsızlık hissiyle başlar: deride ani bir sızlama, parmak uçlarına yapışan sert bir gövde ve ısrarla tutunan minik ağız parçaları. Antikite’de Aristoteles ve Plinius gibi doğa tarihçileri, hayvanların “kan emen parazitleri” arasında keneleri de sayarken, bu canlıların bugün “Ixodes” diye adlandırdığımız cinsinden olduklarını elbette bilmiyorlardı; yine de betimledikleri yapışma, şişme ve zor kopma gibi gözlem notları, morfolojik kimliğin yüzyıllar sonra yapılacak ayrıntılı tanımına önsöz niteliğindeydi. Ortaçağ bitki–hayvan “simya ansiklopedileri” içinde de kene, çoğu kez batıl inançlarla iç içe aktarılır; ancak süre giden pratik bilgi hep aynıdır: yazın daha çok görülür, nemli kıyıda–orman kenarında avını bekler, çıplak deriyi sever.
Modern sınıflandırmanın fitilini ateşleyen 18. yüzyıl, keneleri önce geniş “Acarus” şemsiyesine yerleştirir. Linné’nin 1758 tarihli sistematiğinde bugün Ixodes ricinus olarak bildiğimiz tür, henüz “Acarus ricinus” adını taşır; bu, şekilsel yakınlıkların ve sınırlı mikroskobik tekniğin doğal bir sonucudur. Napolyon sonrası Avrupa’sında doğa tarihi, diseksiyon mikroskoplarının, daha net lenslerin ve bilimsel kulüplerin ivmesiyle hızlanır; 1790’lardan itibaren Latreille ve çağdaşları, sert kalkanlı (ixodid) keneleri yumuşak kenelerden ayıran gövde zırhı, ağız parçalarının yönelimi ve özellikle anal oluğun konumu gibi ince ayrıntılarla cins düzeyine inen bir mimari kurar. Böylece Ixodes adı literatüre yerleşir; türler, kıtanın müzelerinde çekmeceden çekmeceye, kırsaldan kırsala toplanan örneklerle çoğalır.
- yüzyılın ikinci yarısı, keneleri sadece “tiksinç parazit” olmaktan çıkarıp epidemiyolojik aktörlere dönüştürür. Pasteur devriminin mikrop kuramı, parazitin taşıdığı görünmez etkenlerin hastalık yapabileceği fikrini meşrulaştırır. Saha doğa tarihçisi ile hekim arasındaki iş birliği derinleşir: kırsal doktordan orman bekçisine uzanan bir ağ, kenelerin mevsimsel döngülerini not etmeye, hangi hayvanlar üzerinden çoğaldıklarını anlamaya başlar. Bu sahada Ixodes’un ayırt edici davranışı—ot ve çalı uçlarında “kuyruklanma” (questing) duruşu—keneyi bir avcı gibi değil, bir fırsatçı bekleyici gibi konumlandırır. Isı ve nem penceresinin yaz aylarında genişlemesi, insanla kenenin karşılaşma olasılığını artırır; “yaz keneri” imgesi tam da bu gözleme dayanır.
- yüzyılın eşiğinde, Britanya ve Orta Avrupa laboratuvarlarında büyüteçlerin altında Ixodes’un morfolojisi ayrıntıya kavuşur: dişide kısmi, erkekte tam kaplayan scutum; larvada altı, nimf ve erişkinde sekiz bacak; anüsün önünden geçen anal oluk; dişlerin kanca gibi geriye döndüğü uzun hypostom. Bu anatomik alfabe, sahadan gelen örnekleri doğru adlandırmayı ve dağılım haritalarını çizbilmeyi mümkün kılar. Aynı dönemde, av–yırtıcı–parazit ilişkilerini “doğal odak” kavramı içinde düşünen coğrafi epidemiyoloji filizlenir: bir bölgenin vejetasyonu, nem rejimi, ana ve rezervuar konakları, kene bolluğunu ve dolayısıyla hastalık riskini belirler.
Araştırma anlatısında dramatik dönemeç, 20. yüzyılın ilk yarısında kenelerin hastalık vektörü olarak sahneye resmen çıkmasıdır. Doğu Avrupa ve Rusya taygalarında, kene kaynaklı ensefalit etkeninin doğadan izole edilmesi, Ixodes’lu ormanların sadece pastoral bir manzara değil, viral bir peyzaj olduğunu kanıtlar. Aynı yıllarda riketsiyal ve benzeri etkenlerin doğadaki döngüsüne ilişkin sahada geçirilen mevsimler, Ixodes’un üç konaklı yaşam şemasını—larva, nimf, erişkin—ve her evredeki konak tercihlerinin epidemiyolojik sonuçlarını berraklaştırır. Laboratuvarda immünolojik tekniklerin gelişimi, küçük memelilerde ve kuşlarda dolaşan etkenleri göstermeyi kolaylaştırır; böylece “rezervuar konak” ile “ana konak” ayrımı bilimsel bir dil kazanır: geyik populasyonları erişkinlerin beslenmesine imkân verir, ama kimi bakteriler kemirgenler sayesinde döner.
1970’ler ve 80’ler, Lyme borreliyozunun öyküye giriş yaptığı ve Ixodes cinsinin küresel üne kavuştuğu dönemdir. Amerika Birleşik Devletleri’nin kuzeydoğusunda, yazlık kasabaların çeperinde beliren döner lezyonlu olgular, kırsalın yaz bahçelerindeki görünmez bir epideminin işaretleridir. Mikrobiyologların ısrarı ve saha entomolojisinin titizliği, spiroketin izine düşer; kültür, mikroskopi ve seroloji ile Borrelia burgdorferi adı, Ixodes’un tükürük bezi ve orta bağırsağından insan derisine uzanan ince bir patikada belirir. Böylece bir cümlelik, ama büyük bir paradigma değişimi doğar: “Ixodes, sadece kan emen bir eklembacaklı değil; zamanla aktarılan, evreden evreye taşınan çok sayıda patojenin kervanbaşçısıdır.” Aynı yıllarda, Kuzey Amerika’da I. dammini adıyla tanımlanan kıyı kenesinin, morfolojik ve genetik yakınlıkların tartılmasıyla I. scapularis içinde eritilmesi, taksonominin durağan değil, kanıtla yeniden yazılan bir metin olduğunu hatırlatır.
1990’lar, moleküler biyolojinin Ixodes araştırmasını yeni bir düzleme taşıdığı dönemdir. Polimeraz zincir reaksiyonu, hem kenede hem insanda patojen DNA/RNA’sını yakalamayı olanaklı kılar; sahadan toplanan yüzlerce kene, laboratuvarda mikrotüp sıraları hâlinde “çıplak gözle görülmeyeni” görünür kılar. Bu on yılda, co-enfeksiyon fikri yerleşir: aynı ısırıkta Borrelia, Anaplasma, Babesia ve yeni yeni fark edilen diğer etkenlerin bir arada taşınabildiği anlaşılır. Klinik cephede tablo karmaşıklaşır; tanı algoritmaları iki basamaklı serolojiye, seçilmiş olgularda BOS ve PCR’ya yaslanır. Salya bezlerinin “sialom” denen protein repertuvarı ortaya dökülür; antikoagülanlar, immün modülatörler ve “çimento” benzeri yapıştırıcılar, kenenin sessiz cerrahisini anlatan moleküler rollerini ifşa eder.
2000’ler ve 2010’lar, iklim değişikliği ve arazi kullanımı dinamiklerinin, Ixodes’un coğrafyasını adım adım yeniden çizdiği bir uzun hikâyedir. Daha ılıman kışlar, uzayan vejetasyon mevsimi, kenelerin yüksek enlemlere ve daha büyük rakımlara doğru yayılımını kolaylaştırır; kıtasal Avrupa’da I. ricinusun areali kuzeye ve dağ yamaçlarına tırmanır. Kentsel–kırsal sınırlarındaki ekotonlar, koşu parkurlarından köpek gezdirme alanlarına kadar yeni “buluşma noktaları” yaratır. Bu dönemde halk sağlığı gözetim sistemleri, bildirim verileriyle entomolojik sürveyansı birleştirir; hastalık yükü haritaları, sadece olguları değil, kenenin çok yıllı fenolojisini de katman katman işler. Aynı yıllarda, Ixodes’un endosimbiyotları—özellikle dişi üreme dokularında yerleşen bakteriler—metagenomik tekniklerle kataloglanır; kenenin “mikrobiyomu”, vektör yeterliliğini etkileyebilecek ince bir ayar düğmesi olarak gündeme gelir.
Hikâyenin son perdesi, güncel biyoteknolojinin açtığı iki–üç paralel patika üzerinde ilerler. Birinci patika, aşı biliminin iki yönlü stratejisidir: insana yönelik OspA temelli Lyme aşıları klinik sahnede yeniden denenirken, yabani rezervuara yönelik yem–aşı yaklaşımları, patojenin doğadaki dolaşımını kırmayı amaçlar. İkinci patika, anti-kene aşıları ve hedefli immünizasyon çalışmalarının—kenenin salya proteinlerine karşı hızlı kutanöz yanıtı uyaran yeni platformların—deneysellikten translasyona geçiş arayışıdır. Üçüncü patika ise yurttaş bilimi ve sayısal ekolojidir: akıllı telefon uygulamalarına düşen kene fotoğrafları, tarih–konum etiketleriyle birlikte, mevsimsel aktivite eğrilerini gerçek zamanlı besleyen büyük veri setlerine dönüşür. Bu veriler, meteorolojik diziler ve uydu tabanlı yeşillik indeksleriyle birleştirildiğinde, “yaz piki”nin yılı–yılına nasıl öne kayabildiğini, kurak bir baharın nimf bolluğunu nasıl bastırdığını ya da yağışlı bir yazın park kenarlarını nasıl riskli kıldığını nicel olarak anlatır.
Bütün bu uzun hikâyede Ixodes, sabit bir isim ama değişen bir figürdür: Antik gözlemcinin parmaklarına yapışan inatçı parazit; Aydınlanma doğa tarihçisinin çekmecesinde etiketlenen bir örnek; 20. yüzyıl epidemiyologunun ormanında viral bir odak; 1980’lerin mikrobiyoloğu için spiral bakterinin taşıyıcısı; 2000’lerin ekoloğu için ısınan iklimin biyobelirteci; bugünün biyoteknoloğu için salya proteinleriyle örülü bir hedefler galerisi. Yaz aylarında artan etkinliği, sadece sıcaklık–nem fiziğinin değil, insanın yaz davranışlarının, köpeğinin gezdirildiği patikanın, kentin kıyısındaki çalılık şeridin ve gölgelik fıstık çamlarının da bir fonksiyonudur. Ve her yaz, aynı sahne yeniden kurulurken, Ixodes’un hikâyesi yeni bir veri noktası, yeni bir protein bantı, yeni bir harita pikseliyle biraz daha ayrıntı kazanır.
İleri Okuma
- Barbour, A. G., & Persing, D. H. (1990’lar). PCR ve Lyme tanısı/epidemiyolojisi üzerine çalışmalar.
- Bloom, M. E., & Mlera, L. (2022). The role of Ixodes ticks in tick-borne encephalitis virus ecology. Viruses, 14(4), 812.
- Burgdorfer, W. (1978). Discovery of the Lyme disease spirochete. Science, 201(4357), 733–735.
- Burgdorfer, W., Barbour, A. G., Hayes, S. F., Benach, J. L., Grunwaldt, E., & Davis, J. P. (1982). Lyme borreliosis: isolation of a spirochete from Ixodes ticks. Science, 216, 1317–1319.
- Eisen, L., & Eisen, R. J. (2008). Spatial–temporal patterns of Lyme disease vectors in North America. Annual Review of Entomology, 53, 161–179.
- Eisen, L., & Eisen, R. J. (2021). Landscape ecology of ticks and tick-borne pathogens. Annual Review of Entomology, 66, 389–409.
- Eisen, R. J., & Paddock, C. D. (2020). Tick and tickborne pathogen surveillance as public health tools in the United States. Journal of Medical Entomology, 57(5), 1499–1509.
- Fikrig, E., & Narasimhan, S. (2021–2024). Anti-tick salivary target identification and vaccine platform development.
- Gray, J. S. (1994). The development and seasonal activity of Ixodes ricinus (L.) in Ireland. Experimental & Applied Acarology, 18(3), 163–173.
- Gray, J. S., Kahl, O., & Klaus, C. (2023). Seasonal phenology of Ixodes spp. in temperate climates. Parasites & Vectors, 16(1), 122.
- Jaenson, T. G. T., & Lindgren, E. (2021). Ticks and Climate Change in Europe: Technical Report. European Centre for Disease Prevention and Control (ECDC).
- Latreille, P. A. (1790’lar). Histoire naturelle des crustacés et des insectes.
- Linnaeus, C. (1758). Systema Naturae. 10. baskı, Holmiae: Laurentii Salvii.
- Nicholson, W. L., Sonenshine, D. E., Noden, B. H., & Brown, R. N. (2016). Ticks (Ixodida) as vectors of zoonotic pathogens. Ticks and Tick-borne Diseases, 7(4), 1–34.
- Nuttall, G. H. F. (1891). Ticks and their relation to disease. Journal of Hygiene, 1(1), 1–40.
- Pavlovsky, E. N. (1950’ler). Natural nidality of transmissible diseases. Moskva: Medgiz.
- Randolph, S. E. (2002). Dynamics of tick-borne disease systems. Parasitology, 124(S1), S55–S79.
- Rizzoli, A., Hauffe, H. C., Carpi, G., Vourc’h, G., Neteler, M., & Rosa, R. (2013). Ixodes ricinus and its transmitted pathogens in Europe. Clinical Microbiology and Infection, 20(6), 451–465.
- Sonenshine, D. E. (1991). Biology of Ticks. Vol. 1. Oxford: Oxford University Press.
- Spielman, A., Clifford, C. M., Piesman, J., & Corwin, M. D. (1979). Human babesiosis on Nantucket Island, USA: description of the vector, Ixodes dammini. American Journal of Tropical Medicine and Hygiene, 28(4), 687–694.
- Stanek, G., Wormser, G. P., Gray, J., & Strle, F. (2011). Lyme borreliosis. The Lancet, 379(9814), 461–473.
- Süss, J. (2018). Tick-borne encephalitis 2018 update: epidemiology, risk areas, and virus strains. Ticks and Tick-borne Diseases, 9(3), 146–150.
- Tokarz, R., Lipkin, W. I., & çalışma arkadaşları. (2024). Co-infections in Ixodes ticks: clinical implications and surveillance perspectives. Emerging Infectious Diseases, 30(2), 215–224.
- Zilber, L. A., & Chumakov, M. P. (1937–1940). Tick-borne encephalitis’in saha–laboratuvar keşfi. Soviet Medical Reports.











Yorum yazabilmek için oturum açmalısınız.