Eski Yunancada (“bir taç”).
Stephanion yüzeysel bir anatomik işarettir. Linea temporalis superior ile sutura coronalis’in kesiştiği yerdir.

Tıp terimleri sözlüğü
Canlıların yapısı ve düzeni ile ilgilenen bilim dalıdır.
Eski Yunancada (“bir taç”).
Stephanion yüzeysel bir anatomik işarettir. Linea temporalis superior ile sutura coronalis’in kesiştiği yerdir.

Latince torus “bir şişlik, çıkıntı, düğüm; yastık, kanepe”. —>1560’larda, mimaride torus , “bir sütunun tabanındaki büyük, yuvarlak kalıp”. (levator–ius)
Torus levatorius, nazofarenksin lateral kısmında, işitme tüpünün (tubal ostium) birleştiği yerin altında bir yay şeklinde uzanan mukozal bir çıkıntıdır.
Torus levatorius, levator veli palatini kası tarafından kaldırılır. Tubal ostiumun üst kenarında ikinci bir mukozal çıkıntı, torus tubarius vardır.
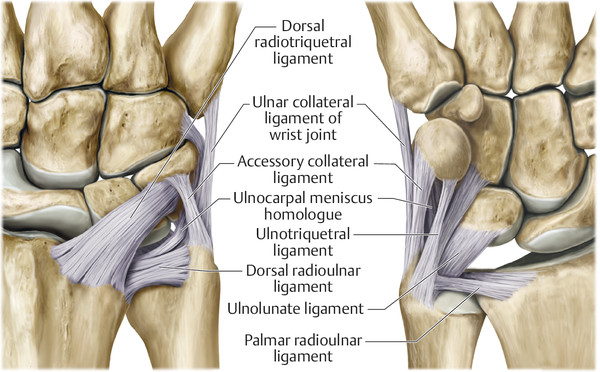
Dorsal radioulnar ligament, distal radioulnar eklemin (articulatio radioulnaris distalis) eklem kapsülü içinde uzanan bir ligamenttir.
Ligamentum radioulnare dorsale radiusun dorsalinden ulnaya kadar uzanır ve TFCC olarak adlandırılan yapının bir parçasıdır. Dorsal radioulnar bağın lifleri, palmar radioulnar bağın lifleri ile birlikte ulnar kaput ve ulnar karpal diske sıkıca kaynaşmış bir halka oluşturur.

Radioulnar dorsal ligament pronasyon sırasında gerilir ve böylece stabilizasyonuna katkıda bulunur.
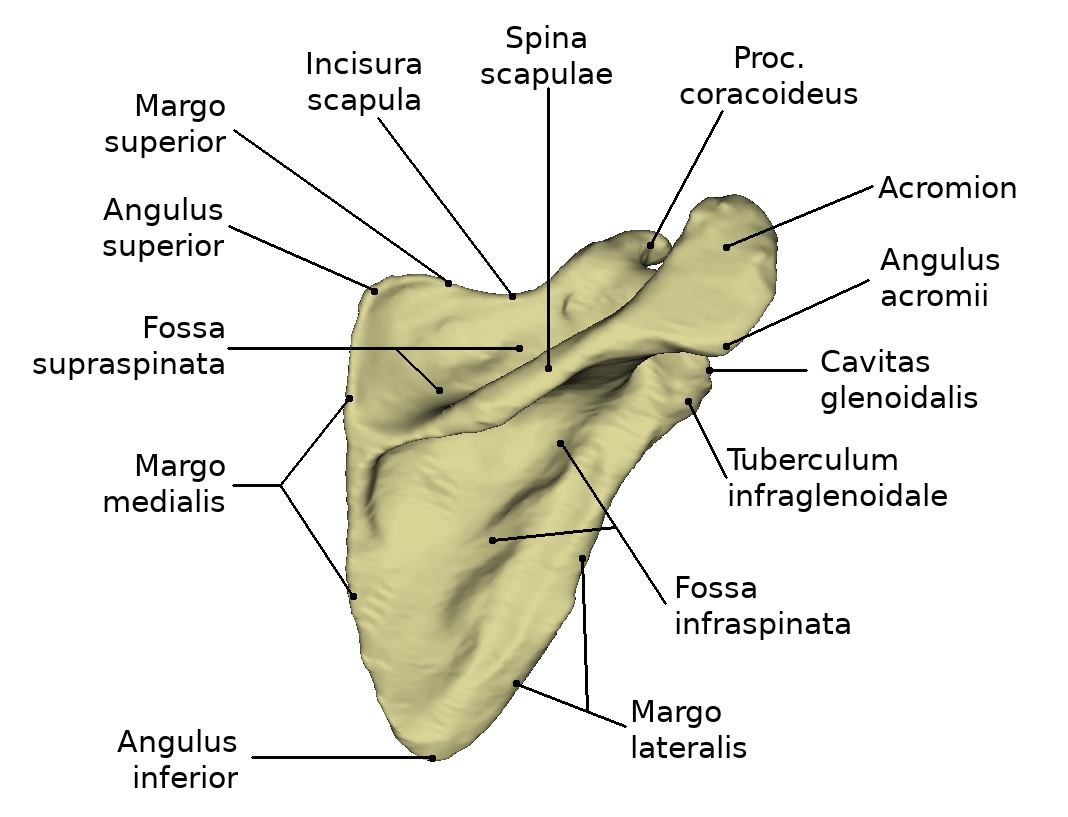
İnfraspinöz fossa, spina skapulanın kaudalinde yer alan skapulanın bir çukurudur. İnfraspinatus kası buradan kaynaklanır. (Bkz; Fossa) (Bkz; infra–spinata)

İnfraspinöz fossa, spina üzerindeki supraspinöz fossadan çok daha büyüktür. Merkezi düz içbükey şekildedir. Medial 2/3’ü infraspinatus kasının orijinidir, lateral üçte biri sadece bu kas tarafından kapsanır.
Böbrek fasyası**, *retroperitoneal boşlukta* böbrekleri ve böbrek üstü bezlerini çevreleyen hayati bir anatomik yapıdır. Bu fasya, böbrekleri ve böbreküstü bezlerini saran koruyucu bir tabaka görevi görür ve bu organların anatomik konumunun korunmasında önemli bir rol oynar.
Aynı zamanda fascia renalis olarak da bilinen böbrek fasyası, capsula adiposa renis olarak bilinen böbrekleri çevreleyen yapısal yağı kapsüller. İki farklı katmandan oluşur:
Her iki tabaka kraniyal ve lateral olarak birleşerek böbrek ve adrenal bezi kapsül benzeri bir şekilde saran bir fasiyal kese oluşturur. Bununla birlikte, bu kese medial ve kaudal olarak açıktır, bu da organların retroperitoneal boşluktaki diğer yapılarla bağlantı kurmasına izin verir.

Dorsal İlişkiler:
Ventral İlişkiler:
Renal fasyanın anatomik ilişkileri, özellikle renal patolojiler, travma gibi durumlarda veya retroperitoneal ameliyatlar sırasında klinik olarak önemlidir. Fasyanın medial ve kaudal olarak açık yapısı, retroperitoneal boşluğun genişlemesini kolaylaştırır, bu da vasküler iletişim ve üreteral fonksiyon sağlar, ancak aynı zamanda retroperitoneal boşluk içinde enfeksiyonların veya malignitelerin yayılması için yollar sağlar.
Böbrek fasyasının** ve sınırlarının ayrıntılı anatomisini anlamak, çeşitli tıbbi durumların teşhisi ve yönetimi için gereklidir:


Fascia obturatoria, pelvisin iç kısmını kısmen kaplayan periosteum ile kısmen kaynaşmış sıkı bir bağ dokusu (fasya) tabakasıdır. (Bkz; Fascia) (Bkz; obturatoria)
Not: Membrana obturatoria ile karıştırmayın.
Fasya obturatoria, iç obturator kasın bazı kısımlarını kaplar. Vasa obturatoria ve obturator sinir etrafında bir yay çizerek pelvisin iç tarafında canalis obturatorius’u tamamlar.
Ventralde fascia obturatoria üst pubik dala, kaudalde ise sakrotuberal ligamente bağlanır. Kranialde fascia iliaca ile, kaudalde ise diaphragma urogenitale’nin superiorundaki fascia diaphragmatis urogenitalis ile birleşir.
Obturator fasyanın bir kopyası kaudal bölümde pudendal kanalı (Alcock kanalı) oluşturur ve buradan pudendal sinir ile internal pudendal arter ve ven geçer.

Conus arteriosus (insanda sık kullanılan eşanlamlısıyla infundibulum), sağ ventrikülün (SV) trunkus pulmonalise (pulmoner gövde) açılan ventriküler çıkış yolu (right ventricular outflow tract, RVOT) segmentidir. Klinik ve anatomik yazında “kalbin hunisi” benzetmesi, bu bölgenin koni/huni biçimli morfolojisini vurgular. İnsan kalbinde sol ventrikül ile aort kapak arasında fibröz süreklilik bulunurken, sağ tarafta pulmoner kapak ile triküspit kapak arasında bu tamamıyla kaslı infundibüler segment yer alır; bu fark, sağ ve sol çıkış yollarının embriyolojik köken ve klinik davranışlarındaki ayrımları açıklar.
Kalp tüpünün kraniyal bölümünde yer alan konus cordis ve truncus arteriosus, nöral krest hücrelerinin katılımıyla gelişen aortopulmoner spiral septum tarafından ayrılarak aortik ve pulmoner çıkışları oluşturur. Sağ ventrikül infundibulumu, bu konotrunkal bölgenin sağ-ventriküler bileşenidir. Septasyon, spiral bir geometri izlediği için, olası malalignmanlar ve rotasyon kusurları Fallot tetralojisi (TOF), çift çıkışlı sağ ventrikül (DORV), transpozisyon gibi konotrunkal anomalilerin anatomik temelini oluşturur. Filogenetik açıdan, alt omurgalılarda “conus arteriosus” terimi, kapakçıklı ayrı bir pompa segmentini ifade edebilir; insanda ise terim, sağ ventrikülün subpulmoner, kaslı çıkış konisini işaret eder.
Infundibüler duvar, çevresel (sirkumferensiyel) ve spiral yönelimli miyosit tabakalarından oluşur; bu lif mimarisi sistolde eşzamanlı daralma ve uzun eksende kısalmayla lümeni düzenler. Endokard, trabekülasyondan yoksun düz bir yüzey sunar; elastik ve kollajen dokuların düzeni, distaldeki kapak aparatına geçişte gerilim dağılımını optimize eder. Purkinje lifleri RVOT’ta bulunmakla birlikte, yoğun ağ yapısı trabeküllü bölgelere kıyasla daha seyrektir; bu durum, RVOT kaynaklı ektopilerin elektrofizyolojik özelliklerine yansır.
Conus arteriosus, laminar akışı destekleyen konik bir geçit sağlar. Proksimal genişlikten distale doğru yumuşak daralma, Reynolds sayısını düşürerek türbülansı sınırlar; bu, pulmoner kapak düzeyinde enerji verimliliğini artırır. Sistolde infundibüler duvarın koordineli kasılması, kapak düzleminin açılımıyla eşzamanlıdır ve pulmoner yatağa akışı hızlandırır. Normal koşullarda subpulmoner bölgede belirgin bir basınç gradyanı oluşmaz; ölçülebilir bir gradyan saptanması, subvalvüler (infundibüler) darlık lehinedir.
Saf veya valvüler stenozla birlikte olabilir. Doppler’de artmış tepe hız ve subvalvüler hızlanma paterni görülür. Uzun dönemde sağ ventrikül basınç yüklenmesi, hipertrofi ve egzersiz intoleransı gelişebilir. Cerrahide rezeksiyon ve gerekirse transanüler patch ile RVOT genişletme uygulanır; bu işlemler sonrası pulmoner yetmezlik gelişimi ve RV dilatasyonu dikkatle izlenir.
TOF’un en karakteristik komponentlerinden biri infundibüler darlık/obstrüksiyondur. Dinamik infundibüler kasılma (“spazm”) hipersiyanoz ataklarını ağırlaştırabilir. Onarım sonrası dönemde geniş RVOT ve pulmoner yetersizlik, sağ ventrikül hacim yüklenmesi, aritmiler ve egzersiz performansında azalma ile ilişkilidir; CMR ile volüm ve regürjitasyon takibi esastır.
Anormal kas bantları, RV kavitesini ikiye böler; proksimal yüksek basınçlı odacık ile distal düşük basınçlı infundibulum arasında hemodinamik gradyan oluşur. Cerrahi rezeksiyon etkindir.
Genellikle yapısal kalbi normal bireylerde, outflow bölgesinden kaynaklanan monomorfik VT’ler görülür. Adrenerjik tetiklenme (egzersiz, stres) tipiktir. Adenozin ve β-blokerlere yanıt verebilir; kateter ablasyonu yüksek başarı oranına sahiptir. Anatomik olarak konusa yakın odaklarda enerji uygulaması, konus arterinin korunmasını gerektirir.
DORV, transpozisyon, persistan truncus arteriosus gibi lezyonlarda infundibulumun konumu, uzunluğu ve ilişkileri cerrahi stratejiyi belirler (ör. intraventriküler tüneller, konduitler, arteriyel switch teknikleri).
Proksimal RCA’nın konus dalı tutulumu, RVOT–anteriyor RV segmentlerinde odak iskemilere neden olabilir; nadiren özgül EKG bulguları ve aritmojenik odak davranışları ile seyreder. Konus dalı ile LAD arasında Vieussens halkası varlığı, kronik proksimal darlıklarda kolateral önem taşır.
Koni biçim, duvar eğriliği ve spiral miyofiber yönelimi, akım çizgilerini kapak düzlemine doğru odaklayan bir nozul etkisi yaratır. Bu, sistolik eylem sırasında enerji kaybını azaltır, kapak yaprakçıklarına binen şer (kayma) stresini homojenleştirir ve distal pulmoner damarlara daha düzgün hız profilleri iletilmesini sağlar. RVOT geometri bozulduğunda (patch ile aşırı genişleme, anulus dilatasyonu), vorteks oluşumu artar ve pulmoner yetersizlikte jet difüzyonu ve enerji verimsizliği gözlenir.
İnsan kalbinde conus arteriosus = infundibulum eşdeğer kullanılır. Alt omurgalılarda “conus arteriosus” terimi, kapakçıklı kaslı bir çıkış segmentini ayrı bir pompa odacığı gibi tanımlayabilir; bu, memelilerdeki kaslı infundibulumla homolog olsa da, işlevsel bağlamı farklıdır. Sol ventrikülde gerçek bir kaslı infundibulum yoktur; mitral–aortik fibröz süreklilik bulunur.
Kalbin sağ ventrikülünde, pürüzsüz duvarlı kaslı bir huni gibi yer alan conus arteriosus (insan kalbinde eşanlamlısıyla infundibulum), anatominin dilinde yüzyıllar boyunca iki ayrı düzlemde konuşuldu: Bir yanda balıklarda ve amfibilerde bağımsız kapakçıklı bir “odacık” olarak karşılaştırmalı anatominin konusu, öte yanda memelilerde özellikle insanda, sağ ventrikülün subpulmoner çıkış kesimi olarak klinik kardiyolojinin hedef bölgesi. Bu ikili kimlik, tarihsel anlatının da çifte kulvarını oluşturur: 1) gözleme dayanan morfolojik betimlemeler ve adlandırmalar; 2) dolaşım fiziolojisi, elektriksel iletim ve hemodinamiğe ilişkin deneysel-klinik kavrayışın giderek incelmesi.
Erken modern çağda kardiyak anatominin mikroyapısal ayrıntıları büyüteç altına girerken, Raymond de Vieussens conus bölgesini besleyen konus dalını ve onun LAD ile yaptığı kolateral bağlantıyı tarif ederek (bugün “Vieussens arteriyel halkası”) subpulmoner alanın damar ağını isimlendirdi; bu, daha sonra girişimsel-cerrahi çağda “üçüncü koroner” varyantı olarak önem kazanacaktı. Aynı yüzyıllarda saptanan doğumsal defekt öyküleri—Stensen’in (1671/1673) TOF’a öncül sayılan tasvirleri gibi—pulmoner çıkış yolunun patolojideki ağırlığını yavaş yavaş tıp literatürüne yazdı.
François Magendie’nin öncülük ettiği canlı-üzerinde deneyci fizyoloji, kalbin de dâhil olduğu çok sayıda sistemi laboratuvara taşıdı; Magendie’nin adı doğrudan conus arteriosus spesifik deneylerle değil, modern deneysel metodun kuruculuğuyla anılır. Aynı yüzyılda Jan Evangelista Purkinje’nin subendokardiyal iletim liflerini (1839) betimlemesi ve Walter Gaskell’in myojenik kuramı, sağ ventrikül çıkışındaki uyarı-yayılım paternlerine dair daha sonra çok şey açıklayacak elektrofizyolojik zeminini kurdu. Yüzyılın sonunda Otto Frank’ın izovolümik basınç-uzunluk deneyleri (1895) ve 20. yüzyıl başında Ernest Starling’in kalp-akciğer hazırlığı, Frank–Starling ilişkisini inşa ederek ventriküler doluş-atım fiziolojisinin temel kanonunu yazdı; bu çerçeve conus/infundibulumun enerji kaybını azaltan geometrisini düşünmenin de dilini verdi. (Not: “Starling eğrisi”, conus’a özgü bir basınç tekniği değil, kalbin global mekanik yanıtını tanımlayan bir ilişkidir.)
Karşılaştırmalı anatominin 19. yüzyıldaki yıldızları (örn. Richard Owen), balık ve amfibilerde çok kapakçıklı, kaslı conus arteriosusun ritmik kasılarla akımı yönlendirdiğini ve spiral valfin rolünü ayrıntılandırdı. Bu çizgi, memelilerde conus’un bağımsız bir “odacık” olmaktan ziyade sağ ventrikül çıkış konisi olarak evrildiği fikrinin tarihini de aydınlatır.
Pulmoner çıkış yolu patolojileri, 20. yüzyılın ortasında kardiyak cerrahinin sahnesine çıktı. Blalock–Taussig–Thomas şantı (1944), Tetralojî of Fallot’lu “mavi bebeklerin” oksijenlenmesini artırarak devrim yarattı. Hemen ardından Lord Russell Brock’un pulmoner valvotomi/infundibüler rezeksiyon girişimleri (1948 ve sonrası), subvalvüler-valvüler darlığın doğrudan cerrahi çözümünü tarif etti. Bu dönem, conus/infundibulumun anatomik sınırlarına ve darlığın dinamik bileşenine dair cerrahi duyarlığı kalıcılaştırdı.
1953’te Inge Edler ve Hellmuth Hertz, endüstriyel ultrasonu göğüs duvarına çevirip ilk M-mod ekokardiyografiyi kaydettiklerinde, RVOT’nin yapısal-dinamik değerlendirmesi bambaşka bir çağın eşiğine girdi. 1980’lerden itibaren kardiyak MR (CMR) ve ardından 4D-flow CMR, infundibulum içindeki hız vektörlerini, vorteksleri ve enerji kaybı/duvar kayma stresi gibi metrikleri nicel olarak ölçmeyi mümkün kıldı; RVOT geometristesinde (örn. geniş transanüler patch sonrası) ortaya çıkan akım düzensizlikleri, bugün artık sayısallaştırılabilir bir fenomendir.
TOF’un patolojik anatomi-cerrahi öyküsü Stensen’den Fallot’ya, oradan transanüler patch ve primer tam onarıma uzanır. Kirklin ekolünün 1960’lar-80’lerde standartlaştırdığı onarımlar, uzun dönemde pulmoner yetersizlik ve RV hacim yüklenmesi pahasına RVOT akışını genişleterek siyanoti sonlandırdı; bu da conus/infundibulum mekaniğinin uzun dönem remodelingini izlemeyi bir takip standardı hâline getirdi.
2000’de Philipp Bonhoeffer’in ilk transkateter pulmoner kapak implantasyonu, eski konduit/patch’li RVOT’larda tekrar kapaklandırmayı cerrahiye alternatif bir kulvara taşıdı (Melody® ve akabinde SAPIEN platformları). Bugün kateter öncesi planlama, RVOT ölçümleri, koroner komşuluk ve olası sıkışma riskinin BT/CMR ile değerlendirilmesine dayanıyor; conus bölgesinin damar varyantları (örn. izole konus arteri, Vieussens halkası) bu planlamanın kritik parçası.
Yapısal kalbi normal bireylerde görülen idiopatik RVOT taşikardisi, 1980’ler-90’lardan beri cAMP aracılı tetiklenmiş aktivite kavrayışıyla açıklanır; çoğu olgu adenozi̇n/β-bloker ile sonlanır ve kateter ablasyonu yüksek başarı oranına sahiptir. RVOT’un pürüzsüz, ince duvarlı mimarisiyle konus arterinin seyrinin yakınlığı, ablasyon stratejisinde güvenlik sınırlarını belirler.
Son beş-on yılda RVOT ve pulmoner kökün 4D-flow CMR ile enerji kaybı (EL), duvar kayma stresi (WSS), vorteks mimarisi gibi metriklerle nicellenmesi; hesaplamalı akışkanlar dinamiği (CFD) ile hasta-özgül modellerin geliştirilmesi; ve PPVI öncesi doğru RVOT boyutlandırması için CMR/BT tabanlı ortak standartların yazılması, conus/infundibulumun klinik karar desteğinde merkezî bir yer tuttuğunu gösteriyor. Bu çalışmalar, RVOT aneurizması gibi post-onarımlı nadir tabloların vortikal akım ve enerji kaybı profilini de ortaya koyuyor.
Conus arteriosus’un hikâyesi, resimli diseksiyonlardan damar halkalarının adlandırılmasına; myosit lif yönelimi ve iletim sisteminin fark edilmesinden cerrahi-kateterik yeniden şekillendirmelere; ekodan CMR’a, oradan 4D-flow ve CFD çağında sayısallaştırılmış hemodinamik haritalara uzanır. Sağ ventrikül çıkışının bu kaslı “hunisi”, bugün doğumsal kalp cerrahisinden aritmi ablasyonuna ve transkateter kapaklandırmaya dek uzanan geniş bir uygulama alanında, geometri-fizyoloji-klinik üçgeninin tam kesişim noktasında durmaktadır.
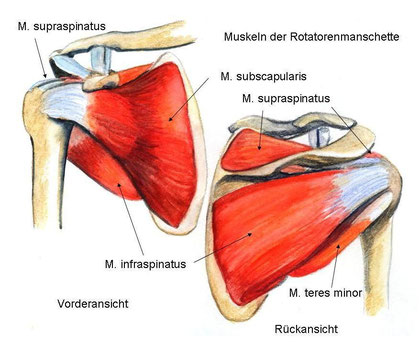
Subskapularis kası, omuz kaslarının ventral grubuna aittir ve rotator manşetin bir parçasıdır. (Bkz; Musculus) (Bkz; sub–scapul–aris)
Subskapularis kasının orijini skapulanın ventral tarafındaki subskapular fossada yer alır ve burayı tamamen doldurur.
Subskapularis kasının insersiyonu humerusun eksi tüberositesindedir. Tendon liflerinin bir kısmı omuz ekleminin kapsülüne yayılır.
Subskapularis kası, brakiyal pleksusun posterior fasikülünden (segmentler: C5-C7) kısa motor dallar olan subskapular sinirler tarafından innerve edilir.

Subskapularis kası üst kolun iç rotasyonu için en önemli kastır ve kol kaldırıldığında adduksiyona katılır. Subskapularis kasının ek bir işlevi de omuz ekleminin nispeten geniş kapsülünü germektir.

Subskapularis kasının felci uzvun dış rotasyonuyla sonuçlanır, bu da iç rotatör olarak işlevinin özellikle önemli olduğunu gösterir.
Teşhis amaçlı olarak, subskapularis kasının işlevi kaldırma testi ve göbek basma testi (“Napolyon testi”) yardımıyla kontrol edilebilir.
Ön serebral arter (ACA), beynin damar sisteminin önemli bir bileşenidir ve internal karotid arterin (ICA) terminal dalı olarak ortaya çıkar. Frontal ve parietal lobların medial kısımlarına ve üst medial parietal bölgelere kan sağlamada önemli bir rol oynar. ACA, yaygın olarak Willis Çemberi olarak bilinen ve beyne kollateral dolaşım sağlayan serebral arteriyel çemberin ayrılmaz bir parçasıdır.
Anatomi ve Segmentasyon
ACA anatomik olarak her biri farklı yollara ve dallara sahip beş segmente ayrılmıştır:
A1 Segmenti (Ön iletişimli veya Yatay Segment):
A2 Segmenti (Post-iletişimli veya İnfrakallozal Segment):
A3 Segmenti (Prekallozal Segment):
A4 Segmenti (Suprakallozal Segment):
A5 Segmenti (Postkallozal Segment):
Beslenen Dallar ve Alanlar
ACA, beynin belirli bölgelerini besleyen birkaç dala yol açar:
İşlevsel Sonuçlar
ACA, öncelikle frontal ve parietal lobların medial ve superior kısımlarını, korpus kallozumun ön dörtte beşini, koku alma soğanını ve yolunu, iç kapsülün ön kolunu ve bazal ganglionların kısımlarını besler.
Klinik Önemi
ACA’nın tıkanması veya enfarktüsü, toplu olarak ön serebral arter sendromu olarak adlandırılan belirli nörolojik eksikliklere yol açabilir. Bunlar şunları içerebilir:
Anatomik Varyasyonlar
ACA anatomisindeki varyasyonlar yaygındır ve klinik etkileri olabilir:
Ön Serebral Arterin Anatomik Varyasyonları
A1 Segmentinin Fenestrasyonları:
Azygos Ön Serebral Arteri:
ACA’nın Trifurkasyonu:
Bihemisferik ACA:
A1 Segmentinin Hipoplazisi veya Yokluğu:
A1 Segmentinin Duplikasyonu:
Birden Fazla Ön İletişim Atardamarları:
A1 Segmentinin Asimetrisi:
Kalıcı İlkel Koku Alma Arteri:

Embriyolojik Gelişim
ACA, başlangıçta optik ve koku bölgelerini besleyen internal karotid arterin ilkel ön bölümünden gelişir. Gelişim ilerledikçe, ön serebral arterler birbirlerine doğru büyür ve ön iletişim arterini oluşturarak Willis Çemberi’nin ön kısmını tamamlar.
İşte ön serebral arterin (ACA) keşfi, tanımı ve anlaşılması hakkında önemli tarihi dönüm noktalarının yer aldığı bir zaman çizelgesi, doğru ve doğrulanabilir ayrıntılar dahil:
Beyin Dolaşımının Antik Tanımları (MÖ 4. Yüzyıl)
Rönesans Anatomisi ve Willis Dairesinin İlk Tanımı (1564-1575)
Serebral Anjiyografinin Gelişimi (1927)
Fonksiyonel Haritalama ve ACA (1930’lar-1940’lar)
ACA Segmentlerinin Sınıflandırılması (1960’lar)
Anatomik Varyantların Keşfi (1970’ler-1980’ler)
ACA Anevrizma Çalışmaları (1980’ler-1990’lar)
Nörovasküler Gelişmeler (2000’ler-Günümüz)
“Truncus intestinalis”, modern tıbbi isimlendirmede, özellikle Terminologia Anatomica (TA) içinde, lenfatik bir yapı olan bağırsak gövdesini tanımlamak için kullanılan bir Latince anatomik terimdir.
Bağırsak gövdesi, çölyak arteri ve üst mezenterik arter tarafından beslenen gastrointestinal sistemin kısımlarından lenf ve kilus’u boşaltarak lenf sisteminde merkezi bir rol oynayan, eşleşmemiş bir lenf gövdesidir. Bunlara özellikle mide, ince bağırsak (duodenum, jejunum, ileum) ve kalın bağırsağın bazı kısımları dahildir.
Çölyak ve üst mezenterik arterler tarafından sağlanan gastrointestinal sistemden lenf ve kilusu boşaltmaktan sorumlu, eşleştirilmemiş bir lenf gövdesi olan Truncus intestinalis, radyografik görüntülemede benzersiz zorluklar ve fırsatlar sunar. Küçük boyutu ve değişken anatomisi onu anlaşılması zor bir yapı haline getirir, ancak görüntüleme teknolojisindeki gelişmeler (özellikle manyetik rezonans görüntüleme (MRI)) hem tanısal hem de cerrahi uygulamalara katkıda bulunarak görselleştirilmesine ışık tutmaya başlamıştır.
MR’da, bağırsak gövdesi bazen ağır T2 ağırlıklı diziler kullanılarak görülebilir; bu diziler, koyu renkli çevre dokulara karşı yüksek sinyal yoğunlukları nedeniyle sıvı dolu yapıları vurgulamada mükemmeldir. Bu bağlamda, bağırsak gövdesi küçük kalibreli, sıvı sinyal yapısı olarak görünür ve sisterna chyli’nin önünde konumlandırılmıştır. Bu anatomik dönüm noktası önemlidir: torasik kanalın kökeninde genişlemiş bir kese olan cisterna chyli, tipik olarak T12–L2 vertebral seviyesinde, aortun hemen arkasında ve omurganın önünde yer alır. Bağırsak gövdesi, diyaframın lomber vertebralara bağlayan kaslı kıvrımları olan diyafragmatik krus‘u geçer ve bu, tanımlanması için kritik bir düzlem haline gelir.
25 hastayı içeren ve özellikle manyetik rezonans kolanjiyopankreatografi (MRCP)** kullanan bir çalışma, sıvı dolu kanallar için optimize edilmiş T2 ağırlıklı bir teknik olan bağırsak gövdesinin görünürlüğünü gösterdi. Araştırmacılar, bunu vakaların %13’ünde veya yaklaşık 16 kişide güvenle tespit ettiler. Bu düşük tespit oranı, yapının inceliğini vurgular: genellikle birkaç milimetreden daha az olan çapı ve derin retroperitoneal konumu, onu bitişik damarlardan veya gürültüden ayırt etmeyi zorlaştırır. Dahası, çalışma bir sınırlamayı vurguladı: gövdenin kendisi bazen tespit edilebilirken, dalları ve periferik mezenterik yolları haritalanmamıştı. Mezenterden ve bağırsak lakteallerinden lenfi boşaltan bu daha ince kollar, mevcut MRI çözünürlüğünün güvenilir bir şekilde yakalaması için çok küçük veya kıvrımlıdır.
Ağır T2 ağırlıklandırmanın kullanımı, lenfin yüksek su içeriğinden yararlanarak bağırsak gövdesinin yağ, kas ve kemiğin daha koyu fonuna karşı parlak, iplik benzeri bir varlık olarak öne çıkmasını sağlar. Ancak, görselleştirilmesi büyük ölçüde hasta faktörlerine (örneğin, vücut yapısı, lenf akışı), görüntüleme parametrelerine (örneğin, dilim kalınlığı, görüş alanı) ve sol lomber gövdeye mi yoksa doğrudan cisterna chyli’ye mi boşaldığı gibi anatomik varyasyona bağlıdır.
Bağırsak gövdesinin radyografik özelliklerini anlamak akademik bir egzersizden daha fazlasıdır; pratik bir zorunluluktur. Tanısal görüntülemede, normal görünümünü tanımak lenfatik drenaj yollarının değerlendirilmesine yardımcı olur. Örneğin, lenfoma veya metastatik hastalıkta, genişlemiş lenf düğümleri veya tıkalı gövdeler, patolojiye işaret ederek seyrini veya sinyal yoğunluğunu değiştirebilir. Kilöz asit veya kilöz sızıntılarda -genellikle ameliyat sonrası komplikasyonlar- bağırsak gövdesinin bütünlüğü kritik hale gelir. Dallarından veya birleşmesinden kaynaklanan bir sızıntı, MRI veya BT’de anormal sıvı birikimleri olarak ortaya çıkabilir ve müdahaleye rehberlik edebilir.
Cerrahi planlamada, özellikle retroperitoneal prosedürler için (örn. aort anevrizması onarımı, pankreatikoduodenektomi), intestinal gövdenin ameliyat öncesi görüntülenmesi, kazara yaralanmayı önlemeye yardımcı olur. Buradaki hasar, iyileşmeyi uzatan komplikasyonlar olan şilöz fistül veya lenfosele yol açabilir. Cerrahlar, cisterna chyli, lomber gövdeler ve diyaframatik krusa göre konumunu tahmin etmek için BT veya MRI’a güvenir ve yaklaşımlarını buna göre ayarlar. Örneğin, cisterna chyli’ye doğrudan drenaj, sol lomber birleşmeye kıyasla risk bölgesini hafifçe kaudad kaydırabilir.
Bağırsak gövdesinin radyografik olarak belirsizliği kısmen anatomik değişkenliğinden kaynaklanmaktadır. Çoğu bireyde (yaklaşık %55), sol lomber gövdeye boşalır ve bu gövde daha sonra cisterna chyli veya torasik kanala katılır. Önemli bir azınlıkta (%45 civarında), lomber gövdeyi atlayarak doğrudan cisterna chyli’ye boşalır. Bu değişkenlik tanımlamayı zorlaştırır: MRI’da, bir radyolog cisterna chyli’nin önünde bir sıvı sinyali yapısı görebilir, ancak bunun tam kimliği (bağırsak gövdesi, lomber gövde veya bir birleşme) yörüngesi veya diyaframatik krus ile ilişkisi gibi bağlamsal ipuçları gerektirir. Gövdenin küçük boyutu (genellikle 1-3 mm çapında) ve aort ve inferior vena kava gibi büyük damarlara yakınlığı, özellikle hareketsiz görüntüleme veya yüksek çözünürlüklü diziler olmadan sınırlarını daha da bulanıklaştırır.
Truncus intestinalis‘in keşfi ve anlaşılması, gastrointestinal sistemin önemli kısımlarından lenf ve kilüsü boşaltmaktan sorumlu olan eşleştirilmemiş bir lenfatik gövde, yüzyıllar boyunca evrimleşmiştir.
Hikaye, hayvan diseksiyonları karşılaştırmalı anatomi için temel oluşturan Aristoteles (MÖ 384-322) ile antik Yunan’da başlar. Lenf sistemini tanımlamasa da, vücuttaki damarlar ve sıvılar hakkındaki gözlemleri iç yapılar hakkında merak uyandırdı. Aynı sıralarda Hipokrat (MÖ 460-370 civarı) dokularda, muhtemelen lenfte “beyaz kan” tanımladı ve kanın ötesindeki sıvı sistemlerinin farkında olduğunu ima etti. Bu erken düşünceler, Truncus intestinalis de dahil olmak üzere lenf sistemi görülmeden kalsa da, daha sonraki keşifler için sahneyi hazırladı.
Helenistik İskenderiye’de, Kalkedonlu Herophilus (MÖ 335-280 civarı) ve Keoslu Erasistratus (MÖ 304-250 civarı) o zamanlar nadir bir uygulama olan sistematik insan diseksiyonları gerçekleştirdi. Herophilus damarları atardamarlardan ayırdı ve küçük damarları kaydetti, Erasistratus ise “pneuma” veya sıvıları taşıyan bir ağ hakkında spekülasyon yaptı. Çalışmaları lenfatikleri tam olarak belirlemedi, ancak damar sistemlerine odaklanmaları anatomiyi bağırsak gövdesi gibi yapıları ortaya çıkarmaya daha da yaklaştırdı.
Bergama’lı Galen (MS 129-MS 216 civarı) hayvan diseksiyonlarına dayanan anatomik incelemeleriyle yüzyıllar boyunca tıbbi düşünceye hakim oldu. Karaciğere ve sindirime bağlı bir damar sistemini tanımladı ancak lenfatikleri damarlarla karıştırdı veya onları tamamen görmezden geldi. Lenf gövdeleri konusundaki sessizliği, dönemin sınırlı araçlarını ve insan diseksiyon yasaklarını yansıtıyor ve Truncus intestinalis keşfedilmemiş halde kaldı, ancak çalışmaları temeline inşa edecek daha sonraki anatomistleri etkiledi.
Erken Gözlemler (16. – 17. Yüzyıl):
Rönesans anatomik keşfi yeniden canlandırdı. Andreas Vesalius (1514–1564), 1543 tarihli başyapıtı De Humani Corporis Fabrica‘da ayrıntılı insan diseksiyonlarıyla anatomide devrim yarattı. Kan damarlarına ve organlara odaklanmış olsa da Vesalius lenfatikleri açıkça tanımlamadı. Ancak, deneysel gözleme yaptığı vurgu, haleflerini apaçık olanın ötesine bakmaya teşvik ederek lenfatik keşifler için sahneyi hazırladı.
Lenfatik sistem, İtalyan bir anatomist olan Gasparo Aselli (1581–1626) ile netlik kazandı. 1622’de bir köpeğin mezenterini keserken, lacteae venae (sütlü damarlar) adını verdiği süt beyazı damarlara rastladı ve bulgularını 1627’de (ölümünden sonra, 1628) De Lactibus sive Lacteis Venis adlı eserinde yayınladı. Bunlar bağırsak lenfatikleri veya lakteallerdi ve sindirimden kilusu emerlerdi; Truncus intestinalis‘in doğrudan öncülleriydi. Aselli’nin keşfi, bağırsağa bağlı lenfatik damarların ilk net görüntüsünü oluşturdu, ancak bunları birleşik bir gövdeye bağlamadı.
Jean Pecquet (1622–1674), Fransız bir doktor, 1651’de köpeklerde cisterna chyli‘yi (o zamanlar receptaculum chyli olarak adlandırılıyordu) tanımlayarak bu anlatıyı ilerletti. 1653 tarihli Experimenta Nova Anatomica adlı eserinde, torasik kanala beslenmeden önce abdominal lenfatiklerden chylus toplayan bu kese benzeri yapıyı tanımladı. Pecquet’in keşfi, cisterna chyli’yi önemli bir kavşak olarak konumlandırdı ve Truncus intestinalis gibi katkıda bulunan gövdelerin varlığını ima etti, ancak buna isim vermedi. Çalışması, lakteallerden drenaj yollarına odaklandı.
Aynı zamanda, İsveçli bir bilgin olan Olof Rudbeck (1630–1702), 1652’de vücuttaki lenf damarlarını haritaladı ve bulgularını Kraliçe Christina’ya sundu. Lenfatikleri damarlardan ayrı, ayrı bir sistem olarak tanıdı ve organlardan kanallara akışını izledi. Rudbeck Truncus intestinalis‘i izole etmese de, bütünsel görüşü bağırsak lenfatiklerini de içeriyordu, daha geniş bir ağdaki rollerini güçlendirdi ve belirli gövdeleri tanımlamaya yaklaştı.

Lenfatik Anatomi Alanındaki Gelişmeler (18. – 19. Yüzyıl):
Modern Anatomik İçgörüler (20. Yüzyıl):