Latince; Miyotonolitik
“Miyotonolitik” teriminin kökleri eski Yunancaya kadar uzanır. Üç kelimenin birleşiminden oluşur: “mys” “kas” anlamına gelir, “tonus” “gerginlik” anlamına gelir ve “lizis” “çöküş” anlamına gelir. Dolayısıyla “miyotonolitik” terimi, kelimenin tam anlamıyla “kas gerginliğinin bozulması” anlamına gelir.
Tıp literatüründe ilk kez 1900’lerin başında ortaya çıkan miyotonolitik, kas spazmlarını ve kontraktürlerini tedavi etmek için açıkça geliştirilen bir ilaç kategorisini ifade eder. İlk miyotonolitik ilaç 1966’da dantrolen oldu. Dantrolen, kas hücreleri içindeki sarkoplazmik retikulumdan kalsiyum salınımını engelleyerek kas kasılmalarını önleyerek kas gerginliğini etkili bir şekilde hafifletir.
- Kas gevşeticiler tabletler, kapsüller ve enjekte edilebilir preparatlar dahil olmak üzere çeşitli formlarda mevcuttur. Ayrıca harici uygulama için özel olarak tasarlanmış topikal ajanlar da mevcuttur.
- Eczacılıkta miyotonolitikleri antispazmodiklerden ayırmak çok önemlidir. Her ikisi de benzer amaçlara hizmet ediyor gibi görünse de, antispazmodikler sindirim ve ürogenital yollarda bulunanlar gibi düz kasları hedef alır. Öte yandan miyotonolitikler öncelikle iskelet kaslarına etki eder.
- Kas gevşeticiler, her biri iskelet kaslarını gevşetmek ve tonlarını azaltmak için tasarlanmış heterojen bir bileşik grubudur. Bu ilaçlar, ağrılı gerginlik, sırt ağrısı, spastisite dahil olmak üzere çeşitli tıbbi senaryolarda ve hatta ameliyat ve yoğun bakım bağlamında uygulama alanı bulmaktadır.
- Bu kas gevşeticilerin etki mekanizmaları oldukça çeşitli olabilir, ancak etkilerini genellikle merkezi sinir sisteminde veya periferik sinir sisteminde bulunan spesifik ilaç hedefleriyle etkileşimler yoluyla gösterirler.
- Kas gevşeticiler oral, parenteral (enjekte edilebilir) ve topikal yollar dahil olmak üzere birçok yolla uygulanabilir. Güzergah seçimi genellikle spesifik tıbbi ihtiyaca, aciliyete ve hastanın genel sağlık durumuna bağlıdır.
- Çoğu ilaç gibi kas gevşeticilerin de dezavantajları vardır. Yaygın yan etkiler arasında kişinin dikkat ve odaklanma gerektiren görevleri yerine getirme becerisini etkileyebilecek yorgunluk ve uyuşukluk yer alır.

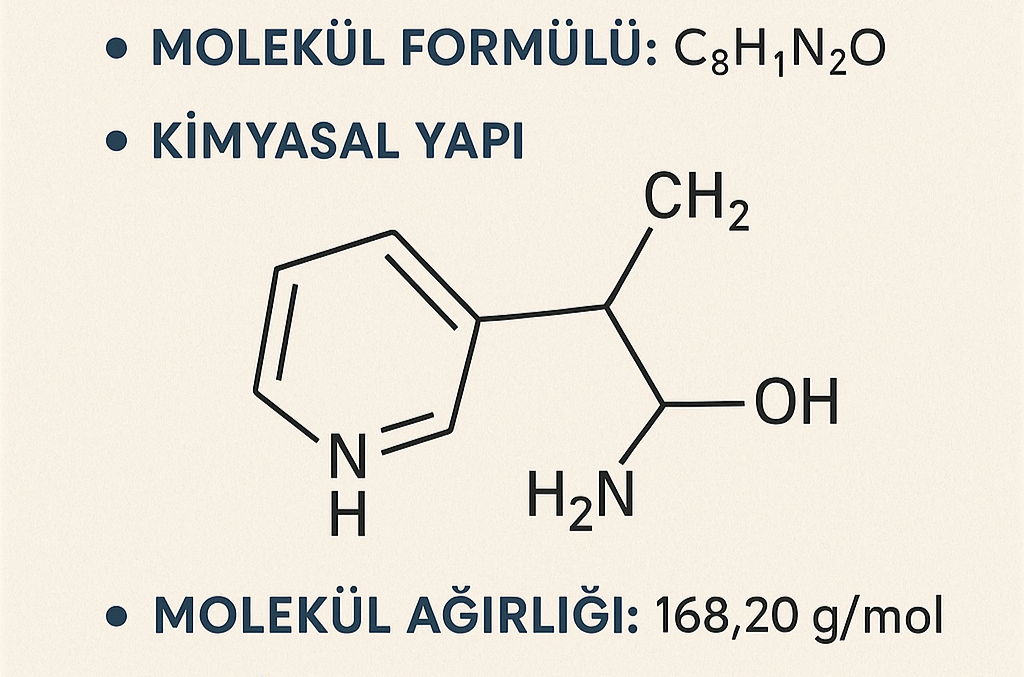
Kimyasal
Yapı ve özellikler
Kas gevşeticiler heterojendir ve tek tip bir kimyasal yapıya sahip değildir, ancak yapısal benzerlikleri olan gruplar, örneğin benzodiazepinler ve nöromüsküler blokerler tanımlanabilir.
Etkileri
- Kas gevşeticilerin kas gevşetici özellikleri vardır, yani çizgili iskelet kaslarını gevşetirler ve tonlarını düşürürler.
- Etkiler, merkezi veya periferik sinir sistemindeki ilaç hedefleriyle etkileşime dayanır.
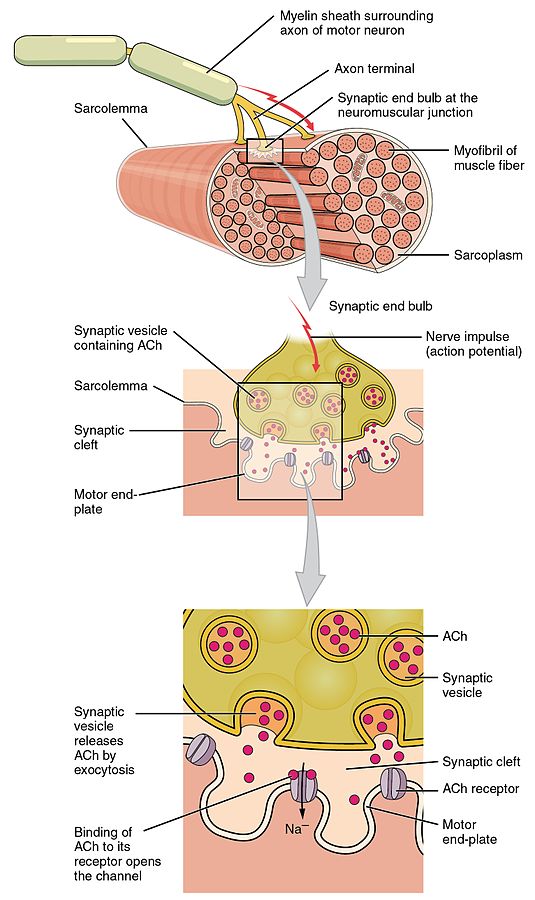
- Bunlara GABA-A reseptörleri, motor uç plakasının nikotinik asetilkolin reseptörleri ve adrenoreseptörler dahildir.
- Kas gevşeticiler de yatıştırıcı (nemlendirici) olabilir.
Aktif içerik
- Baklofen (Lioresal®)
- Barbitüratlar
- Benzodiazepinler
- Botulinum toksini (Botox®)
- Carisoprodol (mevcut değildir)
- Siklobenzaprin ( mevcut değildir)
- Dantrolen (Dantamacrin®, Dantrolen®)
- Guaifenesin (bu endikasyon için onaylanmamıştır)
- Idrocilamid (Talval®, topikal, ticaret hariç)
- Magnezyum (çok sayıda tedarikçi)
- Meprobamat (mevcut değildir)
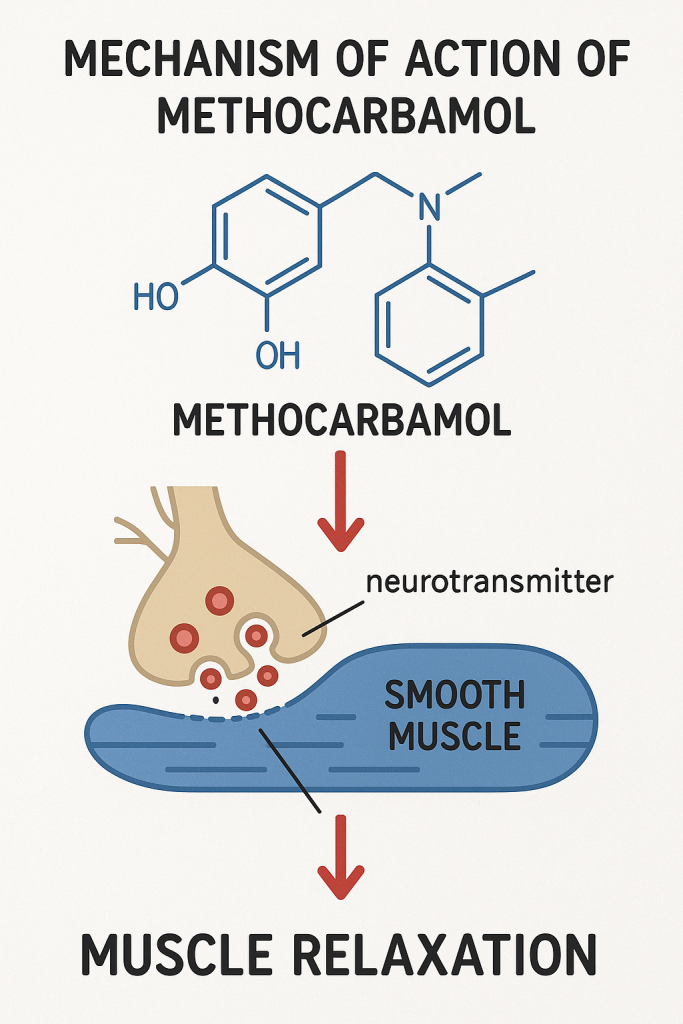
- Metokarbamol (Metoflex®)
- Tolperizon (Mydocalm®)
- Tizanidin (Sirdalud®)
- Nöromüsküler Blokerler:
- Depolarizan ajanlar:
- Suksametonyum klorür (Succinolin®)
- Depolarizan olmayan maddeler:
- Atracurium besilat (Tracrium®)
- Sisatrakuryum besilat (Nimbex®)
- Mivakuryum klorür (Mivacron®)
- Pankuronyum bromür (Pavulon®, ticaret dışı)
- Roküronyum bromür (Esmeron®)
- Vecuronium bromür (Norcuron®, ticaret dışı)
- Depolarizan ajanlar:
Türkiye’de satılan kas gevşetici ilaçlar, içeriğine göre iki ana gruba ayrılabilir:
- Spazm çözücü kas gevşeticiler: Bu ilaçlar, kasların kasılmasını önleyerek çalışır. En yaygın kullanılan spazm çözücü kas gevşeticiler, diazepam, baklofen ve tizanidindir.
- Antiinflamatuar ilaçlar: Bu ilaçlar, iltihaplanmayı azaltarak kas spazmlarını hafifletir. En yaygın kullanılan antiinflamatuar kas gevşeticiler, ibuprofen, diklofenak ve naproksendir.
Türkiye’de satılan bazı kas gevşetici ilaçların marka ve içerikleri şu şekildedir:
Spazm çözücü kas gevşeticiler
- Diazepam: Diazepam, yaygın olarak kullanılan bir benzodiazepin ilaçtır. Kas spazmlarının yanı sıra, anksiyete, uykusuzluk ve titreme gibi durumların tedavisinde de kullanılır.
- Baklofen: Baklofen, merkezi sinir sistemini etkileyerek çalışan bir kas gevşetici ilaçtır. Felç, omurilik yaralanması ve serebral palsi gibi durumların neden olduğu kas spazmlarının tedavisinde kullanılır.
- Tizanidin: Tizanidin, merkezi sinir sistemini etkileyerek çalışan bir kas gevşetici ilaçtır. Omurilik yaralanması, serebral palsi ve multipl skleroz gibi durumların neden olduğu kas spazmlarının tedavisinde kullanılır.
Antiinflamatuar kas gevşeticiler
- Ibuprofen: Ibuprofen, nonsteroidal antiinflamatuar ilaçlar (NSAİİ) grubundan bir ilaçtır. Kas ağrısı, ateş ve iltihaplanmanın tedavisinde kullanılır.
- Diklofenakl: Diklofenakl, NSAİİ grubundan bir ilaçtır. Kas ağrısı, ateş ve iltihaplanmanın tedavisinde kullanılır.
- Naproksen: Naproksen, NSAİİ grubundan bir ilaçtır. Kas ağrısı, ateş ve iltihaplanmanın tedavisinde kullanılır.
Farmakodinamik
Hareket mekanizması
Miyotonolitikler gibi kas gevşeticiler öncelikle kas hücrelerinin sarkoplazmik retikulumundan kalsiyum iyonlarının salınmasını engelleyerek etki gösterir. Bu kas kasılmalarını önler ve böylece kasları gevşetir. Bazı ilaçlar aynı zamanda omurilik veya beyin düzeyinde nörotransmisyonu engelleyerek merkezi olarak da etki eder ve bu da iskelet kaslarını gevşetir.
Sinir Sistemindeki Hedefler
Kas gevşeticiler etkilerini merkezi veya periferik sinir sistemindeki spesifik reseptörleri veya iyon kanallarını hedef alarak gösterirler. Örneğin, popüler bir kas gevşetici olan Baklofen, GABA_B reseptörlerini aktive ederek çalışır, böylece uyarıcı nörotransmitterlerin salınımını engeller.
Tedavi endikasyonları
Bu ilaçlar multipl skleroza bağlı kas spastisitesi, omurilik yaralanmaları veya felç sonrası gibi çeşitli durumlar için endikedir. Ayrıca bel ağrısı gibi kas-iskelet sistemi rahatsızlıklarından kaynaklanan kas spazmlarının tedavisinde de kullanılırlar.
Farmakokinetiği
Emilim
Oral olarak uygulanan kas gevşeticiler genellikle gastrointestinal kanalda emilir. Emilim hızı, midede gıda varlığı ve ilacın spesifik formülasyonu gibi çeşitli faktörlere bağlı olarak değişebilir.
Dağıtım
İlaç emildikten sonra hedef kas dokuları da dahil olmak üzere tüm vücuda dağılır ve merkezi olarak hareket ederse muhtemelen kan-beyin bariyerini geçer. Dağıtım genellikle ilacın dağılım hacmi ve plazma proteinlerine bağlanma afinitesi ile karakterize edilir.
Metabolizma ve Boşaltım
Kas gevşeticilerin metabolizması öncelikle karaciğerde çeşitli enzimatik süreçler yoluyla gerçekleşir. Daha sonra bu metabolitler idrarla atılır. Bir ilacın metabolize edilme ve atılma hızı, dozaj rejimini belirleyen yarı ömrü ile tanımlanır.
Endikasyon
Kas gevşeticilerin tipik uygulama alanları şunlardır:
- İskelet kaslarının ağrılı kas spazmları.
- Sırt ağrısı, lumbago.
- Spastisite, örneğin multipl skleroz, omurilik yaralanmaları ve beyin yaralanmaları nedeniyle.
- Ameliyat ve yoğun bakımda, örneğin entübasyon, ventilasyon ve cerrahi müdahaleler için.
Uzman bilgisine göre dozajlanır. Kas gevşeticiler genellikle oral ve parenteral olarak uygulanır. Bazıları topikal olarak da uygulanabilir.
Kontrendikasyonlar
Tüm ihtiyati tedbirler, sağlık uzmanlarına yönelik bilgilerde bulunabilir.
Etkileşimler
Birçok kas gevşetici, CYP450 izoenimleri ile etkileşime girer. Depresan etkileri nedeniyle santral depresan ilaçlar ve alkol ile birlikte kullanılmamalıdır.
Istenmeyen etkiler
- Kas gevşeticilerin tipik yan etkileri yorgunluk, uyuşukluk, baş dönmesi, merkezi rahatsızlıklar ve gastrointestinal rahatsızlıklardır. Bu nedenle, birçok temsilcinin araç kullanma yeteneği üzerinde olumsuz bir etkisi vardır.
- Benzodiazepinler yüksek bir bağımlılık potansiyeline sahiptir.
Tarih
Kas gevşetici ilaçların bilinen en eski kullanımı, iskelet kası felci nedeniyle ölüme neden olan zehirli uçlu okları kullanan Güney Amerika’daki Amazon Havzası yerlileri tarafından yapıldı. Bu ilk kez 16. yüzyılda Avrupalı kaşiflerin karşılaştığı belgelendi. Bugün kürar olarak bilinen bu zehir, farmakolojideki ilk bilimsel çalışmalardan bazılarına yol açmıştır. Aktif bileşeni olan tubokurarinin yanı sıra birçok sentetik türev, asetilkolinin nöromüsküler iletimdeki işlevini belirlemek için yapılan bilimsel deneylerde önemli bir rol oynamıştır.
1942’de Harold Randall Griffith ve onun asistanı Enid Johnson, Montreal’deki Homeopatik Hastanesi’nde apendektomi geçiren genç bir hastaya küratör uyguladılar. Bu, anestezide kas gevşemesi için NMBA kullanımında ilk büyük adım olarak kabul edildi. Griffith’in çalışması, kas gevşeticilerin ameliyatlarda ve diğer tıbbi prosedürlerde yaygın olarak kullanılmasının önünü açmaya yardımcı oldu.
- 1596 yılında İngiliz kaşif Sir Walter Raleigh, kürarı ilk kez “Guiana’nın Büyük, Zengin ve Güzel İmparatorluğunun Keşfi” adlı kitabında tanımladı. Yerlilerin oklarını ve dartlarını zehirlemek için kürarı nasıl kullandıklarını yazdı.
- 1800’lerin başında Alman doğa bilimci Alexander von Humboldt, Güney Amerika’ya seyahat etti ve yerli halk tarafından kürar üretimine tanık oldu. İlacın özelliklerine hayran kaldı ve daha fazla araştırma için numuneleri Avrupa’ya geri getirdi.
- 1844’te Fransız fizyolog Claude Bernard, kürarın nöromüsküler iletim üzerindeki etkileri üzerine bir makale yayınladı. Curare’in sinir uyarılarının kaslara iletimini engellediğini gösteren ilk kişi oydu.
- 1935 yılında İngiliz farmakolog Harold King, kürarın aktif maddesi olan tubokurarini izole etti. Bu, daha öngörülebilir etkileri ve daha az yan etkisi olan sentetik kas gevşeticilerin geliştirilmesini mümkün kıldı.
- İkinci Dünya Savaşı sırasında her iki taraf da yaralı askerleri tedavi etmek için kas gevşeticiler kullanıyordu. Müttefikler kas spazmlarını ve tetanozu tedavi etmek için kürar kullanırken, Almanlar anestezi olmadan ameliyata alınan hastaları felç etmek için sentetik kas gevşeticiler kullanıyordu.
Modern Kas Gevşeticiler
Günümüzde kas gevşeticiler ameliyat, anestezi, yoğun bakım ve fizik tedavi gibi çeşitli tıbbi ortamlarda kullanılmaktadır. Ayrıca kas spazmları, spastisite ve ağrı gibi çeşitli durumların tedavisinde de kullanılırlar.
- Nöromüsküler bloke edici ajanlar: Bu ilaçlar sinir uyarılarının kaslara iletilmesini bloke ederek felce neden olur. Cerrahların gevşemiş kaslar üzerinde çalışmasına olanak sağlamak için ameliyatta kullanılırlar.
- Merkezi kas gevşeticiler: Bu ilaçlar merkezi sinir sistemini baskılayarak çalışır, bu da kas spazmlarını ve spastisiteyi azaltabilir. Multipl skleroz, serebral palsi ve omurilik yaralanmaları gibi çeşitli durumların tedavisinde kullanılırlar.
- İskelet kası gevşeticiler: Bu ilaçlar doğrudan kaslar üzerinde çalışarak kas spazmlarını ve ağrısını azaltır. Genellikle sırt ağrısı, boyun ağrısı ve fibromiyalji gibi durumların tedavisinde kullanılırlar.
- Kas gevşeticiler ağızdan alınabilir, enjekte edilebilir veya topikal olarak uygulanabilir. Kullanılan kas gevşetici türü ve onu almanın en iyi yolu, hastaya ve durumuna bağlı olacaktır.
Kaynak:
- Pinder, R. M., Brogden, R. N., Speight, T. M., & Avery, G. S. (1977). Dantrolene: A review of its pharmacological properties and therapeutic efficacy in spasticity. Drugs, 13(1), 3-23.
- Smith, H. S. (2009). Skeletal muscle relaxants. In Pharmacotherapy Pain (pp. 191-194). Springer, New York, NY.
- Rosenberg, A. D., & Bettini, L. (2007). Muscle relaxants and postoperative pain. Journal of PeriAnesthesia Nursing, 22(1), 10-12.
- Adeyinka A, Layer DA. Neuromuscular Blocking Agents. In: StatPearls. Treasure Island (FL): StatPearls Publishing; 2023 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK537168/
- Pinder, R. M., Brogden, R. N., Speight, T. M., & Avery, G. S. (1977). Dantrolene: A review of its pharmacological properties and therapeutic efficacy in spasticity. Drugs, 13(1), 3-23.
- VandenBerg, T. M. (2004). Pharmacokinetics and pharmacodynamics of the benzodiazepine muscle relaxants. Journal of Clinical Pharmacology, 44(1), 7-15.
- Vinkers, C. H., & Olivier, B. (2012). Mechanisms Underlying Tolerance after Long-Term Benzodiazepine Use: A Future for Subtype-Selective GABA(A) Receptor Modulators? Advances in Pharmacological Sciences, 2012, 416864.










Yorum yazabilmek için oturum açmalısınız.