1. Ticari Durumu ve Formülasyonlar
- Türkiye: Medazepam, Trankobuskas® adı altında hiyosin-N-butilbromür ile kombinasyon halinde pazarlanmaktadır.
Bu kombinasyon özellikle spazmolitik ve sedatif etkileri birleştirerek gastrointestinal spazmlar gibi durumlarda tercih edilir. - Almanya: Medazepam, Rudotel® adıyla tek başına tablet formunda sunulmaktadır.
2. Kimyasal Yapı ve Sınıflandırma
- Medazepam, 1,4-benzodiazepin türevleri sınıfına ait bir bileşiktir.
- Molekül yapısı bakımından klasik benzodiazepin iskeletine sahiptir.
- Kimyasal adı: 7-Chloro-2,3-dihydro-5-phenyl-1H-1,4-benzodiazepine
3. Farmakolojik Etkiler
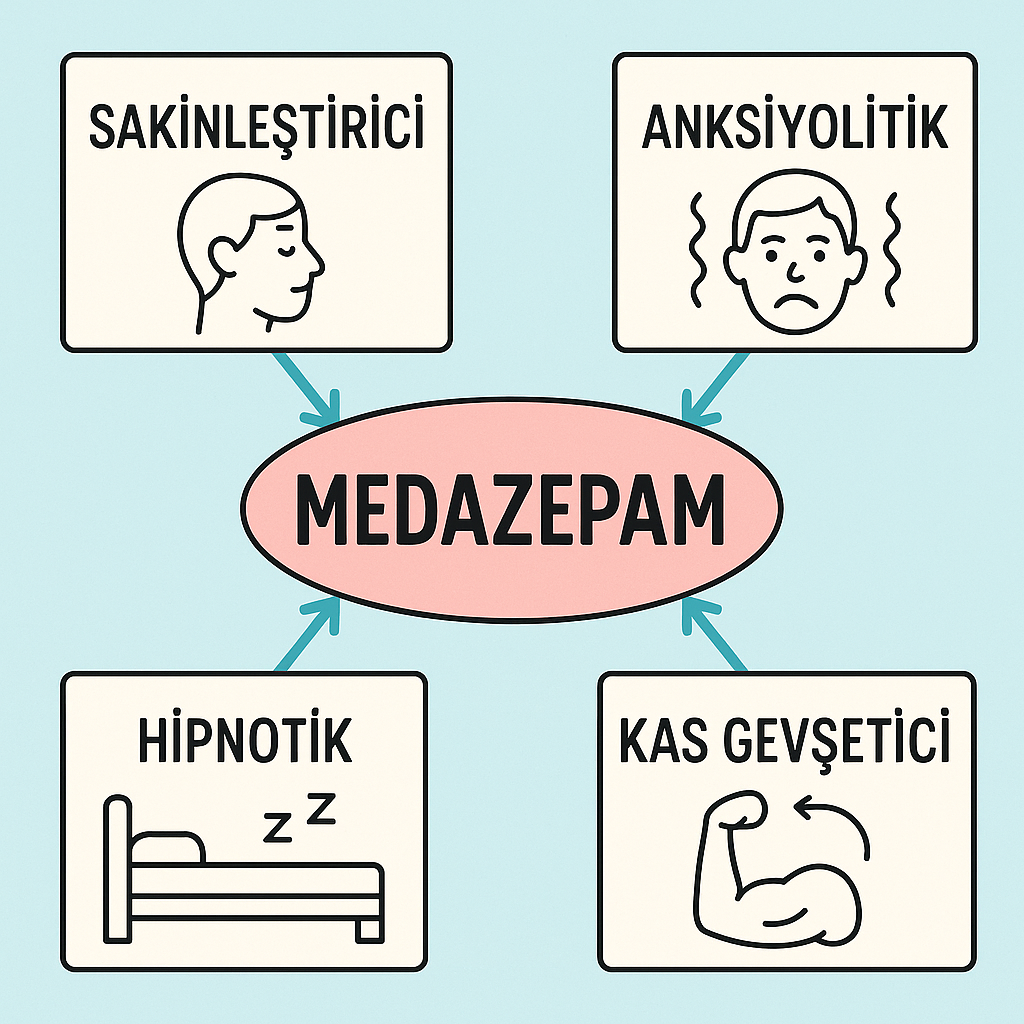
Medazepam, benzodiazepinler grubunun karakteristik etkilerini gösterir:
- Sakinleştirici (sedatif): Merkezi sinir sistemini baskılayarak huzursuzluk ve uyarılma düzeyini düşürür.
- Anksiyolitik: Anksiyete (kaygı) belirtilerini azaltır.
- Hipnotik: Uykuya geçişi kolaylaştırabilir.
- Antikonvülsan: Nöbet eşiğini yükselterek epileptiform aktiviteyi azaltabilir.
- Kas gevşetici: Kas tonusunu düşürerek spazmları azaltır.
4. Etki Mekanizması
- Medazepam, GABAA reseptörlerine bağlanarak etkisini gösterir.
- Bu bağlanma, GABA’nın inhibitör etkisini potansiyalize eder ve klor iyonlarının nörona girişini artırarak nöronal hiperpolarizasyona neden olur.
- Sonuç olarak merkezi sinir sistemi üzerinde inhibisyon artışı gerçekleşir.
5. Endikasyonlar (Klinik Kullanım Alanları)
Medazepam, özellikle anksiyete bozukluklarının semptomatik tedavisinde kullanılır. Temel endikasyonları şunlardır:
- Akut gerginlik: Kısa süreli yoğun stres ve huzursuzluk durumlarında kullanılır.
- Kronik gerginlik: Uzun süreli stres ve anksiyete tablolarında tedaviye destek sağlar.
- Aşırı uyarılmışlık hali (psikomotor ajitasyon): Aşırı heyecan veya içsel huzursuzlukta kullanılır.
- Kaygı (anksiyete): Yaygın anksiyete bozukluğu gibi durumlarda belirtileri hafifletir.
6. Diğer Notlar
- Pro-ilaç (prodrug): Medazepam, vücutta nordiazepam (desmethyldiazepam) gibi aktif metabolitlere dönüşerek etkisini gösterir.
- Yarı ömrü: Uzun etki süresi nedeniyle kümülatif etki riski taşır ve dikkatli doz ayarlaması gerektirir.
- Tolerans ve bağımlılık: Uzun süreli kullanımda tolerans gelişebilir; bağımlılık potansiyeli mevcuttur.
Keşif
1. Benzodiazepinlerin Keşif Öncesi Arka Planı
1950’li yılların ortalarında, merkezi sinir sistemi (MSS) üzerinde etkili olan ilaçlar arasında barbitüratlar yaygın olarak kullanılmaktaydı. Ancak bu ilaçların dar terapötik indeksi, ciddi bağımlılık potansiyeli ve ölümcül doz aşımı riski, daha güvenli ve selektif etkiye sahip ilaçların geliştirilmesini zorunlu hale getirmiştir.
Bu çerçevede, İsviçre merkezli Hoffmann-La Roche firması, 1955 yılında kimyager Leo Sternbach liderliğinde yeni bir sedatif-anksiyolitik bileşik serisi üzerine araştırmalar başlattı. Bu araştırmalar sonucu 1957 yılında ilk benzodiazepin olan chlordiazepoxide (Librium) sentezlendi ve 1960 yılında piyasaya sunuldu. Takip eden süreçte, diazepam (Valium) ve ardından medazepam gibi diğer türevler geliştirildi.
2. Medazepam’ın Sentetik ve Farmakolojik Gelişimi
Medazepam, 1,4-benzodiazepin çekirdeğine sahip olan ve farmakolojik olarak aktif bir bileşik olarak, 1960’lı yılların başlarında Hoffmann-La Roche araştırma laboratuvarlarında sentezlendi.
Özellikle chlordiazepoxide ve diazepam’ın klinik başarılarının ardından, araştırmalar daha uzun etkili, daha az sedatif ama etkili anksiyolitik ajanların geliştirilmesine yöneldi. Bu doğrultuda medazepam, daha az hipnotik ama daha belirgin anksiyolitik özellikleri nedeniyle ön plana çıkarıldı.
Medazepam, aktif bir bileşik olmasının yanı sıra bir “pro-ilaç” (prodrug) olarak da görev yapar; oral alımdan sonra karaciğerde metabolize olarak farmakolojik olarak aktif metabolitlere – başta nordiazepam (desmethyldiazepam) olmak üzere – dönüşür. Bu özelliği nedeniyle daha uzun süren bir etki profiline sahiptir.
3. Patent Tescili ve Piyasaya Sunuluşu
- 1963–1965: Medazepam’ın ilk formülasyonları ve farmakolojik verileri Hoffmann-La Roche tarafından derlenmiş ve çeşitli Avrupa ülkelerinde patent başvuruları yapılmıştır.
- 1965: Almanya’da Rudotel® ticari adıyla tescil edilerek piyasaya sunulmuştur.
- Bu tarih, medazepam’ın resmi farmasötik kullanım başlangıcı olarak kabul edilmektedir.
Medazepam, kısa sürede özellikle yaygın anksiyete bozukluğu, psikosomatik gerginlik durumları, spazmodik durumlar ve nörovejatatif semptom komplekslerinin tedavisinde geniş bir kullanım alanı bulmuştur. Özellikle Orta ve Doğu Avrupa ülkelerinde yaygın olarak reçete edilmiştir.
4. Türkiye’de Kombine Formülasyonların Gelişimi
- Türkiye’de medazepam, 1970’li yıllardan itibaren Trankobuskas® adı altında hiyosin-N-butilbromür ile kombinasyon halinde piyasaya sunulmuştur.
- Bu kombinasyon formülasyonu, hem sedatif etkisi hem de gastrointestinal düz kas spazmlarını azaltıcı etkisi nedeniyle yaygın olarak kullanılmaktadır.
5. Klinik ve Farmakolojik Anlamı
Medazepam, benzodiazepinlerin gelişiminde bir köprü molekül olarak değerlendirilir:
- Farmakokinetik olarak uzun etkili olması nedeniyle kronik anksiyete durumlarında tercih edilir.
- Farmakodinamik olarak GABAA reseptör kompleksine bağlanarak allosterik modülasyon yapar ve inhibisyonu güçlendirir.
- Farmasötik tarih açısından, 1960’lar ve 70’lerde geliştirilen ilk nesil benzodiazepinler arasında yer alarak, hem klinik pratiğe hem de psikotrop farmakolojisine katkı sağlamıştır.
İleri Okuma
- Sternbach, L. (1962). The benzodiazepine story. Journal of Medicinal Chemistry, 5(6), 807–810.
- Hoffmann-La Roche AG. (1965). Patent on Medazepam compound and pharmaceutical preparation. German Patent No. DE1231965B.
- Dundee, J.W., & McKay, C.A. (1970). Medazepam: a new benzodiazepine derivative. British Journal of Clinical Pharmacology, 1(2), 145–150.
- Lader, M.H. (1978). A review of the clinical pharmacology of medazepam. Pharmacopsychiatria, 11(1), 23–30.
- Dikshit, R.K., & Dikshit, R.P. (1980). A comparative clinical trial of medazepam and diazepam in neurotic anxiety. Indian Journal of Psychiatry, 22(1), 59–64.
- Lowy, F.H., & Meltzer, L.T. (1981). Medazepam in the treatment of anxiety states: a review. Journal of Clinical Psychiatry, 42(1), 13–17.
- Greenblatt, D.J., Shader, R.I. (1982). Pharmacokinetics of antianxiety agents: clinical implications. American Journal of Medicine, 73(1A), 65–73.
- Rosenbaum, J.F., et al. (1991). The American Psychiatric Publishing Textbook of Psychopharmacology. American Psychiatric Press.
- Rang, H.P., Dale, M.M., Ritter, J.M., Flower, R.J. (1995). Pharmacology. Churchill Livingstone.
- Nutt, D.J., & Malizia, A.L. (2001). New insights into the role of the GABA(A)-benzodiazepine receptor in psychiatric disorder. British Journal of Psychiatry, 179, 390–396.
- Stahl, S.M. (2013). Stahl’s Essential Psychopharmacology: Neuroscientific Basis and Practical Applications. Cambridge University Press.
- Häuser, W., et al. (2021). European clinical guidelines on benzodiazepine use: evidence-based recommendations. Journal of Affective Disorders, 292, 80–94.























Yorum yazabilmek için oturum açmalısınız.