“Diapedesis” terimi Yunanca kelimelerden türetilmiştir:
- “διά” (dia), “içinden” veya “üzerinden” anlamına gelir.
- “πήδησις” (pēdēsis), “sıçrama” ya da “atlama” anlamına gelir.
Dolayısıyla, diapedesis kelimenin tam anlamıyla “sıçramak” veya “atlamak” anlamına gelir ve kılcal damar duvarının endotel hücrelerini sıkıştıran veya “sıçrayan” beyaz kan hücrelerinin eylemini yansıtır.
Diapedez, immün yanıt sırasında, başta nötrofiller ve monositler olmak üzere beyaz kan hücreleri enfeksiyon veya yaralanma bölgesine göç ettiğinde meydana gelir. Bu süreç birkaç adımdan oluşur:
- Kenarlaşma: Lökositler kan damarlarının kenarlarına doğru hareket eder.
- Yapışma: Lökositler kan damarı duvarlarını kaplayan endotel hücrelerine yapışır.
- Transmigrasyon (diapedez): Lökositler kan dolaşımından çıkmak ve dokuya girmek için endotel hücreleri arasında sıkışır.
Diyapedez, beyaz kan hücrelerinin (lökositler) kan dolaşımından çıkıp enfeksiyonlarla savaşmak, hasarlı hücreleri uzaklaştırmak ve bağışıklık tepkilerini başlatmak için çevre dokulara girmesini sağlayan önemli bir fizyolojik süreçtir. Bu süreç vücudun immün savunmasının ve inflamatuar yanıtın önemli bir parçasıdır ve bağışıklık sisteminin enfeksiyon veya yaralanma alanlarını hedef almasına yardımcı olur.
İçindekiler
1. Diapedezise Genel Bakış
Diapedez özellikle lökositlerin (nötrofiller, monositler ve lenfositler gibi) kılcal damarların ve venüllerin duvarlarından dokulara doğru hareketini ifade eder. Tipik olarak, patojenlerle mücadele etmek veya doku hasarını onarmak için lökositlere ihtiyaç duyulan iltihaplanma bölgelerinde meydana gelir. Hücreler, kan damarlarının endotelyal astarından yüksek oranda düzenlenmiş bir şekilde, damara zarar vermeden hareket eder.
2. Diyapedezin Adımları
Diapedez süreci, lökosit aktivasyonu, yuvarlanan yapışma, sağlam yapışma ve transmigrasyon gibi iyi koordine edilmiş birkaç aşamada gerçekleşir. Bu aşamalar, enfeksiyon veya yaralanma bölgesinde hücreler tarafından salınan kemokinler ve sitokinler gibi sinyal molekülleri tarafından düzenlenir.
a. Kemoatraksiyon
Süreç, enfeksiyon veya doku hasarı bölgesinde inflamatuar sinyaller salındığında başlar. Bu sinyaller hasarlı hücreler, patojenler veya diğer bağışıklık hücreleri tarafından üretilen kemokinleri ve sitokinleri içerir. Bu kimyasal sinyaller, lökositleri etkilenen bölgeye çeken bir gradyan oluşturur. Kan dolaşımında akan beyaz kan hücreleri bu sinyalleri algılar ve enfeksiyon bölgesine doğru yönlendirilir.
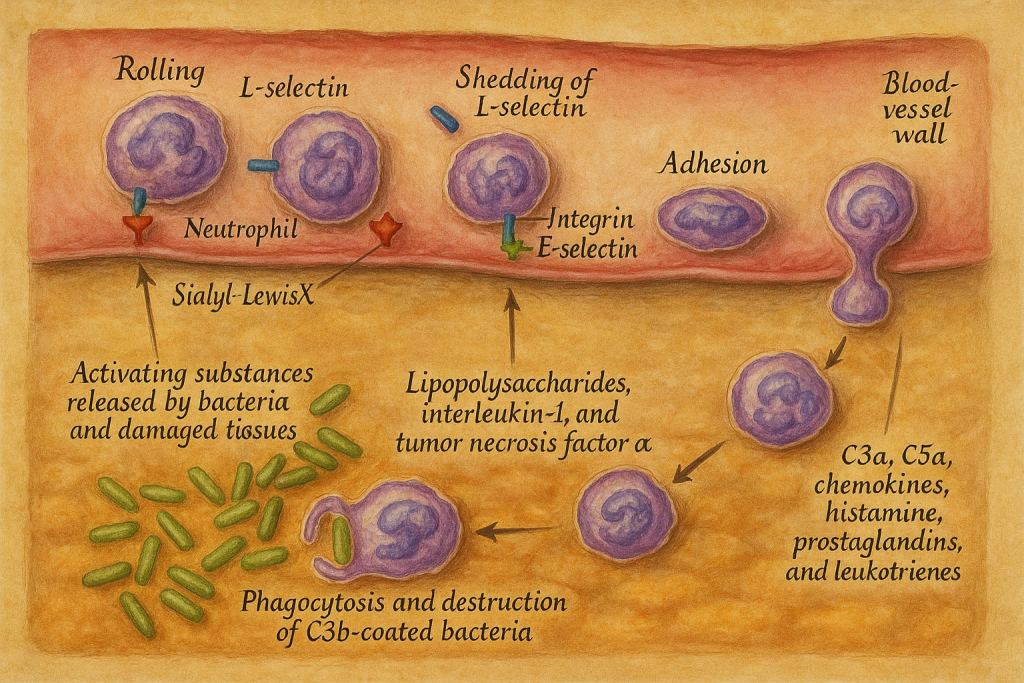
b. Marjinasyon ve Yuvarlanma
Lökositler başlangıçta kan damarlarının merkezinde serbestçe akar. Enflamatuar sinyallere yanıt olarak, beyaz kan hücreleri kan damarının çevresine doğru hareket eder (marjinasyon adı verilen bir süreç) ve damarı kaplayan endotel hücrelerine yaklaşır.
Endotel hücrelerine yaklaştıkça, lökositler yuvarlanma yapışması adı verilen bir sürece başlarlar. Bu aşamada, endotel hücrelerinin yüzeyindeki selektin molekülleri lökositler üzerindeki selektin reseptörlerine gevşek bir şekilde bağlanır. Bu bağlanma lökositlerin yavaşlamasına ve kan damarı yüzeyi boyunca “yuvarlanmasına” neden olur.
c. Sıkı Yapışma
Lökositler endotel boyunca yuvarlandıkça, daha güçlü inflamatuar sinyallerle aktive olurlar. Bu sinyaller lökositlerin yüzeyindeki integrinleri (yapışma proteinleri) aktive eder ve bunlar daha sonra endotel hücrelerindeki integrin reseptörlerine (ICAM-1 ve VCAM-1 gibi) sıkıca bağlanır.
Bu bağlanma, lökositlerin endotel yüzeyine sıkıca yapışmasını sağlayarak kan dolaşımındaki hareketlerini durdurur. Bu noktada, damar duvarından geçmeye hazırdırlar.
d. Transmigrasyon (Diapedez)
Lökositler endotel hücrelerine sıkıca bağlandıktan sonra, diapedez olarak da adlandırılan transmigrasyon sürecine başlarlar. Bu aşama sırasında:
- Lökositler kan damarı duvarının endotel hücreleri arasında sıkışır.
- Endotel hücrelerinin altındaki bir hücre dışı matris tabakası olan taban zarından geçerler.
Bu adım endotel hücrelerine veya kan damarı yapısına zarar vermeden gerçekleşir. Lökositler, paraselüler veya transselüler göç adı verilen bir süreç kullanarak endotel hücreleri arasındaki boşluklardan veya bazen endotel hücrelerinin kendisinden geçer.
e. Doku İçine Göç
Diapedezden sonra lökositler, kendilerini enfeksiyon veya yaralanma bölgesine yönlendiren kemokin gradyanları tarafından yönlendirilen çevre dokuya girer. Dokuya girdikten sonra, aşağıdakileri içerebilen bağışıklık işlevlerini yerine getirirler:
- Fagositoz**: Patojenleri yutmak ve sindirmek (nötrofiller ve makrofajlar söz konusu olduğunda).
- Sitokin salınımı**: Diğer bağışıklık hücrelerine enfeksiyon bölgesine sinyal gönderme.
- Enfekte veya hasarlı hücrelerin öldürülmesi**: Bu, sitotoksik T hücreleri veya doğal öldürücü hücreler gibi spesifik bağışıklık hücreleri tarafından gerçekleştirilir.
3. Diyapedezdeki Kilit Oyuncular
Çeşitli moleküller ve hücreler diapedezde kritik rol oynar:
- Endotel Hücreleri**: Kan damarlarının iç duvarlarını kaplar ve hücrelerin kan dolaşımından dokulara geçişini düzenler. Lökositlerin yuvarlanmasını, yapışmasını ve transmigrasyonunu kolaylaştıran *selektinler*, *integrinler* ve diğer adezyon moleküllerini eksprese ederler.
- Lökositler (Beyaz Kan Hücreleri)**: Nötrofiller, monositler, lenfositler ve diğerlerini içerir. Bağışıklık tepkileri için gereklidirler ve kan dolaşımından çıkmak ve enfeksiyon veya iltihap bölgelerine ulaşmak için diapedezi kullanırlar.
- Kemokinler ve Sitokinler: Enfeksiyon veya yaralanma bölgesinde salınan sinyal molekülleri. Bu moleküller lökositleri bölgeye çeker ve lökositlerin yüzeyindeki integrinleri aktive ederek sıkı bir yapışma sağlar.
- Selektinler ve İntegrinler**: Yuvarlanma ve yapışma aşamaları sırasında lökositler ve endotel hücreleri arasındaki etkileşime aracılık eden yapışma molekülleri. Selektinler yuvarlanmayı başlatırken, integrinler sıkı yapışma oluşturur.
4. Bağışıklık Yanıtında Diapedezin Önemi
Diapedez immün gözetim ve inflamasyon için gereklidir. Beyaz kan hücrelerinin ihtiyaç duyulan bölgelere hızla ulaşmasını sağlayarak bağışıklık sisteminin patojenlere, hasarlı dokulara veya enfeksiyona yanıt verebilmesini sağlar.
- Akut Enflamasyon**: Diapedez özellikle enflamasyonun erken aşamalarında önemlidir. Örneğin, bakteriyel enfeksiyonlar sırasında, *nötrofiller* istilacı mikroplarla savaşmak için kan damarlarından göç eden ilk yanıtlayıcılar arasındadır.
- Kronik Enflamasyon**: Otoimmün hastalıklar (örneğin, *romatoid artrit*) gibi kronik inflamasyon vakalarında, diapedez uzun bir süre boyunca meydana gelebilir, bu da aşırı ve potansiyel olarak zararlı bir bağışıklık tepkisine yol açabilir.
- Yara İyileşmesi**: Doku hasarı bölgelerine göç eden beyaz kan hücreleri, ölü hücrelerin ve döküntülerin temizlenmesinde de rol oynayarak doku onarımını ve iyileşmesini destekler.
5. Klinik Önem
- Bağışıklık Bozuklukları**: Kusurlu diapedez, bağışıklık tepkilerinin bozulmasına neden olarak vücudu enfeksiyonlara karşı savunmasız bırakabilir. Örneğin, *Lökosit Adezyon Eksikliği (LAD)* gibi durumlarda, integrin moleküllerindeki mutasyonlar lökosit adezyonunu ve migrasyonunu bozarak tekrarlayan enfeksiyonlara yol açar.
- Kronik Enflamasyon ve Otoimmünite**: Aşırı aktif diapedez, bağışıklık hücrelerinin sürekli olarak sağlıklı dokulara göç ettiği ve hasara neden olduğu kronik enflamatuar durumlara ve otoimmün hastalıklara katkıda bulunabilir.
- Terapötik Hedefler**: Diapedesis, *astım*, *soriasis* ve multipl skleroz gibi aşırı inflamasyonla karakterize hastalıklarda terapötik müdahale için potansiyel bir hedeftir. İntegrinler gibi lökosit göçünde rol oynayan spesifik molekülleri bloke eden ilaçlar, bu koşulların bazılarını tedavi etmek için geliştirilmiştir.
Keşif
Beyaz kan hücrelerinin (lökositlerin)** kan dolaşımından kan damarlarının duvarları yoluyla çevre dokulara hareketi olan diapedezin fizyolojik süreci, immünoloji ve vasküler biyolojinin daha geniş gelişimine dayanan büyüleyici bir geçmişe sahiptir. Diapedez vücudun bağışıklık tepkisi için çok önemlidir ve lökositlerin enfeksiyon veya yaralanma bölgelerine ulaşmasını sağlar. Mikroskopi, hücre biyolojisi ve immünolojideki ilerlemelerle yakından bağlantılı olarak yüzyıllar boyunca gelişmiştir.
1. Kan ve Bağışıklığa İlişkin İlk Gözlemler (17.-18. Yüzyıl)
Diyapedezi** anlamaya yönelik yolculuk, kan ve kan damarlarına ilişkin ilk gözlemlerle başlamıştır. 17. yüzyılda**, *William Harvey* kan dolaşımını keşfederek tıp alanında devrim yarattı. Kanın kapalı bir damar sistemi içinde hareket ettiğini göstererek, kan hücrelerinin damar duvarlarıyla nasıl etkileşime girdiğini incelemenin temelini attı.
Bu dolaşım anlayışına rağmen, beyaz kan hücrelerinin enfeksiyon veya iltihap bölgelerine ulaşmak için kan dolaşımından nasıl çıktığı henüz bilinmiyordu. Aslında, beyaz kan hücrelerinin kendileri de henüz bağışıklık tepkisinin kilit oyuncuları olarak kabul edilmiyordu. Bu dönemde kan üzerine yapılan çalışmalar öncelikle kırmızı kan hücrelerine ve genel dolaşıma odaklanmış, lökosit davranışının daha ince ayrıntıları keşfedilmemişti.
2. Beyaz Kan Hücrelerinin Keşfi (19. Yüzyıl)
Diyapedezin anlaşılmasında önemli bir dönüm noktası 19. yüzyılda Fransız bilim insanı Gabriel Andral ve Alman doktor Rudolf Virchow tarafından beyaz kan hücrelerinin keşfedilmesiyle yaşandı. Andral, 1843 yılında kan dolaşımındaki beyaz kan hücrelerini ilk tanımlayanlardan biri olmuş, kırmızı kan hücrelerinden farklı olduklarını ve muhtemelen vücudun savunma mekanizmalarında rol oynadıklarını belirtmiştir. Aynı dönemde Virchow da kandaki beyaz kan hücrelerini gözlemledi ve bunları enflamatuar süreçlerle ilişkilendirmeye başladı.
Bu döneme ait en ünlü anekdotlardan biri, beyaz kan hücrelerinin iltihaplı dokularda biriktiğine dair kritik gözlemi yapan Virchow ile ilgilidir. Bu gözlem, bu hücrelerin enfeksiyon veya yaralanma bölgesine nasıl ulaştığına dair sorulara yol açtı. Virchow’un beyaz kan hücrelerinin vücudu hastalıklara karşı korumada rol oynayabileceği hipotezi, bağışıklık yanıtı çalışmalarının başlangıcına işaret etse de, bu hücrelerin kandan dokuya nasıl gittiğine dair mekanizma belirsizliğini koruyordu.
3. Çığır Açan Buluş: Diapedezin Gözlenmesi (19. Yüzyılın Sonları)
Diyapedezin** anlaşılmasındaki kesin atılım 1863 yılında Alman patolog ve Virchow’un eski öğrencisi Julius Cohnheim kurbağalarda inflamasyon üzerinde çalışırken önemli bir keşif yaptığında gerçekleşti. Cohnheim, kan damarlarını gözlemlemek için mikroskopi kullanarak, beyaz kan hücrelerinin iltihaplı dokulara ulaşmak için kılcal damarların duvarlarından geçtiğini gördü. Bu devrim niteliğinde bir keşifti, çünkü beyaz kan hücrelerinin kan dolaşımından çıkış süreci ilk kez doğrudan gözlemlenmişti.
Cohnheim’ın deneyleri, kurbağanın perdeli ayağı veya kemirgenlerin mezenterleri gibi şeffaf dokuları mikroskop altına yerleştirmeyi içeriyordu. Dokuya hafifçe iğne batırarak ya da tahriş edici maddeler uygulayarak lokalize iltihap oluşturdu ve kan hücrelerinin davranışını gözlemledi. Şaşırtıcı bir şekilde, lökositlerin kan damarlarının iç duvarlarına yapıştığını, kendilerini düzleştirdiklerini ve daha sonra endotel hücreleri arasındaki küçük boşluklardan sıkıştıklarını gördü – şimdi diapedesis olarak bildiğimiz bir süreç.
Bu keşif, bağışıklık sisteminin vücudu patojenlere karşı savunmak için beyaz kan hücrelerini nasıl harekete geçirdiğine dair ilk görsel kanıtı sağladı. Cohnheim’ın çalışması, beyaz kan hücrelerinin kan damarlarından dışarı göç edebileceğini ve bağışıklık tepkilerine aktif olarak katılabileceğini doğrulayarak iltihaplanma ve bağışıklık gözetimi anlayışını temelden değiştirdi.
4. Hücresel Biyolojideki Gelişmeler: Diyapedez Mekanizmaları (20. Yüzyılın Başları)
- yüzyılın başlarında**, daha sofistike mikroskopi ve boyama tekniklerinin ortaya çıkmasıyla, bilim insanları diapedezin altında yatan *hücresel mekanizmaları* daha derinlemesine araştırmaya başladılar. Bu dönemin kilit isimlerinden biri, beyaz kan hücrelerinin patojenleri yutma ve sindirme süreci olan fagositoz üzerine yaptığı çalışmalarla 1908 yılında Nobel Ödülü kazanan Rus immünolog Élie Metchnikoff idi.
Metchnikoff’un lökositlerin yabancı istilacıları nasıl tanıdığı ve onlara nasıl tepki verdiği konusundaki araştırması, Cohnheim’ın daha önceki diapedesis keşfini tamamlamıştır. Metchnikoff, beyaz kan hücrelerinin, özellikle de fagositlerin, hasarlı dokulardan gelen kimyasal sinyalleri algılayarak enfeksiyon veya yaralanma bölgesine göç ettiklerini öne sürdü; bu süreç daha sonra kemotaksis olarak adlandırıldı. Bu sinyaller lökositleri etkilenen bölgeye yönlendirdi ve burada diapedez yoluyla endotelyal bariyeri geçtiler.
Metchnikoff’un kariyerinden ünlü bir anekdot, bağışıklık hücrelerinin yabancı bir cisme doğru hareketini ilk kez gözlemlediği denizyıldızı larvaları üzerindeki ilk deneylerini içerir ve bağışıklık sistemi üzerine yaşam boyu çalışmasını ateşler. Beyaz kan hücrelerinin patojenleri aktif olarak arayıp yok ettiğine dair teorisi, bağışıklık tepkisinde diapedezin önemini pekiştirmiştir.
5. Moleküler Dönem: Yapışma Moleküllerinin Keşfi (20. Yüzyılın Sonları)
Hücre biyolojisi ilerledikçe, 20. yüzyılın sonları diyapedezin moleküler mekanizmalarını anlamada büyük atılımlar getirdi. 1980’lerde ve 1990’larda araştırmacılar, beyaz kan hücreleri ile kan damarlarını kaplayan endotelyal hücreler arasındaki etkileşime aracılık eden spesifik adhezyon moleküllerini tanımladılar.
Bu dönemdeki en önemli keşiflerden biri, lökosit adezyonu ve transmigrasyonunda kritik rol oynayan proteinler olan selektinler ve integrinlerin tanımlanmasıydı. Endotel hücrelerinin yüzeyindeki Selektinler lökositlerin damar duvarı boyunca “yuvarlanmasına ‘ izin verirken, lökositler üzerindeki integrinler endotel hücreleri üzerindeki ICAM-1 ve VCAM-1’e bağlanarak sıkı yapışmayı kolaylaştırır. Lökositler damar duvarına yapıştıktan sonra, endotel hücreleri arasındaki bağlantılardan veya bazı durumlarda hücrelerin kendilerinden geçerek diapedezise uğrarlar.
Bu döneme ait önemli bir hikâye, Harvard Üniversitesi’nde immünolog olan Tim Springer’ın 1990 yılında, bağışıklık tepkisi sırasında lökositlerin endotel hücrelerine sıkıca yapışması için çok önemli bir molekül olan LFA-1 integrinini keşfeden araştırmasını içermektedir. Springer’in çalışması, Cohnheim’ın orijinal gözlemlerine kritik ayrıntılar ekleyerek, diapedezdeki yuvarlanma-adhezyon-transmigrasyon olay dizisinin açıklanmasında etkili olmuştur.
Springer’in araştırması, inflamatuar hastalıklar ve otoimmün bozuklukları tedavi etmek için yeni terapötik yaklaşımların geliştirilmesinin temelini atmıştır. Bu adezyon moleküllerini hedef alarak, bağışıklık tepkisini modüle etmek ve romatoid artrit ve multipl skleroz gibi durumlarda zararlı iltihaplanmayı azaltmak mümkün hale geldi.
6. Klinik Alaka: Hastalık ve Tedavide Diyapedez (21. Yüzyıl)
- yüzyılda** diapedez, özellikle inflamatuar hastalıklar, kanser ve otoimmünite bağlamında immünoloji araştırmalarının merkezi bir odağı olmaya devam etmektedir. Genetik mutasyonların lökositlerin kan damarlarına yapışma ve damarlardan geçme yeteneğini bozduğu lökosit yapışma eksikliği (LAD) gibi bozukluklar, etkili bağışıklık fonksiyonu için diapedezin önemini vurgulamaktadır. LAD hastaları, beyaz kan hücreleri kan dolaşımından çıkıp enfekte dokulara ulaşamadığı için tekrarlayan enfeksiyonlardan muzdariptir.
Modern araştırmalar ayrıca tümör hücrelerinin metastaz yapmak ve uzak organlara yayılmak için diapedez sürecini nasıl taklit ettiğini de araştırmıştır. Kanser hücreleri, tıpkı beyaz kan hücrelerinin yaptığı gibi endotel bariyerini geçmek için benzer moleküler mekanizmalardan yararlanmaktadır; bu keşif, bu yolları hedef alarak kanser tedavisi için yeni yollar açmıştır.
2010** yılında, dönüm noktası niteliğindeki bir çalışma, diapedezde rol oynayan spesifik integrinlerin ve selektinlerin hedeflenmesinin hayvan modellerinde meme kanseri hücrelerinin yayılmasını azaltabileceğini göstermiştir. Bu araştırma, diğer çalışmalarla birlikte, sadece bağışıklık tepkileri için değil, aynı zamanda kanser ve diğer koşullarda hastalığın ilerlemesi için de diapedezi anlamanın geniş klinik etkilerini göstermiştir.
İleri Okuma
1. Muller, W.A. (2011). “Mechanisms of leukocyte transendothelial migration.” Annual Review of Pathology: Mechanisms of Disease, 6, 323-344. https://doi.org/10.1146/annurev-pathol-011110-130224
2. Nourshargh, S., Hordijk, P.L., & Sixt, M. (2010). “Breaching multiple barriers: Leukocyte motility through venular walls and the interstitium.” Nature Reviews Molecular Cell Biology, 11(5), 366-378. https://doi.org/10.1038/nrm2889
3. Ley, K., Laudanna, C., Cybulsky, M.I., & Nourshargh, S. (2007). “Getting to the site of inflammation: The leukocyte adhesion cascade updated.” Nature Reviews Immunology, 7(9), 678-689. https://doi.org/10.1038/nri2156
4. Vestweber, D. (2015). “How leukocytes cross the vascular endothelium.” Nature Reviews Immunology, 15(11), 692-704. https://doi.org/10.1038/nri3908
5. Petri, B., & Sanz, M.J. (2018). “Leukocyte adhesion under flow: A brief update.” F1000Research, 7, F1000 Faculty Rev-1940. https://doi.org/10.12688/f1000research.16412.1
6. Schenkel, A.R., Mamdouh, Z., & Muller, W.A. (2004). “Locomotion of monocytes on endothelium is a critical step during extravasation.” Nature Immunology, 5(4), 393-400. https://doi.org/10.1038/ni1051
7. Zarbock, A., & Ley, K. (2008). “Mechanisms and consequences of neutrophil interaction with the endothelium.” American Journal of Pathology, 172(1), 1-7. https://doi.org/10.2353/ajpath.2008.070502
8. Hidalgo, A., Chilvers, E.R., Summers, C., & Koenderman, L. (2019). “The neutrophil life cycle.” Trends in Immunology, 40(7), 584-597. https://doi.org/10.1016/j.it.2019.04.013
9. Herter, J.M., Rossaint, J., Block, H., & Zarbock, A. (2013). “Integrin activation by P-Rex1 is critical for neutrophil recruitment in response to TNF-α and CXCL1 in vivo.” Journal of Experimental Medicine, 210(9), 2081-2093. https://doi.org/10.1084/jem.20120538
10. Imhof, B.A., & Aurrand-Lions, M. (2004). “Adherens junctions and the regulation of endothelial permeability and leukocyte extravasation.” Nature Reviews Molecular Cell Biology, 5(8), 659-670. https://doi.org/10.1038/nrm1438
Yorum yazabilmek için oturum açmalısınız.