İleotransversostomi
Etimolojik ve Terminolojik Temel
İleotransversokolostomi terimi, modern cerrahi terminolojide kullanılan birleşik bir sözcük olup Latince ve Yunanca köklerden türetilmiştir. İleum, Latince “bağırsak” anlamına gelen “ile” kökünden; transversum, “enine, çapraz uzanan” anlamındaki Latince kelimeden; kolon, Yunanca “kalın bağırsak” karşılığı “kolon” sözcüğünden; stomia ise Yunanca “ağız, açıklık” anlamına gelen “stoma” teriminden gelmektedir. Bu etimolojik bileşenler bir araya getirilerek, enine kolon ile ileumun cerrahi olarak birleştirilmesi yoluyla oluşturulan anastomoz yapısı tanımlanmaktadır.
Bu cerrahi prosedür, gastrointestinal sistem cerrahisinin evriminde önemli bir yere sahiptir ve intestinal kontinüitenin yeniden sağlanması amacıyla geliştirilmiş rekonstrüktif tekniklerin kapsamlı bir örneğini teşkil eder.
Embriyolojik ve Evrimsel Perspektif
Gastrointestinal sistemin embriyolojik gelişimi, orta bağırsak ve arka bağırsaktan sorumlu farklı mezoderm ve endoderm türevlerinin koordineli organizasyonunu gerektirir. İleum, embriyonik dönemde orta bağırsağın distal bölümünden köken alırken, kolon yapıları hem orta hem de arka bağırsak derivatiflerinden oluşur. Çıkan kolon ve çekumun orta bağırsak kaynaklı olması, inen ve sigmoid kolonun ise arka bağırsak kökenli bulunması, bu bölgelerin vasküler ve nöral organizasyonlarındaki farklılıkları açıklar.
Evrimsel açıdan, ince ve kalın bağırsak arasındaki fonksiyonel ayrım, omurgalıların besin kaynaklarına adaptasyonunun kritik bir sonucudur. İleosekal valv, memeli sindirim sisteminde ince ve kalın bağırsak arasındaki fizyolojik sınırı oluşturur ve içerik akışının düzenlenmesinde temel rol oynar. Bu anatomik yapının korunması veya bypass edilmesi, ileotransversokolostomi gibi cerrahi rekonstrüksiyon prosedürlerinin sonuçlarını derinden etkiler.
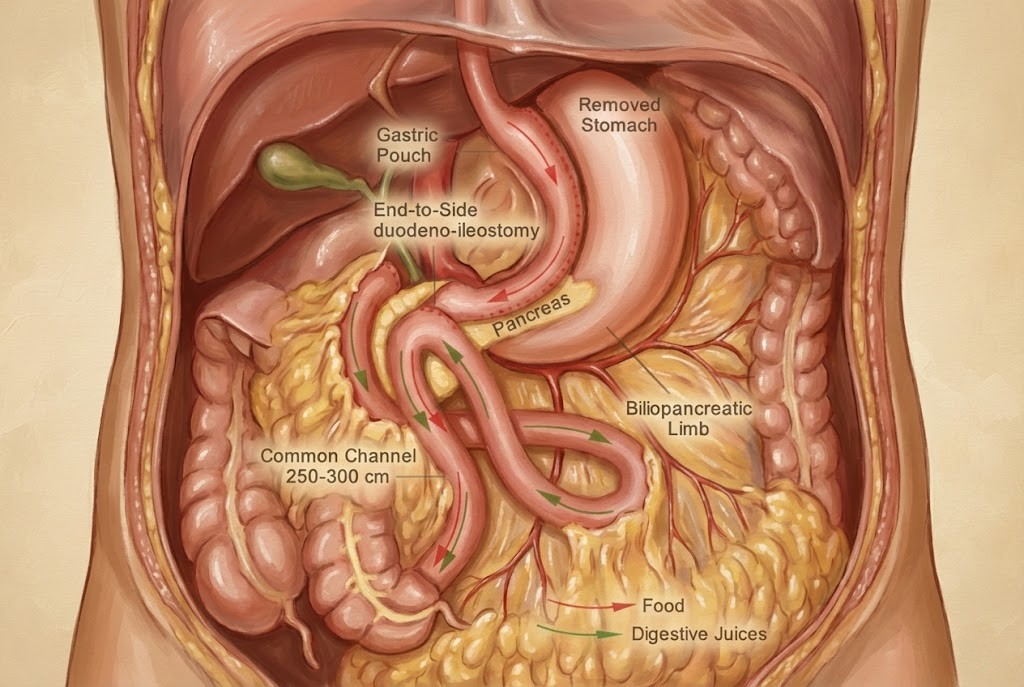
Anatomik Temel ve Cerrahi Endikasyonlar
İleotransversokolostomi, sağ hemikolektomi veya geniş kolon rezeksiyonlarını takiben, intestinal kontinüitenin yeniden kurulması amacıyla uygulanan bir anastomoz tekniğidir. Bu prosedürün primer endikasyonları arasında çekum, çıkan kolon veya proksimal transvers kolonda yerleşim gösteren malign neoplazmlar, inflamatuvar barsak hastalıkları, travmatik yaralanmalar ve nadiren konjenital anomaliler yer alır.
Kolorektal adenokarsinomlar, gelişmiş dünyada gastrointestinal sistemin en sık görülen maligniteleri arasındadır ve sağ kolon tümörleri bu olguların yaklaşık yüzde otuzunu oluşturur. Cerrahi rezeksiyonun kapsamı, tümörün yerleşimi, lenfovasküler invazyon derecesi ve bölgesel lenf nodu tutulumu gibi onkolojik prensiplere göre belirlenir. Çekum, çıkan kolon ve hepatik fleksura tümörlerinde, superior mezenterik arter ve inferior mezenterik arter arasındaki vasküler anatomi göz önünde bulundurularak sağ hemikolektomi uygulanır.
Bu cerrahi prosedürde, terminal ileum ile birlikte çekum, çıkan kolon ve transvers kolonun proksimal kısmı genellikle bir blok halinde rezeke edilir. Geriye kalan distal ileum ve orta veya distal transvers kolon segmentleri, intestinal kontinüitenin yeniden sağlanması için anastomoz edilir. Bu yapının oluşturulması, hem anatomik hem de fizyolojik düzeyde önemli adaptasyonları gerektirir.
Fizyolojik ve Patolojik Süreçler
Normal fizyolojik koşullarda, terminal ileum aktif B12 vitamini emilimi, safra tuzlarının enterohepatik sirkülasyona katılımı ve immünolojik fonksiyonlar açısından kritik bir bölgedir. İleal mukoza, özelleşmiş taşıyıcı proteinler aracılığıyla intrinsik faktör-kobalamin kompleksini absorbe eder. Safra tuzları ise, yağların emilimi için gerekli misel formasyonunu sağladıktan sonra terminal ileumda reabsorbe edilerek karaciğere geri döner.
İleotransversokolostomi sonrasında, ileosekal valfin kaybı önemli fizyolojik sonuçlar doğurur. Bu valfin normal fonksiyonu, ince bağırsak içeriğinin kontrollü şekilde kolona geçişini sağlarken, kolonik bakteriyel floranın ince bağırsağa reflüsünü engellemektir. Valfin yokluğunda, bakteriyel aşırı çoğalma sendromu riski artar ve bu durum malabsorbsiyon, kronik ishal ve vitamin eksikliklerine yol açabilir.
Kolon, primer fonksiyonu su ve elektrolit emilimi olan bir organdır. Günlük yaklaşık bin beş yüz mililitre sıvı ileosekal valvden geçerken, kolonik absorbsiyon mekanizmaları bu miktarın büyük kısmını reabsorbe eder. İleotransversokolostomi sonrası, kalan kolon segmentinin uzunluğu ve fonksiyonel kapasitesi, hastanın dışkı konsistansı ve defekasyon sıklığını doğrudan etkiler.
Cerrahi Teknik ve Anatomik Varyasyonlar
İleotransversokolostomi çeşitli teknik varyasyonlarla gerçekleştirilebilir. En yaygın uygulama, uç-yan veya yan-yan anastomoz konfigürasyonlarıdır. Uç-yan anastomozda, ileumun distal ucu transvers kolonun yan duvarına dikilirken, yan-yan teknikte her iki bağırsak segmenti yan yana getirilerek longitudinal bir açıklık oluşturulur.
Anastomoz hattının oluşturulmasında modern cerrahi pratikte hem elle dikiş teknikleri hem de mekanik stapler cihazları kullanılır. Mekanik stapler kullanımı, özellikle pelvik veya dar anatomik alanlarda teknik kolaylık sağlarken, elle dikiş anastomozlar cerrahın doku manipülasyonu üzerinde daha fazla kontrol sahibi olmasını sağlar. Her iki tekniğin de anastomoz kaçağı, striktür ve kanama gibi komplikasyon oranları karşılaştırılabilir düzeydedir.
Vasküler anatomi, anastomoz güvenliği açısından hayati önem taşır. İleumun kanlanması superior mezenterik arterden gelen ileal arterler tarafından sağlanırken, transvers kolon orta kolik arter ve sol kolik arter dallarından beslenir. Cerrahi rezeksiyon sırasında, anastomoz hattındaki her iki segmentin yeterli perfüzyonunun korunması, iyileşme sürecinin başarısı için zorunludur.
Postoperatif Adaptasyon ve Komplikasyonlar
İleotransversokolostomi sonrası dönemde, gastrointestinal sistem önemli adaptif değişiklikler gösterir. Kalan ince bağırsak segmentleri, mukozal hipertrofi ve villus uzaması yoluyla emilim yüzeyini artırma eğilimindedir. Bu adaptif süreç, kısa bağırsak sendromu gelişme riskini azaltır ancak tamamen kompanse edemez.
En ciddi erken postoperatif komplikasyon anastomoz kaçağıdır. Anastomoz hattındaki bütünlüğün bozulması, intestinal içeriğin peritoneal kaviteye sızmasına ve sonuç olarak peritonit, sepsis ve çoklu organ yetmezliğine yol açabilir. Kaçak riski, hastanın nutrisyonel durumu, anestezi komplikasyonları, doku perfüzyonu ve steroid kullanımı gibi faktörlerden etkilenir.
Geç dönem komplikasyonlar arasında anastomoz striktürü, adhesiv bağırsak tıkanıklığı, kronik ishal ve malabsorbsiyon sendromları yer alır. Anastomoz bölgesinde fibrotik doku oluşumu lümen daralmalarına neden olabilir ve bu durum kısmi veya tam obstrüksiyon semptomlarıyla kendini gösterir.
Metabolik ve Nutrisyonel Sonuçlar
Terminal ileum rezeksiyonu sonrası safra tuzu malabsorbsiyonu, kolesterol metabolizması ve yağda eriyen vitamin emilimi üzerinde uzun vadeli etkiler yaratır. Safra tuzlarının enterohepatik sirkülasyondan kaybı, karaciğerin kompansatuar safra tuzu sentezini artırmasına rağmen, yeterli misel formasyonunun sağlanamaması yağ emiliminde bozulmaya yol açar.
Vitamin B12 eksikliği, terminal ileum rezeksiyonunun klasik bir sonucudur. İntrinsik faktör-kobalamin kompleksinin absorbe edildiği özel reseptörler yalnızca distal ileumda bulunduğundan, bu bölgenin kaybı megaloblastik anemi ve nörolojik komplikasyonlara yol açabilir. Hastalar genellikle ömür boyu parenteral kobalamin desteği gerektirir.
Yağda eriyen vitaminler olan A, D, E ve K vitaminlerinin emilimi de olumsuz etkilenir. Bu durum, özellikle pediatrik hastalarda büyüme geriliği, kemik sağlığı bozuklukları ve koagülasyon anormallikleri riski yaratır. Dikkatli nutrisyonel takip ve gerektiğinde suplemantasyon, bu komplikasyonların önlenmesinde kritik rol oynar.
Mikrobiyom ve İmmünolojik Değişiklikler
Gastrointestinal mikrobiyom, konakçı metabolizması, immün sistem gelişimi ve intestinal bariyer fonksiyonu üzerinde derin etkilere sahiptir. İleotransversokolostomi, özellikle ileosekal valfin kaybı nedeniyle, mikrobiyom kompozisyonunda önemli değişikliklere neden olur.
İleosekal valfin yokluğu, kolon bakterilerinin ince bağırsağa retrograd migrasyonuna olanak tanır. Bu durum, ince bağırsak bakteriyel aşırı çoğalma sendromunun gelişimine zemin hazırlar. Bakteriyel metabolizma ürünleri, özellikle dekonjuge safra tuzları ve organik asitler, mukozal hasara ve inflamasyona katkıda bulunabilir.
Terminal ileumda bulunan Peyer plaklarının kaybı, mukozal immün yanıtları etkiler. Bu lenfoid yapılar, intestinal immünoglobulin A üretimi ve oral tolerans gelişiminde merkezi rol oynar. Rezeksiyon sonrası immün fonksiyonlardaki değişiklikler, enfeksiyon duyarlılığını artırabilir.
Onkolojik Prenspler ve Uzun Dönem Sağkalım
Malign hastalık nedeniyle uygulanan ileotransversokolostomilerde, cerrahi rezeksiyonun yeterliliği prognozu doğrudan etkiler. Onkolojik prensiplere uygun olarak, primer tümörün vasküler pedikülünün kökünden bağlanması ve bölgesel lenf nodlarının yeterli diseksiyonu esastır.
Kolorektal kanser evrelemesinde TNM sınıflaması kullanılır. Tümör penetrasyon derinliği, lenf nodu tutulumu ve uzak metastaz varlığı, hastalığın prognostik parametrelerini oluşturur. Sağ kolon tümörlerinde, sağ hemikolektomi ile birlikte ileokolik, sağ kolik ve orta kolik arter bölgelerindeki lenf nodlarının çıkarılması gerekir.
Adjuvan kemoterapi, evre üç kolorektal kanserlerde standart tedavi yaklaşımıdır. Fluoropirimidin bazlı rejimler, sağkalımda anlamlı iyileşme sağlar. Moleküler belirteçler, özellikle mikrosatellit instabilite durumu ve RAS mutasyon profili, tedavi seçiminde giderek artan önem kazanmaktadır.
Minimal İnvaziv Yaklaşımlar ve Teknolojik Gelişmeler
Laparoskopik ve robotik cerrahi tekniklerin gelişimi, kolorektal rezeksiyon ve anastomoz prosedürlerinde paradigma değişikliği yaratmıştır. Minimal invaziv yaklaşımlar, geleneksel açık cerrahiye kıyasla daha az postoperatif ağrı, kısa hastane yatışı ve hızlı iyileşme sağlar.
Laparoskopik sağ hemikolektomide, trokar girişleri aracılığıyla çalışılır ve specimen ekstraksiyon için küçük bir insizyon kullanılır. İntrakorpora veya ekstrakorpora anastomoz teknikleri uygulanabilir. Onkolojik yeterlilik açısından, minimal invaziv tekniklerin açık cerrahiye eşdeğer sonuçlar sağladığı büyük randomize çalışmalarda gösterilmiştir.
Robotik cerrahi platformları, üç boyutlu görüntüleme, tremor eliminasyonu ve gelişmiş enstrüman artikülasyonu gibi teknik avantajlar sunar. Ancak maliyet-etkinlik analizleri, robotik cerrahinin rutin kullanımının gerekçelendirilmesi için daha fazla kanıta ihtiyaç olduğunu göstermektedir.
Fonksiyonel Sonuçlar ve Yaşam Kalitesi
İleotransversokolostomi sonrası hastaların fonksiyonel sonuçları ve yaşam kalitesi, cerrahinin başarısının önemli göstergeleridir. Gastrointestinal semptomlar, bağırsak alışkanlıklarındaki değişiklikler ve nutrisyonel durum, uzun dönem takipte dikkatle değerlendirilmelidir.
Kronik ishal, bu hasta grubunda en sık karşılaşılan yakınmalardandır. Kalan kolon segmentinin absorbsiyon kapasitesindeki azalma, safra tuzu malabsorbsiyonu ve bakteriyel aşırı çoğalma, ishalin multifaktöryel patofizyolojisine katkıda bulunur. Diyet modifikasyonları, probiyotik kullanımı ve gerektiğinde antimotilite ajanları semptom kontrolünde yardımcı olabilir.
Sosyal ve psikolojik faktörler, hastaların yaşam kalitesini önemli ölçüde etkiler. Bağırsak fonksiyonlarındaki değişiklikler, sosyal aktiviteleri kısıtlayabilir ve anksiyete veya depresyon gelişimine zemin hazırlayabilir. Multidisipliner destek, fiziksel, nutrisyonel ve psikolojik iyileşmeyi optimize eder.
Gelecek Perspektifleri ve Translasyonel Araştırmalar
Rejeneratif tıp ve doku mühendisliği alanındaki ilerlemeler, intestinal rezeksiyon sonrası tedavi yaklaşımlarında yeni ufuklar açmaktadır. Kök hücre teknolojileri ve biyomühendislik yapıların geliştirilmesi, kaybedilen intestinal fonksiyonların potansiyel restorasyonu için umut vaat etmektedir.
Mikrobiyom modülasyonu, prebiyotik ve probiyotik müdahaleler, postoperatif adaptasyonu iyileştirme potansiyeline sahiptir. Spesifik bakteriyel suşların, mukozal iyileşme, bariyer fonksiyonu ve metabolik adaptasyonu desteklediği deneysel çalışmalarda gösterilmiştir.
Farmakogenomik ve kişiselleştirilmiş tıp yaklaşımları, adjuvan tedavi stratejilerinin optimizasyonunda giderek daha fazla rol oynamaktadır. Tümör genetik profilleme, hasta alt gruplarında en etkili tedavi rejimlerinin belirlenmesine olanak tanır ve tedavi toksisite profilini minimize ederken terapötik etkiyi maksimize eder.
Keşif
Ondokuzuncu yüzyılın ortalarında, cerrahi tıp henüz anestezi ve antisepsinin tam olarak yerleşmediği zorlu günlerini yaşıyordu. Bu dönemde bağırsak ameliyatları ölümcül komplikasyonlarla dolu bir maceraydı ve cerrahlar karın içindeki gizemli yapılara müdahale etme konusunda son derece çekingen davranıyorlardı. Ancak bazı cesur ruhlar, tıkanmış bağırsakların yarattığı acımasız tabloya çözüm aramaktan vazgeçmiyordu.
İleotransversokolostomi hikayesi, aslında daha geniş bir hikayenin parçasıydı: bağırsak cerrahisinin doğuşu. 1826’da Antoine Lembert, bağırsak dikişlerinde serozayı seroza ile birleştiren tekniğini tanımladığında, modern bağırsak cerrahisinin temel taşlarından birini atmıştı. Bu basit ama devrim niteliğindeki fikir, bağırsak anastomozlarının güvenle yapılabileceğini gösteriyordu. Ancak o dönemin cerrahları, hangi bağırsak segmentlerinin birleştirilebileceği konusunda henüz netlik kazanmamışlardı.
1881’de Theodor Billroth, mide rezeksiyonlarında gastrojejunostomi tekniğini geliştirdiğinde, farklı bağırsak segmentlerini birleştirme fikri tıp dünyasında büyük yankı uyandırdı. Bu başarı, cerrahları daha cesur anastomozlar denemeye teşvik etti. Aynı yıllarda, kolon cerrahisi üzerinde çalışan cerrahlar, transvers kolonun anatomik konumunun özel bir avantaj sunduğunu fark etmeye başladılar: bu bölge hem mobil hem de erişilebilirdi.
Ancak ileotransversokolostominin gerçek ihtiyacı, yirminci yüzyılın ilk çeyreğinde daha net hale geldi. Paul Mikulicz-Radecki ve diğer Avrupalı cerrahlar, sağ kolon patolojilerinde radikal rezeksiyonlar yapmaya başladıklarında, kalan ileumun transvers kolonla birleştirilmesinin mantıklı bir seçenek olduğunu gördüler. Bu dönemde yapılan ameliyatlar hâlâ yüksek mortalite oranlarına sahipti, ancak teknik mümkündü.
1920’lerde William Mayo ve kardeşi Charles, Mayo Kliniği’nde kolorektal cerrahinin sistematiğini oluşturmaya başladılar. Onların deneyimleri, ileotransversokolostominin özellikle sağ hemikolektomi sonrasında tercih edilebilir bir anastomoz yöntemi olduğunu gösteriyordu. Mayo kardeşler, anastomoz tekniklerini standartlaştırırken, ileumun ince yapısının kolonun daha kalın duvarıyla nasıl uyumlu hale getirilebileceğini araştırdılar.
1930’lar ve 1940’lar, antibiyotiklerin ve gelişmiş anestezi tekniklerinin cerrahi sonuçları dramatik şekilde iyileştirdiği bir dönemdi. Bu yıllarda Owen Wangensteen, bağırsak dekompresyonu ve nazogastrik aspirasyon tekniklerini geliştirerek ameliyat öncesi ve sonrası bakımda devrim yarattı. Bu gelişmeler, ileotransversokolostomi gibi karmaşık prosedürlerin güvenliğini artırdı.
İkinci Dünya Savaşı sonrası dönem, anatomik ve fizyolojik anlayışta önemli ilerlemelere tanık oldu. Cerrahlar, ileosekal valfin önemi ve ileumun transvers kolona bağlandığında fonksiyonel sonuçlarının ne olacağı konusunda daha derinlemesine düşünmeye başladılar. 1950’lerde yapılan araştırmalar, ileosekal valfin kaybedilmesinin diyare ve bakteriyel aşırı büyüme riskini artırabileceğini gösterdi, ancak ileotransversokolostominin bu komplikasyonları minimize edebileceği de anlaşıldı.
1960’larda Turnbull ve arkadaşları, Cleveland Clinic’te yaptıkları kapsamlı çalışmalarla ileotransversokolostominin endikasyonlarını netleştirdiler. Crohn hastalığı, kolon kanseri ve travmatik yaralanmalarda bu tekniğin ne zaman tercih edilmesi geektiğini belirleyen algoritmalar geliştirdiler. Bu dönemde, uç-uca ve uç-yan anastomoz teknikleri arasındaki tartışmalar yoğunlaştı.
1970’ler, staplerların cerrahi pratiğe girmesiyle işaretlendi. Sovyet cerrah Pyotr Androsov’un geliştirdiği ve daha sonra Batı’da da kullanılmaya başlanan mekanik stapler cihazları, anastomozların yapılış şeklini değiştirdi. İleotransversokolostomi artık sadece elle dikişle değil, stapler kullanılarak da güvenle yapılabiliyordu. Bu yenilik, ameliyat sürelerini kısalttı ve anastomoz kaçağı riskini azalttı.
1980’lerde, görüntüleme teknolojilerindeki gelişmeler cerrahi planlamayı dönüştürdü. Bilgisayarlı tomografi, cerrahların ameliyat öncesi dönemde damar anatomisini ve tümör yayılımını daha iyi değerlendirmesine olanak tanıdı. Bu dönemde ayrıca kolonoskopinin yaygınlaşması, kolon patolojilerinin erken tanısını mümkün kıldı ve elektif ileotransversokolostomi vakalarının sayısını artırdı.
1990’lar, minimal invaziv cerrahinin altın çağıydı. Laparoskopik teknikler, önce kolesistektomi için geliştirildi, ardından kolon rezeksiyonlarına uyarlandı. İlk laparoskopik sağ hemikolektomi ve ileotransversokolostomi denemeleri bu dönemde yapıldı. Başlangıçta teknik zorluklar ve uzun öğrenme eğrileri nedeniyle eleştirilen bu yaklaşım, zamanla olgunlaştı.
Yirmibirinci yüzyılın ilk on yılında, laparoskopik kolorektal cerrahinin onkolojik güvenliği kanıtlandı. COST ve COLOR gibi büyük randomize kontrollü çalışmalar, laparoskopik sağ hemikolektomi ve ileotransversokolostominin açık cerrahiye eşdeğer onkolojik sonuçlar verdiğini gösterdi. Aynı zamanda, hastanede kalış süresinin kısalması ve iyileşmenin hızlanması gibi avantajları ortaya koydu.
2010’larda robotik cerrahi platformlar, özellikle da Vinci sistemi, kolorektal cerrahide yerini almaya başladı. Robotik ileotransversokolostomi, cerrahlara üç boyutlu görüntü, titreşimsiz araçlar ve gelişmiş manevra kabiliyeti sundu. İntrakorproeal anastomoz teknikleri geliştirildi; bu sayede bağırsak birleştirme işlemi tamamen karın içinde, daha hassas şekilde yapılabildi.
Enhanced Recovery After Surgery protokolleri, bu yıllarda ileotransversokolostomi sonrası bakımda paradigma değişikliğine yol açtı. Erken mobilizasyon, erken oral beslenme ve ağrı kontrolünde multimodal yaklaşımlar, hastaların ameliyat sonrası dönemde daha hızlı iyileşmesini sağladı. Nazogastrik tüp kullanımından vazgeçilmesi ve mekanik bağırsak hazırlığının sorgulanması gibi değişiklikler, hasta konforunu artırdı.
2015 sonrasında, indosiyanin yeşili floresanı gibi yeni teknolojiler cerrahi sahneye girdi. Bu yöntem, cerrahlara anastomoz bölgesindeki kan akımını gerçek zamanlı olarak görselleştirme imkanı tanıdı. Yetersiz perfüzyonun anastomoz kaçağının en önemli risk faktörlerinden biri olduğu bilindiğinden, bu teknoloji ileotransversokolostominin güvenliğini artırdı.
Son yıllarda, yapay zeka ve makine öğrenmesi algoritmaları kolorektal cerrahide uygulanmaya başlandı. Bu sistemler, ameliyat öncesi görüntülerden damar anatomisini haritalandırabilir, ameliyat sırasında kritik yapıların tanınmasına yardımcı olabilir ve komplikasyon riskini tahmin edebilir. Bazı merkezler, ileotransversokolostomi sonrası anastomoz kaçağı riskini değerlendiren prediktif modeller geliştiriyor.
Günümüzde ileotransversokolostomi, özellikle sağ kolon rezeksiyonlarında standart bir prosedürdür. Teknik çeşitliliği devam etmektedir: elle dikişli uç-uca, uç-yan veya yan-yan anastomozlar; lineer veya sirküler stapler kullanımı; açık, laparoskopik veya robotik yaklaşımlar. Her yaklaşımın kendi avantajları ve sınırlamaları vardır ve seçim, cerrahın deneyimine, hasta anatomisine ve klinik duruma bağlıdır.
Çağdaş araştırmalar, anastomoz tekniğinin ötesine geçerek biyolojik faktörlere odaklanıyor. Bağırsak mikrobiyomunun anastomoz iyileşmesindeki rolü, immünonutrisyonun etkileri ve kişiselleştirilmiş tıp yaklaşımları aktif araştırma alanlarıdır. Ayrıca, neoadjuvan ve adjuvan tedavilerin anastomoz iyileşmesi üzerindeki etkileri detaylı olarak inceleniyor.
Gelecek, daha da heyecan verici olasılıklar sunuyor. Doku mühendisliği ve rejeneratif tıp, anastomoz güçlendirmede yeni yollar açabilir. Nanotteknoloji bazlı yapıştırıcılar ve sealantlar geliştirilmektedir. Telecerrahi ve uzaktan mentorluk sistemleri, ileotransversokolostomi tekniklerinin dünya çapında standardizasyonunu sağlayabilir.
İleotransversokolostominin hikayesi, tıbbi merakın, teknik yeniliğin ve hasta bakımına adanmışlığın kesiştiği noktada durmaktadır. Ondokuzuncu yüzyılın cesur ilk adımlarından yirmibirinci yüzyılın teknolojik zarafetiine kadar uzanan bu yolculuk, cerrahi bilimin sürekli evriminin mükemmel bir örneğidir. Her yeni nesil cerrah, öncekilerinin omuzlarında durmakta ve ileotransversokolostomiyi daha güvenli, daha etkili ve hastalar için daha az travmatik hale getirmektedir.
İleri Okuma
- Lembert A. (1826). Mémoire sur l’entéro-raphie avec la description d’un procédé nouveau pour pratiquer cette opération chirurgicale. Répertoire Général d’Anatomie et de Physiologie Pathologiques et de Clinique Chirurgicale, 2, 100–112.
- Billroth T. (1881). Allgemeine chirurgische Pathologie und Therapie in 51 Vorlesungen. Berlin, Georg Reimer.
- Mikulicz-Radecki J. von. (1903). Beiträge zur Chirurgie des Dickdarms. Archiv für Klinische Chirurgie, 69, 28–79.
- Mayo W.J. (1906). The surgery of the alimentary canal. Journal of the American Medical Association, 47, 1783–1789.
- Mayo C.H. (1913). Resection of the colon with special reference to cancer. Annals of Surgery, 58, 1–13.
- Wangensteen O.H. (1937). Intestinal obstruction. Springfield, IL, Charles C. Thomas.
- Wangensteen O.H., Paine J.R. (1942). Treatment of acute intestinal obstruction by suction with the duodenal tube. Journal of the American Medical Association, 120, 341–347.
- Brooke B.N. (1954). The ileocaecal valve: its function and clinical significance. The Lancet, 266(6826), 745–748. https://doi.org/10.1016/S0140-6736(54)92503-6
- Androsov P.I. (1960). Mechanical suture in surgery of the gastrointestinal tract. Khirurgiya, 36, 3–8.
- Turnbull R.B., Weakley F.L. (1961). Surgical management of right-sided colonic disease. Cleveland Clinic Quarterly, 28, 109–123.
- Turnbull R.B., Kyle K., Watson F.R., Spratt J. (1967). Cancer of the colon: the influence of the no-touch isolation technique on survival rates. Annals of Surgery, 166, 420–427. https://doi.org/10.1097/00000658-196709000-00008
- Steichen F.M., Ravitch M.M. (1973). Mechanical sutures in gastrointestinal surgery. Annals of Surgery, 177, 653–660. https://doi.org/10.1097/00000658-197305000-00014
- Heald R.J. (1988). The ‘holy plane’ of rectal surgery. Journal of the Royal Society of Medicine, 81, 503–508.
- Jacobs M., Verdeja J.C., Goldstein H.S. (1991). Minimally invasive colon resection (laparoscopic colectomy). Surgical Laparoscopy & Endoscopy, 1, 144–150.
- Delaney C.P., Kehlet H., Senagore A.J., et al. (2001). Postoperative ileus: profiles, risk factors, and definitions—a framework for optimizing surgical outcomes in patients undergoing major abdominal and colorectal surgery. Clinical Consensus Update in General Surgery, 3, 1–12.
- Lacy A.M., García-Valdecasas J.C., Delgado S., et al. (2002). Laparoscopy-assisted colectomy versus open colectomy for treatment of non-metastatic colon cancer: a randomised trial. The Lancet, 359(9325), 2224–2229. https://doi.org/10.1016/S0140-6736(02)09290-5
- Clinical Outcomes of Surgical Therapy (COST) Study Group. (2004). A comparison of laparoscopically assisted and open colectomy for colon cancer. New England Journal of Medicine, 350, 2050–2059. https://doi.org/10.1056/NEJMoa032651
- Veldkamp R., Kuhry E., Hop W.C.J., et al. (2005). Laparoscopic surgery versus open surgery for colon cancer: short-term outcomes of a randomised trial. The Lancet Oncology, 6(7), 477–484. https://doi.org/10.1016/S1470-2045(05)70221-7
- Pigazzi A., Ellenhorn J.D.I., Ballantyne G.H., Paz I.B. (2006). Robotic-assisted laparoscopic low anterior resection with total mesorectal excision for rectal cancer. Surgical Endoscopy, 20, 1521–1525. https://doi.org/10.1007/s00464-005-0778-4
- Kehlet H., Wilmore D.W. (2008). Evidence-based surgical care and the evolution of fast-track surgery. Annals of Surgery, 248, 189–198. https://doi.org/10.1097/SLA.0b013e31817f2c1a
- Shogan B.D., Belogortseva N., Luong P.M., et al. (2015). Collagen degradation and MMP9 activation by enteric bacteria in intestinal anastomotic leak. Science Translational Medicine, 7(286), 286ra68. https://doi.org/10.1126/scitranslmed.3010650
- Boni L., David G., Mangano A., et al. (2016). Clinical applications of indocyanine green (ICG) enhanced fluorescence in laparoscopic surgery. Surgical Endoscopy, 29, 2046–2055. https://doi.org/10.1007/s00464-014-3895-x
- Hashimoto D.A., Rosman G., Rus D., Meireles O.R. (2018). Artificial intelligence in surgery: promises and perils. Annals of Surgery, 268, 70–76. https://doi.org/10.1097/SLA.0000000000002693
- van den Bos J., Al-Taher M., Schols R.M., et al. (2018). Near-infrared fluorescence imaging for real-time intraoperative guidance in anastomotic surgery. Journal of Surgical Oncology, 118, 315–322. https://doi.org/10.1002/jso.25115
- van Praagh J.B., de Greef B.T.A., Maas M., et al. (2021). Biological factors in colorectal anastomotic healing: a systematic review. Annals of Surgery, 273, 877–884. https://doi.org/10.1097/SLA.0000000000004094