İçindekiler
(ICD-10: A98.4)
Kısa tanım
Ebola-virüs hastalığı (EVH), Filoviridae ailesine bağlı Ebolavirus cinsi tarafından oluşturulan, sıklıkla ağır seyreden, zaman zaman hemorajik belirtilerle karakterize, yüksek mortaliteli bir zoonotik enfeksiyondur. Bulaş başlıca enfekte bireylerin vücut sıvılarıyla doğrudan temas yoluyla gerçekleşir; sağlık hizmeti sunumundaki yetersizlikler ve cenaze ritüelleri gibi sosyokültürel etmenler salgın dinamiklerini önemli ölçüde etkiler.
Sözlükçe (seçilmiş terimler)
- DİK (DİK): Yaygın damar içi pıhtılaşma.
- NPC1: Endozomal kolesterol taşıyıcısı; EBOV girişinde zorunlu konak faktörü.
- Ring aşılama: Vaka çevresindeki temas halkalarının hedefli aşılanması.
- Post-Ebola sendromu: İyileşme sonrası haftalar–aylar süren çok sistemli semptom kümesi.
Etimoloji ve tarihsel arka plan
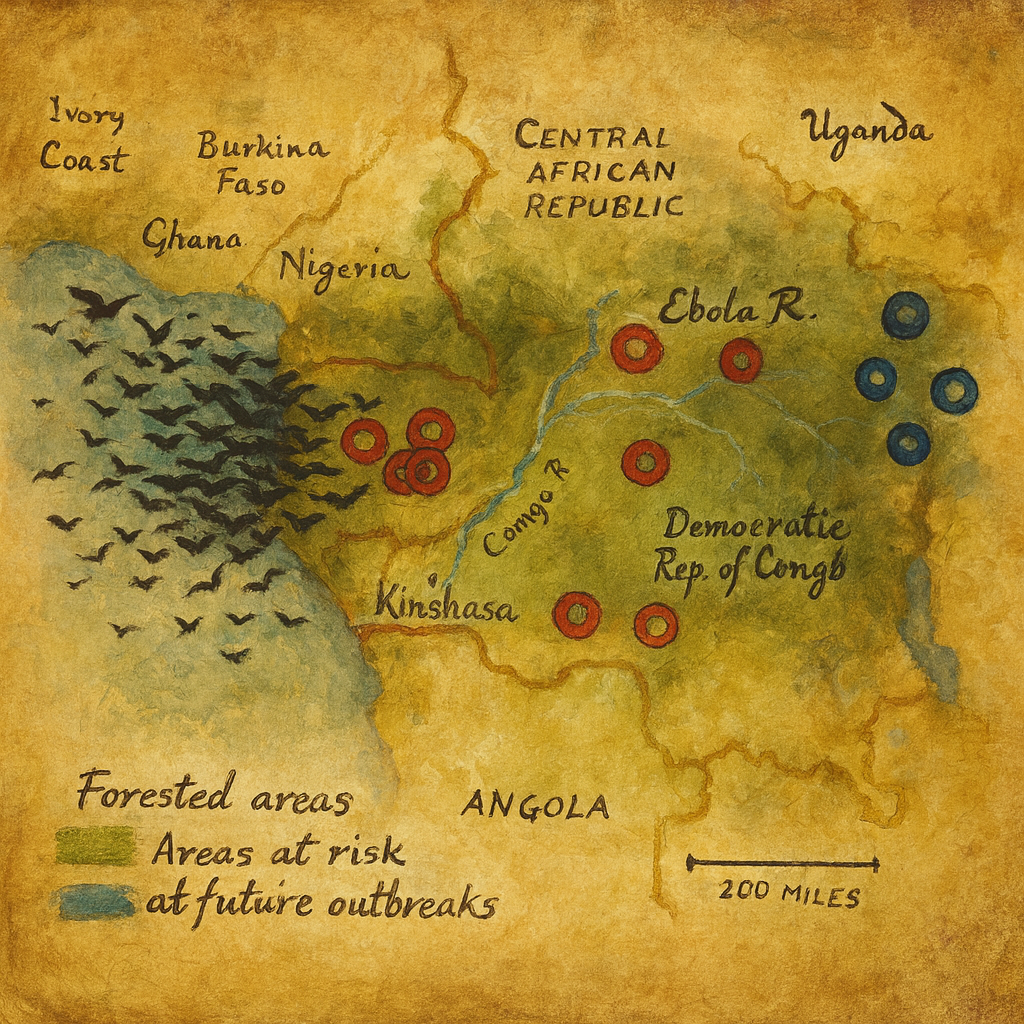
“Ebola” adı, 1976’daki ilk tanımlı büyük salgın sırasında Demokratik Kongo Cumhuriyeti’ndeki Ebola Nehri’nden esinle verilmiştir; amaç, odak bölgesi Yambuku’yu doğrudan damgalamadan hastalığı adlandırmaktı. 1976’da Yambuku (eski Zaire) ve eşzamanlı olarak Nzara (Güney Sudan) odaklı iki bağımsız salgın, güncel klinik–virolojik tanımlamanın miladı kabul edilir. 1995 Kikwit, 2000 Gulu, 2007 Bundibugyo odakları, nihayet 2014–2016 Batı Afrika mega-salgını, modern salgın yönetimi ve klinik bakım standartlarının evriminde dönüm noktalarıdır.
Taksonomi ve evrimsel konum
- Aile: Filoviridae
- Cins: Ebolavirus
- Türler: Zaire ebolavirus (EBOV), Sudan ebolavirus (SUDV), Bundibugyo ebolavirus (BDBV), Taï Forest ebolavirus (TAFV), Reston ebolavirus (RESTV).
İnsanlarda ağır hastalık tipik olarak EBOV, SUDV ve BDBV ile ilişkilidir; RESTV primatlarda patojenik olmakla birlikte insanlarda bugüne dek klinik hastalıkla ikna edici biçimde ilişkilendirilmemiştir.
Filogenetik ve moleküler evrim
Ebolavirus genomu ≈19 kb uzunlukta tek iplikli, negatif polariteli RNA’dır. Yedi yapısal gen (NP, VP35, VP40, GP, VP30, VP24, L) kodlar. Evrim hızı, RNA virüslerine özgü biçimde yüksektir; buna karşın konak ve ekolojik niş kısıtları, coğrafi kümelenme ve tür-spesifik soylar üretir. VP24 ve VP35’teki işlevsel motifler, konak interferon yanıtını baskılama kapasitesi nedeniyle konak uyumunda seçilim hedefleridir. EBOV soyları, geçmiş büyük salgınlarda halka aşılama ve temaslı izleme stratejilerinin baskısıyla epidemiyolojik darboğazlar yaşamış, bu da yerel genetik çeşitliliği belirlemiştir.
Viroloji ve patogenez
Virion morfolojisi ve replikasyon
Filovirüsler elektron mikroskobisinde filamentöz, kimi zaman U veya 6 şeklinde görünür; çap ~80 nm, uzunluk değişkendir. Zarf ile çevrili virionlar, yüzeyde trimerik glikoprotein (GP) taşır. Hücre girişinde:
- Makropinositoz baskındır;
- Endozomal kaçış ve füzyon için NPC1 kritik konak faktördür;
- DC-SIGN/TIM-1 gibi yardımcı alıcılar hücre tipine göre katkı verebilir.
Sitoplazmada transkripsiyon ve replikasyon L polimeraz aracılığıyla yürütülür. VP40 tomurcuklanma ve virion salınımını düzenler.
İmmün kaçış ve doku tropizmi
- VP35, RIG-I/MDA5 yolaklarını baskılayarak tip I interferon yanıtını inhibe eder.
- VP24, STAT1’in nükleer translokasyonunu bozarak interferon sinyalini engeller.
- Soluble GP (sGP), antikorları “sünger” gibi bağlayarak nötralizan yanıtı seyreltir.
Doku tropizmi geniştir: mononükleer fagositik sistem, hepatositler, endotel, adrenal ve dalak dokuları başlıca hedeflerdir. Sonuçta vaskülit/kapiller sızıntı, koagülopati (DİK), şok ve multiorgan yetmezliği gelişebilir.
Epidemiyoloji
Rezervuar ve türler arası geçiş
Ekolojik veriler meyve yarasalarını (ör. Pteropodidae) güçlü rezervuar adayları yapar. Yabanî hayvan ölüsü/etiyle temas (ör. primatlar, antiloplar) ve çevresel kontaminasyon olası aracı maruziyet yollarıdır. İnsanlar arası bulaşın tetiklenmesi, çoğu kez indeks temas ile sağlık altyapısının kısıtlı olduğu kırsal odaklarda başlar.
Bulaş dinamikleri
- Doğrudan temas: Kan, kusmuk, ishal, idrar, tükürük, gözyaşı, anne sütü, semen.
- Dolaylı temas: Kontamine iğne–şırınga, yüzey, giysi.
- Aerosol/damlacık: Rutin toplum koşullarında baskın yol değildir; ancak yakın mesafede yoğun sekresyon saçılımı (öksürük, tıbbi işlemler) riski artırır.
- Cinsel bulaş: Semende viral RNA haftalar–aylar kalabilir; nadir de olsa geç sekonder bulaş olguları bildirilmiştir.
- Sağlık hizmeti ilişkili: Kişisel koruyucu ekipman (KKE) giyip-çıkarma hataları kritik risk faktörüdür.
Salgın bağlamı
Salgınlar sağlık sistem kapasitesi, güvenli defin uygulamaları, toplumsal güven ve hareketlilik ile şekillenir. 2014–2016 Batı Afrika salgını, kentleşmiş ortamlarda temaslı izlemenin ve halkla risk iletişiminin belirleyici olduğunu göstermiştir. 2018–2020 döneminde Kongo Demokratik Cumhuriyeti’nde güvenlik sorunları ve yerel güvensizlik, aşılama ve sürveyansı zorlaştırmıştır.
Klinik tablo
Kuluçka ve başlangıç
İnkübasyon genellikle 2–21 gün (çoğu 6–12 gün). Başlangıç nonspesifik: ateş, belirgin hastalık hissi, miyalji, baş ağrısı, boğaz ağrısı.
Sistem bulguları
- Solunum: farenjit, öksürük, dispne, nadiren hıçkırık.
- Gastrointestinal: iştahsızlık, bulantı–kusma, bol sulu ishal, kramp tarzı karın ağrısı—sıvı-elektrolit kaybı ve hipovolemiye yol açar.
- Dermatolojik: 4–6. günlerde makülopapüler döküntü gelişebilir.
- Nörolojik: letarji, konfüzyon, nöbet; ağır olgularda koma.
- Hemorajik bulgular: peteşi, purpura, ekimoz, hematemez/hematokezya/melena; prognoz açısından olumsuz göstergedir.
Komplikasyonlar ve mortalite
Kapiller kaçak, DİK, septik benzeri şok, hepatik disfonksiyon ve renal yetmezlik çoklu organ yetmezliğine ilerleyebilir. Vaka-ölüm oranı, tür ve bağlamla değişir (yaklaşık %40–90 aralığı raporlanmıştır). Yaş, başlangıç viral yükü, böbrek ve karaciğer biyokimyası prognostik önemdedir. Asemptomatik veya hafif seyir nadir fakat bildirilmiştir.
İyileşenlerde geç dönem bulguları (“post-Ebola sendromu”)
Günler–aylar içinde artralji, miyalji, yorgunluk, işitme bozukluğu, psikiyatrik semptomlar ve özellikle üveit görülebilir. Göz, testis ve santral sinir sistemi gibi immün ayrıcalıklı bölgelerde viral RNA kalıcılığı saptanabilir; klinik ve halk sağlığı yönetimi buna göre planlanmalıdır.
Ayırıcı tanı
Akut ateşli hasta bağlamında:
- Plasmodium sıtması
- Viral hemorajik ateşler: Lassa, Sarı humma, Dengue, Kırım-Kongo, Marburg
- Bakteriyel: Tifo/paratifo, meningo-sepsis, riketsiyoz
- Diğer: Leptospiroz, şiddetli gastroenteritler
Epidemiyolojik maruziyet öyküsü (evvelki 21 gün içinde etkilenen bölgede bulunma/temas) triyajda merkezî önemdedir.
Tanı
Numune ve biyogüvenlik
Numuneler BSL-4 koşulları gözetilerek alınmalı, sızdırmaz şekilde taşınmalıdır. Klinik bakım ünitelerinde standart-temas-damlacık önlemleri ve riskli işlemlerde aerosol önlemleri uygulanır.

Laboratuvar yöntemleri
- RT-PCR: Akut fazda altın standart; tam kan/plazma başlıca materyaldir.
- Antijen testleri: Sahada hızlı triyaj için yararlı, doğrulama PCR ile yapılır.
- Seroloji (ELISA IgM/IgG): Geç faz/epidemiyoloji için tamamlayıcıdır.
- Viral yük ölçümü ve tüm genom dizileme: Prognoz ve sürveyans (soy takibi, bulaş zincirleri).
- Hücre kültürü/EM: Araştırma ve referans merkezleri düzeyinde.
Tedavi
Destekleyici bakım (bakımın çekirdeği)
- Yoğun sıvı-elektrolit replasmanı (oral/IV), hipovolemi ve laktat takibi.
- Analjezi/antipiretik, antiemetik, erken beslenme.
- Koagülopati yönetimi (hemostaz takibi; endikasyon varsa tromboprofilaksi).
- Sekonder bakteriyel/fungal enfeksiyonların ampirik yönetimi, stewardship ilkeleriyle.
- Böbrek yetmezliğinde renal replasman tedavileri; hipoksemi/ARDS için oksijen/ventilasyon stratejileri.
Spesifik/etiyotropik yaklaşımlar
- Monoklonal antikorlar: EBOV’a özgül nötralizan antikor kombinasyonları ağır olgularda sağkalımı artırabilir (erken uygulama en etkilidir).
- Antiviral adaylar: Nükleotid/nükleozid analogları (örn. RNA polimeraz inhibitörleri) ve RNAi-temelli ajanlar farklı dönemlerde denenmiştir; klinik etkinlikleri bağlama duyarlıdır.
- Konvalesan plazma: Kanıta dayalı etkinlik sınırlı ve heterojendir; yerel kapasite/etik çerçeveye bağlı değerlendirilir.
Not: Spesifik ajanların seçimi ve uygulanması, güncel kılavuz ve erişilebilirliğe göre uzman merkezlerde kararlaştırılmalıdır.
Aşılama ve salgın kontrolü
- rVSV-ZEBOV temelli tek dozluk aşı, EBOV (Zaire) türüne karşı sahada halka (ring) aşılama stratejisinde yaygın kullanıma girmiş ve salgınların kırılmasında belirgin katkı sağlamıştır.
- Ad26.ZEBOV/MVA-BN-Filo gibi iki dozlu rejimler immünolojik dayanıklılık hedefiyle geliştirilmiştir.
- Aşılamanın etkinliğini temaslı/temaslının temaslısı izleme, güvenli defin, toplum katılımı, sınır sağlığı ve laboratuvar ağları ile entegre etmek esastır.
Enfeksiyon kontrolü: klinik ve saha uygulamaları
- KKE: Tip 3B düzeyinde sıvı geçirmez önlük/tulum, çift eldiven, göz-yüz koruyucu, FFP3/N95 maske veya PAPRs (yüksek riskli işlemlerde).
- Giyme-çıkarma protokolleri: Gözlemci eşliğinde adım adım uygulanmalı; hata payı en kritik risk noktasıdır.
- Atık ve çevre yönetimi: Dekontaminasyon, güvenli atık bertarafı, iğne ucu yaralanmalarının önlenmesi.
- Güvenli defin: Bulaşın kesilmesinde kilit basamak; kültürel hassasiyet gözetilerek yürütülmelidir.
Halk sağlığı, etik ve “Tek Sağlık” perspektifi
EVH, yabanıl yaşam–insan–çevre arayüzündeki değişimlere duyarlıdır: ormansızlaşma, yabanî hayvan ticareti, çatışma ve yer değiştirme, sağlık altyapısındaki kırılganlıklar salgın riskini yükseltir. Risk iletişimi, güven inşası ve yerel liderlerle ortaklık, teknik müdahaleler kadar belirleyicidir. Klinik araştırmalarda adil erişim, topluluk rızası ve veri paylaşımı ilkeleri etik çerçeveyi oluşturur.
Özelleşmiş klinik noktalar
- Gebelik: Ağır seyir ve perinatal kayıp riski yüksektir; obstetrik işlemler çok yüksek bulaş riski taşır, ileri düzey hazırlık gerektirir.
- Pediatri: Dehidratasyon ve hipoglisemiye yatkınlık nedeniyle sık ve proaktif destek gerekir.
- Transmüsyon/organ bağışı: Ayrıntılı tarama ve bekleme süreleri zorunludur.
- İyileşenlerin izlemi: Göz rahatsızlıkları (üveit dâhil), nöropsikiyatrik sekeller, kas-iskelet yakınmaları için çok disiplinli takip.
Özet akış şeması (klinik pratikte zihinsel model)
- Epidemiyoloji: Son 21 günde risk bölgesi/temas?
- Triyaj: Ateş + GIS belirtileri ± hemorajik ipuçları → izolasyon ve KKE.
- Tanı: Hızlı antijen (uygunsa) + RT-PCR (altın standart).
- Bakım: Erken ve agresif sıvı-elektrolit yönetimi, organ destekleri.
- Spesifik tedavi: Uygun adaylarda EBOV’a özgü monoklonal antikor.
- Halk sağlığı: Temaslı izleme, halka aşılama, güvenli defin.
Keşif
Efsanenin değil, ampul ışığında ter döken saha hekimlerinin, laboratuvar teknisyenlerinin, köy liderlerinin ve hastaların hikâyesi bu: Ebola ateşinin keşiften güncel bilime uzanan, damarları boyunca hem acının hem ilerlemenin aktığı uzun bir anlatı.
1976 sonbaharında, Ekvator kuşağının yeşil çizgileri üzerinde küçük bir nokta olan Yambuku Misyoner Hastanesi’nde öğretmen Mabalo Lokela, sıradan bir ateşle geldiğinde kimse bunun bir çağ açacağını bilmiyordu. İntravenöz tedaviler için yeniden kullanılan iğneler, kalabalık bir poliklinik, yetersiz malzeme… Hastane koridorlarında hızla yayılan, kanla ve gözyaşıyla iz bırakan bir tablo ortaya çıktı. Belçika’dan Anvers Tropikal Tıp Enstitüsü’ne gönderilen örnekler, CDC’de karantina kabinlerinin içinde dikkat ve korku arasında çalışan bir ekibe ulaştı: Karl Johnson, Joel Breman, David Heymann ve meslektaşları; Anvers’te genç bir mikrobiyolog olan Peter Piot; Kinşasa ve Kikwit hattında erken saha refleksleriyle öne çıkan Jean-Jacques Muyembe-Tamfum… Elektron mikroskobunda tele gibi kıvrılan, bazen “U” harfi çizen o ipliksi şekil görüldüğünde, tanı sadece bir görüntü değildi; yeni bir dünyanın kapısı aralanmıştı. Hastalığa ad verilirken, Yambuku’nun damgalanmaması için yakınlardan akan küçük bir nehrin adı seçildi: Ebola.
Aynı yıl, Nil’in kollarına yakın Nzara ve Maridi’de, bağımsız bir odak daha belirdi. Klinik tablo benzer, epidemiyolojik bağlam farklıydı; bu çift başlangıç, bugün hâlâ kullandığımız tür ayrımının ipuçlarını verdi: Zaire ebolavirus ve Sudan ebolavirus. Filovirüslerin –Marburg’dan tanıdık– morfolojik akrabası oldukları kısa sürede anlaşıldı; ama bunlar başka bir hikâyeydi. 1995’te Kikwit’teki salgın, hastane hijyeninin kader olduğu gerçeğini kemiklere işledi: tek kullanımlık malzemelerin lüks sayıldığı bir bağlamda, bir iğnenin iki kere kullanılması, onlarca hayatın eksilmesi demekti. O yıllarda “kanı donduran” başlıklar, bilim insanlarının kanı soğutmak yerine akıl yürütmesini hızlandırdı: Bulaş yolu, hangi dokulara saldırdığı, neden bazı hastalarda fırtına gibi ilerlediği soruları laboratuvarların gecelerini uzattı.
Batı Afrika’nın kıyıdan içeri uzanan pazaryerlerinde, 2000’lerin başında Gabon ve Kongo Cumhuriyeti’nde av hayvanı (bushmeat) etrafında şekillenen trajediler, ormanda bulunan ölü gorillerle aynı halkanın parçasıydı. Eric Leroy ve meslektaşları, büyük maymunlardaki ölümleri yalnızca “yan hikâye” olarak değil, insan salgınlarının körüklenmesinde bir uyarı zili olarak okudu. Aynı hat üzerinde yürüyen ekolojistler, meyve yarasalarını –Epomops, Hypsignathus, Myonycteris– doğanın sessiz rezervuar adayları arasına yerleştirdiler. Virüs, insanı hedef seçmiş değildi; ekosistemin yeni temas yüzeyleri, ormansızlaşma ve hareketlilik virüse fırsatlar yaratıyordu.
2007’de Uganda’nın Bundibugyo bölgesinde yeni bir isim sahneye çıktı: Bundibugyo ebolavirus. Filogenetik ağacın dalları kalınlaşıyor, epidemiyologların not defterleri tür kısaltmalarıyla doluyordu. Aynı dönemde bilim, mikroskopla yetinmeyi bırakıp moleküler sözlüğünü genişletiyordu: negatif iplikçikli RNA genomunun yaklaşık 19 kilobazlık düzeni, NP’den L polimeraza uzanan yedi genin uyumu; VP35’in interferon yanıtını boşa çıkaran hilesi; VP24’ün STAT1’in nükleer yolunu sabote eden hamlesi; yüzeydeki trimerik GP’nin (glikoprotein) makropinositozu tetikleyen, endozomda NPC1’e bağımlı giriş ritüeli… Patogenez artık yalnız klinik sıfatlarla değil, hücre içi fiillerle de anlatılıyordu.
Sonra 2014 geldi. Guéckédou pazarındaki bir kıvılcım, sınır çizgilerinin anlamını kaybettiği bir yangına dönüştü. Ebola, ilk kez yoğun kentsel ağlarda dolaştı; temaslı izlemenin bir kas mı yoksa bir kavram mı olduğunu sınadı. Médecins Sans Frontières erken uyardı; Dünya Sağlık Örgütü ağustos ayında “uluslararası önemi haiz halk sağlığı acil durumu” ilan etti. Kenema’dan Monrovia’ya, Freetown’dan Conakry’ye uzanan bir zincirde, yalnız bir virüs değil, bilgi ve güven de el değiştirdi. Sahra altı Afrika’nın klinikleri sadece hasta bakmadı; bilim üretti. Saha tanısı için kartuş temelli moleküler testler, soğuk zincir kırıklarına rağmen çalışabilir oldu; taşınabilir dizileme cihazları, genomların “soyağacını” afet çadırlarında okuyabildi. Halk sağlığının kalbi, güvenli defin ritüelleri ve topluluk liderleriyle kurulan ilişkilere taşındı; antropologlar, hemşireler, din insanları ve lojistikçiler aynı cümlede yer buldu.
Aynı kriz, koruyucu önlemler ile biyomedikal müdahalelerin evliliğini hızlandırdı. Kanada’da geliştirilen veziküler stomatit virüsü temelli rVSV-ZEBOV aşısı, Gine’de “halka aşılama” fikriyle sınandı: vakanın çevresindeki temas halkaları hedeflenerek alev, çevresinden söndürüldü. Bu yalnızca bir klinik deneme değildi; salgın yönetiminin epistemolojisinde bir kırılmaydı. Eşzamanlı olarak şempanze adenovirüsü ve MVA tabanlı iki dozlu şemalar, bağışıklığın dayanıklılığına oynayan alternatif yollar açtı. Tedavide, önce umut sonra hayal kırıklığı ile anılan kokteyllerin ardından, nötralizan monoklonal antikor kombinasyonları, iyi tasarlanmış karşılaştırmalı çalışmalarla ağır hastalarda sağkalımı artırdıklarını gösterdi. ZMapp’ın başlattığı hattı, REGN-EB3 ve mAb114 (ansuvimab) gibi ajanlar olgunlaştırdı; ders açıktı: erken uygulanırsa kazanılan saatler, kazanılan hayatlardı.
Virüs, klinik sahnede yalnızca akut bir fırtına olarak kalmadı; perde kapanınca da fısıldamaya devam etti. İyileşenlerin gözlerinde üveit, eklemlerinde artralji, ruh hallerinde uzun gölgeler… İmmün ayrıcalıklı dokularda –göz küresi, testis, SSS– kalabilen viral RNA, nadir de olsa geç bulaş olasılığıyla halk sağlığına yeni sorular sordu: taburculuk sonrası danışmanlık, semen testleri, damgalamadan sakınan dikkatli iletişim. “İyileşti” sözcüğünün tıbbi ve toplumsal anlamının yeniden yazılması gerekti.
2018–2020 arasında Demokratik Kongo Cumhuriyeti’nin doğusunda, mikrobun değil, insanların güvenliği brifinglerin ilk maddesiydi. Aşılama ekiplerinin korunduğu, hastanelerin ateş hattında kaldığı bir bağlamda, bilimin teknik doğruluğu tek başına yetmedi; topluluk katılımı, söylenti dinamiklerinin anlaşılması ve şiddet sarmalının ortasında insani erişim, epidemiyolojik eğrilerin kaderini çizdi. Ebola’nın hikâyesi, hep olduğu gibi, bilimin toplumla imtihanıydı.
Bugün laboratuvar ışıkları altında, hikâye hâlâ sürüyor. Yapısal biyoloji, GP’nin nötralizan antikorlarla dansını atomik çözünürlükte izlerek “geniş çapraz reaktivite” hayalini kovalıyor; rasyonel immünojen tasarımı, yalnız Zaire hattı için değil, Sudan ve Bundibugyo türleri için de kapsayıcı çözümler arıyor. Vektör kombinasyonları ve adjuvan seçenekleri, ilk dozda hızlı koruma ile orta vadede dayanıklı bellek yanıtını dengelemeye çalışıyor. Saha tanısında izotermal çoğaltıma dayalı, enerji bağımlılığı düşük platformlar, yoğun bakım ile çadır klinik arasındaki mesafeyi kısaltıyor. Genomik sürveyans, her yeni dalgada yalnız “nereden geldi?” sorusuna değil, “hangi soydan, hangi uyum işaretleriyle?” sorusuna da yanıt arıyor; VP24 ve GP’deki kritik değişimlerin fenotipe izdüşümü, tedavi ve aşı uyarlamalarını bilgilendiriyor. Ekoloji cephesinde Tek Sağlık merceği, orman mozaiğindeki kırıkların –madencilik, yol yapımı, yabanî hayvan ticareti– insan-yarasa ara yüzlerini nasıl artırdığını haritalandırıyor; riskin “nerede” ve “ne zaman” yoğunlaştığını öngören modeller, yalnız salgın çıktıktan sonra değil, çıkmadan önce de konuşulsun diye.
Klinikte ise gerçekler yalın: Erken izolasyon ve kişisel koruyucu ekipman protokollerinin titiz uygulanması; agresif sıvı-elektrolit yönetimi; hipoksemiyle yarışan oksijen stratejileri; böbrek yetmezliğinde renal replasman; hemostazın ince ayarı… Bu “destekleyici bakım”, hangi yeni ilacın geldiğinden bağımsız olarak hayat kurtaran çekirdek olmaya devam ediyor. Ve evet, yeni ilaçlar geliyor: polimeraz inhibitörleri, küçük RNA yaklaşımları, konak faktörü hedefleyen küçük moleküller… Ancak hepsi, sahadaki bir hemşirenin KKE’yi çıkarırken tek bir adımı atlamamasına bağlı olan o büyük resmin küçük parçaları.
Ebola’nın evrimi, aslında bizim evrimimiz: hastanın elini tutarken göz koruyucunun buğusunun ardından da iletişim kurabilmek; güvenli defin için aileye saygı ile bulaş kontrolünün matematiğini aynı masaya koyabilmek; bir köy toplantısında “neden aşı?” sorusuna yalnız sayılarla değil, hikâyelerle cevap verebilmek. Keşfin ilk günlerinde elektron mikroskobunun altındaki o ipliksi şekil, bugün yalnızca bir virüsü değil, birbirine bağlı sistemleri temsil ediyor: hücre içi yollar, toplum içi bağlar, orman içi ekolojiler.
Yambuku’dan Guéckédou’ya, Kikwit’ten Beni’ye uzanan çizgi, sonuçta tek bir kavise benziyor: bilgiden güvene, güvenden işbirliğine. Keşif günlerinde seçilen o nehir adı, bir coğrafyayı değil, bir hareketi simgeliyor artık—akışı kesintiye uğrasa da denize varmaya kararlı bir hareketi. Ve güncel araştırmaların her sayfası, aynı cümleyi hatırlatıyor: Bu hastalık, laboratuvarların ve kliniklerin değil, laboratuvarlarla kliniklerin ve toplulukların ortak çalışmasıyla kontrol edilecek. Çünkü Ebola’nın hikâyesi, en başından beri, birlikte yazılan bir hikâyeydi.
İleri Okuma
- Feldmann, H., Geisbert, T. W. (2011). Ebola haemorrhagic fever. The Lancet, 377(9768), 849–862. doi:10.1016/S0140-6736(10)60667-8. (PubMed)
- Henao-Restrepo, A. M., et al. (2017). Efficacy and effectiveness of an rVSV-vectored vaccine in preventing Ebola virus disease: final results from the Guinea ring vaccination, open-label, cluster-randomised trial (Ebola Ça Suffit!). The Lancet, 389(10068), 505–518. doi:10.1016/S0140-6736(16)32621-6. (PubMed)
- Mulangu, S., et al. (2019). A randomized, controlled trial of Ebola virus disease therapeutics. The New England Journal of Medicine, 381(24), 2293–2303. doi:10.1056/NEJMoa1910993. (New England Journal of Medicine)
- Levine, M. M. (2019). Monoclonal Antibody Therapy for Ebola Virus Disease. The New England Journal of Medicine, 381(24), 2365–2366. doi:10.1056/NEJMe1915350. (PubMed)
- Wolf, J., Jannat, R., Dubey, S., et al. (2021). Development of Pandemic Vaccines: ERVEBO Case Study. Vaccines, 9(3), 190. doi:10.3390/vaccines9030190. (MDPI)
- European Medicines Agency (2021). Ervebo (rVSV∆G-ZEBOV-GP, live): EPAR – Medicine overview. Tam onay: 14 Ocak 2021 (ilk koşullu onay: 11 Kasım 2019). EMA/344888/2023. (European Medicines Agency (EMA))
- U.S. FDA (2020). INMAZEB (atoltivimab, maftivimab, odesivimab-ebgn) — BLA 761169: Approval & Reviews. 14 Ekim 2020; takip yazışmaları 2021. (FDA Access Data)
- U.S. FDA (2020). Ansuvimab-zykl (EBANGA, mAb114) — BLA 761172: Approval & Reviews. 21 Aralık 2020. (FDA Access Data)
- WHO (2025). Ebola disease — Fact sheet (updated 24 April 2025). Dünya Sağlık Örgütü. (Weltgesundheitsorganisation)
- WHO SAGE (2024). Systematic review of safety, efficacy, immunogenicity and duration of protection of licensed Ebola virus vaccines (SAGE, July 2024 briefing). (WHO CDN)
- CDC (2024). Ebola Disease Basics. Centers for Disease Control and Prevention (updated 23 April 2024). (CDC Deutschland)
- WHO (2024). Psychological first aid during Ebola virus disease outbreaks — Facilitator’s manual. Dünya Sağlık Örgütü, 19 Kasım 2024. (Weltgesundheitsorganisation)
- WHO (2025). Sudan virus disease — Uganda: Disease Outbreak News (21 Feb 2025). (Weltgesundheitsorganisation)
- ECDC (2023). Ebola virus disease outbreak — Uganda, 2022 (SUDV): Final epidemiological update. European Centre for Disease Prevention and Control. (ECDC)
- CDC (2024). Outbreak History — Ebola (güncel özet ve arşiv). Centers for Disease Control and Prevention. (CDC Deutschland)
- WHO (2021–2024). Ebola and Marburg virus outbreak toolbox & clinical management resources (bakım, tedarik paketleri, havuzlanmış CFR özetleri). Dünya Sağlık Örgütü. (Weltgesundheitsorganisation)


Yorum yazabilmek için oturum açmalısınız.