İçindekiler
1 | ICD-10 Kodları
- J44.0 Akut alt solunum yolu enfeksiyonlu KOAH
- J44.1 Akut alevlenme ile birlikte KOAH, tanımlanmamış
- J44.8 Diğer tanımlanmış KOAH
- J44.9 KOAH, tanımlanmamış
2 | Tanım
Kronik bronşitle amfizemin patolojik birlikteliği sonucu geri dönüşsüz hava akımı kısıtlanmasına yol açan, progresif, sistemik etkileri de olan kronik bir inflamatuar akciğer hastalığıdır. Tipik yakınmalar kronik balgamlı öksürük, dispne ve egzersiz intoleransıdır.
3 | Epidemiyoloji (Almanya, 2015)
- Yatarak tedavi edilen KOAH olgusu: 241 742
- Ortalama yaş: 70,5 yıl
- Ölüm sayısı: 31 073 (6’ncı en sık ölüm nedeni)
4 | Etiyoloji & Risk Faktörleri
- Tütün dumanı ≈ %90
- Hava kirliliği (ince toz, SO₂, NOₓ)
- Mesleki maruziyet (organik-inorganik toz, gaz, çözücü buharı)
- Tekrarlayan çocukluk İYE
- Genetik yatkınlık (örn. α-1 antitripsin eksikliği)
5 | Patoloji
- Bronş/bronşiyol duvarında kronik inflamasyon
- Bazal membran kalınlaşması
- Goblet hücre hiperplazisi + mukus artışı
- Alveolar septa yıkımı → amfizem boşlukları
- Pigmente makrofaj birikimi (antrakozis)
6 | Semptomlar ve Klinik Değerlendirme
- Kronik öksürük ± balgam (beyaz → viral, sarı/yeşil → bakteriyel)
- Efor dispnesi, göğüste sıkışma
- CAT (0-40) ve mMRC (0-4) skorlamalarıyla semptom yükü
- Son evrede “barel göğüs”, hiperinflasyon, amfizem bulguları
7 | Tanı Yaklaşımı
| Yöntem | Bulgular / Amaç |
|---|---|
| Spirometri | Post-BD FEV₁/FVC < 0,70 → tanısal |
| Kan gazı (BGA) | Kronik/akut hiperkapni, asit-baz durumu |
| Göğüs radyografisi / BT | Pnömoni, pnömotoraks dışlama, amfizem |
| Balgam kültürü & mikrobiyoloji | Alevlenmede patojen belirleme |
| Kan sayımı & CRP | Enflamasyon, poliglobüli |
| PFT (DLCO, RV, TLC) | Hiperinflasyon, diffüzyon kusuru |
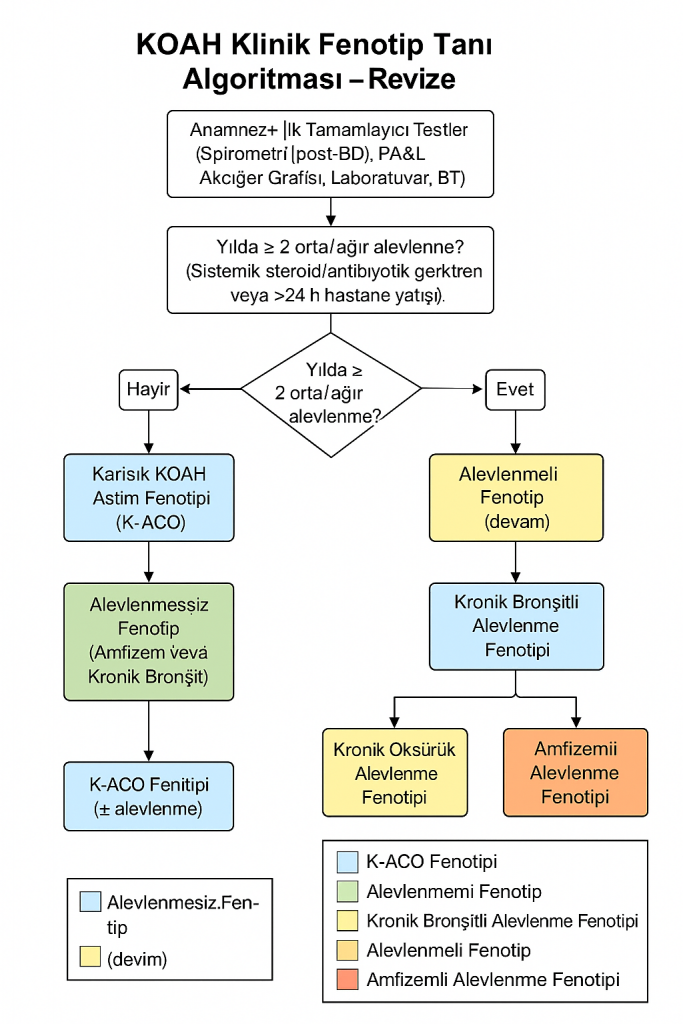
8 | Sınıflandırma
a. Hava akımı kısıtlanması (GOLD derecesi)
- GOLD 1 ≥ %80
- GOLD 2 50–79 %
- GOLD 3 30–49 %
- GOLD 4 < %30 (FEV₁, post-BD)
b. Semptom/alevlenme matrisi (ABCD/2023 E-REFORM)
- A Düşük semptom & düşük risk
- B Yüksek semptom & düşük risk
- C Düşük semptom & yüksek risk
- D Yüksek semptom & yüksek risk
9 | Ayırıcı Tanı
Bronşiyal astım, bronşektazi, kistik fibroz, sarkoidoz, bronşiolit obliterans.
10 | Uzun Süreli Tedavi Stratejisi
| Hedef | Müdahaleler |
|---|---|
| Risk azaltma | SİGARA BIRAKMA, grip & pnömokok aşısı |
| İlaç | – Bronkodilatörler: • SABA/SAMA (gerektiğinde) • LABA veya LAMA (1’inci basamak) • LABA + LAMA (semptom yüksek) • LABA + ICS (eoz ≥ 300/mm³ veya ≥2 alevlenme/yr) • LABA + LAMA + ICS (ileri) • PDE-4 inh. (roflumilast) – kronik bronşit + FEV₁ < %50 • Teofilin (3’üncü seçenek) |
| Spesifik biyolojik | Dupilumab (IL-4Rα); eoz ≥ 300/mm³, T2-yüksek fenotip |
| Non-farmakolojik | Pulmoner rehabilitasyon, direnç-egzersiz, hasta eğitimi, uzun süreli O₂ (PaO₂ ≤ 55 mmHg veya SaO₂ ≤ %88), ev mekanik ventilasyonu |
| Cerrahi/Endoskopik | Bulektomi, LVRS, endobronşiyal valf (heterojen amfizem & CV–), akciğer transplantasyonu (FEV₁ < %20 veya BODE ≥ 7) |
11 | Akut Alevlenme Yönetimi
a. Farmakolojik
- Sistemik kortikosteroid: Prednizon 40 mg p.o. × 5 gün
- Bronkodilatör nebül: Berodual®, Combivent® (SABA + SAMA)
- Antibiyotik (süpüratif balgam ± CRP↑):
- Sefazolin 2 g i.v. 8-12 s
- Piperasilin/Tazobaktam 4,5 g i.v. 8-12 s
- İntravenöz kortikosteroid: Deksametazon 25-50 mg (Solu-Dac®)
- İnhale mukolitik/serum fizyolojik nebul: NaCl %0,9
b. Solunum desteği
- NIV başlama eşiği: pH 7,30–7,35 & PaCO₂ > 45 mmHg (Yoğun bakım dışı)
- pH < 7,25 → Yoğun bakım değerlendirmesi/intübasyon olasılığı
12 | İleri Tedaviler
| Yöntem | Uygun Hasta Profili | Klinik Kazanç |
|---|---|---|
| Endobronşiyal Valf (Zephyr®, Spiration®) | Tek lob‐dominant heterojen amfizem, Chartis® ile CV(–) | FEV₁ +%20, 6-DKY +35 m, SGRQ –7 |
| Dupilumab | Eoz ≥ 300/mm³, T2-yüksek KOAH | Alevlenme –%30, FEV₁ +160 mL |
| Akciğer Transplantasyonu | FEV₁ < %20, BODE ≥ 7, ≥3 ağır alevlenme/yıl | Yaşam süresi & QoL artışı |
Keşif
Erken Keşifler:
- 1814: Charles Badham, günümüzde KOAH’ın erken bir belirtisi olarak kabul edilen bronşiti tanımlamak için “nezle” terimini kullandı.
- 1837: René Laennec, stetoskopla yaptığı çalışmalarla KOAH’ın önemli bir bileşeni olan amfizemin ilk net tanımlarını yaptı.
20. Yüzyıl Gelişmeleri:
- 1953: George L. Waldbott, sigara dumanının kronik akciğer hastalığıyla ilişkili zararlı etkilerini tanımlayarak KOAH’ın ana risk faktörlerinden birini anlamanın yolunu açtı.
- 1963: İngiliz Tıbbi Araştırma Konseyi, bronşit ve amfizemin kronik doğasının altını çizdi ve klinik tanı için kriterler oluşturarak bu durumları diğer solunum yolu hastalıklarından daha net bir şekilde ayırdı.
- 1965: Noël Christopher Snell, tıp literatüründe “KOAH” terimini ilk kullananlardan biri oldu ve bu da KOAH’ın ayrı bir hastalık olarak ayırt edilmesine yardımcı oldu.
- 1972: Peter J. Sterk ve meslektaşları KOAH’ta hava yolu enflamasyonu mekanizmalarını öne sürerek alevlenmelerin artmış enflamatuar aktivite evreleri olarak tanınmasına yol açtı.
20. Yüzyılın Sonlarından 21. Yüzyılın Başlarına
- 1977: Bartolome R. Celli ve arkadaşları alevlenmelerin tetiklenmesinde bakteriyel enfeksiyonların önemini ve tedavisinde antibiyotiklerin rolünü vurguladılar.
- 1981: Paul T. Macklem ve Jere Mead, alevlenmeler sırasında hiperinflasyon ve hava hapsi kavramını ortaya atarak akciğer hacmini azaltmayı amaçlayan tedavi stratejilerini etkiledi.
- 1995: Avrupa Solunum Derneği (ERS) ve daha sonra 2001 yılında Kronik Obstrüktif Akciğer Hastalığı Küresel Girişimi (GOLD), alevlenmeler için standartlaştırılmış yönetim protokollerini içeren kılavuzlar sunarak küresel tedavi uygulamalarını önemli ölçüde etkiledi.
- 2000: KOAH’ta tedavi stratejilerini inceleyen en büyük çalışmalardan biri olan ve özellikle kombinasyon tedavileriyle alevlenmelerin azaltılmasını hedefleyen TORCH (Towards a Revolution in COPD Health) çalışması başladı.
21. Yüzyıl Yenilikleri:
- 2007: Marc Decramer ve arkadaşları, bir fosfodiesteraz-4 inhibitörü olan roflumilastın ağır KOAH’ta alevlenme sıklığını azaltma üzerindeki etkilerini gösterdi.
- 2010s: 2018’deki IMPACT çalışması da dahil olmak üzere birçok çalışmada alevlenme oranlarında önemli azalma gösteren üçlü inhalasyon tedavisinin (ICS/LABA/LAMA) tanıtılması.
- 2020: KOAH’ta spesifik enflamatuar yolakları hedefleyen biyolojik tedavilerin kullanımı araştırılmakta ve alevlenmelerin kişiselleştirilmiş tedavisinde yeni bir çağın habercisi olmaktadır.
İleri Okuma
- Rodriguez-Roisin, R., et al. “Toward a Consensus Definition for COPD Exacerbations.” Chest, vol. 117, no. 5, 2000, pp. 398S-401S.
- Calverley, P. M. A., Anderson, J. A., Celli, B., et al. (2007). “Salmeterol and fluticasone propionate and survival in chronic obstructive pulmonary disease.” New England Journal of Medicine, 356(8), 775-789.
- Celli, B. R., & MacNee, W. (2004). “Standards for the Diagnosis and Treatment of Patients with COPD: A Summary of the ATS/ERS Position Paper.” European Respiratory Journal, 23(6), 932-946.
- Reddel, H. K., Taylor, D. R., Bateman, E. D., et al. (2009). “An Official American Thoracic Society/European Respiratory Society Statement: Asthma Control and Exacerbations.” American Journal of Respiratory and Critical Care Medicine, 180(1), 59-99.
- Leuppi J D et al. (2013). Short-Term vs Conventional Glucocorticoid Therapy in Acute Exacerbations of COPD. JAMA 309(21): 2223-2231.
- Wedzicha, J. A., et al. “Management of COPD Exacerbations: a European Respiratory Society/American Thoracic Society Guideline.” European Respiratory Journal, vol. 47, no. 3, 2016, pp. 698-713.
- Ergan B et al. (2017). ERS/ATS Clinical Practice Guidelines for Non-Invasive Ventilation. Eur Respir J 50(4): 1602426.
- Vogelmeier, C., Criner, G. J., Martinez, F. J., et al. (2017). “Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Lung Disease 2017 Report: GOLD executive summary.” European Respiratory Journal, 49, 557-582.
- Criner G J et al. (2018). Zephyr Endobronchial Valve Therapy for Emphysema. Am J Respir Crit Care Med 198(9): 1151-1164.
- Celli B R, Wedzicha J A. (2019). Lung Transplantation in COPD. J Thorac Dis 11(Suppl 14): S1927-S1934.
- Singh, D., Agusti, A., Anzueto, A., et al. (2019). “Global strategy for the diagnosis, management, and prevention of chronic obstructive lung disease: the GOLD science committee report 2019.” European Respiratory Journal, 53.
- Global Initiative for Chronic Obstructive Lung Disease (GOLD). “Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease.” 2020 Report.
- Global Initiative for Asthma (GINA). “Global Strategy for Asthma Management and Prevention.” 2020 Update.
- Rochester C L et al. (2021). Pulmonary Rehabilitation after COPD Hospitalization. Am J Respir Crit Care Med 204(3): 222-224.
- Global Initiative for Chronic Obstructive Lung Disease (GOLD). “GOLD Reports,” 2023.
- Lehtimäki L et al. (2023). Dupilumab for COPD with Type 2 Inflammation. N Engl J Med 389: 1035-1048.
- Rabe K F et al. (2024). Dupilumab in COPD with Blood Eosinophils. N Engl J Med 390: 456-468.
- Global Initiative for Chronic Obstructive Lung Disease. (2024). GOLD Executive Report.