Sinonim: Magnetic resonance imaging (MRI)
Genellikle Manyetik Rezonans Görüntüleme (MRG) olarak adlandırılan manyetik rezonans (NMR) prensibine dayalı tomografinin **tanısal bilgisayar destekli görüntüleme prosedürü, iç vücut yapılarının ayrıntılı olarak görüntülenmesi için kullanılan oldukça gelişmiş bir görüntüleme yöntemidir. MRG, iyonlaştırıcı radyasyon kullanmadan yüksek çözünürlüklü görüntüler oluşturmak için güçlü manyetik alanlar, radyofrekans darbeleri ve bilgisayar işleme kullanır. Aşağıda MRG, endikasyonları, kontrendikasyonları ve yaygın MRG sekanslarının ayrıntılı bir açıklaması hakkında genişletilmiş bir açıklama yer almaktadır.

İçindekiler
MRI endikasyonları
MR, üstün yumuşak doku kontrastı ve çok düzlemli görüntüleme yetenekleri nedeniyle klinik teşhislerde yaygın olarak kullanılmaktadır. Yaygın endikasyonlar şunlardır:
Nörolojik Bozukluklar:
- Beyin tümörleri
- Multipl skleroz
- İnme
- Epilepsi
- Travmatik beyin hasarı
- Nörodejeneratif hastalıklar (örn. Alzheimer, Parkinson)
- Beyin apseleri veya enfeksiyonları
Omurilik ve Omurga Bozuklukları:
- Fıtıklaşmış diskler
- Omurilik sıkışması veya yaralanması
- Dejeneratif disk hastalığı
- Spondilit veya spondiloz
Kas-İskelet Sistemi Bozuklukları:
- Eklem yaralanmaları (örn. ACL yırtıkları, menisküs yırtıkları)
- Kas yırtılmaları ve gerilmeleri
- Osteomiyelit
- Kemik veya yumuşak dokudaki tümörler
- Artrit
Kalp ve Damar Görüntüleme:
- Doğuştan kalp hastalığı
- Kardiyak fonksiyon analizi (örn. ejeksiyon fraksiyonu)
- Kan damarı görüntülemesi (örn. anevrizma veya stenoz için MR anjiyografi)
Abdominal ve Pelvik Görüntüleme:
- Karaciğer veya böbrek tümörleri
- Pelvik organ değerlendirmesi
- Rahim veya yumurtalık patolojisi
- Prostat görüntüleme
Diğer Uygulamalar:
- Meme kanseri görüntülemesi (kontrastlı MRG)
- Metastazlar veya gizli hastalık için tüm vücut taraması
MRI için kontrendikasyonlar
MRG genellikle güvenli olmakla birlikte, güçlü manyetik alan ve radyofrekans enerjisi nedeniyle bazı kontrendikasyonlar göz önünde bulundurulmalıdır:
Mutlak Kontrendikasyonlar:
- Ferromanyetik yabancı cisimlerin** varlığı (örn. şarapnel, bazı anevrizma klipsleri).
- İmplante Edilebilir Kardiyoverter-Defibrilatörler (ICD’ler)**.
- Bazı eski koklear implantlar.
Göreceli Kontrendikasyonlar:
- Yapay kalp pilleri (uyumluluk kalp pili tipine ve MRI ayarlarına bağlıdır).
- Klaustrofobi (sedasyon veya açık MRG sistemleri gerektirebilir).
- Hamilelik (özellikle ilk trimesterde, faydaları risklerinden daha ağır basmadıkça).
- Nefrojenik sistemik fibrozis (NSF) riski nedeniyle kontrast maddeler (örn. gadolinyum) gerektiğinde Ciddi böbrek yetmezliği.
Önlemler:
- Ferromanyetik pigmentler içeren dövmeler veya kalıcı makyaj.
- Ortopedik implantlar (örn. eklem protezleri, çubuklar) MRG uyumluluğu açısından doğrulanmalıdır.
Yaygın MRI Sekansları ve Kısaltmaları
MRG sekansları, çeşitli doku özelliklerini vurgulamak için veri elde etmenin farklı yöntemleridir. Aşağıda yaygın olarak kullanılan dizilerin ayrıntılı bir açıklaması bulunmaktadır:
| Kısaltma | Açıklama | Eşanlamlı/Anahtar Notlar |
|---|---|---|
| CE-FAST (Contrast Enhanced Fast Acquisition in Steady State) | Sabit Durumda Kontrast Geliştirilmiş Hızlı Edinim | Dengeli manyetizasyon kullanır. |
| CISS (Constructive Interference in Steady State) | Sabit Durumda Yapıcı Girişim | İki gradyan eko (GE) sekansını sinyal ekleme ile birleştirir. |
| CORE (Clinically Optimized Regional Exams) | Klinik Olarak Optimize Edilmiş Bölgesel İncelemeler | Bölgesel görüntüleme için özelleştirilebilir sekanslar. |
| CSFSE (Contiguous Slice Fast-Acquisition Spin Echo) | Contiguous Slice Fast-Acquisition Spin Echo | Dokuların yüksek çözünürlüklü görüntülenmesi. |
| CSI (Chemical Shift Imaging) | Kimyasal Kaydırmalı Görüntüleme | Kimyasal bileşime dayalı olarak doku tiplerini ayırt eder. |
| DANTE (Delays Alternating with Nutations for Tailored Excitation) | Özel Uyarım için Nutasyonlarla Değişen Gecikmeler | Gelişmiş yağ bastırma tekniği. |
| DE-FLASH (Dual Echo – Fast Low Angle Shot) | Dual Echo – Hızlı Düşük Açılı Çekim | Özellikle dinamik çalışmalar için yüksek hızlı görüntüleme. |
| DESS (Double Echo Steady State) | Double Echo Steady State | SNR’yi iyileştirmek için çift gradyan ekolarını birleştirir. |
| EPI (Echo Planar Imaging) | Echo Planar Imaging | Fonksiyonel MRI (fMRI) ve difüzyon görüntülemede kullanılan hızlı edinim. |
| FLAIR | Fluid Attenuated Inversion Recovery | Sıvı sinyallerini bastırarak beyindeki lezyon tespitini artırır. |
| FAST | Fast Acquired Steady State Technique | Balanced gradient echo imaging. |
| FISP | Fast Imaging with Steady-state Precession | Mükemmel kontrastlı gradyan eko sekansı. |
| FLASH (Fast Low Angle Shot) | Hızlı Düşük Açılı Çekim | Bozulmuş gradyan eko, dinamik çalışmalarda ve kardiyak görüntülemede kullanışlıdır. |
| GRASS | Gradient Recalled Acquisition in Steady State | Yüksek zamansal çözünürlüğe sahip görüntüler üretir. |
| HASTE | Half Fourier Acquired Single-shot Turbo Spin Echo | Abdominal görüntüleme için etkilidir. |
| IR | Inversion Recovery | Belirli sinyalleri bastırarak doku kontrastını artırır. |
| STIR | Short-Tau Inversion Recovery | Kas-iskelet sistemi görüntülemesi için yağ bastırma. |
| MP-RAGE | Magnetization Prepared Rapid Gradient Echo | Yüksek çözünürlüklü 3D görüntüleme, genellikle beyin çalışmaları için kullanılır. |
| RARE | Rapid Acquisition with Relaxation Enhancement | Hızlı görüntüleme için turbo spin eko sekansı. |
| SENSE (Sensitivity Encoding) | Hassasiyet Kodlaması | Daha hızlı alım için paralel görüntüleme. |
| SPGR | Spoiled Gradient Recalled Acquisition | Mükemmel anatomik detay sağlar. |
| SSFP | Steady State Free Precession | Sıvı bakımından zengin dokular için yüksek sinyal sunar. |
| TRUE-FISP | True Fast Imaging with Steady State Precession | Kardiyak ve abdominal görüntüleme için yüksek kontrast. |
| TSE | Turbo Spin Echo | Daha az hareket hassasiyeti ile hızlı, yüksek kaliteli görüntüler üretir. |
| UTE (Ultra-short Echo Time) | Ultra kısa Eko Süresi | Kısa T2 gevşeme sürelerine sahip dokular (örn. tendonlar, bağlar) için özel olarak tasarlanmıştır. |
| VIBE (Volume Interpolated Breathhold Examination) | Volume Interpolated Breathhold Examination | Dinamik karaciğer ve abdominal görüntüleme için kullanılır. |
Manyetik Rezonans Görüntülemenin (MRI) Çalışma Mekanizması
Manyetik Rezonans Görüntüleme (MRI), insan vücudundaki yumuşak dokuların ayrıntılı görüntülerini oluşturmak için nükleer manyetik rezonans (NMR) ilkelerine dayanır. Bu süreç, atom çekirdeklerinin (öncelikle hidrojen) güçlü bir manyetik alan ve radyofrekans (RF) dalgaları ile etkileşimini içerir.
1. Hidrojen Çekirdekleri ve Manyetik Alanlar
- Hedef Olarak Hidrojen Atomları:
İnsan vücudu büyük ölçüde su ve yağdan oluşur ve bunların her ikisi de bol miktarda hidrojen atomu içerir. Hidrojen çekirdekleri (protonlar) spin adı verilen bir özelliğe sahiptir, bu da onları küçük çubuk mıknatıslar gibi hareket ettirir. - Manyetik Alanda Hizalama:
Bir kişi MRI tarayıcısına yerleştirildiğinde, güçlü bir manyetik alan (B₀ olarak gösterilir) uygulanır. Bu alan hidrojen çekirdeklerinin çoğunu manyetik alana paralel (düşük enerji durumu) ya da antiparalel (yüksek enerji durumu) olarak hizalar. Biraz daha fazla çekirdek paralel hizalanarak manyetik alan boyunca bir net manyetizasyon vektörü (M₀) oluşturur.
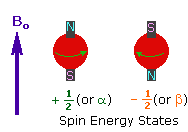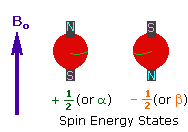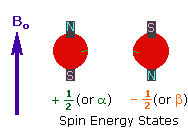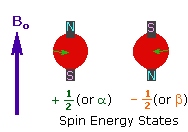
2. Radyofrekans Darbeleri ile Uyarma
- Rezonans ve Enerji Emilimi:
Hidrojen çekirdeklerinin rezonans frekansında, tipik olarak Tesla başına 42 MHz (Larmor frekansı) aralığında bir radyo frekans (RF) darbesi uygulanır. Bu RF enerjisi çekirdekleri uyararak bazılarının yüksek enerjili duruma geçmesine neden olur ve net mıknatıslanma vektörünü ana manyetik alanla hizalanmasından uzaklaştırır. - Enine Mıknatıslanma:
RF darbesi ayrıca hidrojen çekirdeklerinin fazda ilerlemesine (senkronize olmasına) neden olarak ana manyetik alana dik bir düzlemde ölçülebilir bir manyetik sinyal oluşturur.

3. Gevşeme ve Sinyal Üretimi
RF darbesi kapatıldıktan sonra, hidrojen çekirdekleri yavaş yavaş orijinal hizalamalarına geri döner, bu süreç rahatlama olarak bilinir. İki gevşeme süreci meydana gelir:
T₁ Gevşemesi (Boylamsal Gevşeme):
- Protonlar çevreleyen dokuya enerji salar ve ana manyetik alanla yeniden hizalanır.
- Manyetizasyonun %63’ünün yeniden hizalanması için geçen süre T₁ zamanıdır.
- T₁ ağırlıklı görüntüler yağ ve yumuşak dokuları vurgular.
T₂ Gevşemesi (Enine Gevşeme):
- Protonlar, yakındaki çekirdeklerle etkileşimler nedeniyle faz tutarlılığını kaybeder.
- Enine manyetizasyonun %63’ünün bozunması için geçen süre T₂ zamanıdır.
- T₂ ağırlıklı görüntüler beyin omurilik sıvısı ve ödem gibi sıvıları vurgular.
Rahatlama sırasında azalan sinyaller, makinenin RF bobinleri tarafından algılanan salınımlı manyetik alanlar üretir.

4. Gradyan Manyetik Alanlar Kullanarak Mekansal Lokalizasyon
Bir görüntü oluşturmak için, MRI makinesi sinyali lokalize etmek için ek manyetik alan gradyanları kullanır:
- Dilim Seçimi:
Bir gradyan manyetik alan (örneğin Z ekseni boyunca) vücuttaki Larmor frekansını değiştirir. Belirli bir frekansta bir RF darbesi uygulayarak, yalnızca belirli bir dilim içindeki çekirdekler uyarılır. - Frekans ve Faz Kodlaması:
- Frekans kodlama gradyanları, bir eksen boyunca sinyal frekansında uzamsal varyasyon yaratır.
- Faz kodlayan gradyanlar, dik bir eksen boyunca presesyon fazını değiştirir.
Bu gradyanlar, MR sinyalinin üç boyutta lokalize edilmesini sağlayarak uzamsal kodlamanın temelini oluşturur.
5. Görüntü Yeniden Yapılandırma
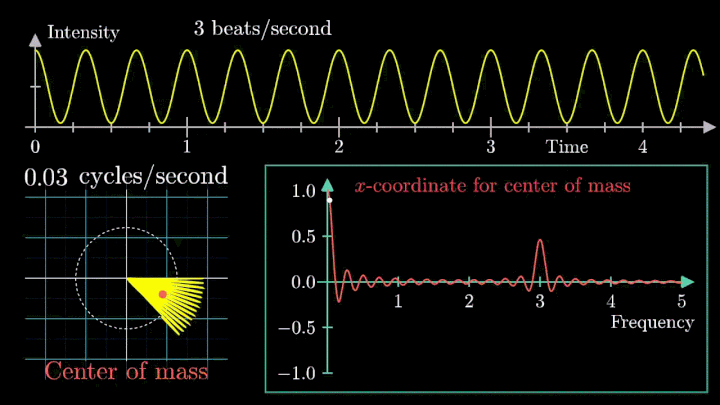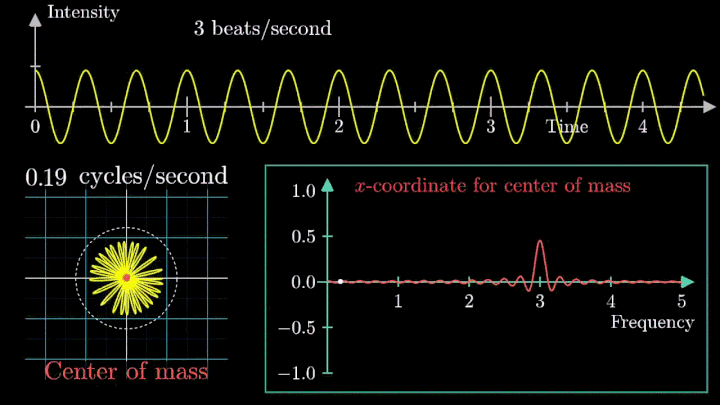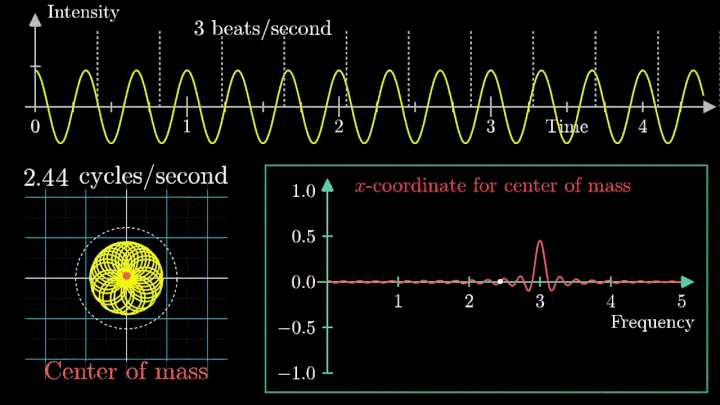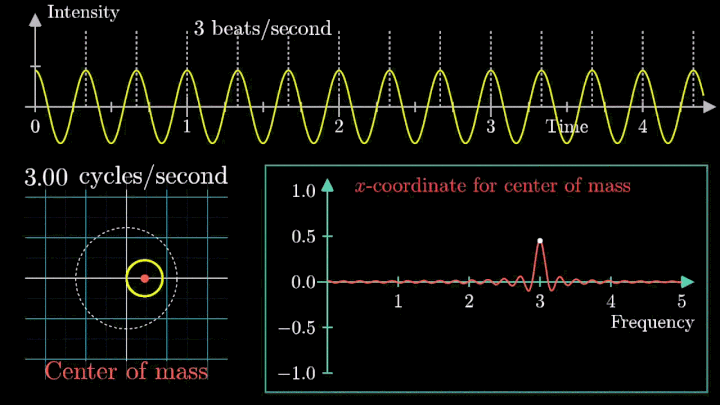
Toplanan sinyaller sayısallaştırılır ve Fourier Dönüşümü (FT) adı verilen matematiksel bir algoritma kullanılarak analiz edilir. Bu işlem, ham frekans ve faz verilerini vücut diliminin ayrıntılı bir uzamsal görüntüsüne dönüştürür.
MRI Makinesinde Beton Uygulaması
Bir MRI makinesi bu ilkeleri temel bileşenleri aracılığıyla uygular:
Mıknatıs:
- Süper iletken bir mıknatıs, nükleer hizalama için gereken güçlü ve tekdüze manyetik alanı (B₀) üretir.
- Alan güçleri tipik olarak 1,5 Tesla ile 7 Tesla arasında değişir ve daha yüksek alanlar daha iyi çözünürlük sağlar.
Radyofrekans (RF) Sistemi:
- RF bobinleri hidrojen çekirdeklerini uyarmak için darbeler iletir ve gevşeme sırasında yayılan sinyalleri alır.
- Hedefe yönelik görüntüleme için özel bobinler (örn. baş bobinleri, diz bobinleri) kullanılır.
Gradyan Sistemi:
- Gradyan bobinler, kesit seçimi ve uzamsal kodlama için değişken manyetik alanlar oluşturur.
- Bu gradyanların hızlı bir şekilde değiştirilmesi, hızlı görüntüleme sekansları sağlar.
Bilgisayar Sistemi:
- Algılanan sinyalleri işler, Fourier Dönüşümü gerçekleştirir ve verileri görüntüler halinde yeniden yapılandırır.
- Gelişmiş yazılım 3D görüntüleme, fonksiyonel çalışmalar ve dinamik kontrastlı görüntülemeye olanak sağlar.
Örnek: MRI Beyin Taraması
Hazırlık:
- Hasta tarayıcı masasına uzanır ve başının etrafına bir baş bobini yerleştirilir.
- Makine, beyindeki hidrojen çekirdeklerini hizalamak için tek tip bir manyetik alan oluşturur.
Görüntüleme Süreci:
- Bir RF darbesi, belirli bir beyin dilimindeki hidrojen çekirdeklerini uyarır.
- Gri madde, beyaz madde ve beyin omurilik sıvısını ayırt etmek için T₁ ve T₂ gevşeme sinyalleri tespit edilir.
Çıktı:
- Yeniden yapılandırılan görüntüler beynin yapısal ayrıntılarını ortaya çıkararak tümör, multipl skleroz veya inme gibi durumların teşhisine olanak tanır.
Keşif
Aslen Nükleer Manyetik Rezonans (NMR) olarak bilinen Manyetik Rezonans Görüntüleme (MRI)nin gelişimi, tıbbi görüntülemedeki en önemli başarılardan birini temsil etmektedir. Geçmişi, her biri bugün güvendiğimiz modern MRI sistemlerine katkıda bulunan önemli kilometre taşlarıyla doludur. Aşağıda bu kilometre taşlarının bütünleşik bir anlatımı yer almaktadır.
1. Nükleer Manyetik Rezonansın Keşfi (1930’lar-1940’lar)
MRG’nin hikayesi, atom çekirdeklerinin manyetik alan varlığında elektromanyetik radyasyonu emdiği ve yaydığı fiziksel bir fenomen olan nükleer manyetik rezonansın (NMR) keşfiyle başlar.
- 1938 yılında Isidor Rabi bu fenomeni ilk olarak moleküler ışınlarda tespit etmiş ve 1944 yılında Nobel Fizik Ödülü’nü kazanmıştır.
- Daha sonra, 1946’da Felix Bloch ve Edward Purcell bağımsız olarak sıvılarda ve katılarda NMR’yi gösterdiler. Çalışmaları, manyetik rezonansın hem fizik hem de tıp biliminde uygulanmasının temelini attı ve 1952’de Nobel Fizik Ödülü’nü kazandı.
2. Biyolojik Uygulamalara Geçiş (1950’ler-1960’lar)
1950’ler ve 1960’lar boyunca bilim insanları biyolojik sistemlerde NMR kullanımını araştırdılar.
- Spektroskopik tekniklerdeki gelişmeler, araştırmacıların biyolojik dokuların moleküler yapılarını analiz etmelerine olanak sağladı.
- Bu deneyler, farklı doku türlerinin farklı NMR sinyalleri sergilediğini göstererek, teknolojinin non-invaziv görüntüleme potansiyeline işaret etti.
3. Tıbbi Görüntüleme Aracı Olarak MRG’nin Doğuşu (1970’ler)
1970’lerin başında spektroskopiden görüntülemeye geçiş başladı.
- Paul Lauterbur** 1973 yılında uzaysal lokalizasyon kavramını ortaya atarak NMR’da devrim yarattı. Manyetik alan gradyanlarının iki boyutlu görüntüler oluşturmak için kullanılabileceğini göstererek ilk gerçek MRI görüntüsünü oluşturdu.
- Aynı dönemde Sir Peter Mansfield, tarama sürelerini önemli ölçüde azaltan eko-planar görüntüleme (EPI) yöntemini geliştirerek görüntü alma tekniklerini iyileştirdi.
- Bu çığır açan katkılar Lauterbur ve Mansfield’e 2003 yılında Nobel Fizyoloji veya Tıp Ödülü kazandırmıştır.
4. İlk İnsan MRI Taramaları (1977)
1970’lerin başında MRG’nin kanserli ve kanserli olmayan dokuları ayırt edebileceğini öne süren Raymond Damadian 1977’de bir insanın ilk tüm vücut MRG taramasını gerçekleştirdi. İşlem yaklaşık beş saat sürdü, ancak MRG’nin tıbbi teşhis için potansiyelini doğruladı. Damadian’ın katkıları, ticari olarak kullanılabilen ilk MRI makinelerinin geliştirilmesine yol açtı.
5. Ticarileştirme ve Yaygın Benimseme (1980’ler)
1980’lerde MR teknolojisinde ve hastanelerde benimsenmesinde hızlı ilerlemeler görüldü:
- Süper iletken mıknatısların** kullanılmaya başlanması daha güçlü manyetik alanların oluşmasını sağlayarak görüntü çözünürlüğünü artırdı.
- 1980’lerin ortalarında, yumuşak dokuların X-ışınları veya BT taramalarından daha üstün olan net görüntülerini sağlayan MRI makineleri ticari olarak kullanılabilir hale geldi.
- Gadolinyum bazlı kontrast maddeler* geliştirilerek MRG’nin tanısal yetenekleri daha da artırıldı.
6. Fonksiyonel MRG’deki (fMRI) Gelişmeler (1990’lar)
1990’lar, araştırmacıların kan oksijenasyonundaki değişiklikleri ölçerek beyin aktivitesini gerçek zamanlı olarak görselleştirmelerine olanak tanıyan fonksiyonel MRG’nin (fMRI) ortaya çıkmasıyla önemli bir dönüm noktası oldu.
- Seiji Ogawa** ve meslektaşları bu tekniğe öncülük ederek biliş, duygu ve nörolojik bozuklukların non-invaziv olarak incelenmesini sağlayarak nörobilimde yeni sınırlar açmıştır.
7. Paralel Görüntüleme ve Daha Hızlı Taramalar (2000’ler)
2000’li yıllardaki teknolojik gelişmeler tarama hızını ve görüntü kalitesini artırmaya odaklanmıştır.
- Çözünürlükten ödün vermeden çekim sürelerini azaltmak için SENSE (Sensitivity Encoding) ve GRAPPA (Generalized Autocalibrating Partially Parallel Acquisitions) gibi Paralel görüntüleme teknikleri geliştirildi.
- Bu yenilikler MRG’yi rutin klinik kullanım için daha erişilebilir ve verimli hale getirdi.
8. 7-Tesla ve Ultra Yüksek Alanlı MR (2010’lar)
2010’larda 7-Tesla (7T) MRI tarayıcılarının geliştirilmesi, görüntü çözünürlüğü ve detayında bir sıçramayı temsil ediyordu.
- Bu ultra yüksek alanlı tarayıcılar, ince beyin yapıları ve diğer anatomik ayrıntılar hakkında benzeri görülmemiş bilgiler sağladı.
- FDA, 2017 yılında klinik kullanım için ilk 7T tarayıcıyı onaylayarak nöroloji ve ileri tanı alanlarındaki uygulamalarını genişletti.
9. Yapay Zeka Entegrasyonu ve Spektroskopik Gelişmeler (2020’ler)
2020’ler, yapay zekayı (AI) MRG analizine getirerek tanısal doğruluğu artırdı ve yoğun zaman alan görevleri otomatikleştirdi.
- Yapay zeka algoritmaları artık ince anormalliklerin tespit edilmesine ve görüntü rekonstrüksiyonunun iyileştirilmesine yardımcı oluyor.
- MR spektroskopisindeki** gelişmeler, klinisyenlerin dokuların kimyasal bileşimini analiz etmesine olanak tanıyarak kanser ve metabolik bozukluklar gibi hastalıklar hakkında moleküler düzeyde bilgi sağlar.
10. COVID-19 Pandemisi Sırasında MRG’nin Rolü (2020’ler)
MRG, COVID-19 salgını sırasında özellikle virüsle ilişkili akciğer, kalp ve beyin komplikasyonlarının belirlenmesi ve izlenmesinde çok önemli bir rol oynamıştır.
- Taşınabilir MRI sistemlerindeki yenilikler de kritik bakım ortamlarında yatak başı görüntülemeye olanak sağladı.
İleri Okuma
- Bloch, F., Hansen, W. W., & Packard, M. (1946). The nuclear induction experiment. Physical Review, 70(7–8), 474–485.
- Purcell, E. M., Torrey, H. C., & Pound, R. V. (1946). Resonance absorption by nuclear magnetic moments in a solid. Physical Review, 69(1–2), 37–38.
- Lauterbur, P. C. (1973). Image formation by induced local interactions: Examples employing nuclear magnetic resonance. Nature, 242(5394), 190–191.
- Damadian, R. (1971). Tumor detection by nuclear magnetic resonance. Science, 171(3976), 1151–1153.
- Mansfield, P. (1977). Multi-planar image formation using NMR spin echoes. Journal of Physics C: Solid State Physics, 10(3), L55–L58.
- Ogawa, S., Tank, D. W., Menon, R., et al. (1992). Intrinsic signal changes accompanying sensory stimulation: Functional brain mapping with magnetic resonance imaging. Proceedings of the National Academy of Sciences, 89(13), 5951–5955.
- Edelstein, W. A., Hutchison, J. M. S., Johnson, G., & Redpath, T. (1980). Spin warp NMR imaging and applications to human whole-body imaging. Physics in Medicine and Biology, 25(4), 751–756.
- Haacke, E. M., Brown, R. W., Thompson, M. R., & Venkatesan, R. (1999). Magnetic Resonance Imaging: Physical Principles and Sequence Design. Wiley-Liss.
- Slichter, C. P. (1990). Principles of Magnetic Resonance. Springer-Verlag.
- Salomir, R., de Oliveira, P. L., & Moonen, C. T. (2003). Dynamic magnetic resonance imaging of hyperthermia-induced tissue changes. Magnetic Resonance in Medicine, 49(3), 527–532.
