Montreal Bilişsel Değerlendirme (MoCA)
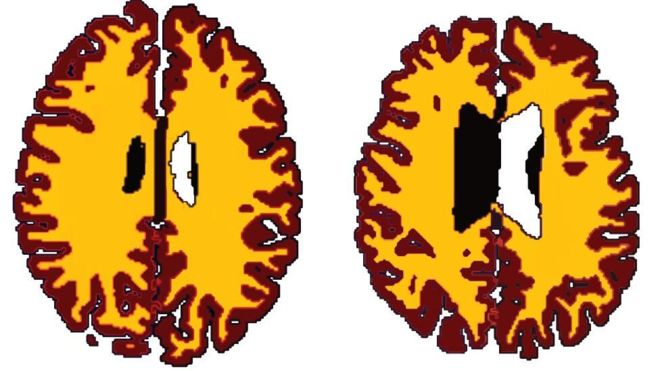
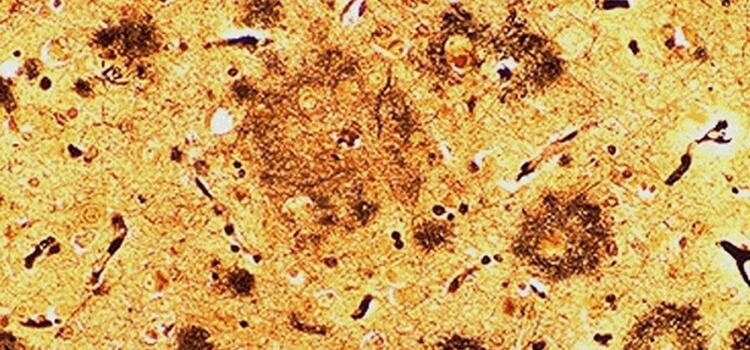
Montreal Bilişsel Değerlendirme (MoCA), bilişsel bozukluğu tespit etmek için yaygın olarak kullanılan bir tarama değerlendirmesidir. Montreal, Quebec’te Dr. Ziad Nasreddine tarafından 1996 yılında oluşturulmuştur. Hafif bilişsel işlev bozukluğu için çeşitli bilişsel alanları değerlendiren hızlı bir tarama aracı olarak tasarlanmıştır: Kısa süreli hafıza hatırlama görevi: Bu, beş isimden oluşan iki öğrenme denemesini ve yaklaşık beş dakika … Devamını oku