“Aort” terimi, Yunanca “büyük arter” anlamına gelen “aortē” kelimesinden türetilmiştir. “Anevrizma” terimi, Yunanca “genişleme” anlamına gelen “anevrizma” kelimesinden gelmektedir.
Anevrizma kavramı binlerce yıldır bilinmektedir. Eski uygarlıklar, yaralanmalardan sonra arterlerde “anevrizma” adını verdikleri şişlikler gözlemlemişlerdi. Rönesans’la birlikte Andreas Vesalius gibi anatomistler arteriyel anevrizmaların tanımlarını detaylandırmaya başlıyorlardı. Aort anevrizmalarına yönelik ilk başarılı ameliyatlar, büyük ölçüde cerrahi teknik ve teknolojideki gelişmelere bağlı olarak 20. yüzyılda gerçekleştirildi.
Aort anevrizması, vücuttaki ana arter olan aortun bir bölümünde şişlik veya genişlemedir. Aort, oksijenli kanı kalpten vücudun geri kalanına taşır. Anevrizmalar aort boyunca herhangi bir yerde meydana gelebilir, ancak en sık görülen yerler abdominal aort (abdominal aort anevrizmaları) ve torasik aorttur (torasik aort anevrizmaları).
Nedenleri:
- Ateroskleroz (atardamar duvarlarında yağ ve kolesterol birikmesi)
- Yüksek tansiyon
- Genetik faktörler
- Tütün kullanımı
- Yaşlanma
- Enfeksiyon
Komplikasyonlar:
Aort anevrizmasının yırtılması hayati tehlike oluşturan iç kanamaya yol açabilir. Daha küçük anevrizmaların genellikle hiçbir semptomu yoktur ve başka nedenlerle yapılan tıbbi testler sırasında tespit edilebilirler.
Teşhis
Aort anevrizmasının tanısı tipik olarak, doktorun ilgisiz bir çalışmadaki semptomlara veya tesadüfi bulgulara dayanarak varlığından şüphelenmesinin ardından tıbbi görüntüleme çalışmalarına dayanır.
Tanısal görüntüleme:
Abdominal ve Torasik Ultrason: Non-invazif doğası, radyasyon içermemesi ve maliyet etkinliği nedeniyle özellikle abdominal aort anevrizmaları için yaygın olarak kullanılan birinci basamak görüntüleme yöntemidir.
Bilgisayarlı Tomografi (BT) Taraması: Bu, ayrıntılı bir görünüm sunar ve birçok durumda altın standarttır. BT anjiyografi anevrizmanın boyutu, şekli ve yeri hakkında kesin bilgi verebilir.
Manyetik Rezonans Görüntüleme (MRI): Bu, bazı durumlarda anevrizmayı ve çevresindeki yapıları değerlendirmek için kullanılabilir. Hastaların BT taramalarında kullanılan kontrast maddelere alerjisi varsa özellikle faydalıdır.
Anjiyografi: Bu, geçmişte aort anevrizmalarını değerlendirmek için kullanılmıştı, ancak BT ve MRI’nın ilerlemesiyle tanı amaçlı olarak daha az sıklıkla kullanıldı. Ancak bazı terapötik müdahaleler için hala gereklidir.
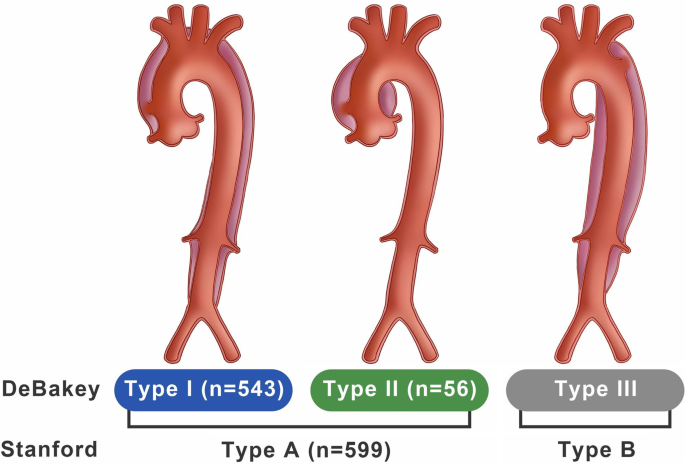
Teşhis Sınıflandırması:
Görüntülemede aort anevrizmaları morfolojilerine göre sınıflandırılabilir:
Sakküler Anevrizma: Arter çevresinin sadece bir kısmını kapsayan lokalize bir keseciktir.
Fusiform Anevrizma: Damar segmentinin tüm çevresini kapsayarak yaygın dilate artere yol açar.

Operasyon için Boyut Dikkate Alınması:
Aort anevrizmasını ameliyat etme kararı tipik olarak büyüklüğüne, büyüme hızına ve konumuna, ayrıca semptomlara ve hastaya özgü diğer faktörlere bağlıdır.
Abdominal Aort Anevrizması (AAA): Elektif onarım genellikle aşağıdakiler için düşünülür:
- AAA’sı 5,5 cm’den büyük olan erkekler.
- AAA’sı 5,0 cm veya daha büyük olan kadınlar.
- Altı ayda 0,5 cm’den fazla büyüyen anevrizmalar.
Torasik Aort Anevrizması (TAA): Kriterler daha karmaşıktır, ancak genellikle aşağıdaki durumlarda ameliyat düşünülür:
- 5,5 cm’den büyük çıkan aort veya aort kökü anevrizmaları.
- 6,5 cm’den büyük inen aort anevrizmaları.
Semptomatik anevrizmaların veya bağ dokusu bozukluklarına bağlı anevrizmaların daha küçük boyutlarda ameliyat edilmesi düşünülebilir.
Bunların genel kurallar olduğunu belirtmekte fayda var. Ameliyat kararı bireyseldir ve hastanın genel sağlığı, yaşam beklentisi ve semptomatoloji gibi diğer faktörler dikkate alınır.
Tedavi:
Tedavi anevrizmanın büyüklüğüne ve büyüme hızına bağlıdır. Düzenli izleme, kan basıncını ve kolesterolü düşüren ilaçlar ve ameliyat (endovasküler onarım veya açık ameliyat gibi) yaygın tedavilerdir.
Kaynak:
- Sakalihasan N., Limet R., Defawe O. D. (2005). Abdominal aortic aneurysm. The Lancet, 365(9470), 1577-1589.
- Erbel R., Aboyans V., Boileau C., et al. (2014). 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases. European Heart Journal, 35(41), 2873-2926.
- Chaikof E.L., et al. (2018). The Society for Vascular Surgery practice guidelines on the care of patients with an abdominal aortic aneurysm. Journal of Vascular Surgery, 67(1), 2-77.e2.
- Hiratzka L.F., et al. (2010). 2010 ACCF/AHA/AATS/ACR/ASA/SCA/SCAI/SIR/STS/SVM guidelines for the diagnosis and management of patients with thoracic aortic disease. Journal of the American College of Cardiology, 55(14), e27-e129.










Yorum yazabilmek için oturum açmalısınız.