Sedimantasyon, katı partiküllerin bir sıvı süspansiyonundan çökerek bir tortu oluşturduğu süreci ifade eder. Tıbbi bağlamlarda sedimantasyon, mikropların veya hücresel anormalliklerin tespit edilmesine yardımcı olarak sıvılardaki katı bileşenleri konsantre etmek için yaygın olarak kullanılır. Bu işlem, özellikle katı bileşenler düşük konsantrasyonlarda mevcut olduğunda numunelerin daha verimli bir şekilde incelenmesini sağlar. İdrar**, *beyin omurilik sıvısı* ve punktatlar gibi tıbbi numuneler, çeşitli tanı testlerini kolaylaştırmak için doğal çökeltme yoluyla veya santrifüj yardımıyla yaygın olarak sedimantasyon yoluyla işlenir.
Sedimantasyonun Tıbbi Uygulamaları
Bakteriyolojik İncelemeler:
- Mikrobiyal tespit çökeltilerde orijinal sıvıdan çok daha kolaydır. Bu nedenle, doğrudan sıvılardan “yayma” yapmak yerine, tipik olarak santrifüj edilerek tortu elde edilir ve bu tortu daha sonra mikroskop altında incelenir.
Sitolojik İncelemeler:
- Şüpheli plevral metastazlar gibi durumlar için idrar, beyin omurilik sıvısı veya punktatların sitolojik incelemeleri sıklıkla gereklidir. Hücresel bileşenleri yapılarını koruyarak konsantre etmek için Sitosantrifüjler veya Cyc odaları kullanılır. Hücresel dejenerasyon hızla gerçekleştiği için numunenin hızlı transferi çok önemlidir.
İdrar Sedimenti:
- İdrar sedimenti, böbrek hastalığı, idrar yolu enfeksiyonları veya hematüriyi tespit etmek için kullanılan yaygın bir tanı aracıdır. Bu, idrardaki konsantre katı partiküllerin anormal hücreler, döküntüler, kristaller veya bakteriler açısından incelenmesini içerir.
Beyin Omurilik Sıvısı Sedimenti:
- Beyin omurilik sıvısındaki enfeksiyonları (örn. bakteriyel menenjit) veya kanserli hücreleri tespit etmek için kullanılan beyin omurilik sıvısının sedimantasyonu, bu bileşenlerin daha yakından incelenmek üzere izole edilmesine yardımcı olur.
İnflamatuar Hastalıklarda Sedimantasyon
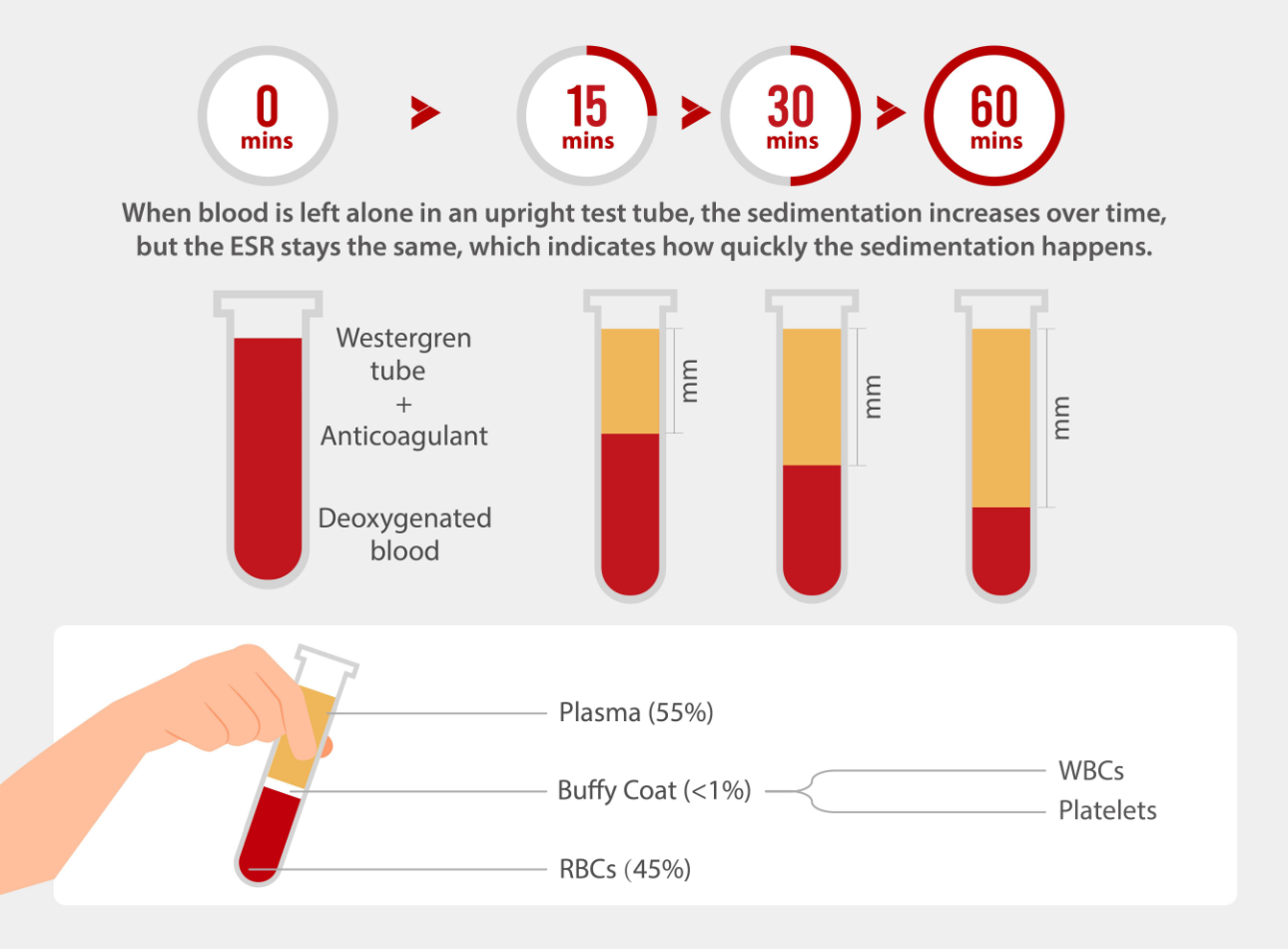
Sedimantasyon ayrıca eritrosit sedimantasyon hızı (ESR) testi yoluyla inflamatuar hastalıkların teşhisinde ve izlenmesinde önemli bir rol oynar. Bu test, eritrositlerin (kırmızı kan hücreleri) kan örneği içeren bir test tüpünün dibine ne kadar hızlı çöktüğünü ölçer. Normalde kırmızı kan hücreleri yavaş çöker, ancak iltihap varlığında daha hızlı çökerler.
Yaygın İnflamatuar Hastalıklar ve Sedimantasyon Hızı
- Yağlı Karaciğer Hastalığı**: Kötü beslenmeye bağlı iltihaplanma sedimantasyon oranlarının yükselmesine yol açabilir.
- Endometriozis**: Kronik enflamasyon ile ilişkilidir.
- Tip 1 ve Tip 2 Diabetes Mellitus**: Kronik enflamasyon her iki diyabet türünde de rol oynar.
- İnflamatuar Bağırsak Hastalığı (IBD)**: Sindirim sisteminin kronik enflamasyonu ESR’nin yükselmesine neden olur.
- Astım**: Hava yollarındaki enflamatuar yanıt sedimantasyon oranlarını artırabilir.
- Romatoid Artrit**: Yüksek ESR’nin sıklıkla görüldüğü ayırt edici durumlardan biri.
- Obezite**: Obez bireylerde kronik düşük dereceli enflamasyon ESR’nin yükselmesine neden olabilir.
Yüksek Sedimantasyon Oranına Sahip Hastalıklar
Yüksek sedimantasyon hızı çeşitli durumlara işaret edebilir:
- Sistemik lupus eritematozus** veya romatoid artrit gibi otoimmün hastalıklar genellikle kronik enflamasyon nedeniyle yüksek ESR’ye neden olur.
- Kanser**, özellikle *lenfoma* ve multipl miyelom, tümörler enflamatuar proteinler ürettiği için ESR’yi yükseltebilir.
- Kronik böbrek hastalığı**, *pnömoni*, *pelvik inflamatuar hastalık* ve apandisit de enfeksiyon veya inflamasyon nedeniyle daha yüksek sedimantasyon oranına neden olabilir.
Sedimantasyon Hızı ve Romatoid Artrit
Romatoid artritte**, *eritrosit sedimantasyon hızı (ESR)* iltihabın boyutunu değerlendirmek için bir belirteç olarak kullanılır. Normal sedimantasyon hızı seviyeleri yaşa ve cinsiyete göre değişir:
- Erkekler**: 0-15 mm/saat (50 yaşın üzerindekiler için 20 mm/saate kadar).
- Kadınlar**: 0-20 mm/saat (50 yaşın üzerindekiler için 30 mm/saate kadar).
- Çocuklar**: ≤10 mm/saat.
İnflamasyonun Teşhisi ve İzlenmesi
Enflamasyonu teşhis etmek ve izlemek için kullanılan testler şunlardır:
- Eritrosit Sedimantasyon Hızı (ESR)**: Kırmızı kan hücrelerinin bir test tüpüne ne kadar hızlı yerleştiğini ölçer.
- C-reaktif Protein (CRP): Enflamasyona yanıt olarak karaciğer tarafından üretilen bir proteini ölçer.
- Plazma Viskozitesi (PV): Enflamasyonla birlikte artan kan kalınlığını değerlendirir.
Normal Sedimantasyon Hızı
Normal sedimantasyon hızı yaş ve cinsiyet gibi faktörlere bağlı olarak farklılık gösterir. ESR için Westergren yöntemi kullanılır:
- Erkekler**: ≤15 mm/saat.
- Kadınlar**: ≤20 mm/saat.
- Çocuklar: ≤10 mm/saat.
Yüksek Sedimantasyon Oranlarının Tedavisi
Yüksek sedimantasyon oranını düşürmek ve enflamasyonu azaltmak için yaşam tarzı değişiklikleri çok önemlidir:
- Düzenli egzersiz yapın**: Fiziksel aktivite enflamasyonu azaltabilir.
- Kilo kaybı**: Sağlıklı bir kiloda kalmak ESR de dahil olmak üzere enflamatuar belirteçleri azaltır.
- Sağlıklı beslenme: Şeker ve işlenmiş gıdalardan kaçınırken besleyici, anti-enflamatuar gıdalar yemek enflamasyonu azaltabilir.
- Hidrasyon**: Yeterince su içmek enflamatuar tepkilerin düzenlenmesine yardımcı olabilir.
- Anti-inflamatuar ilaçlar**: Ciddi iltihaplı hastalıklarda, iltihabı azaltmak için *NSAID’ler* veya steroidler gibi tıbbi tedaviler kullanılabilir.
Yüksek ESR Hakkında Ne Zaman Endişelenilmeli
100 mm/saat** üzerindeki bir **ESR genellikle altta yatan ciddi bir duruma işaret eder, örneğin:
- Tüberküloz veya doku nekrozu gibi Enfeksiyonlar.
- Romatoid artrit veya lupus gibi otoimmün bozukluklar.
- Kanserler, özellikle metastaz yapmış kanserler gibi sistemik etkileri olanlar.
İnflamasyon ve Sedimantasyon Hızının Azaltılması
Enflamasyonu azaltmanın en hızlı yolları şunlardır:
- Şekeri ve işlenmiş gıdaları kesmek**: Bunlar vücutta iltihaplanmaya katkıda bulunur. Tam gıdalar, meyveler, sebzeler ve yağsız proteinler açısından zengin bir anti-enflamatuar diyet benimsemek, enflamasyonu hızla azaltmaya yardımcı olabilir.
- Anti-enflamatuar besinleri artırmak**: Balık, çilek ve yeşil sebzeler gibi gıdalarda bulunan omega-3 yağ asitleri, antioksidanlar ve polifenoller anti-enflamatuar özelliklere sahiptir.

Keşif
İşte eritrosit sedimantasyon hızının (ESR) anlaşılması ve geliştirilmesindeki önemli kilometre taşları ve inflamasyonun tespit edilmesi ve izlenmesindeki rolü:
1897 – Edmund Faustyn Biernacki tarafından Sedimantasyon Hızının Tanıtılması
- Polonyalı doktor Edmund Faustyn Biernacki ilk olarak sedimantasyon oranını iltihaplanmayı ölçmek için bir test olarak tanımladı. Kan örneklerindeki kırmızı kan hücrelerinin sedimantasyonunun sağlıklı bireyler ile hastalıktan, özellikle de iltihaplı durumlardan muzdarip olanlar arasında farklılık gösterdiğini gözlemledi.
1918 – Robin Fahraeus’un Katkısı
- İsveçli patolog Robin Fahraeus, enflamatuar süreçleri ölçmek için eritrosit sedimantasyon hızını (ESR) bağımsız olarak tanıttı. Çalışmaları, ESR’nin hamilelik ve bulaşıcı hastalıklar gibi durumlarda inflamasyonu değerlendirmek için bir tanı aracı olarak kullanılmasını resmileştirdi.
1921 – Westergren Yöntemi Geliştirildi
- İsveçli doktor Robert Westergren sedimantasyon hızını ölçmek için daha standart bir teknik olan Westergren yöntemini geliştirmiştir. Bu yöntem günümüzde en yaygın kullanılan yöntem olmaya devam etmektedir ve ESR ölçümü için altın standart olarak kabul edilmiştir.
1940’lar – ESR Romatoid Artrit ve Diğer Otoimmün Hastalıklar için Tanı Aracı Olarak Kullanıldı
- ESR, romatoid artrit ve sistemik lupus eritematozus gibi otoimmün hastalıklar için rutin bir tanı aracı haline gelmiştir. Hastalığın ilerlemesini ve tedavi yanıtını izlemede kullanılması, onu otoimmün bozukluk yönetiminin önemli bir parçası haline getirdi.
1960’lar – Bulaşıcı Hastalık Teşhisi için Yaygın Kabul
- ESR testi, özellikle tüberküloz ve endokardit gibi kronik enfeksiyonlar olmak üzere bulaşıcı hastalıkların teşhisinde ve izlenmesinde yaygın olarak kullanılmaya başlanmıştır. Kronik enflamatuar durumları tanımlamak için önemli bir belirteç haline geldi.
1980’ler – C-reaktif Proteinin (CRP) Tamamlayıcı Bir Belirteç Olarak Kullanıma Girmesi
- C-reaktif protein (CRP)** testinin keşfi ve geliştirilmesi, enflamasyonu ölçmek için ek bir araç sağlamıştır. ESR’nin enflamasyondaki değişikliklere yanıt vermesi daha yavaşken, CRP enflamatuar aktivitenin daha hızlı bir göstergesini sunar. CRP ve ESR artık inflamasyonun daha kapsamlı bir görünümünü sağlamak için sıklıkla birlikte kullanılmaktadır.
1990’lar – Kardiyovasküler Hastalık Araştırmalarında ESR
- ESR’nin kalp krizi ve felç gibi kardiyovasküler hastalıklar riskiyle ilişkili olduğu bulunmuştur. Daha yüksek ESR değerleri sistemik enflamasyonla ilişkilendirildi ve enflamasyonun kardiyovasküler hastalıklarda oynadığı rolün daha iyi anlaşılmasına katkıda bulundu.
2000’ler – Enflamasyon ve ESR’nin Rolünü Anlamada Gelişmeler
-
- yüzyılın başlarında yapılan araştırmalar ESR’nin inflamatuvar bağırsak hastalığı (IBD), vaskülit ve çeşitli artrit türleri gibi kronik inflamatuvar hastalıkların teşhisinde oynadığı rolü sağlamlaştırmıştır. ESR, anti-inflamatuar tedavilerin etkinliğini izlemek için yerleşik bir araç haline geldi.
2010’lar – ESR ve CRP’nin Klinik Uygulamada Kombine Kullanımı
- 2010’lara gelindiğinde, ESR klinik ortamlarda inflamasyonun daha net bir resmini sunmak için CRP ile birlikte sıklıkla kullanılmaya başlanmıştır. Bu iki belirteç birlikte romatoid artrit, büyük hücreli arterit ve sistemik lupus eritematozus gibi durumların değerlendirilmesinde standart hale gelmiştir.
Sunum – ESR’nin İnflamatuar Durumların Teşhisinde Devam Eden Önemi
- ESR, kronik enflamatuar hastalıkların**, enfeksiyonların ve otoimmün durumların **izlenmesinde hayati bir test olmaya devam etmektedir. Ayrıca, tanısal doğruluğu ve hasta bakımını iyileştirmek için CRP ve plazma viskozitesi (PV) gibi yeni biyobelirteçlerle birlikte sıklıkla kullanılmaktadır.
İleri Okuma
- Hurlimann, J., Thorbecke, G. J., & Hochwald, G. M. (1966). The liver as the site of C-reactive protein formation. Journal of Experimental Medicine, 123(2), 365-378.
- Kushner, I., & Rzewnicki, D. L. (1994). The acute phase response: An overview. Methods in Enzymology, 233, 341-349.
- Gabay, C., & Kushner, I. (1999). Acute-phase proteins and other systemic responses to inflammation. New England Journal of Medicine, 340(6), 448-454.
- Brigden, M. L. (1999). The erythrocyte sedimentation rate: still a helpful test when used judiciously. Postgraduate Medicine, 105(5), 104-116.
- Pearson, T. A., Mensah, G. A., Alexander, R. W., Anderson, J. L., Cannon III, R. O., Criqui, M., & Rifai, N. (2003). Markers of inflammation and cardiovascular disease: application to clinical and public health practice. Circulation, 107(3), 499-511.
- Weyand, C. M., & Goronzy, J. J. (2003). Medium- and large-vessel vasculitis. New England Journal of Medicine, 349(2), 160-169.
- Saag, K. G., & Teng, G. G. (2005). Assessing inflammatory activity in rheumatoid arthritis: The use of clinical and laboratory measures. Arthritis Research & Therapy, 7(5), 189-195.
- Cleland, S. J., & Sattar, N. (2005). Inflammation, obesity, and metabolic syndrome. Journal of Clinical Endocrinology & Metabolism, 90(6), 2454-2461.
- Aletaha, D., & Smolen, J. S. (2007). The definition and measurement of disease modification in inflammatory rheumatic diseases. Rheumatic Disease Clinics of North America, 33(3), 293-303.
- Youssef, P., & Marzouk, S. (2014). Erythrocyte sedimentation rate and C-reactive protein in clinical practice. Australian Prescriber, 37(3), 93-96.









Yorum yazabilmek için oturum açmalısınız.