Bronş
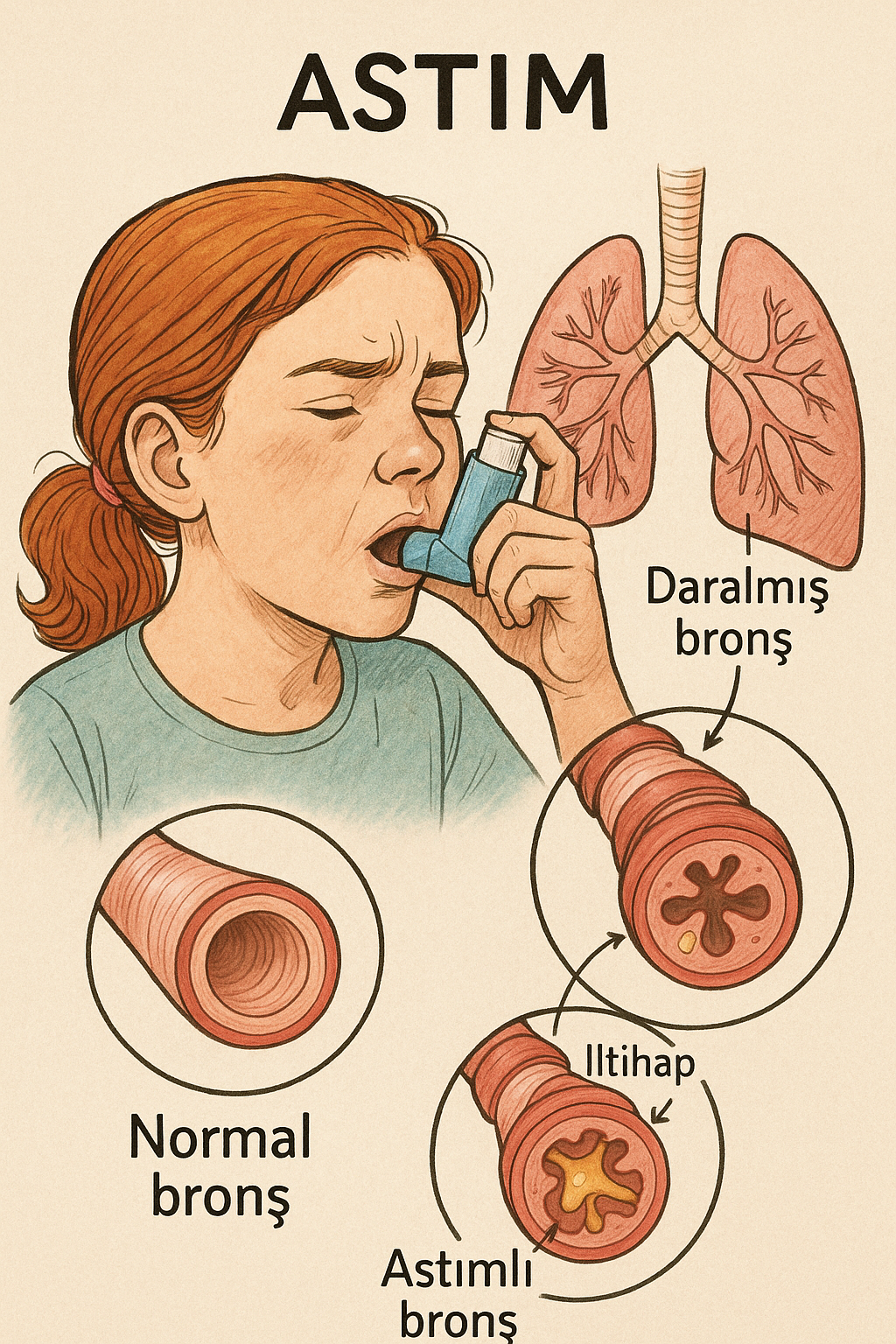
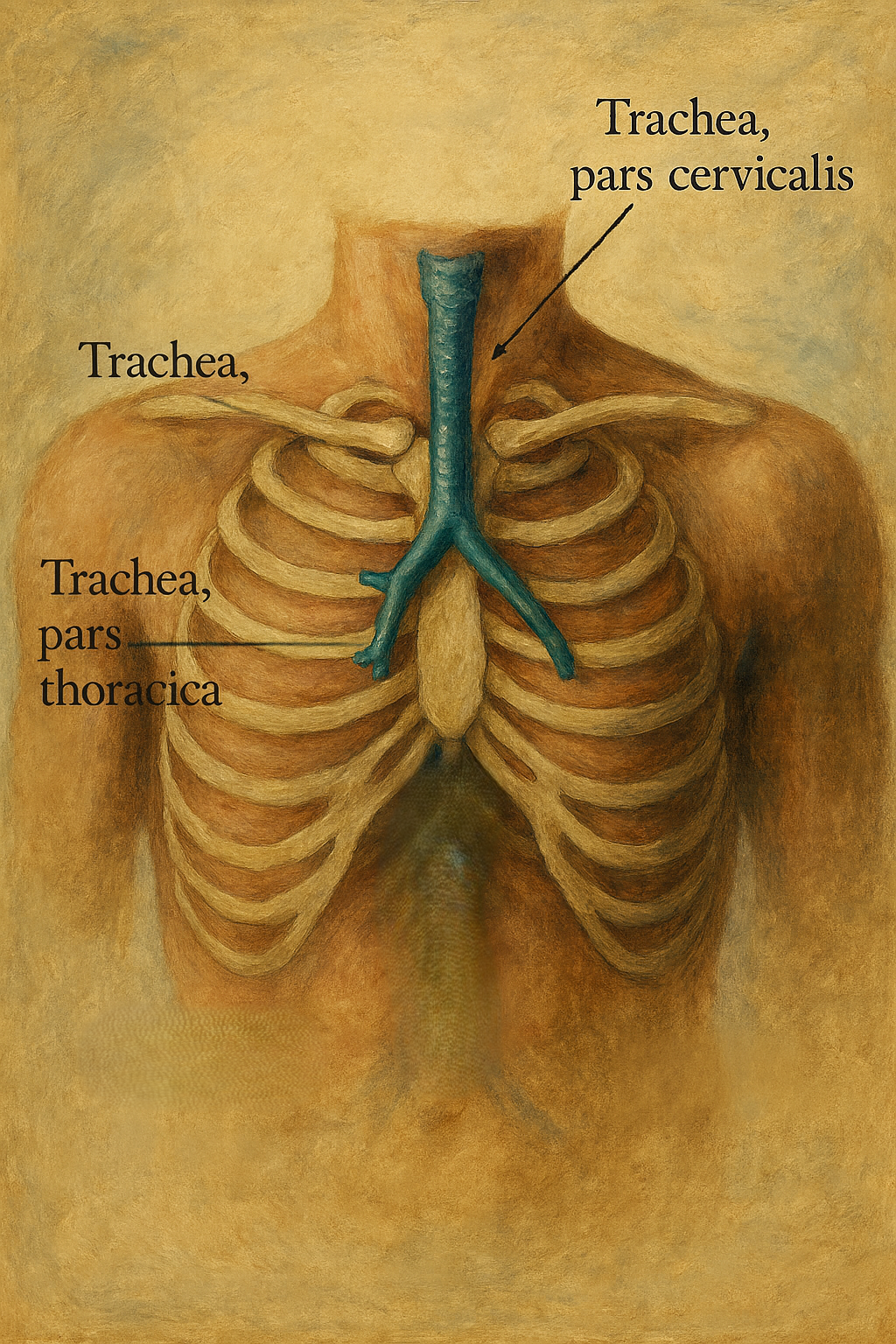
Sinonim: bronchus, broncho-, bronchio-, bronko-, bronkus. Ana Hint-Avrupa dilindeki gʷerh₃- kelimesinden türeyen gʷro-nkh₃- kelimesi, eski yunancada βρόγχος (brónkhos) şeklinde ifade edilmiştir. Bu kelime Latinceye bronchus şeklinde geçmiştir. Bronş kelimesi de burdan türemiştir. Bronşiyal (bronchi/al) bronşa ait anlamına gelen sıfattır. Trakea ile bronşçuk arasındaki bağlantıyı sağlayan dal, soluk borusu dalı. Alveollara hava taşıyan boru şeklinde soluk yolunun kısmıdır.