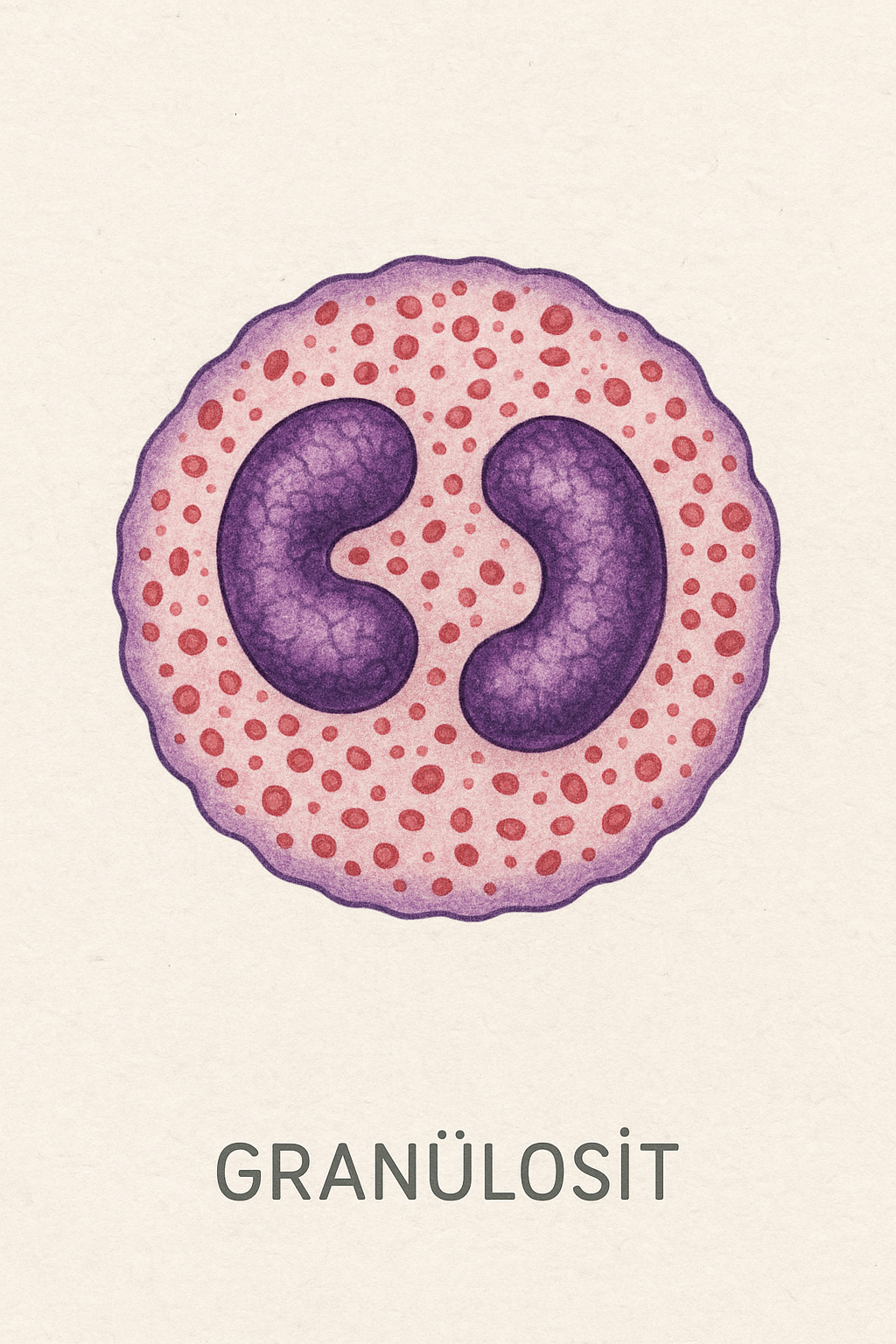
Granülositlerin Tanımı
- Granülositler, sitoplazmalarında belirgin granüller içeren akyuvarlardır.
- Wright-Giemsa boyaması ile tanınan bu hücreler, lökositlerin yaklaşık %60–70’ini oluştururlar.
- “Granülosit” terimi, Latince “granulum” (tanecik) ve “zytos” (hücre) kelimelerinin birleşiminden türetilmiştir (granül-o-sit) (Abbas ve diğ., 2018).
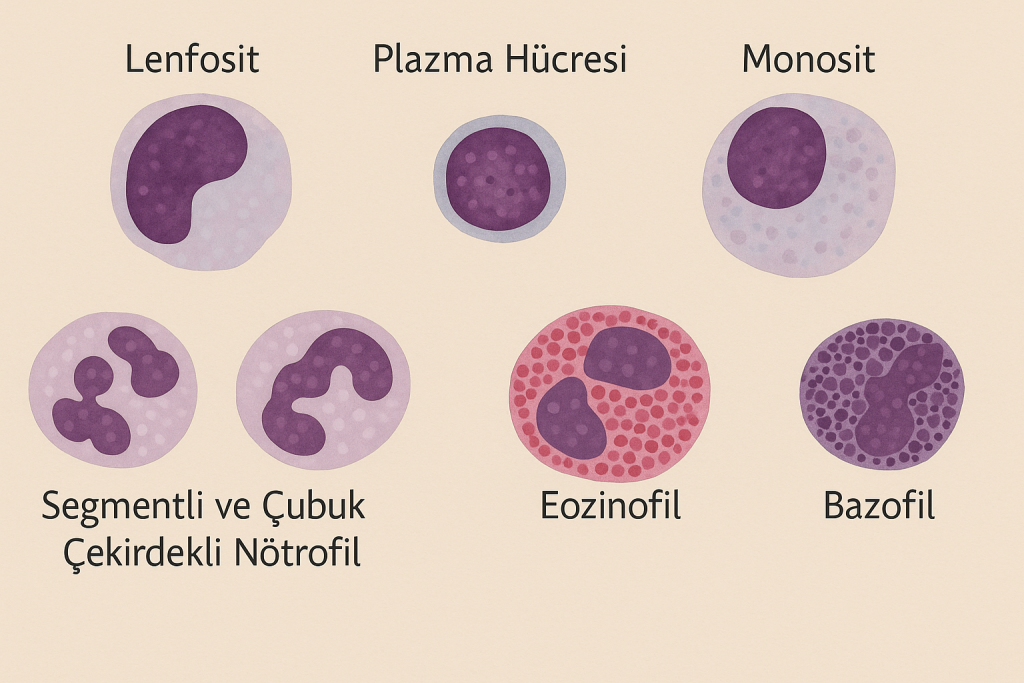
Granülosit Tipleri
- Nötrofil Granülositler
- Kan dolaşımındaki en yaygın granülosit türüdür.
- Mikrobiyal enfeksiyonlarda ilk savunma hattını oluşturur ve fagositoz yoluyla patojenleri yok eder (Mantovani ve diğ., 2011).
- Çekirdek segmentasyonu sayesinde olgunlaştıkları ayırt edilir; segment sayısı enfeksiyon ve kemik iliği durumu hakkında bilgi verir.
- Eozinofil Granülositler
- Parazitik enfeksiyonlara karşı ve alerjik reaksiyonlarda rol oynar.
- Sitoplazmalarındaki eozinofilik granüller, kristal yapılı proteinler (örn. majör temel protein, MBP) içerir (Rothenberg & Hogan, 2006).
- Dokulara göç ederek histamin ve diğer mediatörleri düzenler; astım ve atopik hastalıklarda belirgin artış gösterir (Valent ve diğ., 2012).
- Bazofil Granülositler
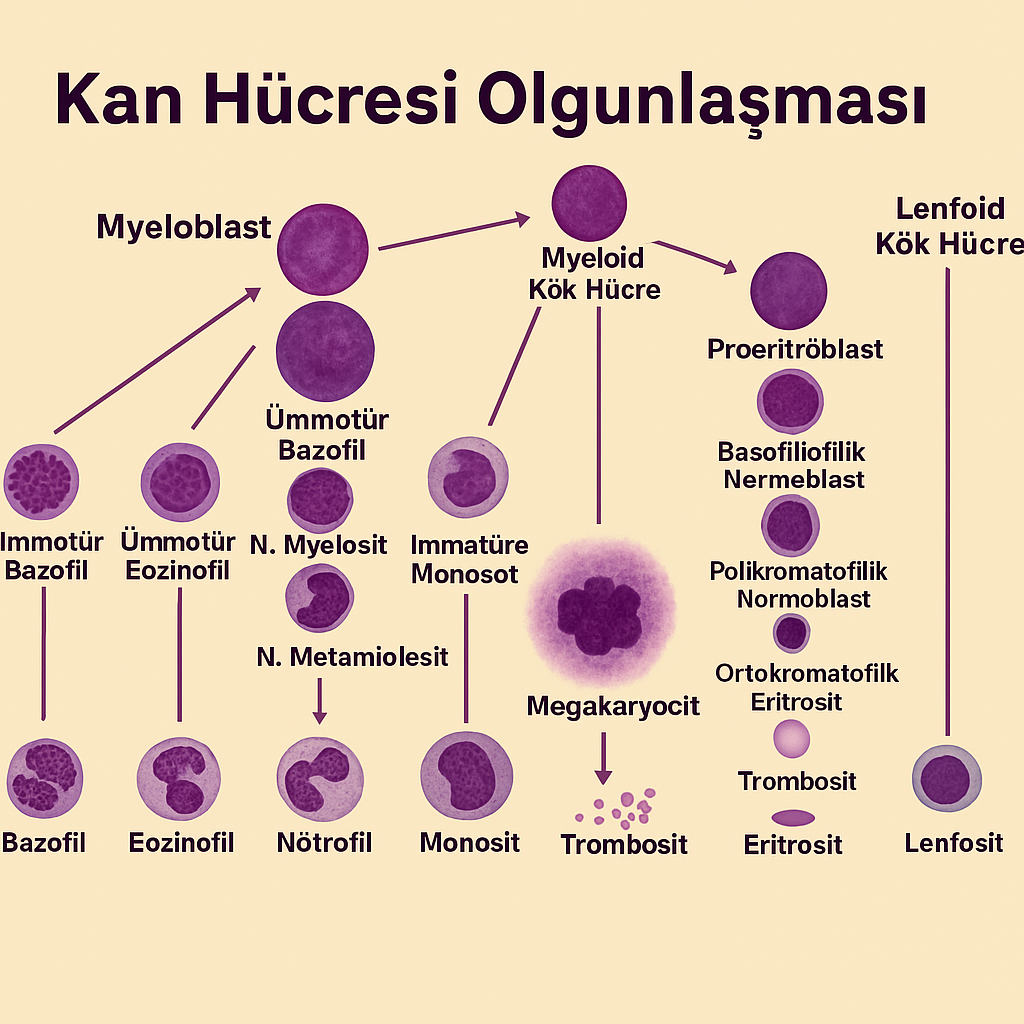
Granülositopoez (Granülosit Üretimi)
- Granülositopoez, kemik iliğinde gerçekleşen granülosit üretim sürecine verilen addır.
- Hematopoetik Kök Hücre → Miyeloblast → Promiyelosit → Miyelosit → Metamiyelosit → Bant Hücre → Olgun Granülosit şeklinde aşamalı farklılaşma görülür (Hoffbrand & Moss, 2016).
- Myeloblast evresinde, çekirdek büyük ve az kondanse olurken; metamiyelosit evresinde granüllerin sayısı ve tipine göre farklılaşma belirginleşir.
- Granülositopoetik sitokinler arasında G-CSF (Granülosit Koloni Stimüle Edici Faktör), GM-CSF (Granülosit-Makrofaj Koloni Stimüle Edici Faktör) ve IL-3’ün rolü büyüktür (Abbas ve diğ., 2018).
Kan Düzeyindeki Durumlar
- Granülositoz
- Kanda granülosit sayısının normalin üzerinde olması hâlidir.
- Genellikle enfeksiyon, inflamasyon, miyeloproliferatif hastalıklar veya stres yanıtı sonucu ortaya çıkar (Hoffbrand & Moss, 2016).
- Referans aralık: Yetişkinde yaklaşık 1.800–7.700/mm³ nötrofil; artış, “nötrofili” terimiyle de tanımlanabilir (Abbas ve diğ., 2018).
- Granülositopeni
- Kanda granülosit sayısının normalin altında seyretmesidir.
- Kemik iliği supresyonu, ilaç toksisitesi, kemik iliği infiltrasyonu veya vitamin eksiklikleri (B12, folat) gibi nedenlere bağlı gelişebilir (Hoffbrand & Moss, 2016).
- Klinik tablo, enfeksiyon riskinin artmasıyla karakterizedir.
- Agranülositoz
- Kanda 1 μL başına 500’den az granülosit olması durumu olarak tanımlanır; genellikle nötropeni daha da şiddetlidir (örn. < 100–200/mm³) (Dale, 2010).
- İlaçlara bağlı idiyopatik agranülositoz, kemoterapi, immün aracılı süreçler veya otoimmün hastalıklar agranülositoza neden olabilir.
- Hastalar febril, ciddi bakteriyel ve fungal enfeksiyonlara yatkın hale gelir ve acil müdahale gerektirir.
Keşif
Granülositlerin keşfi, mikroskop teknolojisindeki gelişmelerle birlikte 19. yüzyılın ortalarına kadar uzanır. Hücrelerin granüllü yapısının fark edilmesi ve sınıflandırılması özellikle hematolojik boyama tekniklerinin gelişmesiyle mümkün olmuştur.
İçindekiler
1. Mikroskobik Gözlemler ve İlk Tanımlamalar (1840–1870)
- 1843: Alman anatomist Friedrich Henle, lökositlerin farklı görünümlerine dair ilk sistematik gözlemleri yaptı. Ancak granüllü hücrelere özel bir ayrım getirilmemişti.
- 1860’lar: Alman hücre biyoloğu Ernst Haeckel, hücrelerin mikroskobik özelliklerine göre sınıflandırılması gerektiğini savundu ve hücresel morfolojinin sistematik analizini teşvik etti.
2. Wright Boyası ve Fonksiyonel Sınıflama (1890–1900)
- 1891–1899: Amerikalı patolog James Homer Wright, günümüzde hâlen yaygın olarak kullanılan Wright boyasını geliştirdi.
- Bu boyama yöntemi sayesinde nötrofil, eozinofil ve bazofil granülositler mikroskop altında ayırt edilebilir hâle geldi.
- Wright, bu hücrelerin granüllerini boyama özelliklerine göre tanımlayarak günümüzde kullanılan sınıflamayı başlattı.
3. Fonksiyonel ve İmmünolojik Tanımlar (20. yüzyıl başı – 1950)
- 1900–1930: Paul Ehrlich’in asidik, bazik ve nötr boyalar kullanarak hücreleri ayırt eden teknikleri, granülositlerin alt tiplerinin morfolojik olarak sınıflandırılmasını sağladı.
- Ehrlich, “eozinofil” ve “bazofil” terimlerini tanımlamış; granüllerin boya alma özelliklerine göre adlandırmıştır.
- 1930’lar: Fagositoz ve kemotaksi gibi fonksiyonların tanınmasıyla granülositlerin bağışıklıkta önemli rolleri olduğu anlaşılmıştır.
4. Moleküler ve Sitokin Temelli Keşifler (1970–2000)
- 1977: Granülosit gelişimini yöneten ilk sitokin olan Granülosit-Koloni Uyarıcı Faktör (G-CSF) tanımlandı.
- 1980–2000: Granülosit gelişimi ve farklılaşmasında görev alan genetik yollar, hücre içi sinyalleşmeler ve kök hücre kaynakları detaylı olarak aydınlatıldı.
5. Modern Tanı ve Klinik Uygulama (2000–günümüz)
- Akış sitometrisi, moleküler boyama teknikleri ve immünhistokimya ile granülosit alt grupları daha ayrıntılı şekilde incelenebilmekte; granülositopeni, granülositoz ve lösemilerde tanı aracı olarak kullanılmaktadır.
İleri Okuma
- Ehrlich P. 1879. Beiträge zur Kenntnis der Anilinfärbungen und ihrer Verwendung in der mikroskopischen Technik. Archiv für mikroskopische Anatomie, 16:263–277.
- Wright JH. 1899. The histogenesis of the blood platelets. Journal of Morphology, 16(2): 415–499.
- Bainton DF, Farquhar MG. 1966. Origin of granules in polymorphonuclear leukocytes. Two types derived from the Golgi complex in developing granulocytes. Journal of Cell Biology, 28(2):277–301.
- Metcalf D. 1977. The granulocyte-macrophage colony-stimulating factors. Science, 199(4326):603–610.
- Rothenberg ME, Hogan SP. 2006. The eosinophil. Annual Review of Immunology, 24:147–174.
- Borregaard N. 2010. Neutrophils, from marrow to microbes. Immunity, 33(5):657–670.
- Dale DC. 2010. Causes and Management of Neutropenia in the Adult. In: Lichtman MA, Beutler E, Kipps TJ, Seligsohn U, Kaushansky K, Prchal JT (eds). Williams Hematology, 8th ed. McGraw Hill; s. 477–495.
- Stone KD, Prussin C, Metcalfe DD. 2010. IgE, mast cells, basophils, and eosinophils. Journal of Allergy and Clinical Immunology, 125(2 Suppl 2):S73–S80.
- Mantovani A, Cassatella MA, Costantini C, Jaillon S. 2011. Neutrophils in the activation and regulation of innate and adaptive immunity. Nature Reviews Immunology, 11(8):519–531.
- Valent P, Klion AD, Horny HP, et al. 2012. Contemporary consensus proposal on criteria and classification of eosinophilic disorders and related syndromes. Journal of Allergy and Clinical Immunology, 130(3):607–612.
- Hoffbrand AV, Moss PAH. 2016. Hoffbrand’s Essential Haematology. 7th ed. Wiley-Blackwell.
- Abbas AK, Lichtman AH, Pillai S. 2018. Cellular and Molecular Immunology. 9th ed. Elsevier.