İçindekiler
Kavramın adı ve etimolojik kökeni
PASI skoru, dermatoloji literatüründe yerleşik biçimiyle Psoriasis Area and Severity Index ifadesinin kısaltmasıdır. Terim, üç bileşenin bir araya getirilmesiyle oluşur: psoriasis (sedef hastalığı), area (tutulan alan) ve severity (şiddet); bunların tümünü tek bir nicel değerde birleştiren bir index (indeks) yaklaşımını ifade eder. “Skor” sözcüğü klinik pratikte çoğu zaman “indeks” ile eş anlamlı kullanılsa da, PASI’nin özgül anlamı; belirli morfolojik bulguları ve vücut yüzey alanı dağılımını standartlaştırılmış bir ağırlıklandırma ile sayısallaştıran bileşik bir klinik ölçektir. Kısaltmanın kendisi, modern klinik ölçüm kültürünün tipik bir ürünüdür: uzun ve çok bileşenli değerlendirmeleri, araştırma ve klinik iletişimde kolay aktarılabilir bir akronime dönüştürür.
Tanım ve kavramsal çerçeve
PASI, plak tip psoriasis başta olmak üzere psoriasis şiddetini ve yaygınlığını 0 ile 72 arasında değişen tek bir sayısal değerle ifade etmeyi amaçlar. Bu amaç doğrultusunda iki ana boyutu birleştirir:
- Yaygınlık (extent): Vücudun farklı bölgelerinde tutulan yüzey alanı yüzdesi
- Lezyon şiddeti (intensity): Psoriatik plağın üç temel klinik bulgusunun derecelendirilmesi
- Eritem (kızarıklık; koyu fototiplerde daha çok “discoloration” olarak değerlendirilir)
- İndürasyon / infiltrasyon (kalınlık, kabarıklık)
- Deskuamasyon (skuam, kepeklenme)
Bu yaklaşım, psoriasis değerlendirmesindeki iki klasik soruya sistematik yanıt üretir: “Ne kadar alan tutulmuş?” ve “Tutulan alanın lezyonları ne kadar şiddetli?”
Tarihsel gelişim ve standardizasyon mantığı
PASI’nin ortaya çıkışının arka planında, psoriasis gibi dalgalı seyirli, heterojen ve tedavi yanıtı değişken bir hastalıkta, klinik araştırmalar için güvenilir bir “ortak dil” ihtiyacı vardır. Psoriasiste tedavi etkinliğini değerlendirmek, sadece “daha iyi/daha kötü” izleniminden ibaret bırakıldığında; farklı klinisyenler, farklı merkezler ve farklı hasta alt grupları arasında karşılaştırılabilirlik zayıflar. Bu nedenle dermatoloji, özellikle sistemik tedavilerin ve biyolojik ajanların gelişimiyle birlikte, tekrarlanabilir ve nicel ölçütleri daha fazla benimsemiştir.
PASI’nin tarihsel evrimi, iki paralel çizgide okunabilir:
- Klinik araştırma standardı olarak kurumsallaşma: PASI, uzun yıllar boyunca randomize kontrollü çalışmalarda “birincil/ikincil sonlanım noktası” olarak kullanılagelmiş; bu da onu, araştırma metodolojisi içinde adeta referans ölçüt haline getirmiştir.
- Tedavi hedefleri diline dönüşme: Zamanla PASI, yalnızca bir başlangıç şiddet ölçümü değil; aynı zamanda tedavi başarısını tanımlayan oran temelli hedeflerin (ör. PASI 75, PASI 90, PASI 100) çekirdeği olmuştur. Böylece PASI, klinik karar verme süreçlerinde “ne kadar iyileşti?” sorusunu sayısallaştıran bir çerçeve sunmuştur.
Bu gelişim çizgisi, modern tıpta giderek güçlenen “ölçülebilirlik” ve “kanıta dayalı karşılaştırılabilirlik” idealleriyle uyumludur.
PASI’nin biyolojik ve klinik gerekçesi: Neyi ölçmeye çalışır?
Psoriasis, temelinde immün aracılı kronik inflamatuvar bir hastalık olup; epidermal hiperproliferasyon, anormal keratinosit diferansiyasyonu ve dermal-epidermal immün hücre infiltrasyonu ile karakterizedir. PASI’nin üç şiddet parametresi, bu biyolojinin klinik yüzeydeki izdüşümlerini yakalamaya çalışır:
- Eritem: Dermal vazodilatasyon ve inflamatuvar hücre trafiğinin yüzey yansıması
- İndürasyon: Epidermal kalınlaşma + dermal infiltrasyonun palpe edilebilen sonucu
- Deskuamasyon: Hızlanmış keratinizasyon döngüsü ve stratum corneum’da biriken skuamın görünür ifadesi
Alan bileşeni ise, inflamasyonun “toplam yükünü” kabaca temsil eder; çünkü aynı şiddetteki lezyonların daha geniş alana yayılması, sistemik inflamatuvar yük ve yaşam kalitesi etkisi açısından çoğu zaman daha ağır bir tabloya işaret eder.
Evrimsel biyolojik bağlam: Psoriasis neden bu kadar yaygın ve kalıcı bir fenotip?
Psoriasis, yalnızca klinik bir sendrom değil; aynı zamanda insan popülasyonlarında görece sık görülen, belirgin kalıtımsal bileşeni olan ve bağışıklık sistemiyle sıkı ilişkili bir fenotiptir. Evrimsel biyoloji açısından bu durum, tek bir “zararlı mutasyon” anlatısından daha karmaşık bir tabloyu düşündürür. Güncel yaklaşımlar, psoriasisle ilişkili bazı genetik varyantların popülasyonda korunmasını açıklamak için birkaç çerçeve kullanır:
- Dengeleyici seçilim (balancing selection): Aynı varyant, belirli çevresel koşullarda avantaj sağlarken başka koşullarda risk doğurabilir.
- Patojen baskısı ve bağışıklık avantajı hipotezleri: Doğuştan ve kazanılmış bağışıklık yanıtını güçlendiren varyantlar, tarihsel olarak enfeksiyon yükünün yüksek olduğu dönemlerde hayatta kalma avantajı sağlayabilir; bunun bedeli ise otoinflamatuvar/otoimmün yatkınlığın artması olabilir.
- Bariyer ve yara-iyileşmesi eksenleri: Keratinosit yanıtı, epidermal bariyer dinamikleri ve inflamasyon arasında yer alan bazı yollar, enfeksiyonlara karşı bariyer savunmasını güçlendirirken kronikleşmeye eğilimli inflamasyon paternlerini de kolaylaştırabilir.
Bu evrimsel okuma, PASI’nin “neden sadece deri bulgusu” ölçüyor gibi göründüğü sorusunu da ilginçleştirir: Psoriasis, pratikte deride görünür olsa bile, biyolojik olarak sistemik inflamasyon ağlarına bağlanan bir sendromdur; PASI ise bunun deri fenotipini sayısallaştırır.
Ölçeğin yapısı: Bölgesel ağırlıklandırma ve puanlama mantığı
PASI hesaplaması iki düzeyli bir standardizasyona dayanır:
1) Vücudun bölgelere ayrılması ve ağırlıklar
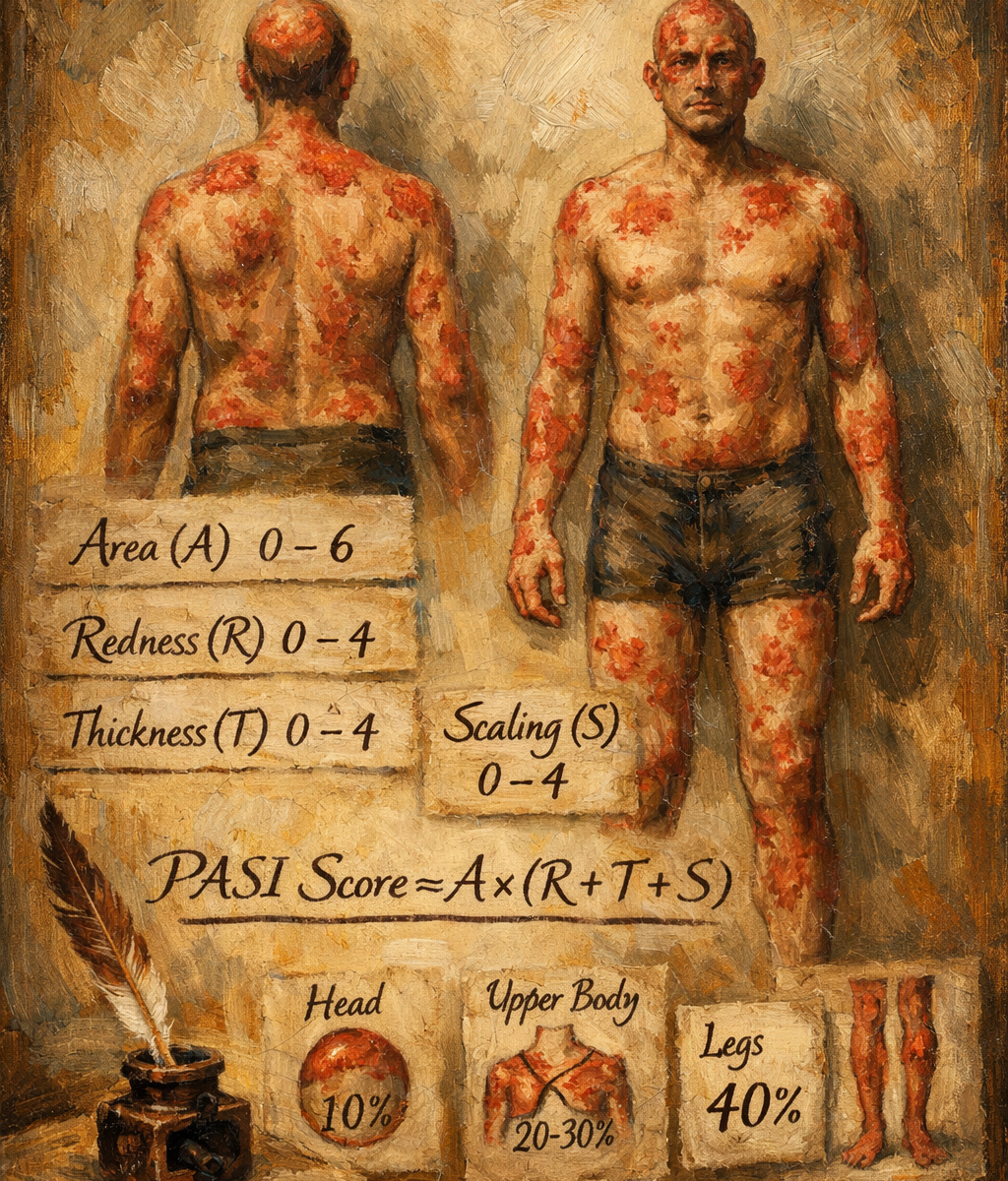
Vücut dört anatomik bölgeye ayrılır ve her bir bölgenin toplam skor içindeki ağırlığı, yaklaşık vücut yüzey alanı oranlarını temsil eder:
- Baş (H): %10
- Üst ekstremiteler (A): %20
- Gövde (T): %30
- Alt ekstremiteler (L): %40
Bu ağırlıklar, aynı şiddetteki lezyonların bacaklarda daha geniş yüzey kaplama eğilimi ve toplam yüzey katkısı gibi pratik gerçekliklerle uyumlu bir yaklaşım sunar.
2) Her bölgede iki bileşenin hesaplanması
Her bölge için iki değerlendirme yapılır:
a) Alan skoru (0–6): Bölgedeki tutulum yüzdesi, kategorik bir dereceye çevrilir (örneğin hiç yok, çok az, hafif, orta, belirgin, çok yaygın gibi). Kategorik dönüştürme, gözlemsel belirsizliği azaltmayı amaçlar; ancak aynı zamanda “ince farkların” kaybına da yol açabilir.
b) Şiddet skoru (0–12): Eritem, indürasyon ve deskuamasyon her biri 0–4 arasında derecelendirilir ve toplanır. Böylece her bölge için lezyon şiddeti toplamı 0 ile 12 arasında değişir.
3) Bölgesel skorların ağırlıklı toplamı
Her bölge için bulunan değer, bölgenin ağırlığı ile çarpılarak toplam PASI elde edilir. Bu yapı, PASI’yi “salt toplama” ölçeği olmaktan çıkarır; anatomik dağılımı hesaba katan ağırlıklı bileşik indeks haline getirir.
PASI’nin klinik kullanım alanları
Hastalık şiddetinin sınıflandırılması
PASI, özellikle klinik araştırmalarda, hastalık şiddetini kabaca sınıflandırmak için kullanılır. Pratikte şiddet sınıfları, ülke/kurum ve rehberlere göre değişebilmekle birlikte, PASI’nin en önemli katkısı “aynı hastayı zaman içinde” izlerken nicel kıyas sağlayabilmesidir.
Tedavi yanıtının tanımlanması: PASI 75, PASI 90, PASI 100
Modern psoriasiste tedavi hedefleri sıklıkla “başlangıca göre yüzde iyileşme” üzerinden ifade edilir:
- PASI 75: Başlangıç PASI’ye göre %75 azalma
- PASI 90: %90 azalma
- PASI 100: Tam temizlenme (klinik olarak tamamen düzelme)
Biyolojik ajanların ve hedefe yönelik küçük moleküllerin etkinlik profilinin güçlenmesiyle, tarihsel olarak “çok iyi yanıt” sayılan PASI 75 eşiğinin yer yer daha iddialı hedeflerle (PASI 90/100) tamamlandığı görülür. Bu, hem hasta beklentilerini hem de klinik başarı tanımlarını değiştiren bir dönüşümdür.
Klinik araştırma tasarımı ve karşılaştırılabilirlik
PASI, tedavi grupları arasında karşılaştırma yapmayı kolaylaştırır; ancak bunun bedeli, bazı klinik ayrıntıların tek sayıya indirgenmesi olabilir. Bu nedenle araştırmalarda PASI çoğu zaman başka ölçütlerle birlikte kullanılır.
Güncel bilimsel anlayış: Güçlü yönler, sınırlılıklar ve modern tamamlayıcı ölçütler
Güçlü yönler
- Yaygınlık + şiddeti birlikte ölçer: Sadece alanı değil, lezyon morfolojisini de hesaba katar.
- Araştırmalarda geniş kullanım: Büyük veri birikimi, tarihsel karşılaştırma imkânı sağlar.
- Tedavi yanıtını nicel hedeflere dönüştürür: Yüzde yanıt kavramları (PASI 75/90/100) iletişimi kolaylaştırır.
Sınırlılıklar ve metodolojik sorunlar
- Gözlemciye bağımlılık (inter-rater variability): Eritem/indürasyon/deskuamasyon derecelendirmesi, klinisyen deneyimine ve değerlendirme koşullarına duyarlıdır.
- Kategorik alan derecelendirmesi: Tutulum yüzdesinin 0–6 kategorisine çevrilmesi, küçük ama klinik açıdan anlamlı değişimleri “basamak etkisi” nedeniyle görünmez kılabilir.
- Özel bölgelerde duyarlılık sorunu: Genital bölge, yüz, saçlı deri, el-ayak gibi alanlarda küçük yüzdesel tutulum bile yüksek işlev kaybı ve yaşam kalitesi etkisi doğurabilir; PASI’nin alan ağırlıklandırması bu etkiyi her zaman yeterince temsil etmez.
- Semptomları ve hasta deneyimini sınırlı yansıtma: Kaşıntı, yanma, ağrı, yorgunluk, uyku bozukluğu, sosyal damgalanma gibi boyutlar PASI’nin doğrudan bileşenleri değildir.
- Tavan ve taban etkileri: Çok hafif hastalıkta değişimi yakalamak zorlaşabilir; çok ağır hastalıkta ise bazı ayrıntılar tek sayıya sıkışabilir.
Tamamlayıcı ölçütler ve modern yaklaşım
Güncel klinik bilim, psoriasisi yalnızca “deri yüzeyi” olarak değil; komorbiditeler, sistemik inflamasyon ve yaşam kalitesiyle birlikte ele alır. Bu nedenle PASI sıklıkla şu tür ölçütlerle birlikte düşünülür:
- BSA (Body Surface Area): Sadece alan tutulumunu daha basit bir biçimde ifade eder.
- PGA / IGA (Physician/Investigator Global Assessment): Hekimin genel şiddet izlenimini derecelendirir.
- DLQI (Dermatology Life Quality Index) ve benzeri PRO’lar (hasta bildirimli sonuçlar): Hastalığın yaşam kalitesi etkisini yakalar.
- Dijital ve görüntü-tabanlı yaklaşımlar: Son yıllarda fotoğraflama standardizasyonu, yapay zekâ destekli lezyon tanıma ve otomatik şiddet ölçümü gibi alanlar, PASI’nin “zaman alıcılık” ve “gözlemci değişkenliği” sorunlarını azaltma hedefiyle gündemdedir.
Bu çerçevede PASI, tek başına “hastalığın tüm gerçekliği” olmaktan çok, çok boyutlu psoriasis değerlendirmesinin merkezî ama tekil olmayan bir bileşeni olarak konumlanır.
Uygulama ve yorumlama: Klinik pratikte nüanslar
PASI’nin klinikte doğru yorumlanması için bazı nüanslar önem taşır:
- Aynı hastada trend takibi: PASI’nin en güçlü kullanımı, aynı hastanın zaman içindeki değişimini izlemektir. Farklı klinisyenlerin ölçtüğü tekil değerler, standardizasyon çabalarına rağmen değişkenlik gösterebilir.
- Başlangıç şiddetinin etkisi: Yüzde yanıt metrikleri (PASI 75 vb.), başlangıç değerine duyarlıdır; düşük başlangıç PASI’de yüksek yüzdeli değişimler farklı klinik anlamlar taşıyabilir.
- Fenotip çeşitliliği: Guttat, eritrodermik veya püstüler gibi alt tiplerde klinik görünüm farklılaştıkça PASI’nin temsil gücü ve pratik uygulanabilirliği değişebilir.
- Komorbiditeler ve eklem tutulumu: Psoriatik artritte deri şiddeti ile eklem hastalığının şiddeti her zaman paralel değildir; bu nedenle PASI, eklem değerlendirmesi için yeterli değildir.
Keşif
Sedef hastalığının ölçülmesi fikri, aslında hastalığın kendisi kadar “eski” bir zihinsel itkiden doğar: deride görülen bir olgunun, yalnızca betimlenmekle kalmayıp karşılaştırılabilir ve izlenebilir hale getirilmesi. PASI’nin keşif hikâyesi bu yüzden tek bir buluş anından değil; yüzyıllar boyunca biriken klinik gözlemlerden, sınıflandırma çabalarından, tedavi deneylerinden ve nihayet modern klinik araştırmaların sayısal disiplininden örülmüş uzun bir zincirden oluşur.
1) İlk gözlemler: “pul pul dökülen hastalık” ile “aynı isimli olmayan” yüzyıllar
Antik çağ hekimleri derinin dökülmesi, çatlaması, kalınlaşması ve kızarması gibi bulguları dikkatle kaydettiler; fakat bugün “psoriasis” dediğimiz varlık, uzun süre boyunca başka durumlarla iç içe geçmiş halde, geniş bir klinik yelpazenin içinde algılandı. Erken tıpta hastalıklar, modern anlamda histopatoloji veya immünolojiyle değil; görünüş, seyir ve bazen de kokuyla sınıflanıyordu. Bu yüzden sedef benzeri lezyonlar, özellikle lepra (cüzzam) ve diğer kronik dermatozlarla karıştırılabildi. Buradaki epistemik sorun basitti ama belirleyiciydi: Hastalığı ayırdığınız kadar ölçebilirsiniz. “Aynı şey mi, değil mi?” sorusu yanıt bulmadan “ne kadar?” sorusu bilimsel bir ölçüye dönüşemezdi.
Bu dönemde ölçüm fikri, sayısal bir skor değil; daha çok “yaygın–sınırlı”, “hafif–ağır”, “yeni–eski” gibi sezgisel ikiliklerle yürüdü. PASI’ye giden yolun ilk taşı, işte bu ayrım ihtiyacının giderek keskinleşmesidir.
2) 18.–19. yüzyıl: Dermatolojinin doğuşu ve sınıflandırma devrimi
Modern dermatolojinin kurucu döneminde, hastalıkların adlandırılması ve ayrıştırılması büyük bir entelektüel sıçrama yarattı. Klinik gözlem, sistematik bir “deri nosolojisine” dönüştü: lezyon morfolojisi (papül, plak, skuam), dağılım ve kronisite üzerinden hastalıklar birbirinden ayrılmaya başlandı. Bu dönemin belirleyici katkısı, psoriasisi “kendine özgü” bir klinik varlık olarak görünür kılmasıdır.
Bu kademeli ayrışma, sedefin temel görsel imzasını—skuamlı plakları—merkeze alırken, hekimlerin zihninde ikinci bir soru giderek büyüdü: Aynı hastalık, neden bazı hastalarda küçük birkaç alanda kalıyor, bazılarında tüm vücudu kaplıyor? Yani “yaygınlık” kavramı doğrudan klinik düşüncenin içine yerleşti. PASI’nin ileride kuracağı matematiksel iskeletin bir ayağı—vücut alanı—işte burada filizlendi.
3) 20. yüzyılın ilk yarısı: Fenotip çeşitliliği ve “şiddet”in çok boyutluluğu
- yüzyılın başından itibaren psoriasisin yalnızca tek biçimli bir plak hastalığı olmadığı daha net anlaşıldı: eritrodermiye giden yaygın tablolar, püstüler formlar, tırnak tutulumu ve eklem belirtileri gibi varyantlar klinik literatürde belirginleşti. Hastalığın şiddeti artık sadece “ne kadar alan”la değil; lezyonun niteliğiyle, kalınlığıyla, kızarıklığıyla ve dökülmesiyle de ilişkili görülüyordu.
Bu dönem, PASI açısından kritik bir kavrayışı olgunlaştırdı: Psoriasisin şiddeti tek eksenli değildir. Bir hastanın birkaç bölgede kalın, aşırı skuamlı, inflamatuvar plakları olabilir; başka bir hasta daha geniş alanda ama daha yüzeyel lezyonlar taşıyabilir. Ölçmek istenen şey, yaygınlık ile lezyon niteliğinin aynı denklemde buluşturulmasıydı.
4) 1960’lar–1970’ler: Sistemik tedaviler, klinik araştırma disiplini ve “ortak dil” ihtiyacı
Psoriasis tedavisi 20. yüzyıl ortalarında daha “sistemik” bir meseleye dönüştükçe, araştırma tasarımları da keskinleşti. Retinoidler gibi yeni tedavi seçenekleri, klinik araştırmaların ölçek ve yöntem beklentilerini yükseltti: bir ilacın etkisini göstermek için hastaları “iyileşti” demek yetmiyor; etkisi sayıyla ifade edilebiliyor olmalıydı. Araştırma merkezleri arasında karşılaştırılabilirlik, randomize çalışma tasarımları, standart sonlanım noktaları giderek zorunlu hale geldi.
İşte PASI’nin sahneye çıktığı entelektüel atmosfer budur: Klinik gözlemin, araştırma metodolojisinin talep ettiği ölçülebilirliğe dönüştürülmesi.
5) 1978: Fredriksson ve Pettersson’un hamlesi—PASI’nin doğumu
1978’de PASI, sedef hastalığının klinik şiddetini nicelleştirmek üzere tanıtıldı. Bu girişim, basit bir puan çizelgesinden ziyade, dönemi için iddialı bir “kompozit indeks” düşüncesiydi:
- Vücut, klinik pratikte kolay ayırt edilebilen bölgelere ayrıldı (baş, üst ekstremite, gövde, alt ekstremite).
- Her bölge için iki şey aynı anda ölçülmek istendi: alan ve lezyon şiddeti.
- Lezyon şiddeti, üç görünür/elle hissedilir boyutta standardize edildi: eritem, indürasyon, deskuamasyon.
- Bölgelere, kabaca vücut yüzey alanı katkısını temsil eden ağırlıklar verildi.
Bu tasarımın parlak yanı, psoriasisin “gözle görülen biyolojisini” yakalama çabasıydı: kızarıklık inflamasyonun, kalınlık infiltrasyon ve hiperproliferasyonun, skuam ise keratinizasyon hızının klinik izdüşümüydü. PASI, bu üç fenomeni “tek bakışta anlaşılır” bir sayıya indirirken, yaygınlığı da aynı denklemde tutmayı başardı.
PASI’nin hızlı benimsenmesinin nedeni yalnızca pratikliği değildi; daha derinde, dermatolojinin araştırma diliyle klinik dilini birbirine bağlayan bir köprü kurmuş olmasıydı. Klinik gözlem ilk kez, çok merkezli araştırmaların ihtiyaç duyduğu ortak ölçüm birimine dönüşüyordu.
6) 1980’ler–1990’lar: “Altın standart”ın bedeli—zaman, değişkenlik ve hasta deneyimi
PASI yaygınlaştıkça, onunla birlikte iki tür eleştiri büyüdü.
Birincisi metodolojikti: PASI hesaplamak zaman alıyordu; özellikle yoğun klinik akışta her hastada bölge bölge puanlama yapmak zorlaşabiliyordu. Daha önemlisi, ölçümün bazı parçaları kaçınılmaz biçimde gözlemciye bağımlıydı. Eritem derecesi, plak kalınlığının palpasyonla değerlendirilmesi ve skuamın görsel yorumu; farklı klinisyenlerde farklı puanlara kayabiliyordu.
İkincisi kavramsaldı: PASI, deriyi ölçüyordu; ama hastalığın “hastada yarattığı hayatı” doğrudan ölçmüyordu. Kaşıntı, yanma, ağrı, uyku bölünmesi, utanç, işlev kaybı gibi boyutlar PASI’ye sığmıyordu. Bu farkındalık, dermatolojide hasta bildirimli sonuçların ve yaşam kalitesi ölçeklerinin daha görünür olmasına zemin hazırladı.
Bu dönemde bir başka önemli adım da, psoriasisin yalnızca hekim değerlendirmesiyle değil, hastanın kendi kendini değerlendirebilmesi fikrinin araştırılmasıydı. Böylece “ölçüm” kavramı, klinisyen merkezli olmaktan çıkıp hastanın deneyimini de hesaba katan daha geniş bir zemine taşındı.
7) 2000’ler: Basitleştirme girişimleri, alternatif indeksler ve ölçüm ekosisteminin genişlemesi
2000’lerle birlikte PASI’nin çevresinde adeta bir “ölçüm ekosistemi” oluştu. Amaç aynıydı: psoriasisi karşılaştırılabilir biçimde izlemek. Yöntemler ise çoğaldı:
- PASI’yi daha hızlı ve pratik hale getirmeyi amaçlayan basitleştirilmiş türevler geliştirildi.
- BSA gibi yalnızca alanı ölçen yaklaşımlar, günlük pratikte hız kazandırdı.
- PGA/IGA gibi daha bütüncül hekim izlenimine dayalı global değerlendirmeler, PASI’ye alternatif veya tamamlayıcı olarak benimsendi.
Bu dönemde PASI’nin rolü bir bakıma netleşti: PASI, özellikle araştırmalarda güçlü bir ortak dil sunuyor; klinikte ise çoğu zaman daha hızlı ölçütlerle birlikte kullanıldığında anlam kazanıyordu.
8) 2010’lar: İmmünoloji devrimi, biyolojik tedaviler ve PASI’nin “hedef dili”ne dönüşmesi
Psoriasis biyolojisinin T-hücre aracılı inflamasyon ve belirli sitokin eksenleri (özellikle IL-23/IL-17 hattı) üzerinden daha iyi anlaşılmasıyla, tedaviler de dramatik biçimde etkinleşti. Klinik araştırmalar artık “bir miktar iyileşme”yi değil, yüksek oranlı temizlenmeyi hedefleyebilir hale geldi.
Bu, PASI’nin kullanım biçimini değiştirdi. PASI artık yalnızca bir şiddet skoru değil; tedavinin başarısını tanımlayan bir performans göstergesiydi. PASI 75 uzun süre “çok iyi yanıt” sayılırken, giderek PASI 90 ve PASI 100 gibi daha iddialı eşikler klinik araştırmaların dili haline geldi.
Aynı dönemde “treat-to-target” yaklaşımı güç kazandı: Hedef, sadece başlangıca göre relatif iyileşme değil; hastanın güncel durumunu ifade eden mutlak hedefler ve klinik olarak anlamlı eşikler üzerinden yönetimdi. Bu yaklaşım, PASI’nin baseline bağımlılığı gibi sınırlılıklarını daha görünür kıldı ve mutlak PASI hedeflerinin tartışılmasını hızlandırdı.
9) 2010’lar sonu–2020’ler: Dijitalleşme ve nesnelleştirme arzusu—3D araçlar, görüntü analizi, yapay zekâ
PASI’nin en eski eleştirisi—gözlemciye bağımlılık—teknoloji çağında yeni bir “bilimsel merak” başlığını doğurdu: Acaba bu skor, görüntü işleme ve yapay zekâ ile daha nesnel, daha hızlı, daha tekrarlanabilir hale getirilebilir mi?
Bu sorunun peşinden birkaç çizgi halinde ilerleyen çalışmalar ortaya çıktı:
- Dijital/hesaplamalı PASI araçları: Vücut yüzeyinin daha doğru modellenmesi, alan hesabının iyileştirilmesi ve puanlamanın standardize edilmesi hedeflendi. Üç boyutlu beden modelleriyle alan değerlendirmesini daha tutarlı hale getiren yaklaşımlar bu bağlamda önem kazandı.
- Klinik fotoğraf üzerinden otomatik şiddet tahmini: Lezyonun eritemini, skuamını ve kalınlıkla ilişkili görsel ipuçlarını görüntüden çıkaran sistemler geliştirilmeye başlandı.
- Derin öğrenme ve klinik çalışma görüntülerinin kullanımı: Özellikle klinik araştırmalardan gelen standardize görüntülerin, PASI’nin ara bileşenlerini ve toplam skorunu tahmin etmek üzere kullanılması; hem araştırmada körlüğü ve standardizasyonu destekleme hem de klinikte pratik yükü azaltma potansiyeli taşıdı.
Bu dönemdeki entelektüel ilerleme duygusu şuradan gelir: PASI’nin 1978’de çözmeye çalıştığı problem aynı kalmıştır—yaygınlık ve şiddeti tek bir ortak dilde birleştirmek—ama araçlar değişmiştir. O gün insan gözünün ve elinin standardizasyonu hedeflenirken, bugün algoritmaların standardizasyonu hedeflenmektedir.
10) En güncel yaklaşım: PASI’nin çağdaş rolü—ölçümün merkezinde, fakat tek başına değil
Bugün PASI, hâlâ orta-ağır plak psoriasiste araştırmaların en güçlü ortak ölçütlerinden biridir. Bununla birlikte çağdaş yaklaşım, PASI’yi tek başına “hastalığın tamamı” olarak görmez:
- Yaşam kalitesi ve hasta bildirimli sonuçlar, PASI’nin yanına yerleştirilir.
- Mutlak hedefler, baseline’a bağımlı relatif hedefleri tamamlar.
- Klinik kararlar, komorbiditeler ve psoriatik artrit gibi ek boyutlarla birlikte verilir.
- Dijital ölçüm ve yapay zekâ, PASI’yi daha nesnel ve tekrarlanabilir kılma iddiasıyla hızla gelişir; ancak klinik geçerlik, farklı fototiplerde güvenilirlik, veri yanlılıkları ve gerçek-dünya uygulanabilirliği gibi sorular, bu alanın bilimsel çekim merkezini oluşturur.
İleri Okuma
- Fredriksson, T. (1978). Severe Psoriasis—Oral Therapy with a New Retinoid.
- Fleischer, A.B. (1994). Patient measurement of psoriasis disease severity with a structured instrument. Journal of Investigative Dermatology.
- Louden, B.A. (2004). A simplified psoriasis area severity index (SPASI) for rating psoriasis severity. Dermatology Online Journal.
- NCBI Bookshelf (2018). Validity of Outcome Measures – Clinical Review Report: Psoriasis outcome measures including PASI and response thresholds. National Center for Biotechnology Information.
- Mahil, S.K. (2019). Psoriasis treat to target: defining outcomes in psoriasis and limitations of relative PASI thresholds.
- Mattei, P.L. (2014). Psoriasis Area Severity Index (PASI) and the Dermatology Life Quality Index (DLQI): the correlation between disease severity and quality of life. Journal of the European Academy of Dermatology and Venereology, 28, DOI: 10.1111/jdv.12106.
- Bożek, A. (2017). Psoriasis area and severity index, body surface area and physician global assessment: reliability and variability considerations. Advances in Clinical and Experimental Medicine, 26(5), 851–856.
- Goon, P.K.C. (2017). Assessment of a 3-dimensional computerised PASI tool for calculating psoriasis severity.
- DermNet New Zealand (2023). PASI (psoriasis area and severity index). DermNet.
- Manchanda, Y. (2023). Disease Assessment in Psoriasis.
- Huang, K. (2023). Artificial Intelligence–Based Psoriasis Severity Assessment. Journal of Medical Internet Research, 25:e44932.
- Xing, Y. (2024). Deep learning-based psoriasis assessment: clinical trial imaging for PASI prediction. Digital Biomarkers.
- MDCalc (2025). Psoriasis Area and Severity Index (PASI) Calculator: clinical interpretation and use in monitoring.
- Ożóg, M.K. (2025). New Therapies in the Biological Treatment of Psoriasis.